2. 中国食品药品检定研究院, 北京 100050
2. National Institutes for Food and Drug Control, Beijing 100050, China
青霉素酶在自然界的多细菌中广泛存在,能够水解青霉素类抗生素,是临床致病菌最重要的耐药机制之一[1]。1940年Abraham和Chain发现并命名青霉素酶[2]。国内1951年制得青霉素酶,并作为灭活剂用于青霉素药品的无菌试验,消除青霉素类抗生素的抑菌性,避免造成假阴性的判断[3]。1990年版中国药典收录青霉素酶及其活力测定条目,并延续至2015年版中国药典[4]。
目前青霉素酶活力测定方法主要有碘量法[5-8]和羟胺法[3, 9],2015年版中国药典收录的方法为碘量法。青霉素在青霉素酶的作用下,酶中亲核性基团向β-内酰胺环进攻,开环后可重排生成中间体青霉噻唑酸[10],青霉噻唑酸能与碘发生定量反应,即每8个碘与1个青霉噻唑酸分子反应,根据碘的消耗量,得出单位时间内降解的青霉素的量,计算青霉素酶的活力。羟胺法根据β-内酰胺类抗生素与羟胺反应生成羟肟酸,羟肟酸与三价铁离子结合显色,在515 nm处有最大吸收,可测得青霉素的量,根据单位时间内青霉素酶反应前后青霉素含量的差,推算青霉素酶的活力,这2种方法均操作复杂。
中国药典对青霉素酶活力的定义为:在一定条件下(37 ℃,pH 7.0的磷酸盐缓冲液),1 h内转化1单位青霉素所需的酶量,酶活力单位(U)写作:U·(mL·h)-1。国际单位(IU)指:在特定条件下(最适pH、30 ℃,最适底物浓度最适缓冲液),1 min内能转化1 μmol底物所需的酶量,单位为μmol·(min·μL)-1。酶反应对温度十分敏感,温度每变化1 ℃,反应速度可相差±10%[11],反应温度的不同和表述的差异使得按中国药典方法测定的青霉素酶活力无法与国际单位进行对比,对生产及检测造成极大的不便。
本文采用紫外分光光度法测定青霉素酶活力,该方法与碘量法相比,快速、简便。利用青霉素及其水解产物青霉噻唑酸在紫外区均有吸收且吸光系数不同的特点,选取232 nm作为工作波长[11],随着一定量的青霉素被青霉素酶不断水解,吸光度逐渐下降,通过吸光度的改变测得反应时间来间接测定青霉素酶的活力。用该方法分别测定30 ℃和37 ℃下的青霉素酶活力,建立中国药典青霉素酶活力单位与国际单位之间的关系。
1 仪器与试剂Lambda 35紫外分光光度计、PTP-A控温附件(PerkinElmer公司);AE 163电子天平(梅特勒公司);Sevenmulti pH计(梅特勒公司);DKN412C恒温箱(Yamato公司)。
青霉素酶(中国食品药品检定研究院,批号201601007、201601008、201601013、201601018、201601022、201601024、201601027、201601028);青霉素G(华北制药股份有限公司,批号20101505112)。
2 方法与结果 2.1 溶液配制取磷酸氢二钾7.36 g与磷酸二氢钾3.14 g,加水使成1 000 mL,即得pH 7.0磷酸盐缓冲液(PBS)。称取青霉素G约30 mg,精密称定,置50 mL量瓶中,加pH 7.0的磷酸盐缓冲液溶解并稀释至刻度,摇匀,即得青霉素G溶液,37 ℃保存备用。精密量取青霉素酶3.00 mL,置25 mL量瓶中,加PBS稀释至刻度,摇匀,即得青霉素酶溶液,37 ℃保存备用。
2.2 检测方法精密量取37 ℃预热的PBS 2.4 mL和青霉素酶溶液0.10 mL,置于1 cm石英池中,由控温附件保持37 ℃恒温,快速加入青霉素G溶液0.50 mL,使用timedrive模式,立即开始计时,在232 nm处每0.5 s扫描1次,记录吸光度随时间变化的曲线。
2.3 计算2015年版中国药典四部通则1202中对青霉素酶活力单位定义为U·(mL·h)-1,从反应的吸光度-时间曲线图中读取反应时间t,按下式计算:
| $E = \frac{{{C_{{\rm{PG}}}}\cdot{V_{{\rm{PG}}}}\cdot F}}{{t\cdot{V_{{\rm{PE}}}}\cdot{C_{{\rm{PE}}}}}}$ |
式中,E为青霉素酶活力,U·(mL·h)-1;CPG为青霉素G溶液的质量浓度,mg·mL-1;VPG为比色皿中加入的青霉素G的体积,mL;CPE为青霉素酶的体积分数,mL·mL-1;VPE为比色皿中加入的青霉素酶的体积,mL;F为每毫克青霉素的单位数,U·mg-1;t为反应所需要的时间,h。
2.4 重复性试验取同一批青霉素酶,分别配制6份上述青霉素酶溶液,按“2.2”项下方法操作,按“2.3”项下公式计算,结果见表 1。RSD为2.8%,该方法重复性良好。
|
|
表 1 重复性试验结果 Table 1 The results of repeated experiments |
对8批青霉素酶分别用本文的紫外分光光度法和中国药典的碘量法测定其活力,实验结果见表 2。用SPSS 16.0软件进行数据分析,两方法没有显著性差异(P=0.302 > 0.05)。
|
|
表 2 紫外分光光度法与碘量法比较[×104 U·(mL·h)-1] Table 2 Comparison between UV method and iodimetry method |
按“2.2”所述方法,分别在30 ℃和37 ℃测定青霉素酶的活力并进行线性拟合考察其相关性,结果如表 3和图 1。
|
|
表 3 30 ℃和37 ℃下青霉素酶活力[×104 U·(mL·h)-1,n=3] Table 3 Penicillinase activity(E) at 30 ℃ and 37 ℃ |
|
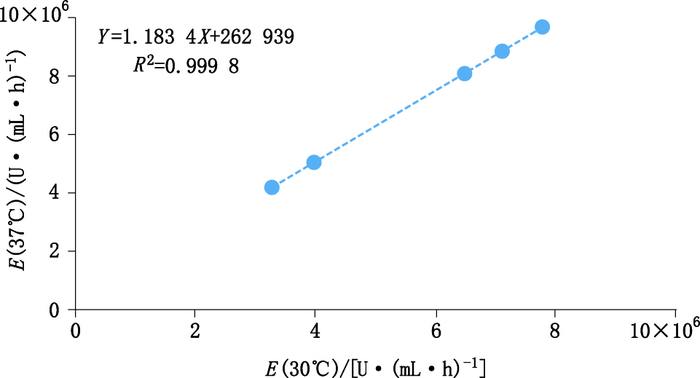
图 1 30 ℃与37 ℃酶活力相关性 Figure 1 correlation between penicillinase activity at 30 ℃ and 37 ℃ |
由回归方程可得,在30 ℃和37 ℃下青霉素酶活力的关系为:E(37 ℃)=1.183 4E(30 ℃)+262 939
3 讨论碘量法与紫外分光光度法都是对青霉素的开环产物即青霉噻唑酸进行测定。碘量法采用的是中止反应法,在反应进行一段时间后通过加酸使酶失活,人为中止反应后对反应产物进行定量测定来计算青霉素酶活力;而紫外分光光度法采用的是终点法,通过测定一定量底物被完全酶解所需时间来计算青霉素酶活力。2种方法的酶促反应进行程度不同,但对于酶活力测定结果没有影响。
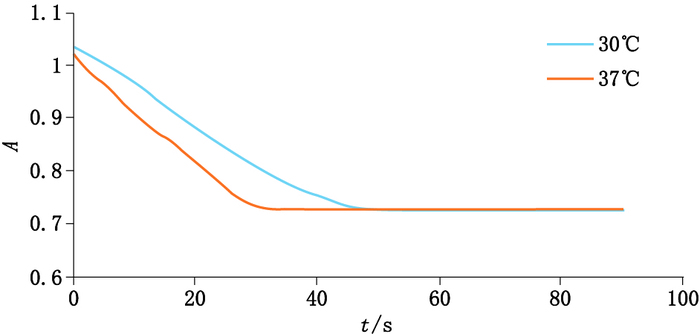
青霉素与青霉素酶反应的吸光度与时间的关系如图 2所示。有2种方法可以确定反应时间,一是从曲线直接读取反应拐点的时间,该方法方便,快速,但由于反应速度快,反应时间短,误差较大;二是根据反应进行时的斜率和反应结束后的吸光度计算反应时间,该方法消除了偶然误差,提高了准确度。
|
图 2 反应吸光度-时间曲线图 Figure 2 Reaction curves on time-absorption of penicillin and penicillinase |
在实际测定中,酶活力单位往往与测定底物、条件、方法有关。因此,不同的酶会有不同的活力单位,同一种酶也会出现不同的活力单位[12-14]。1961年,国际生化学会酶学委员会提出,采用统一的“国际单位”来表示酶活力。中国药典青霉素酶活力单位写作U·(mL·h)-1,国际单位写作μmol·(min·μL)-1,根据1 mg C16H17N2NaO4S相当于1 670青霉素单位[15],计算得2个单位之间的数值关系为1 U·(mL·h)-1=3.72×107 μmol·(min·μL)-1。中国药典所用单位和国际单位最主要的差别是反应温度不同,国际单位、BP[15]、EP[16]及相关文献中均都采用30 ℃作为反应温度,而中国药典采用37 ℃作为反应温度。温度对酶活力的影响体现在反应阶段曲线斜率的差别,中国药典酶反应温度较高,反应速度快,曲线斜率高(如图 2),测得的酶活力高。根据本文研究的30 ℃与37 ℃下青霉素酶活力的关系可得中国药典青霉素酶活力单位(U)与国际单位(IU)的换算关系为:1 U=4.4×107 IU+2.6×105。
紫外分光光度法测定青霉素酶活力与目前中国药典使用的碘量法相比,具有操作简单、快速、干扰因素少等优点。本文利用该方法针对反应温度的不同测定了青霉素酶活力中国药典单位与国际单位之间的换算关系,使中国药典青霉素酶活力测定与国际接轨,以便加强国际学术交流。
| [1] |
张凤凯, 张枫. 蜡样芽孢杆菌CMCC(B)63301产生青霉素酶的特性及其应用的研究[J]. 药物分析杂志, 1999, 19(3): 159. ZHANG FK, ZHANG F. Study on characters and its application of penicillinase from Bacillus cereus CMCC(B)63301[J]. Chin J Pharm Anal, 1999, 19(3): 159. |
| [2] |
ABRAHAM EP, CHAIN E. An enzyme from bacteria able to destory penicillin[J]. Nature, 1940, 146: 837. |
| [3] |
沈注飞, 周冰, 张加慧. 紫外分光光度法检测金属β-内酰胺酶活性的研究[J]. 中国抗生素杂志, 2015, 40(12): 930. SHEN ZF, ZHOU B, ZHANG JH. Study on determination of metallo-β-lactamase used in sterility test by UV spectrophotometry[J]. J Chin Antibiot, 2015, 40(12): 930. DOI:10.3969/j.issn.1001-8689.2015.12.009 |
| [4] |
中国药典2015年版. 四部[S]. 2015: 165 ChP 2015. Vol Ⅳ[S]. 2015:165 |
| [5] |
PERRET CJ. Iodometric assay of penicillinase[J]. Nature, 1954, 174: 1012. DOI:10.1038/1741012a0 |
| [6] |
SAWAI T, TAKAHASHI I, YAMAGISHI S. Iodometric assay method for beta-lactamase with virous beta-lactam antibiotics as substrates[J]. Antimicrob Agents Chemother, 1978, 13: 910. DOI:10.1128/AAC.13.6.910 |
| [7] |
NOVICK RP. Micro-iodometric assay for penicillinase[J]. Biochem J, 1962, 83: 236. DOI:10.1042/bj0830236 |
| [8] |
MICHAEL G, SARGENT T. Rapid fixed-time assay for penicillinase[J]. J Bacteriol, 1968, 95(4): 1493. |
| [9] |
王芳, 仪宏, 王丽丽. 羟胺法测定青霉素酶酶活的研究[J]. 中国抗生素杂志, 2010, 35(4): 316. WANG F, YI H, WANG LL. Study on hydroxylamine method of determining penicillinase activity[J]. J Chin Antibiot, 2010, 35(4): 316. |
| [10] |
郭宗儒. 药物化学[M]. 北京: 高等教育出版社, 2005. GUO ZR. Medicinal Chemistry[M]. Beijing: Higher Education Press, 2005. |
| [11] |
厉滔, 陈知本, 陈小英. 紫外分光光度法测定青霉素酶动力学常数[J]. 中国药科大学学报, 1990, 21(4): 211. LI T, CHEN ZB, CHEN XY. A spectrophotometric method of estimating the kinetic parameters of penicillinase on penicillin substrates[J]. J Chia Pharm Univ, 1990, 21(4): 211. |
| [12] |
姜涌明, 戴祝英, 陈俊刚, 等. 分子酶学导论[M]. 北京: 中国农业大学出版社, 2000, 12. JIANG YM, DAI ZY, CHEN JG, et al. Introduction of Enzymology[M]. Beijing: China Agricultural University Press, 2000, 12. |
| [13] |
陈石根, 周润琦. 酶学[M]. 上海: 复旦大学出版社, 2001, 224. CHEN SG, ZHOU RQ. Enzymology[M]. Shanghai: Fudan University Press, 2001, 224. |
| [14] |
王丽芳, 吴克力, 郭学兰, 等. 几种自定义酶活性单位常见错误辨析及规范使用建议[J]. 中国科技期刊研究, 2013(05): 1009. WANG LF, WU KL, GUO XL, et al. Discrimination of several customized enzyme activity units and advice on specification usage[J]. Chin J Sci Techn Period, 2013(05): 1009. DOI:10.3969/j.issn.1001-7143.2013.05.050 |
| [15] |
中国药典2015年版. 二部[S]. 2015: 599 ChP 2015. Vol Ⅱ[S]. 2015:599 |
| [16] |
BP 2015. Vol Ⅴ[S]. 2015:V-A99
|
| [17] |
EP 8. 0. Vol Ⅰ[S]. 2013:498
|
 2017, Vol. 37
2017, Vol. 37 
