2. 河南省中医药研究院, 郑州 450004;
3. 河南中医药大学, 郑州 450008
2. Henan Academy of Traditional Chinese Medicine, Zhengzhou 450004, China;
3. Henan University of Traditional Chinese Medicine, Zhengzhou 450008, China
速克感冒胶囊是由忍冬藤、野菊花、射干3味中药与乙酰水杨酸、马来酸氯苯那敏、维生素C 3种化学药物制成的中西药复方制剂,具有清热解毒的功效,用于流行性感冒、上呼吸道感染等症的治疗[1]。方中忍冬藤主要含有绿原酸、咖啡酸等有机酸类成分[2],野菊花含蒙花苷等黄酮类和绿原酸等有机酸类成分[3],射干中含有次野鸢尾黄素等异黄酮类成分[4]。其中绿原酸是忍冬藤和野菊花中的重要有效成分,具有抗氧化、抑菌、抗病毒、抗炎等多种活性[5],常作为指标性成分对忍冬藤和野菊花进行定量控制[6-7],野菊花中的蒙花苷等黄酮具有抗氧化作用[8],次野鸢尾黄素等射干中的异黄酮可通过抑制NO生成或5-LOX酶途径发挥抗炎作用[9-10]。在现行速克感冒胶囊的质量标准中仅有马来酸氯苯那敏的薄层定性鉴别,不能全面反映药品内在质量。HPLC法是乙酰水杨酸、马来酸氯苯那敏和维生素C的常用定量方法[11-13],文献报道[14-17]曾对速克感冒胶囊中的乙酰水杨酸、马来酸氯苯那敏和维生素C的1种或2种化学药物及蒙花苷、绿原酸等中药成分的含有量进行了测定。考虑到除乙酰水杨酸、马来酸氯苯那敏和维生素C外,绿原酸等有机酸、蒙花苷等黄酮苷和次野鸢尾黄素等异黄酮类成分均是与速克感冒胶囊功效相关的重要活性成分,本文采用反相高效液相色谱法,分别以绿原酸、蒙花苷、次野鸢尾黄素、乙酰水杨酸、马来酸氯苯那敏5种成分为指标,进行含量测定研究,建立定量方法,为更全面评价和控制速克感冒胶囊的质量提供参考依据。
1 仪器与试药Waters 2695高效液相色谱仪(配有2996二极管阵列检测器,柱温箱和Empower Ⅱ色谱工作站;Waters公司);Venusil XBP色谱柱(4.6 mm×250 mm,5 µm;填料:十八烷基硅烷键合硅胶;博纳艾杰尔科技公司);KQ-250超声波提取器(昆山市超声仪器有限公司);XR 205SM-DR十万分之一分析天平(PRECISA公司)。
对照品绿原酸(批号110753-201415)、蒙花苷(批号111528-201308)、次野鸢尾黄素(批号111557-200602)、乙酰水杨酸(批号100113-201405)、马来酸氯苯那敏(批号100047-200602) 均购自中国食品药品检定研究院。速克感冒胶囊(0.4 g·粒-1),由河南辅仁堂制药有限公司提供,批号分别为20151201、20151202和20151203。
甲醇、乙腈为色谱纯,水为超纯水,其余试剂均为分析纯。
2 方法与结果 2.1 溶液的配制 2.1.1 混合对照品溶液精密称取绿原酸、马来酸氯苯那敏、乙酰水杨酸、蒙花苷和次野鸢尾黄素的对照品适量,用0.5%磷酸的甲醇溶液制成每1 mL分别含绿原酸15.5 μg、马来酸氯苯那敏39.1 μg、乙酰水杨酸813.3 μg、蒙花苷33.0 μg和次野鸢尾黄素9.5 μg的混合溶液,即得。
2.1.2 供试品溶液取本品胶囊内容物5粒,研细,取约0.2 g,精密称定,置50 mL量瓶中,加0.5%磷酸的甲醇溶液40 mL,超声(功率250 W,频率40 kHz)处理30 min,放冷,用0.5%磷酸的甲醇溶液稀释至刻度,摇匀,用0.45 μm微孔滤膜滤过,即得。
2.1.3 阴性样品溶液按处方和工艺,分别制备缺忍冬藤、缺野菊花、缺射干、缺乙酰水杨酸、缺马来酸氯苯那敏及缺忍冬藤与野菊花的阴性样品,按“2.1.2”项下方法操作,分别制备阴性样品溶液。
2.2 色谱条件及系统适用性试验色谱柱:Venusil XBP C18色谱柱(4.6 mm×250 mm,5 µm);流动相:乙腈(A)-0.5%磷酸水溶液(B),梯度洗脱(0~12 min,12%A→20%A;12~25 min,20%A→40%A;25~39 min,40%A→60%A;39~40 min,60%A→12%A);流速:1.0 mL·min-1;检测波长:327 nm(0~8.2 min,绿原酸),260 nm(8.2~16.0 min,氯苯那敏),276 nm(16.0~22.0 min,乙酰水杨酸),334 nm(22.0~32.0 min,蒙花苷),266 nm(32.0~40.0 min,次野鸢尾黄素);柱温:35 ℃;进样量:10 µL。理论塔板数按绿原酸峰计算应不低于3 000。
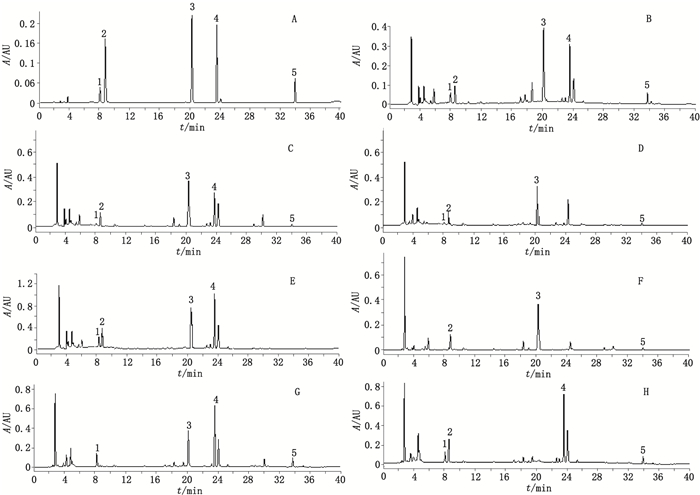
在上述色谱条件下,分别取混合对照品溶液、供试品溶液及各阴性样品溶液各10 μL,进样测定,色谱图见图 1。样品色谱中,可清晰检出绿原酸、氯苯那敏、乙酰水杨酸、蒙花苷和次野鸢尾黄素的色谱峰;缺野菊花阴性样品色谱中在与蒙花苷色谱峰相对应的保留时间无干扰;缺忍冬藤和野菊花阴性样品色谱中在与绿原酸和蒙花苷相对应的保留时间无干扰;缺射干阴性样品色谱中在与次野鸢尾黄素对应的保留时间无干扰;缺马来酸氯苯那敏阴性样品色谱中在与氯苯那敏相对应的保留时间无干扰;缺乙酰水杨酸阴性样品色谱中在与乙酰水杨酸相对应的保留时间无干扰。
|
1.绿原酸(chlorogenic acid) 2.氯苯那敏(chlorphenamine) 3.乙酰水杨酸(acetylsalicylic acid) 4.蒙花苷(linarin) 5.次野鸢尾黄素(irisflorentin) A.混合对照品(mixed reference substances) B.样品(sample) C.缺忍冬藤阴性样品(negative sample without Lonicerae Japonicae Caulis) D.缺野菊花阴性样品(negative sample without Chrysanthemi Indici Flos) E.缺射干阴性样品(negative sample without Belamcandae Rhizoma) F.缺忍冬藤和野菊花阴性样品(negative sample without Lonicerae Japonicae Caulis and Chrysanthemi Indici Flos) G.缺马来酸氯苯那敏阴性样品(negative sample without chlorphenamine maleate) H.缺乙酰水杨酸阴性样品(negative samples without acetylsalicylic acid) 图 1 混合对照品、速克感冒胶囊和阴性样品的HPLC色谱图 Figure 1 HPLC chromatograms of mixed reference substances, Suke Ganmao capsules and negative samples |
精密吸取“2.1.1”项下的混合对照品溶液5、10、15、20、25 μL,分别注入液相色谱仪,进行测定。以峰面积Y为纵坐标,进样量X(μg)为横坐标,进行线性回归,回归方程、相关系数及线性范围见表 1。
|
|
表 1 回归方程、线性关系及相关系数 Table 1 Regression equations, linear ranges & correlation coefficients |
吸取“2.1.1”项下混合对照品溶液10 μL,连续重复进样6次,测定峰面积并计算RSD,结果绿原酸、氯苯那敏、乙酰水杨酸、蒙花苷和次野鸢尾黄素峰面积的RSD分别为0.93%、0.31%、1.9%、0.30%和1.3%,表明仪器精密度较好。
2.3.3 稳定性试验取同一供试品溶液,分别于0、2、4、6、8、10 h注入液相色谱仪,测定各待测成分的峰面积并计算RSD,结果绿原酸、氯苯那敏、乙酰水杨酸、蒙花苷和次野鸢尾黄素峰面积的RSD分别为2.0%、1.9%、1.7%、1.1%和1.1%,表明供试品溶液中5个待测成分室温放置10 h内基本稳定。
2.3.4 重复性试验取速克感冒胶囊(批号20151201),按“2.1.2”项下方法平行制备6份供试品溶液,按“2.1”项下色谱条件进行测定。绿原酸、马来酸氯苯那敏、乙酰水杨酸、蒙花苷和次野鸢尾黄素的平均含量分别为0.879、2.290、110.025、2.242和0.058 g·粒-1,RSD分别为1.7%、2.5%、1.4%、2.4%和1.3%,表明本法重复性较好。
2.3.5 加样回收率试验精密取已知含量的速克感冒胶囊(批号20151201)0.1 g,置50 mL量瓶中,分别精密加入用0.5%磷酸的甲醇溶液配制的混合对照品溶液(绿原酸0.028 mg·mL-1,马来酸氯苯那敏0.055 mg·mL-1,乙酰水杨酸2.771 mg·mL-1,蒙花苷0.064 mg·mL-1,次野鸢尾黄素1.68 μg·mL-1)10 mL,按“2.1.2”项下方法制备加样供试溶液。按“2.2”项下条件测定分析,计算各待测成分的加样回收率,结果见表 2。
|
|
表 2 加样回收率试验结果(n=6) Table 2 Results of recovery tests |
取3批速克感冒胶囊样品,按“2.1.2”项下方法制备供试品溶液,按“2.2”项下条件测定,外标一点法计算含量,结果见表 3。
|
|
表 3 3批速克感冒胶囊中5种成分的含量测定结果(mg·粒-1,n=3) Table 3 Contents of five components of Suke Ganmao capsules(mg per capsule, n=3) |
速克感冒胶囊由忍冬藤、野菊花、射干3味中药经水煎煮提取、醇沉浓缩后与乙酰水杨酸、马来酸氯苯那敏、维生素C 3种化学药物混合制成,现行质量标准中无定量方法。在预试验中,根据忍冬藤、野菊花和射干的化学成分文献报道,拟选择以忍冬藤中的绿原酸、马钱苷、咖啡酸和异绿原酸A、B、C,野菊花中的蒙花苷和木犀草苷,射干中的次野鸢尾黄素和射干苷等多种成分,与乙酰水杨酸、马来酸氯苯那敏、维生素C共同作为测定指标,进行速克感冒胶囊的含量测定研究。结果由于样品中马钱苷、咖啡酸、木犀草苷、射干苷和异绿原酸A、B、C的含量较低,无法检出或误差较大,不宜作为定量指标。另外,维生素C的保留时间较短,经反复调整流动相配比,降低乙腈比例,仍无法将其与色谱前部的杂质峰分离开,维生素C的测定方法有待今后开展深入研究。通过方法学研究,建立了速克感冒胶囊中绿原酸、马来酸氯苯那敏、乙酰水杨酸、蒙花苷和次野鸢尾黄素5种成分的含量测定方法。
3.2 流动相的选择速克感冒胶囊系中西药复方制剂,化学成分较复杂,且成分的含量差异较大。马来酸氯苯那敏在溶液中可解离为马来酸和氯苯那敏,氯苯那敏是针对感冒症状的有效成分,经反复试验,建立了绿原酸、氯苯那敏、乙酰水杨酸、蒙花苷和次野鸢尾黄素5种成分分离和检测的流动相梯度洗脱程序。按照本文方法,5种待测成分峰保留时间适宜,峰形基本对称,与相邻峰可达较好的分离度,总分析时间控制在40 min。经试用不同品牌的色谱柱,HPLC色谱差异不大,能够保证测定的准确性和适用性。
3.3 测定波长的确定在实验中,分别对待测成分色谱峰进行吸收光谱扫描,根据其最大吸收光谱,参照中国药典有关规定,选定绿原酸、氯苯那敏、乙酰水杨酸、蒙花苷和次野鸢尾黄素的测定波长分别为327、260、276、334和266 nm。采用Waters Empower Ⅱ色谱工作站的定时波长功能,按时间改变检测波长,提高了测定的灵敏度和准确性。
3.4 供试品溶液的制备根据待测成分的理化性质,在试验中,试用了甲醇、乙醇和稀乙醇等提取溶剂,超声制备供试品溶液,结果供试品溶液中乙酰水杨酸的测得量仅为标示量的60%~70%,且色谱在24 min出现一色谱峰,进样水杨酸对照品溶液,确认该色谱峰为乙酰水杨酸的水解产物水杨酸。为抑制供试品溶液在制备过程中乙酰水杨酸的水解,使用含有0.5%磷酸的甲醇溶液为提取溶剂。经试验,酸性甲醇溶液可以较好地解决乙酰水杨酸的水解,同时还能提高绿原酸、蒙花苷和次野鸢尾黄素等有机酸和黄酮成分的转移率。按文中供试品溶液的制备方法和色谱条件测定,5种成分的回收率均>95%,且马来酸氯苯那敏和乙酰水杨酸的测得量均在处方标示量的90%~110%范围内,提示测定数据合理。
3.5 小结本文采用高效液相色谱法建立了同时测定速克感冒胶囊中3种中药成分和2种化学药成分含量的定量方法,所建立方法操作简便,快捷准确,重复性好,可为速克感冒胶囊的全面质量评价提供参考。
| [1] |
卫生部药品标准. 中药成方制剂. 第二十册[S]. 1998: 307 Drug Specifications Promulgated by Ministry of Public Health, PR China. Chinese Medicines Formula Preparation. Vol 20[S]. 1998:307 |
| [2] |
鲁思爱. 忍冬藤的化学成分及其药理应用研究进展[J]. 临沂大学学报, 2012, 34(3): 132. LU SA. The chemical composition of the Caulis Lonicerae and pharmacological application research progress[J]. J Linyi Univ, 2012, 34(3): 132. |
| [3] |
刘丹丹, 苗明三. 野菊花现代研究及作用特点分析[J]. 中医学报, 2014, 29(4): 551. LIU DD, MIAO MS. Modern research and characteristics analysis on Chrysanthemum indicum[J]. China J Chin Med, 2014, 29(4): 551. |
| [4] |
张杰, 曾铖, 常义生, 等. 射干化学成分研究[J]. 安徽农业科学, 2015, 43(24): 57. ZHANG J, ZENG C, CHANG YS, et al. Study on chemical constituents of Belamcanda chinensis(L.)DC[J]. J Anhui Agric Sci, 2015, 43(24): 57. DOI:10.3969/j.issn.0517-6611.2015.24.021 |
| [5] |
赵金娟, 戴雪梅, 曲永胜, 等. 绿原酸药效学研究进展[J]. 中国野生资源, 2013, 32(4): 1. ZHAO JJ, DAI XM, QU YS, et al. Progress in the pharmacodynamics of chlorogenic acid[J]. Chin Wild Plant Res, 2013, 32(4): 1. |
| [6] |
左霞, 刘春霞, 杨金霞, 等. HPLC法测定不同来源不同采收期忍冬藤和金银花中绿原酸含量[J]. 中国药师, 2015, 18(4): 682. ZUO X, LIU CX, YANG JX, et al. Determination of chlorogenic acid in honeysuckle stem and honeysuckle from different sources in different harvest periods by HPLC[J]. China Pharm, 2015, 18(4): 682. |
| [7] |
郭巧生, 房海灵, 申海进. 不同产地野菊花中绿原酸、咖啡酸和蒙花苷含量[J]. 中国中药杂志, 2010, 35(9): 1160. GUO QS, FANG HL, SHEN HJ. Determination of chlorogenicacid, caffeic acid and linarin in Flos Chrysanthemi Indici from different places by RP-HPLC[J]. China J Chin Meter Med, 2010, 35(9): 1160. |
| [8] |
孟庆玉, 符玲, 高振, 等. 野菊花总黄酮提取方法比较及其抗氧化活性研究[J]. 中草药, 2015, 46(21): 3194. MENG QY, FU L, GAO Z, et al. Comparison of different extraction processes of total flavonoids in Chrysanthemum indicum and its antioxidant effect[J]. Chin Tradit Herb Drugs, 2015, 46(21): 3194. DOI:10.7501/j.issn.0253-2670.2015.21.012 |
| [9] |
邹桂欣, 尤献民, 王光函, 等. 野鸢尾中异黄酮与其抗炎作用的相关性分析[J]. 中华中医药学刊, 2016, 34(10): 2406. ZOU GX, YOU XM, WANG GH, et al. Correlation of isoflavones components and anti-inflammatory effects in Iris dichotma[J]. Chin Arch Tradit Chin Med, 2016, 34(10): 2406. |
| [10] |
康愿涛, 邹桂欣, 尤献民, 等. 射干异黄酮成分对5-脂氧合酶的作用研究[J]. 中药与临床, 2015, 6(1): 43. KANG YT, ZOU GX, YOU XM, et al. The effece of isoflavone in Shegan on 5-lipoxyqenase[J]. Pharm Clin Chin Mater Med, 2015, 6(1): 43. |
| [11] |
王腾, 王晓敏, 张亚运, 等. 高效液相色谱法同时测定复方乙酰水杨酸片中各有效成分的含量[J]. 北京石油化工学院学报, 2012, 20(1): 41. WANG T, WANG XM, ZHANG YY, et al. Simultaneous determination of three components in compound aspirin tablets by HPLC[J]. J Beijing Inst Petro-Chem Technol, 2012, 20(1): 41. |
| [12] |
王丽琼, 赵雪, 刘明容, 等. RP-HPLC法同时测定复方酚咖伪麻胶囊5种组分的含量[J]. 药物分析杂志, 2016, 36(8): 1403. WANG LQ, ZHAO X, LIU MR, et al. Simultaneous determination of five ingredients in compound paracetamol caffeine and pseudoephedrine hydrochloride capsules by RP-HPLC[J]. Chin J Pharm Anal, 2016, 36(8): 1403. |
| [13] |
金鹏飞, 夏路风, 李铮, 等. 高效液相色谱同时测定多维元素片中的维生素B1、维生素B6、维生素C、烟酰胺和泛酸[J]. 药物分析杂志, 2012, 32(9): 1606. JIN PF, XIA LF, LI Z, et al. Simultaneous determination of vitamin B1, vitamin B6, vitamin C, niacinamide and pantothenic acid in vitamins with minerals tablets by HPLC[J]. Chin J Pharm Anal, 2012, 32(9): 1606. |
| [14] |
王静, 袁子民, 张振秋, 等. HPLC法测定速克感冒胶囊中马来酸氯苯那敏的含量和含量均匀度[J]. 药物分析杂志, 2009, 29(3): 467. WANG J, YUAN ZM, ZHANG ZQ, et al. HPLC determination of content and content uniformity of chlorphenam inemaleate in Sukeganmao capsules[J]. Chin J Pharm Anal, 2009, 29(3): 467. |
| [15] |
高颖, 郭鹏, 李建宇, 等. RP-HPLC同时测定速克感冒胶囊中乙酰水杨酸、维生素C含量[J]. 武警后勤学院学报(医学版), 2014, 23(5): 409. GAO Y, GUO P, LI JY, et al. Determination of acetylsalicylic acid, vitamin C in Sukeganmao capsule by RP-HPLC[J]. J Log Univ PAPF(Med Sci), 2014, 23(5): 409. |
| [16] |
冯秋红. 高效液相色谱法测定速克感冒胶囊中蒙花苷的含量[J]. 中国药房, 2006, 17(4): 297. FENG QH. Determination of linarin in Sukeganmao capsules by HPLC[J]. China Pharm, 2006, 17(4): 297. |
| [17] |
任占军, 谷学新, 侯士果, 等. HPLC法测定速克感冒片中绿原酸的含量[J]. 药物分析杂志, 2007, 27(5): 752. REN ZJ, GU XX, HOU SG, et al. HPLC determination of chlorogenic acid in Suke Ganmao tablets[J]. Chin J Pharm Anal, 2007, 27(5): 752. |
 2017, Vol. 37
2017, Vol. 37 
