妇科分清丸由当归、白芍、川芎、栀子、黄连、甘草、木通、地黄、石韦、海金沙、滑石共11味药材组成,具清热利湿,活血止痛之功效[1]。妇科分清丸为2015年版中国药典收录的中药制剂,但是未对其进行质量控制,且有关其含量测定和质量控制文献较少[2-4],最多测定2种成分,包含的药物少,为了更好地控制制剂质量,本文建立了高效液相色谱法同时测定其中8种成分的含量。妇科分清丸中当归和川芎中含有阿魏酸,其具有抗氧化、抑菌消炎、抗血栓、抗癌等作用[5];白芍中含有芍药苷,其具有免疫调节的作用[6];川芎中含有川芎嗪,栀子中含有京尼平龙胆双糖苷和栀子苷,其具有抗炎、抗肝损伤作用[7];黄连中含有小檗碱,甘草中含有甘草酸,木通中含有木通苯乙醇苷B,涵盖了君药臣药佐使药的主要有效成分,这对于妇科分清丸的质量控制具有重要意义,也可以为下一部中国药典增加此药的成分测定提供借鉴。
1 仪器与试药日本岛津LC-20AT高效液相色谱仪,包括SPD-M20A二极管阵列检测器、SIL-20A自动进样器、LC-solution工作站;迪马科技有限公司DIKMA Platisil ODS色谱柱(250 mm×4.6 mm,5 μm;填料:十八烷基硅烷键合硅胶);MILLIPORE公司Synergy 185超纯水仪;昆山市超声仪器有限公司KQ-250DE型数控超声波清洗器。
对照品川芎嗪(批号110817-201307)、栀子苷(批号110749-201316)、芍药苷(批号110736-201539)、甘草酸(批号110731-201418)、阿魏酸(批号110773-201313)、木通苯乙醇苷B(批号111910-201303)、盐酸小檗碱(批号110713-201212) 均购自中国食品药品检定研究院;京尼平龙胆双糖苷(批号141120,纯度≥98%)购自成都普菲德生物技术有限公司;妇科分清丸(北京勃然制药有限公司,批号140805、140602、150408)。乙腈为色谱纯,水为超纯化水,其他试剂均为分析纯。
2 方法与结果 2.1 混合对照品溶液的制备精密称取京尼平龙胆双糖苷、栀子苷、芍药苷、甘草酸、阿魏酸、木通苯乙醇苷B、盐酸小檗碱、川芎嗪的对照品适量,分别配制成质量浓度为99、250、117 μg·mL-1、120、244、219、230、125 μg·mL-1的储备液;取各储备液适量,置于同一10 mL量瓶中,用甲醇稀释制成含京尼平龙胆双糖苷9.9 μg·mL-1,栀子苷25 μg·mL-1,芍药苷5.85 μg·mL-1,甘草酸6 μg·mL-1,阿魏酸4.88 μg·mL-1,木通苯乙醇苷B 4.38 μg·mL-1,盐酸小檗碱4.6 μg·mL-1,川芎嗪3.125 μg·mL-1的混合溶液,即得。
2.2 供试品溶液的制备取妇科分清丸内容物1.0 g,精密称定,置具塞锥形瓶中,精密加50%甲醇50 mL,密塞,称量,超声(250 W,40 kHz)处理30 min,放冷,再称量,用50%甲醇补足减失的量,摇匀,经0.45 μm微孔滤膜过滤,即得。
2.3 阴性样品溶液的制备按处方制备缺栀子,缺白芍,缺甘草,缺当归和川芎,缺木通,缺黄连以及缺川芎的阴性样品,分别按“2.2”项方法制备各阴性样品溶液。
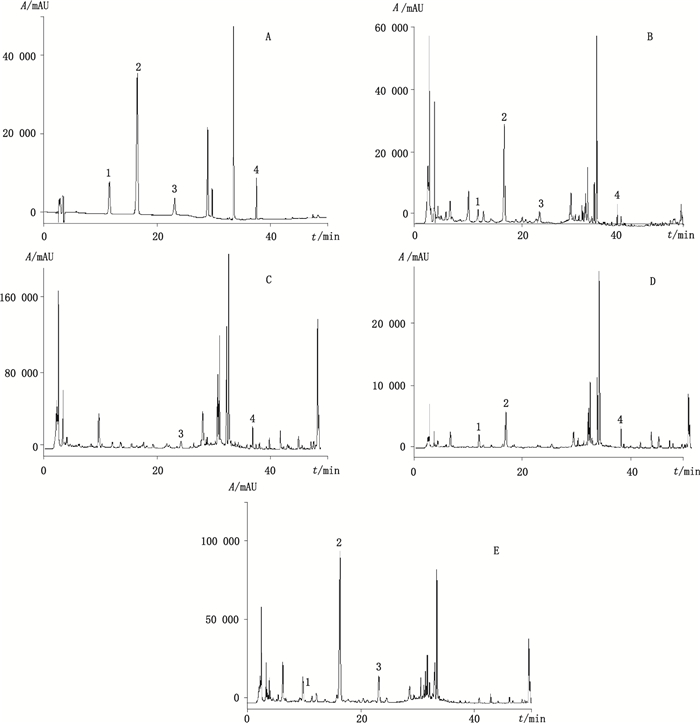
2.4 色谱条件色谱柱:DIKMA Platisil ODS C18色谱柱(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱(0~20 min,10%A→16%A;20~30 min,16%A→40%A;30~50 min,40%A→80%A);流速:1 mL·min-1;柱温:30 ℃;检测波长:240 nm(京尼平龙胆双糖苷、栀子苷、芍药苷、甘草酸),327 nm(阿魏酸、木通苯乙醇苷B、小檗碱),295 nm(川芎嗪);进样量:20 μL。在上述色谱条件下,各待测组分分离度均大于1.5,理论塔板数均大于5 000。混合对照品溶液、样品溶液及各阴性样品溶液色谱图见图 1~3。
|
1.京尼平龙胆双糖苷(genipin 1-gentiobioside) 2.栀子苷(geniposide) 3.芍药苷(peoniflorin) 4.甘草酸(glycyrrhizic acid) 图 1 混合对照品(A)、样品(B)、缺栀子的阴性样品(C)、缺白芍的阴性样品(D)及缺甘草的阴性样品(E)在240 nm处色谱图 Figure 1 HPLC chromatograms of mixed reference substances(A), sample(B), negative sample without Gardeniae Fructus(C), negative sample without Paeoniae Radix Alba(D), negative sample without Glycyrrhizae Radix et Rhizoma(E)at 240 nm |
|
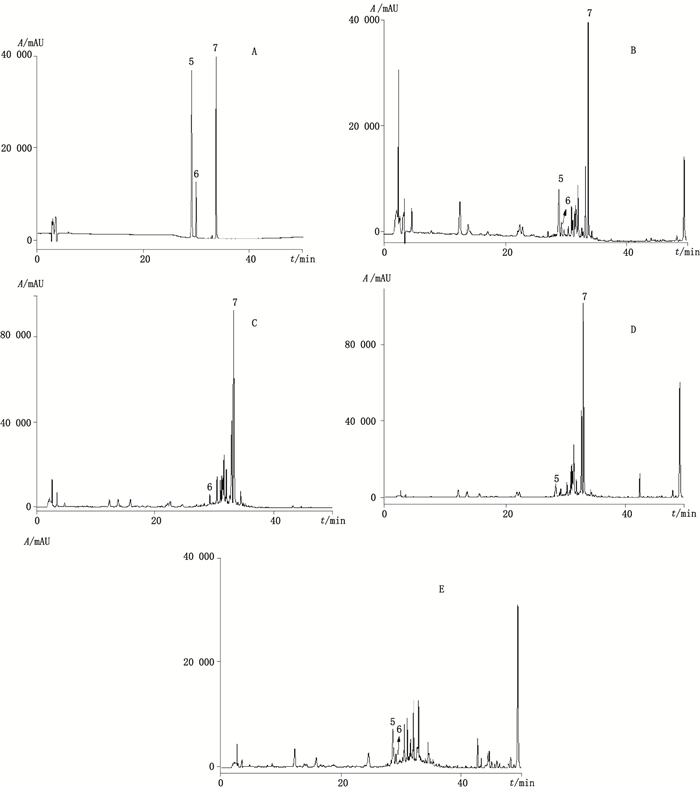
5.阿魏酸(ferulic acid) 6.木通苯乙醇苷B(calceolarioside B) 7.小檗碱(berberine) 图 2 混合对照品(A)、样品(B)、缺当归、川芎的阴性样品(C)、缺木通的阴性样品(D)、缺黄连的阴性样品(E)在327 nm处色谱图 Figure 2 HPLC chromatograms of mixed reference substances(A), sample(B), negative sample without Chinese Angelicae Sinensis Radix and Chuanxiong Rhizoma(C), negative sample without Akebiae Caulis(D), negative sample without Coptidis Rhizoma(E)at 327 nm |
|
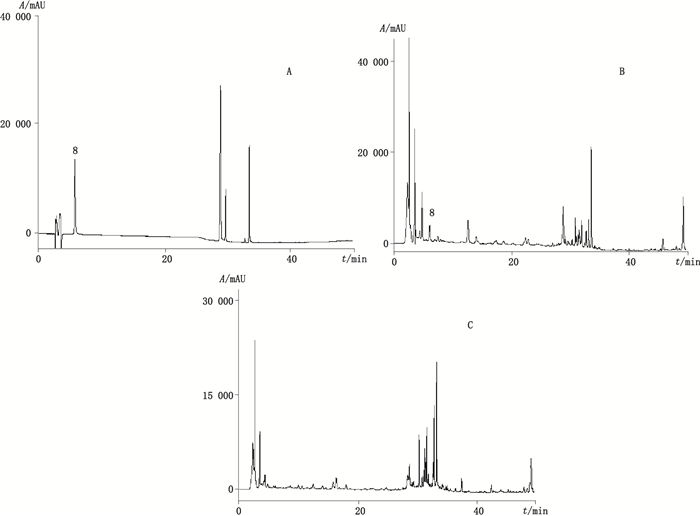
8.川芎嗪(ligustrazine) 图 3 混合对照品(A)、样品(B)、缺川芎的阴性样品(C)在295 nm处色谱图 Figure 3 HPLC chromatograms of mixed reference substances(A), sample(B)and negative sample without Chuanxiong Rhizoma(C)at 295 nm |
精密吸取混合对照品溶液5、10、15、20、25、30 μL,分别进样测定,以峰面积(Y)为纵坐标,进样量(X)为横坐标进行线性回归,得京尼平龙胆双糖苷、栀子苷、芍药苷、甘草酸、阿魏酸、木通苯乙醇苷B、小檗碱、川芎嗪的线性回归方程见表 1。
|
|
表 1 回归方程、相关系数(r)及线性方范围 Table 1 Regression equations, correlation coefficients (r) and linear ranges |
取混合对照品溶液,按“2.4”项下色谱条件连续进样6次,测得京尼平龙胆双糖苷、栀子苷、芍药苷、甘草酸、阿魏酸、木通苯乙醇苷B、小檗碱、川芎嗪峰面积的RSD(n=6) 分别为0.25%、0.36%、0.48%、0.65%、0.62%、0.55%、0.41%、0.75%。
2.7 稳定性试验取同一供试品溶液(样品批号140805),室温放置,分别于0、2、4、6、12、24 h进行测定,测得京尼平龙胆双糖苷、栀子苷、芍药苷、甘草酸、阿魏酸、木通苯乙醇苷B、小檗碱、川芎嗪峰面积的RSD(n=6) 分别为0.64%、0.71%、0.84%、0.65%、0.92%、1.1%、0.98%、1.0%,表明供试品溶液在常温下24 h内稳定。
2.8 重复性试验取妇科分清丸样品(批号140805),按“2.2”项下方法平行制备6份供试品溶液,以“2.4”项下色谱条件进行测定,得京尼平龙胆双糖苷、栀子苷、芍药苷、甘草酸、阿魏酸、木通苯乙醇苷B、小檗碱、川芎嗪的平均含量(n=6) 分别为0.130、0.589、0.163、0.135、0.044、0.059、0.170、0.048 mg·g-1,RSD分别为0.67%、0.92%、1.0%、1.1%、1.2%、0.85%、1.2%。
2.9 加样回收率称取已知含量样品(批号140805) 约0.5 g,共9份,精密称定,平均分为3组,按低、中、高浓度(0.8倍、1倍、1.2倍)分别加入一定量的京尼平龙胆双糖苷、栀子苷、芍药苷、甘草酸、阿魏酸、木通苯乙醇苷B、盐酸小檗碱、川芎嗪的对照品,按照“2.2”项下方法制备供试溶液,进样20 μL进行测定,结果见表 2。
|
|
表 2 妇科分清丸中8种成分的加样回收率 Table 2 Results of recovery test for the eight compounds of Fuke Fenqing pills |
取3批样品,每批样品取3份各1.0 g,按“2.2”项下方法制备供试品溶液,按“2.4”项下条件进行分析,外标法计算各组分含量,结果见表 3。
|
|
表 3 妇科分清丸中8个成分的测定(mg·g-1,n=3) Table 3 Determination of eight components in Fuke Fenqing pills |
妇科分清丸相关文献较少,在流动相的选择上,笔者考察了乙腈-磷酸水[8-10]、甲醇-磷酸水2个溶剂系统[11-15],结果发现等度洗脱时,由于测定的成分较多,各个组分分离不理想,因此采用梯度洗脱,应用甲醇-磷酸水为流动相时,京尼平龙胆双糖苷、栀子苷和川芎嗪出峰时间较快,分离效果不好。采用乙腈-磷酸水为流动相时,前期水相占比较高,保证前3种组分分离,后期调高有机相比例减少分析时间。
3.2 检测波长的选择波长扫描得到京尼平龙胆双糖苷和栀子苷最大吸收波长为240 nm,240 nm虽然不是芍药苷、甘草酸的最大吸收波长,但是在此波长下,其附近杂质峰较少,出峰比较理想,符合实验要求,所以选择在240 nm下测定京尼平龙胆双糖苷、栀子苷、芍药苷、甘草酸这4个组分。波长扫描得到阿魏酸、木通苯乙醇苷B、小檗碱最大吸收波长分别为321、330、263 nm;小檗碱由于其在制剂中含量相对较高,采用327 nm作为测定波长能够达到方法学考察的要求,所以阿魏酸、木通苯乙醇苷B、小檗碱在327 nm同一波长下进行测定。
3.3 总结首先,在样品的处理上,中国药典并没有给出相应的操作方法,也没有进行含量的测定,作者根据药典中单味药材中有效成分的处理方法,进行了供试品的处理;其次,妇科分清丸最早收录于1977年版中国药典,说明此药应用历史很早,范围较广,但是直到2015年版中国药典,也未对其中成分的含量做要求,这样就使得其药品质量不易控制,中药是多种成分相辅相成及协同作用,各种潜在活性成分的含量与临床治疗效果密切相关,而本实验测定了妇科分清丸中7种药材的8种活性成分,涵盖了其组方中的大部分药材,对提高此种药物质量控制具有重要的意义。
| [1] |
中国药典2015年版. 一部[S]. 2015: 905 ChP 2015. Vol Ⅰ[S]. 2015:905 |
| [2] |
苏超, 刘君怡, 张盛, 等. RP-HPLC法测定妇科分清丸中栀子苷和芍药苷的含量[J]. 光明中医, 2015, 30(5): 956. SU C, LIU JY, ZHANG S, et al. Determination of geniposide and peoniflorin in Fuke Fenqing pills by RP-HPLC[J]. Guangming J Chin Med, 2015, 30(5): 956. |
| [3] |
李中娥. HPLC法同时测定妇科分清丸中阿魏酸和芍药苷[J]. 中成药, 2012, 34(3): 487. LI ZE. Determination of ferulic acid and paeoniflorin in Fuke Fenqing pills by HPLC[J]. Chin Tradit Pat Med, 2012, 34(3): 487. |
| [4] |
武婕, 张晓雪, 余河水, 等. 妇科分清丸的质量标准研究[J]. 辽宁中医药大学学报, 2016, 18(9): 38. WU J, ZHANG XX, YU HS, et al. Quality standards of Fuke Fenqing pills[J]. J Liaoning Univ Tradit Chin Med, 2016, 18(9): 38. |
| [5] |
张艳, 李海龙, 王虎平, 等. 阿魏酸对人胃癌MGC-803细胞增殖的影响[J]. 中国中医药信息杂志, 2016, 23(9): 70. ZHANG Y, LI HL, WANG HP, et al. Effects of ferulic acid on gastric cancer cell line MGC-803 proliferation[J]. Chin J Inf TCM, 2016, 23(9): 70. |
| [6] |
王晓庆, 刘建春, 田倩倩, 等. 芍药苷对细胞免疫调节作用的研究进展[J]. 中华中医药学刊, 2016, 34(6): 1306. WANG XQ, LIU JC, TIAN QQ, et al. Research development of cellular immune regulation of paeoniflorin[J]. Chin Arch Tradit Chin Med, 2016, 34(6): 1306. |
| [7] |
KIM J, KIM HY, LEE SM. Protective effects of geniposide and genipin against hepatic ischemia/reperfusion injury in mice[J]. Biomol Ther, 2013, 21(2): 132. DOI:10.4062/biomolther.2013.005 |
| [8] |
李珂, 余哲旻, 杨铭. HPLC法测定清胃合剂中盐酸小檗碱和黄芩苷的含量[J]. 中国临床药学杂志, 2015, 24(3): 181. LI K, YU ZM, YANG M. HPLC for simultaneous determination of berberine hydrochloride and Baicalin in Qinwei liquor[J]. Chin J Clin Pharm, 2015, 24(3): 181. |
| [9] |
周赛妮, 刘明平, 文艺, 等. HPLC同时测定川芎-天麻药对中4种指标性成分的含量[J]. 中国实验方剂学杂志, 2016, 22(3): 53. ZHOU SN, LIU MP, WEN Y, et al. Simultaneous determination of four index components in extracts of Ligusticum chuanxiongGastrodia elata by HPLC[J]. Chin J Exp Tradit Med Form, 2016, 22(3): 53. |
| [10] |
涂星, 唐洪梅, 柴玉娜, 等. 反相高效液相色谱法测定肠激安胶囊中芍药苷、盐酸小檗碱和盐酸巴马汀含量[J]. 药物分析杂志, 2015, 35(1): 115. TU X, TANG HM, CHAI YN, et al. Determination of paeoniflorin, berberine hydrochloride and palmatine hydrochloride in Changji'an capsules by RP-HPLC[J]. Chin J Pharm Anal, 2015, 35(1): 115. |
| [11] |
张宏梅, 崔佰吉, 姚鑫, 等. HPLC同时测定茵山莲颗粒中5个有效成分的含量[J]. 中国实验方剂学杂志, 2015, 21(24): 57. ZHANG HM, CUI BJ, YAO X, et al. Simultaneous determination of contents of five components in Yinshanlian granules by HPLC[J]. Chin J Exp Tradit Med Form, 2015, 21(24): 57. |
| [12] |
刘桂联, 吴康郁, 袁伟彬, 等. HPLC法同时测定温性经筋通贴膏中3种成分的含量[J]. 中药材, 2015, 38(9): 1977. LIU GL, WU KY, YUAN WB, et al. Simultaneous determination of three compounds in Wenxing Jingjintong by HPLC[J]. J Chin Med Mater, 2015, 38(9): 1977. |
| [13] |
郭东晓, 林林, 汪冰, 等. HPLC波长切换法同时测定抗感颗粒中7个成分的含量[J]. 药物分析杂志, 2015, 35(10): 1796. GUO DX, LIN L, WANG B, et al. Simultaneous determination of the content of seven components in Kanggan granules by HPLC wavelength switching technology[J]. Chin J Pharm Anal, 2015, 35(10): 1796. |
| [14] |
龙厚宁, 印酬, 孟小夏, 等. HPLC同时测定炎热清软胶囊中栀子苷黄芩苷和汉黄芩苷的含量[J]. 中国实验方剂学杂志, 2016, 22(6): 34. LONG HN, YIN C, MENG XX, et al. Simultaneous detemination of geniposide, baicalin and wogonoside inYanreqing soft capsules by HPLC[J]. Chin J Exp Tradit Med Form, 2016, 22(6): 34. |
| [15] |
夏忠庭, 鲍丽颖, 惠婷婷, 等. HPLC同时测定郁舒片中5种成分的含量[J]. 中国实验方剂学杂志, 2015, 21(3): 47. XIA ZT, BAO LY, HUI TT, et al. Simultaneous determination of five components in Yushu tablets by HPLC[J]. Chin J Exp Tradit Med Form, 2015, 21(3): 47. |
 2017, Vol. 37
2017, Vol. 37 
