2. 新疆医科大学中心实验室, 乌鲁木齐 830011
2. The Central Laboratory of Xinjiang Medical University, Urumqi 830011, China
硫酸氢氯吡格雷是用于心肌梗死、缺血性卒中或确诊外周动脉性疾病的患者及急性冠脉综合征-非ST段抬高性急性冠脉综合征患者的溶栓药[1-2]。目前国内外测定硫酸氢氯吡格雷含量的主要方法有高效液相色谱法[3-4]和萃取荧光法[5]。高效液相色谱法操作复杂,对样品要求高,样品前处理烦琐;萃取荧光法则有使用具有毒性的有机萃取剂等缺点。
本研究建立使用可调激光光纤传感技术联微顺序注射-阀上实验室(MicroSIA Lab-on-valve,μSIA-LOV)荧光反猝灭法测定硫酸氢氯吡格雷含量。激光光源是20世纪60年代的新光源,与氘灯、氙灯光源相比,可调激光光源具有方向性好,光信号强,单色性好,不需要对样品进行预处理,具有较高的灵敏度,不需要复杂的样品制备,属于绿色分析技术,不污染环境[6]。
微顺序注射-阀上实验室是第3代流动注射分析技术,在该分析系统中,所有的单元操作,如样品稀释,试剂试样的加入、混合以及多种联用技术的结合,使得整个实验测定过程能够可控、高效地进行[7-9]。该系统能将试剂及样品消耗降低至微升级水平,减少了试剂的使用量,适用于长时间检测和比较昂贵的试剂分析。阀上实验室系统不仅可以与光纤传感结合[10],也可以灵活与电化学[11]、色谱[12]、化学发光[13]、固相萃取[14]、原子荧光[15]等方法联用。
本研究将可调激光光源光纤传感技术与μSIA-LOV相结合,以光纤作为传导介质,将光纤光谱仪、微顺序注射分析仪和激光光源连接,用计算机控制,利用该系统与光纤传感的实时监测相连,可以实现样品在线监测。该方法与高效液相色谱法、萃取荧光法相比,对硫酸氢氯吡格雷片含量测定具有操作简单易行和连续快速测定的优势。经过课题组前期研究发现,激光光强度等于氙灯发出光的2~3倍。
1 实验部分 1.1 仪器、试剂与样品 1.1.1 仪器微量顺序注射仪(FIAlab Instruments公司),QE65000荧光光谱仪(海洋光学公司),AG135电子天平(梅特勒托利多公司),C9860A超声仪(CBL Photoelectron Tecnology公司),0.45 μm分注器过滤器(易购安北京科技有限公司),可调激光光源(Fianium公司),FIA-P200-SR光纤(海洋光学公司),QP600-2-UV-VIS光纤(海洋公司)。
1.1.2 试药罗丹明B(分析纯,北京朝阳西会化工厂,批号871226),四苯硼钠(分析纯,上海试剂一厂,批号80-G2-10),盐酸(优级纯,四川西陇化工有限公司,批号160106),99.9%的硫酸氢氯吡格雷对照品(中国食品药品检定研究院,批号100819-201102),实验用水为超纯水。
1.1.3 样品硫酸氢氯吡格雷片。样品1:赛诺菲(杭州)制药有限公司,规格为每片75 mg;样品2:深圳信立泰药业股份有限公司,规格为每片25 mg;样品3:乐普药业股份有限公司,规格为每片25 mg;样品4:乐普药业股份有限公司,规格为每片75 mg。
1.2 溶液的配制罗丹明B储备液:准确称取罗丹明B 23.95 mg于洁净烧杯中,加入超纯水溶解并定容至50 mL量瓶中,配制成1 000 μmol·L-1罗丹明B储备液,使用时稀释至8 μmol·L-1。
四苯硼钠储备液:准确称取四苯硼钠17.1 mg,加超纯水溶解并稀释定容至50 mL,配制成1 000 μmol·L-1四苯硼钠储备液,使用时稀释至20 μmol·L-1。
硫酸氢氯吡格雷对照品储备液:准确称取硫酸氢氯吡格雷对照品10.48 mg,加入超纯水溶解并稀释定容至25 mL,配制成1 000 μmol·L-1的硫酸氢氯吡格雷对照品储备液。使用时稀释至所需浓度。
盐酸:精密量取12 mol·L-1的浓盐酸1.00 mL至100 mL量瓶中,加入超纯水定容至刻度,配制成0.1 mol·L-1的稀盐酸。
氢氧化钠溶液:准确称取氢氧化钠4 g,加入超纯水溶解并稀释定容至100 mL,配制成0.1 mol·L-1的氢氧化钠溶液。
供试品溶液:取标示量为75 mg·片-1和25 mg·片-1的硫酸氢氯吡格雷片10片,研碎混匀后,分别称取250 mg和85 mg硫酸氢氯吡格雷的药粉(相当于总重量的十分之一)于烧杯中,加超纯水溶解搅拌并转移至100 mL和50 mL容量瓶中,用超纯水定容至刻度,过滤,取过滤液为待测储备液。使用时加超纯水稀释至10 μmol·L-1。
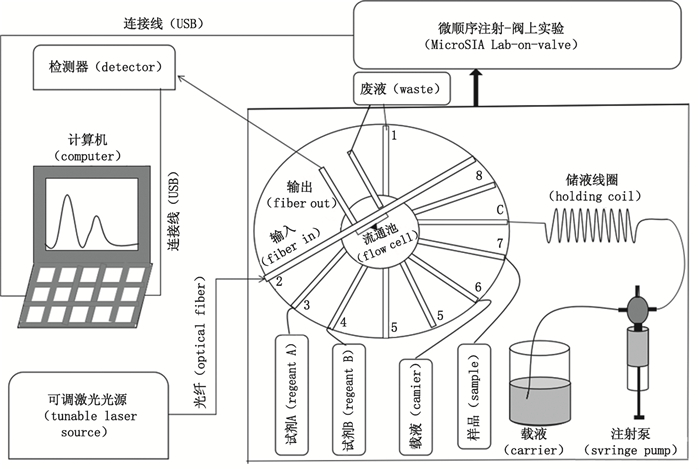
1.3 实验装置可调激光光源有专用的传输光纤(QP600-2-UV-VIS光纤,图 1右下),不同于荧光传输光纤;而图 1左中可调激光光源与流通池(2号通道)的连接需要用荧光传输光纤,因此把激光专用光纤采用特制针头(图 1右上,内置毛细管)和固定配件(图 1右中),改制成适合荧光传输的光纤(图 1右下)。实验发现,光的亮度强,实验结果良好,改制并激光诱导荧光成功。

|
图 1 实验装置图 Figure 1 Experimental apparatus figure |
实验流路如图 2所示。在注射泵的驱动下,首先由多位阀的3号口以50 μL·s-1的速度吸入罗丹明B(8 μmol·L-1)溶液50 μL,以50 μL·s-1由7号口吸入适量样品溶液,4号口以50 μL·s-1的速度先后从中心通道吸入四苯硼钠(20 μmol·L-1)溶液50 μL,再通过6号口以50 μL·s-1吸入100 μL载液(超纯水)。在注射泵的驱动下,被吸入的载液推动试剂和样品迅速混合,形成混合区带,并充分反应,然后再反向以20 μL·s-1的流速将混合区带从连接有光纤的多功能流通池流出,通过光纤光谱仪读取反应后的溶液荧光强度。每次测定结束后,用超纯水以200 μL·s-1流速冲洗整个流路。
|
图 2 实验流路图[7] Figure 2 The flow diagram |
由FIAlab for Windows软件进行八通阀控制及程序的编译和自动完成;SpectraSuite软件通过光纤光谱仪进行控制并采集光谱图;通过Fiaium AOTF Controller软件对可调激光光源进行控制。
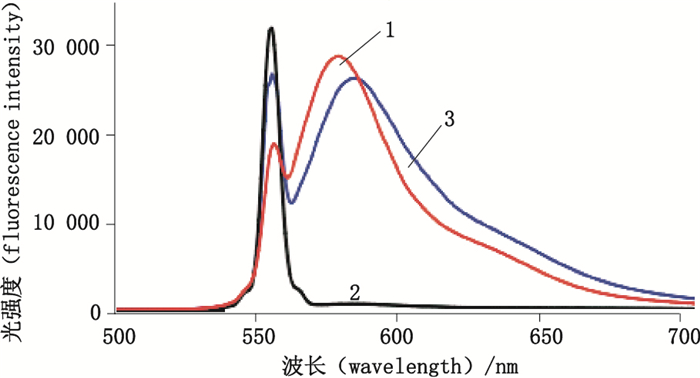
2 结果与讨论 2.1 不同溶液组合对荧光强度的影响硫酸氢氯吡格雷和四苯硼钠本身并无荧光,而罗丹明B能产生较强的荧光,其最大激发和发射波长(λex、λem)分别位于554 nm和578 nm处。罗丹明B的浓度定为8 μmol·L-1,向其中加入四苯硼钠溶液,使罗丹明B发生明显的荧光猝灭现象,而硫酸氢氯吡格雷对四苯硼钠-罗丹明B体系具有明显的荧光反猝灭作用,如图 3所示。随着溶液中硫酸氢氯吡格雷的浓度增加,荧光反猝灭作用增强,具有良好的线性关系。本研究正是利用这个原理对硫酸氢氯吡格雷进行定量测定。样品溶液的加入,使罗丹明B的最大发射峰发生了红移(从λem=578 nm至λem=582 nm),这可认为是由溶剂效应引起的。由于罗丹明B电子激发态比基态的极性大,随着溶剂极性的增加,荧光发射逐渐向驰豫态发射过渡。因此,随着溶剂极性的增加,λem发生红移。加入硫酸氢氯吡格雷(样品用盐酸调pH,盐酸属于强极性溶液)后使溶剂极性增加,这就解释了色谱图中,加入硫酸氢氯吡格雷溶液后,检测出罗丹明B的荧光发射波长发生红移的现象。
|
1.罗丹明B(rhodamine B) 2.罗丹明B+四苯硼钠(rhodamine B and sodium tetraphenylboron) 3.罗丹明B+四苯硼钠+硫酸氢氯吡格雷(rhodamine B,sodium tetraphenylboron and clopidogrel) 图 3 不同溶液的荧光光谱 Figure 3 The fluorescence spectra in different solution |
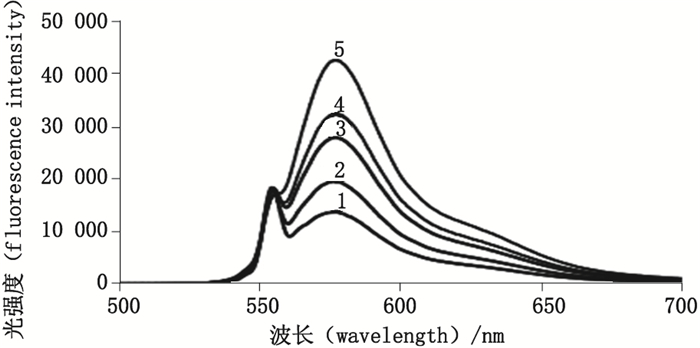
考察不同罗丹明B浓度(4、6、8、10、12 μmol·L-1)的影响,由于μSIA-LOV为封闭的管道系统,管径较小,若罗丹明B浓度太大,则会吸附在管道内,不易清洗,影响测定效率;若浓度太小,会影响测定灵敏度,故本实验选择罗丹明B浓度为8 μmol·L-1。溶液体积越大,混合程度越低,为了确保充分混合,反应完全,选择罗丹明B溶液体积为50 μL。见图 4。
|
1. 4 μmol·L-1 2. 6 μmol·L-1 3. 8 μmol·L-1 4. 10 μmol·L-1 5. 12 μmol·L-1 图 4 罗丹明B浓度的考察 Figure 4 Investigation of rhodamine B concentration |
荧光猝灭原理:罗丹明B本身具有较强荧光,在水溶液中离解出Cl-后带一正电荷,四苯硼钠在水溶液中离解出Na+后带一负电荷,两者1:1缔合,生成了一个没有荧光的新物质而改变了罗丹明B分子中的蒽醌π键的电子分布,使罗丹明B发生荧光猝灭。
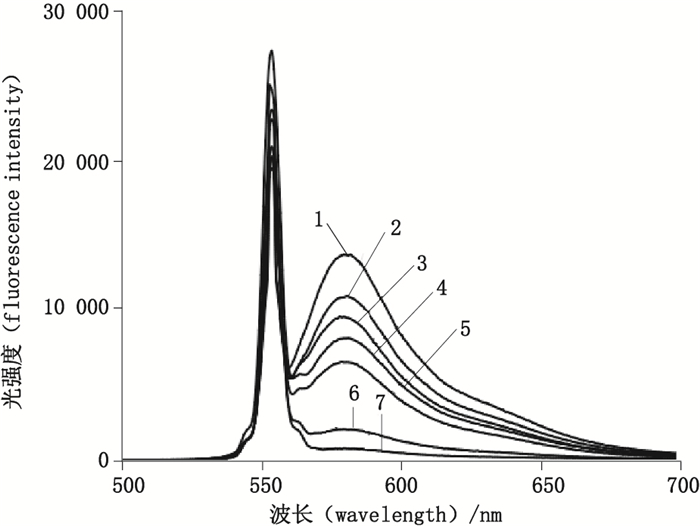
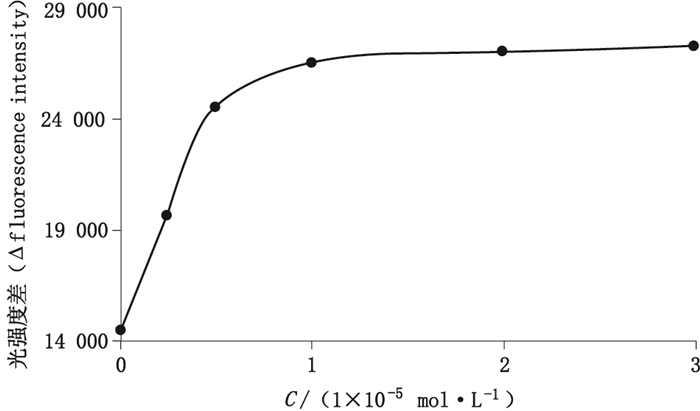
按照实验方法,设定罗丹明B体积为50 μL(8 μmol·L-1),储备溶液稀释分别准备0.1~30 μmol·L-1的7份不同浓度四苯硼钠溶液,分别测定荧光猝灭后荧光强度,其荧光猝灭效果随四苯硼钠浓度增加而增加,当四苯硼钠浓度增加到20 μmol·L-1后,ΔF值并无明显变化,因此选为最佳浓度。结果见图 5~7。
|
1. 0 μmol·L-1 2. 0.1 μmol·L-1 3. 1 μmol·L-1 4. 2.5 μmol·L-1 5. 6 μmol·L-1 6. 20 μmol·L-1 7. 30 μmol·L-1 图 5 四苯硼酸钠浓度对体系荧光强度的影响光谱图 Figure 5 The effect of different sodium tetraphenylborate concentration on the fluorescence intensity |
|
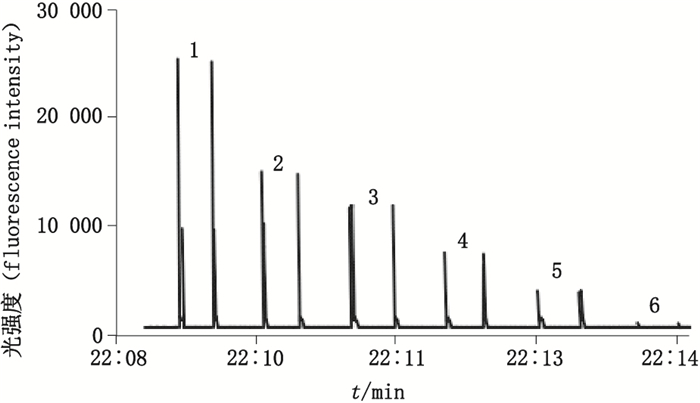
1. 0 μmol·L-1 2. 0.1 μmol·L-1 3. 1 μmol·L-1 4. 2.5 μmol·L-1 5. 6 μmol·L-1 6. 20 μmol·L-1 图 6 四苯硼酸钠浓度对体系荧光强度的影响时序图 Figure 6 The time sequence diagram of the effect of different sodium tetraphenylborate on the fluorescence intensity |
|
图 7 四苯硼酸钠的浓度对体系荧光强度的影响曲线图 Figure 7 The effect of different sodium tetraphenylborate on the fluorescence intensity |
硫酸氢氯吡格雷结构含有1个叔氮和1个硫酸基,易溶于水,在水中溶解后,解离出H+离子与叔氮相结合,形成带正电荷的质子化叔胺离子,可以与四苯硼钠阴离子形成高稳定的疏水性离子缔合物。加入盐酸使硫酸氢氯吡格雷分子质子化更完全,反猝灭更明显,使方法灵敏度更高。
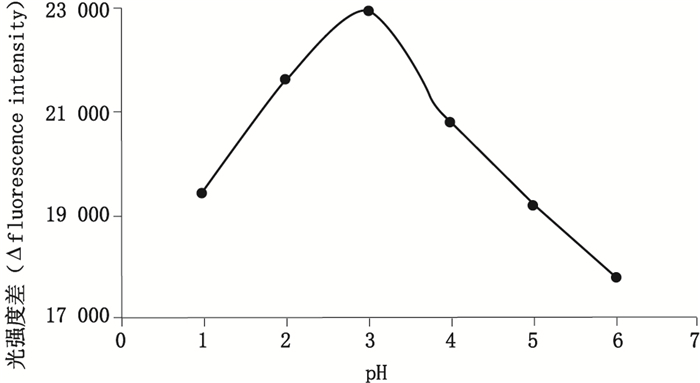
在50 μL罗丹明B(8 μmol·L-1)和50 μL四苯硼钠(20 μmol·L-1)的条件下,10 mL硫酸氢氯吡格雷对照品溶液(20 μmol·L-1)中加入0.1 mol·L-1的盐酸或氢氧化钠溶液,分别配制7份pH在1~6范围的溶液,测定相同浓度不同pH时硫酸氢氯吡格雷溶液反猝灭后荧光强度。结果发现,随着pH增加测量值ΔF逐渐增大:当pH=3时,ΔF值最大并稳定,较适于四苯硼钠和硫酸氢氯吡格雷的缔合。而pH>3时ΔF值开始下降。溶液的pH调到3时,荧光强度最大,因此选择pH为3的溶液。结果见图 8、9。
|
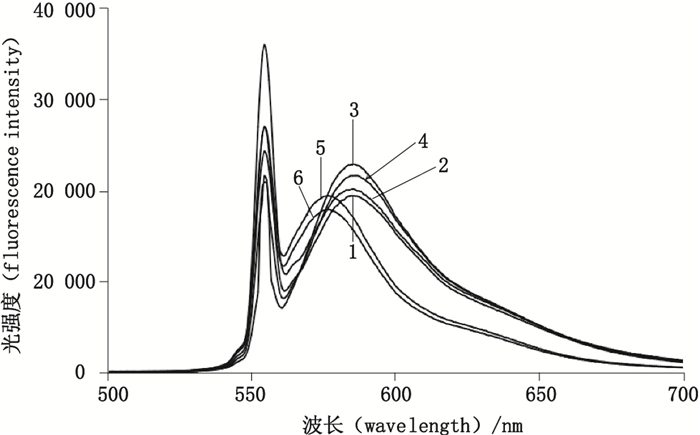
1. pH=1 2. pH=2 3. pH=3 4. pH=4 5. pH=5 6. pH=6 图 8 pH对体系荧光强度的影响光谱图 Figure 8 The effect of different pH values on the fluorescence intensity |
|
图 9 pH对体系荧光强度的影响曲线图 Figure 9 The effect of different pH values on the fluorescence intensity |
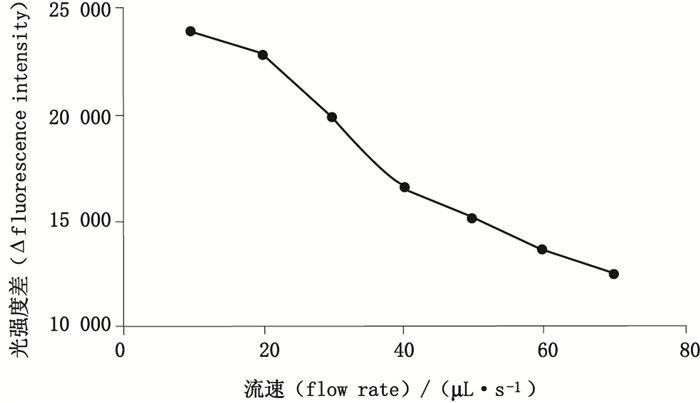
在50 μL罗丹明B(8 μmol·L-1),50 μL四苯硼钠(20 μmol·L-1)和50 μL硫酸氢氯吡格雷对照品溶液(20 μmol·L-1,pH=3) 的条件下,在10~70 μL·s-1范围内考察进样流速,测定相应的荧光强度,见图 10。流速太小,影响进样量(分析频率为40样·h-1);流速太大,影响ΔF。因此,流速与进样量之间需做调整。根据图 10所示,选20 μL·s-1为最佳流速。
|
图 10 流速对体系荧光强度的影响曲线图 Figure 10 The effect of different flow rate on fluorescence intensity |
根据IUPAC建议,罗丹明B+四苯硼钠作为空白连续进样10次,其噪音平均值为4 194。根据检出下限的荧光强度为3倍噪音值,将其值带入线性方程,得检出下限0.067 μmol·L-1。
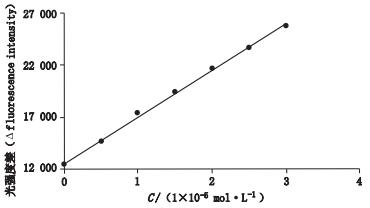
按照前面优化的实验条件,50 μL罗丹明B(8 μmol·L-1)、50 μL四苯硼钠(20 μmol·L-1)、50 μL硫酸氢氯吡格雷对照品溶液(0.1、5、10、15、20、25、30 μmol·L-1,pH=3),以20 μL·s-1的流速准确吸入,测定一系列溶液反应体系,同时也测定空白溶液,按照实验方法测出ΔF值,以浓度为横坐标,ΔF值为纵坐标,进行线性回归,得到的回归方程:
| $ \Delta \mathit{F}\rm{=4}\ \rm{471}\rm{.7}\mathit{C}\rm{+12}\ \rm{552}\ \ \ \mathit{r}\rm{=0}\rm{.998}\ \rm{4} $ |
线性范围为0.7~28.2 μmol·L-1。结果见图 11。
|
图 11 硫酸氢氯吡格雷片标准曲线 Figure 11 The standard curve of clopidogrel hydrogen sulfate |
取2号样品7份,分别按“1.2”项下方法配制供试品溶液,按照上述已优化的实验条件测定,结果含量平均值为9.5 μmol·L-1,RSD为3.9%。
3.3 精密度试验取10 μmol·L-1的对照品溶液按照上述已优化的实验条件,进行7次测定考察精密度,含量平均值为9.8 μmol·L-1,RSD为1.5%。说明本方法精密度良好。
3.4 加样回收率试验应用本方法对市场上购买的不同厂家硫酸氢氯吡格雷片进行了加样回收率试验。按照实验方法,在已选定的实验条件下测定已配制的样品的溶液与空白的ΔF值,将测得的ΔF值带入回归方程求出样品中药物含量,平行进行3次。所有样品配制成10 μmol·L-1的浓度,取样5 mL至10 mL量瓶中(每个样品3份),分别加入适量硫酸氢氯吡格雷对照品溶液准备低、中、高浓度的测定体系(用样品溶液滴定至刻度)进行加样回收率试验,结果见表 1。
|
|
表 1 样品加样回收率测定结果 Table 1 Results of sample recovery |
取4个厂家的样品制备供试品溶液,按本文确定的方法进行测定,通过回归方程计算含量,结果见表 2。
|
|
表 2 样品药物含量测定结果(n=3) Table 2 Results of determination of drug content in sample |
本文建立了可调激光光源光联微顺序注射-阀上实验室荧光反猝灭法测定硫酸氢氯吡格雷的含量。本方法与激光光纤传感技术相结合可实现硫酸氢氯吡格雷的在线监测,经过改制光纤激光诱导荧光而提高灵敏度。该法专属性强,操作简便,不需要复杂的样品预处理,不需要复杂的样品制备,属于绿色分析技术,不污染环境。将本法用于硫酸氢氯吡格雷片中硫酸氢氯吡格雷的测定,线性范围宽,检测限低,RSD均小于3%,加标回收率在93.0%~99.5%之间,结果令人满意。
| [1] |
朱海彦, 孙杰, 张曼红. 硫酸氢氯吡格雷的临床应用进展[J]. 齐鲁药事, 2010, 29(11): 674. ZHU HY, SUN J, ZHANG MH. Recent development of clinical utility of cblopidogrel bisulfate[J]. Qilu Pharm Aff, 2010, 29(11): 674. |
| [2] |
陈红梅, 徐开联, 付延导. 硫酸氢氯吡格雷治疗不稳定型心绞痛的临床究[J]. 当代医学, 2012, 18(16): 151. CHEN HM, XU KL, FU YD. Clinical effect of clopidogrel bisulfate treatment of unstable angina[J]. Contemp Med, 2012, 18(16): 151. DOI:10.3969/j.issn.1009-4393.2012.16.111 |
| [3] |
吕洁, 孟祥军, 王凤秋. 高效液相色谱法测定硫酸氢氯吡格雷的含量[J]. 中国医药导报, 2011, 8(9): 60. LÜ J, MENG XJ, WANG FQ. Content determination of clopidogrel hydrogen sulfate by HPLC[J]. China Med Her, 2011, 8(9): 60. |
| [4] |
郭旭光, 郭海波. 高效液相法测定硫酸氢氯败格雷片的含量[J]. 海峡药学, 2012, 24(5): 50. GUO XG, GUO HB. Determination of the content of clopidogrel hydrogen sulfate in clopidogrel hydrogen sulfate tablets by HPLC[J]. Strait Pharm J, 2012, 24(5): 50. |
| [5] |
练伟芹, 龚爱琴, 王露, 等. 萃取荧光法测定药物及体液中硫酸氢氯吡格雷含量[J]. 光谱学与光谱分析, 2014, 34(11): 3030. LIAN WQ, GONG AQ, WANG L, et al. Determination of clopidogrel hydrogen sulfate in drug and body fluid by fluorescence extraction[J]. Spectrosc Spect Anal, 2014, 34(11): 3030. DOI:10.3964/j.issn.1000-0593(2014)11-3030-04 |
| [6] |
阿依姑再丽·斯马依, 尔西丁·买买提, 艾尔肯·依不拉音, 等. 可调激光-光纤传感快速检测药品中盐酸小檗碱和维生素B2的含量[J]. 新疆医科大学学报, 2016, 39(10): 1307. ISMAYIL A, MAIMAITI E, IBURAYIM A, et al. Rapid determination of berberine hydrochloride and vitamin B2 in pharmaceuticals by tunable laser optical fiber sensor[J]. J Xinjiang Med Univ, 2016, 39(10): 1307. |
| [7] |
侯俊峰, 关明, 李新霞. 基于荧光素汞荧光法结合光纤传感-微顺序注射-阀上实验室测定肠灌流液中H2S[J]. 分析化学, 2015, 43(1): 132. HOU JF, GUAN M, LI XX. Based on mercury fluorescein fluorescence combined with optical fiber sensing-determination of intestinal laboratory sequential injection valve-micro perfusion with H2S[J]. Chin J Anal Chem, 2015, 43(1): 132. |
| [8] |
过治军. 顺序注射分析及其在药物和食品分析中的应用[D]. 新乡: 河南师范大学, 2005 GUO ZJ. Sequential Injection Analysis and Its Application in Pharmaceutical and Food Analysis[D].Xinxiang:Henan Normal University, 2005 http://d.wanfangdata.com.cn/Thesis/Y885399 |
| [9] |
陈旭伟, 范世华. 顺序注射分析的新进展[J]. 冶金分析, 2004, 24(2): 23. CHEN XW, FAN SH. Development of sequential injection analysis[J]. Metall Anal, 2004, 24(2): 23. |
| [10] |
章立华, 艾尼娃尔·艾克木, 艾尔肯·依不拉音. 流动注射-光纤化学传感荧光法测定维生素B2的含量[J]. 应用化工, 2014, 43(11): 2014. ZHANG LH, AIKEMU A, YIBULAYIN A. Determination of VB2 tablets using fiber optic chemical sensor fluorescence and flow injection[J]. Appl Chem Ind, 2014, 43(11): 2014. |
| [11] |
刘在青. 顺序注射阀上实验室电化学联用技术在痕量镉分析中的应用[D]. 扬州: 扬州大学, 2010 LIU ZQ. Application of Laboratory Electrochemical Technique in the Analysis of Trace Cadmium in Sequential Injection Valve[D]. Yangzhou:Yangzhou University, 2010 http://d.wanfangdata.com.cn/Thesis/Y885399 |
| [12] |
刘贵花, 韩德满, 梁华定, 等. 流动注射在线预富集-高效液相色谱法测定水产品中4种磺胺类药[J]. 分析化学, 2012, 40(3): 432. LIU GH, HAN DM, LIANG HD, et al. Determination of 4 kinds of drugs in aquatic products by flow injection on-line preconcentration and high performance liquid chromatography[J]. Chin J Anal Chem, 2012, 40(3): 432. |
| [13] |
赵叙. 顺序注射-阀上实验室-化学发光法同步检测ATP和ROS[D]. 大连: 辽宁师范大学, 2013 ZHAO X. Simultaneous Determination of ATP and ROS by Employing Sequential Injection Analysis Lab-on-valve Chemiluminescence Technique[D]. Dalian:Liaoning Normal University, 2013 http://cdmd.cnki.com.cn/Article/CDMD-10165-1014138378.htm |
| [14] |
牛超, 陈央央, 何慧清, 等. 流动注射-固相萃取-光度法测定环境水样中的Cr(Ⅵ)[J]. 绍兴文理学院学报, 2012, 32(7): 57. NIU C, CHEN YY, HE HQ, et al. Determination of flow injectionsolid phase extraction spectrophotometry of Cr(Ⅵ)[J]. J Shaoxing Univ, 2012, 32(7): 57. |
| [15] |
崔健, 赵学玒, 汪嚥, 等. 流动注射-氢化物发生-原子荧光光谱仪数学模型优化研究[J]. 光谱学与光谱分析, 2014, 34(1): 246. CUI J, ZHAO XH, WANG Y, et al. Optimization of mathematical model of flow injection hydride generation atomic fluorescence spectrometer[J]. Spectrosc Spectral Anal, 2014, 34(1): 246. |
 2017, Vol. 37
2017, Vol. 37 
