利胆排石片自1995年开始收载于历版中国药典一部。该方由金钱草、黄芩、郁金、槟榔、芒硝、茵陈、木香、大黄、麸炒枳实、姜厚朴共计10味药组成,功能清热利湿、利胆排石,用于湿热蕴毒、腑气不通所致的胁痛、胆胀,症见胁肋胀痛、发热、尿黄、大便不通;胆囊炎、胆石症见上述证候者[1]。利胆排石片疗效确切,是常用中成药,全国共有批准文号102个,生产企业97家。相较于众多的生产厂家,现行法定标准中国药典2015年版一部中仅有黄芩苷的含量限值,在质量控制中尚显不足。目前单独测定利胆排石片中某一类成分的研究已有报道[2-3],但由于中成药复方的药味较多,化学成分复杂,只采用单一或者少数几个指标成分进行质量评价,不能全面反映其内在质量。为了有效地控制该方的成药质量,保证临床疗效,本实验选取了方中5味主要药材——茵陈(绿原酸)、枳实(柚皮苷、橙皮苷、新橙皮苷)、黄芩(黄芩苷、汉黄芩苷、黄芩素、汉黄芩素)、大黄(芦荟大黄素、大黄酸、大黄素、大黄酚)、木香(木香烃内酯、去氢木香内酯),采用HPLC法同时进行定量分析,可以高效、准确地为控制该复方制剂的质量提供依据。
1 仪器与试药 1.1 仪器安捷伦科技有限公司Agilent 1260型液相色谱仪(配置四元泵,二极管阵列检测器DAD);岛津公司Phenomenex Luna 5u-C18色谱柱(4.6 mm×250 mm,5 µm;填料:十八烷基硅烷键合硅胶);METTLER公司AE240十万分之一电子分析天平;济宁科技超声电子有限责任公司GT-350W型ASS150超声波提取器;江苏省金坛市医疗仪器厂HH-S数显恒温水浴锅。
1.2 试药对照品绿原酸(批号110753-201415,含量96.2%)、柚皮苷(批号110722-201312,含量94.7%)、橙皮苷(批号110721-201316,含量95.3%)、新橙皮苷(批号111857-201102,含量99.66%)、黄芩苷(批号110715-201318,含量93.3%)、黄芩素(批号111595-201306,含量97.8%)、芦荟大黄素(批号110795-201308,含量97.8%)、大黄酸(批号110757-200206)、汉黄芩素(批号111514-200403)、大黄素(批号110756-200110)、木香烃内酯(批号111524-201209,含量98.4%)、去氢木香内酯(批号111524-201208,含量99.5%)、大黄酚(批号110796-200615,含量99.6%)均购自中国食品药品检定研究院,含量测定用;汉黄芩苷(批号20051214,含量>99%)购自上海友思生物技术有限公司;乙腈为色谱纯,水为超纯水,其余试剂为分析纯。
利胆排石片10批,分别为上海医药集团青岛国风药业股份有限公司(批号150203、150304、150501)、天津同仁堂集团股份有限公司(批号FP08001、FP08003、FP08002)、葵花药业集团(伊春)有限公司(批号20130903、20140502、20140808)和广西万寿堂药业有限公司(批号150101)产品。
2 方法与结果 2.1 混合对照品溶液的制备分别取待测成分的对照品适量,精密称定,加甲醇溶解并稀释,制成质量浓度为绿原酸46.71 µg·mL-1、柚皮苷285.60 µg·mL-1、橙皮苷139.36 µg·mL-1、新橙皮苷145.22 µg·mL-1、黄芩苷92.94 µg·mL-1、汉黄芩苷87.49 µg·mL-1、黄芩素56.98 µg·mL-1、芦荟大黄素23.67 µg·mL-1、大黄酸41.52 µg·mL-1、汉黄芩素57.90 µg·mL-1、大黄素31.75 µg·mL-1、木香烃内酯89.14 µg·mL-1、去氢木香内酯74.38 µg·mL-1、大黄酚81.26 µg·mL-1的混合对照品溶液,冷藏(4 ℃),备用。
2.2 供试品溶液的制备取利胆排石片10片,除去包衣,精密称量,求得平均片重,研细,精密称取0.5 g,置具塞锥形瓶中,精密加入甲醇25 mL,超声处理(功率250 W,频率40 kHz)30 min,放冷,再称量,用甲醇补足减失的量,滤过,取续滤液,以0.45 µm微孔滤膜滤过,即得。
2.3 阴性样品溶液的制备按工艺方法制备缺少茵陈、枳实、黄芩、大黄及木香的阴性样品,并按“2.2”项下的方法,制得阴性样品溶液。
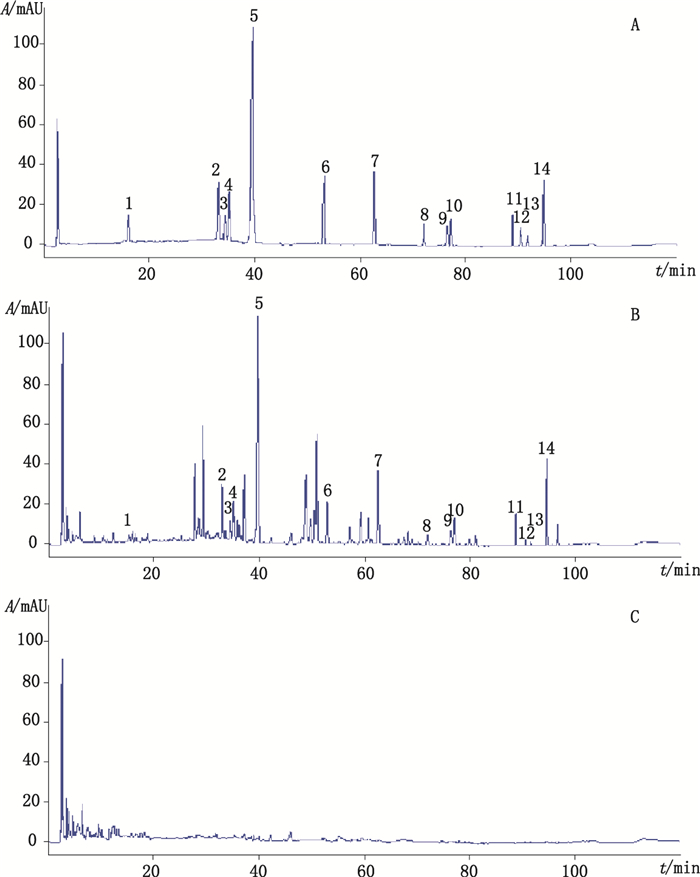
2.4 色谱条件采用Phenomenex Luna 5u-C18色谱柱(4.6 mm×250 mm,5 µm),以乙腈(A)-0.5%磷酸水溶液(B)为流动相,梯度洗脱(0~24 min,4%A→18%A,96%B→82%B;24~31 min,18%A→23%A,82%B→77%B;31~41 min,23%A,77%B;41~65 min,23%A→35%A,77%B→65%B;65~80 min,35%A→45%A,65%B→55%B;80~100 min,45%A→100%A,55%B→0%B),流速1 mL·min-1,柱温30 ℃,检测波长254 nm,进样量10 µL。色谱图见图 1。
|
1.绿原酸(chlorogenic acid)2.柚皮苷(naringin)3.橙皮苷(hesperidin)4.新橙皮苷(neohesperidin)5.黄芩苷(baicalin)6.汉黄芩苷(wogonoside)7.黄芩素(baicalein)8.芦荟大黄素(aloeemodin)9.大黄酸(rhein)10.汉黄芩素(wogonin)11.大黄素(emodin)12.木香烃内酯(costunolide)13.去氢木香内酯(dehydrocostus lactone)14.大黄酚(chrysophanol) 图 1 混合对照品(A)、利胆排石片样品(B)与阴性样品(C)HPLC色谱图 Figure 1 HPLC chromatograms of mixed reference substances(A), sample of Lidanpaishi tablets(B)and negative sample without the corresponding Chinese herbal medicines(C) |
分别精密吸取“2.1”项下混合对照品溶液0.5、1、2、5、10 µL,依次注入液相色谱仪,按“2.4”项色谱条件进行测定,记录色谱图。分别以绿原酸、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷、黄芩素、芦荟大黄素、大黄酸、汉黄芩素、大黄素、木香烃内酯、去氢木香内酯、大黄酚的进样量(µg)为横坐标,相应的峰面积为纵坐标绘制标准曲线,计算回归方程,结果见表 1。实验结果表明,14个成分均有较好的线性关系。
|
|
表 1 14个成分的标准曲线方程、相关系数和线性范围 Table 1 Regression equations, correlation cofficients, and linear ranges of fourteen constituents |
分别精密吸取混合对照品溶液10 µL,按“2.4”项色谱条件连续进样6次,结果绿原酸、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷、黄芩素、芦荟大黄素、大黄酸、汉黄芩素、大黄素、木香烃内酯、去氢木香内酯、大黄酚峰面积的RSD分别为0.7%、1.0%、0.7%、0.9%、0.4%、0.5%、0.5%、0.6%、0.8%、1.1%、0.9%、0.9%、0.8%、1.2%,表明精密度良好。
2.7 稳定性试验取同一供试品溶液,室温下放置,按“2.4”项下色谱条件分别在0、2、8、12、24 h依法进样测定,测得供试品溶液中绿原酸、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷、黄芩素、芦荟大黄素、大黄酸、汉黄芩素、大黄素、木香烃内酯、去氢木香内酯、大黄酚峰面积的RSD分别为1.1%、0.9%、1.2%、1.2%、0.5%、0.8%、1.0%、1.1%、0.6%、0.9%、0.8%、0.9%、1.0%、1.3%,表明供试品溶液在24 h内稳定。
2.8 重复性试验取同一批利胆排石片(批号FP08003)样品6份,每份0.5 g,分别精密称定,按“2.2”项下方法制得供试品溶液,按“2.4”项色谱条件进行测定并计算待测成分的含量。结果绿原酸、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷、黄芩素、芦荟大黄素、大黄酸、汉黄芩素、大黄素、木香烃内酯、去氢木香内酯、大黄酚的含量平均值分别为0.18、0.69、0.43、1.39、2.95、0.32、0.97、0.25、0.19、0.43、0.36、0.12、0.14、0.39 mg·片-1,RSD依次为1.0%、1.3%、1.1%、1.4%、0.5%、0.8%、0.9%、0.5%、0.8%、1.0%、1.2%、0.9%、1.1%、1.4%,表明本方法重复性良好。
2.9 加样回收率试验取“2.8”项已测知含量的利胆排石片(批号FP08003)0.25 g,精密称定,置具塞锥形瓶中,精密加入质量浓度依次为16.59、64.21、56.61、155.67、264.04、33.08、104.06、23.67、21.12、57.90、28.72、11.00、12.88、31.63 µg·mL-1的绿原酸、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷、黄芩素、芦荟大黄素、大黄酸、汉黄芩素、大黄素、木香烃内酯、去氢木香内酯、大黄酚混合对照品溶液5 mL及甲醇20 mL,按“2.2”项下方法操作,平行制备6份加样供试溶液,按“2.4”项色谱条件进行测定,计算回收率,结果见表 2。
|
|
表 2 14个成分的回收率试验结果 Table 2 Recoveries of fourteen constituents |
取不同厂家的10批利胆排石片,分别按“2.2”项下方法制得供试品溶液,按“2.4”项色谱条件进行测定,依照“2.5”项回归方程计算各成分的含量,结果见表 3。
|
|
表 3 样品含量测定结果(mg·片-1,n=6) Table 3 Assay results of samples |
实验中分别选取了超声、回流、索氏提取3种提取方法进行考察,结果表明,超声提取效率与回流提取相仿,且简便快捷,故实验选用超声提取法制备供试品溶液。同时对比了15、30、45 min超声提取时间,表明超声提取30 min即可取得较为满意的提取效果。对提取溶剂(甲醇、50%甲醇水溶液和乙醇)进行优选,发现,甲醇提取样品中各检测组分总含量优于乙醇提取,且杂质明显少于50%甲醇水溶液提取,因此选择甲醇作为该样品的提取溶剂。
3.2 波长的选择为了实现绿原酸、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷、黄芩素、芦荟大黄素、大黄酸、汉黄芩素、大黄素、木香烃内酯、去氢木香内酯和大黄酚的同时测定,实验中利用DAD扫描结果,结合色谱峰数量和峰强度综合考虑,对200~400 nm波段范围内的HPLC图谱进行分析。结果发现,在254 nm波长条件下,HPLC图谱中的色谱峰个数和峰强度均较为理想,故选择254 nm作为检测波长。
3.3 流动相的考察对不同流动相的组成比例进行考察[4-5],采用不同比例的甲醇-水系统、甲醇-磷酸水系统、乙腈-水系统、乙腈-磷酸水系统,发现在流动相中加入一定比例的酸有助于提高待测定成分与干扰峰的分离度,改善峰形,经过进一步考察,确定利用由乙腈-0.5%磷酸水溶液组成的流动相系统进行梯度洗脱,即可达到较好的基线分离,获得理想的色谱图。
3.4 不同生产厂家的影响本文考察了4个生产厂家生产的10个批号利胆排石片中绿原酸、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷、黄芩素、芦荟大黄素、大黄酸、汉黄芩素、大黄素、木香烃内酯、去氢木香内酯和大黄酚的含量。由表 3可知:不同厂家生产的利胆排石片中各成分含量有所差异,其中柚皮苷和新橙皮苷的含量差异明显,最高和最低含量相差超过24倍;而各厂家生产的制剂中绿原酸、橙皮苷、黄芩苷、汉黄芩苷、黄芩素、芦荟大黄素、大黄酸、汉黄芩素、大黄素、木香烃内酯、去氢木香内酯和大黄酚虽有差异,但不是很显著,其中黄芩苷的含量均不小于2.8 mg·片-1。不同厂家生产的利胆排石片各类化合物含量存在一定程度的差异,可能是由于药品生产工艺差别、原药材的产地不同、采收期不同等原因引起的。
3.5 其他HPLC图谱中君药金钱草的主峰均较小,故未对其设置检验项目[6]。该中药制剂中茵陈占总处方量的22.7%,是该方的君药,但在现行检验标准中无检测项目,而茵陈药材本身有绵茵陈和花茵陈之分,含量测定指标不同,分别为绿原酸(绵茵陈)、滨蒿内酯(花茵陈),通过反复实验均未能检测到滨蒿内酯,这与传统上习惯采用绵茵陈投料相一致[7-8]。枳实虽为利胆排石片处方组成中的臣药,用量较少,但却是复方中的贵重药材,对制剂的质量影响较大[9]。文献报道,黄芩的主要有效部位是黄酮类化合物,本实验选取黄芩苷、汉黄芩苷、黄芩素、汉黄芩素作为制剂中黄芩药材的质控指标[10-11]。处方中臣药大黄具有泻下攻积,清热泻火,凉血解毒,逐瘀通径,利湿退黄之功效,是泻火、破积、行瘀的要药,临床用于实热积滞便秘,目赤咽肿,淤血经闭,湿热痢疾等症。主要活性成分为蒽醌类化合物,但近年有研究发现该类成分具有潜在的肝肾毒性和致癌性[12-13]。木香行气止痛,特征成分木香烃内酯、去氢木香内酯在HPLC色谱图中可清晰分辨[14]。厚朴的特征成分厚朴酚与和厚朴酚经姜汁炮制、提取后含量降低,未能在成药的液相图谱中检出;槟榔、郁金和芒硝在该色谱条件下未发现特征成分峰。
基于中药成方的复杂性,中成药的质量控制的特点要求必须采取多指标和综合量化的手段控制中成药质量的稳定性和有效性。本实验建立了高效液相法同时测定利胆排石片中绿原酸、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷、黄芩素、芦荟大黄素、大黄酸、汉黄芩素、大黄素、木香烃内酯、去氢木香内酯、大黄酚的方法。该方法前处理条件简便、快速,所建立的梯度洗脱方法灵敏,分离度良好,测定结果稳定可靠、重复性好,实用性强,实现了从多成分、系统化角度控制利胆排石片的质量,适用于利胆排石片的产品质量控制分析。
| [1] |
中国药典2015年版. 一部[S]. 2015: 970 ChP 2015.Vol Ⅰ[S]. 2015:970 |
| [2] |
刘意, 曹演威, 何洋. HPLC法同时测定利胆排石片中4种蒽醌类成分的含量[J]. 海峡药学, 2009, 21(2): 35. LIU Y, CAO YW, HE Y. Simultaneous determination of four anthraquinones in Lidanpaishi tablet by HPLC[J]. Strait Pharm J, 2009, 21(2): 35. |
| [3] |
韩旭, 许丽娜, 王丽, 等. HPLC法测定利胆排石片中5种黄酮苷的含量[J]. 药物分析杂志, 2009, 29(6): 1036. HAN X, XU LN, WANG L, et al. HPLC simultaneous determination of five flavonoid glycosides in Lidanpaishi tablets[J]. Chin J Pharm Anal, 2009, 29(6): 1036. |
| [4] |
吕萍, 张娜娜, 张振巍. 清热解毒口服液HPLC指纹图谱及4种主要成分的含量分析[J]. 中国实验方剂学杂志, 2013, 19(2): 98. LÜ P, ZHANG NN, ZHANG ZW. Analysis of HPLC fingerprints of Qingrejiedu oral liquid and content of four main factors[J]. Chin J Exp Tradit Med Form, 2013, 19(2): 98. |
| [5] |
杨跃华, 胡春丽, 张洪霞. RP-HPLC法同时测定利胆排石片中5种有效成分的含量[J]. 沈阳药科大学学报, 2012, 29(5): 373. YANG YH, HU CL, ZHANG HX. Simultaneous determination of five effective components in cholagogic and lithagogue tablets by RP-HPLC[J]. J Shenyang Pharm Univ, 2012, 29(5): 373. |
| [6] |
郭林林, 赵德, 邓君. 金钱草药材的HPLC指纹图谱研究[J]. 中药材, 2012, 35(3): 382. GUO LL, ZHAO D, DENG J. Study on HPLC fingerprint of herba Lysimachiae[J]. J Chin Med Mater, 2012, 35(3): 382. |
| [7] |
文志云, 路国寿. 清热解毒颗粒中绿原酸的含量测定[J]. 医学文选, 2005, 24(6): 892. WEN ZY, LU GS. Determination of chlorogenic acid in Lidanpaishi tablets[J]. Anthol Med, 2005, 24(6): 892. |
| [8] |
胡彦武, 关颖丽, 姚慧敏, 等. 野生绵茵陈和花茵陈中绿原酸含量的比较[J]. 中国实验方剂学杂志, 2011, 17(9): 78. HU YW, GUAN YL, YAO HM, et al. Comparison on chlorogenic acid content of Artemisia capillaries from different harvest time[J]. Chin J Exp Tradit Med Form, 2011, 17(9): 78. |
| [9] |
朱露, 雷鹏, 黄琪. 反相高效液相色谱法测定枳实中芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷的含量[J]. 中南药学, 2013, 11(12): 934. ZHU L, LEI P, HUANG Q. Determinition of narirutin, naringin, hesperidin and neohesperidin in Fructus Aurantii Immaturus by RPHPLC[J]. Cent South Pharm, 2013, 11(12): 934. DOI:10.7539/j.issn.1672-2981.2013.12.016 |
| [10] |
侯学智, 张振秋, 尤春雪. HPLC测定黄芩中6个成分的含量[J]. 中国现代应用药学, 2012, 29(11): 1010. HOU XZ, ZHANG ZQ, YOU CX. Determination of six constituents in Scutellaria baicalensis Georgi by HPLC[J]. Chin J Mod App Pharm, 2012, 29(11): 1010. |
| [11] |
赵亮, 王新霞, 吕磊. HPLC法测定清肝散结颗粒中黄芩苷、汉黄芩苷、野黄芪苷、黄芩素及汉黄芩素[J]. 中成药, 2014, 36(2): 313. ZHAO L, WANG XX, LÜ L. Determination of baicalin, wogonoside, scutellarin, baicalein and wogonin in Qinggan Sanjie granules by HPLC[J]. Chin Tradit Pat Med, 2014, 36(2): 313. |
| [12] |
秦云, 李祥, 陈建伟. 大黄中蒽醌类成分配伍前后的量变规律[J]. 中国实验方剂学杂志, 2010, 16(5): 94. QIN Y, LI X, CHEN JW. Content variation of anthraquinones in rhubarb before and after compatibilities[J]. Chin J Exp Tradit Med Form, 2010, 16(5): 94. |
| [13] |
National Toxicology Program(NTP). Toxicology and carcinogenesis studies of emodin feed studies in F344/N rats and B6C3F1 mice[J]. Natl Toxicol Program Tech Rep Ser, 2001, 493: 1. |
| [14] |
魏华, 彭勇, 马国需. 木香有效成分及药理作用研究进展[J]. 中草药, 2012, 43(3): 613. WEI H, PENG Y, MA GX. Advances in studies on active components of Saussurea lappa and their pharmacological actions[J]. Chin Tradit Herb Drugs, 2012, 43(3): 613. |
 2017, Vol. 37
2017, Vol. 37 