麦麸为禾本科植物小麦的种皮,性平,味甘、淡,具有和中益脾的功效[1]。明代陈嘉谟在《本草蒙荃》中提出“麸制抑酷性,勿伤上膈”的理论,《本草通玄》中也有“麦麸资本谷气“的记载,表明麦麸与药物共制能缓和药物的燥性,增强疗效,除去药物不快之气味[2]。蜜麸为麦麸和蜂蜜共制后的产物,麦麸经蜜制后作为辅料可增强共制药物的色泽和疗效,是中药炮制中常用的固体辅料[3]。目前对麸炒炮制原理的研究多集中在炮制前后药物本身和辅料麦麸成分的变化[4-6],而对整个麸炒过程中麦麸的成分变化未见报道。
白术始载于《神农本草经》,具有健脾益气,燥湿利水,止汗,安胎的功效[7]。目前,白术的炮制方法较多,以麸炒白术应用最广,白术麸炒后挥发油含量降低,但健脾止泻作用增强[8-10],有人提出麸炒白术“减酮增酯”的炮制原理[11-12],白术和蜜麸在麸炒过程中相互作用如何,值得深入研究。
本文以白术麸炒过程中不同麸炒时间点蜜麸为研究对象,采用静态顶空进样,GC-MS结合自动质谱退卷积定性系统(AMDIS)和Kováts保留指数(RI)的方法,对不同麸炒时间点蜜麸的挥发性成分的动态变化进行分析,为阐释麸炒白术炮制机理提供科学依据。
1 仪器与试药Agilent 7890 A GC气相色谱仪,HP-5MS 5%Phenyl Methyl Siloxane色谱柱(0.25 μm×30 m×0.25 mm;涂层材料:苯基甲基硅氧烷),Agilent 5975C MSD质谱仪,Agilent 7697 A HS顶空进样器,色谱数据处理系统(MSD Chemstation Data Analysis Applica-tion、AMDIS Chromatogam);NIST 11质谱数据库。380Lc型二维红外成像仪(DIAS公司),CY-900型炒药机(南京宏钢盛机械设备厂)。
正构烷烃混合对照品C7~C30(Sigma公司,编号49451-U)。
白术和辅料蜜麸由四川新荷花饮片公司提供。
2 方法 2.1 不同麸炒时间点蜜麸的制备不同麸炒时间点蜜麸由四川新荷花饮片公司进行炮制。炮制过程中采用二维红外成像仪检测炒药机的锅中温度,等温度达到280 ℃后时加入蜜麸,待冒烟时,迅速加入净白术80 kg,净白术与蜜麸投料比为10:1,在白术麸炒过程中每几分钟取样1次,每次取样(蜜麸和白术)约1 kg,为研究不同炮制时间点辅料蜜麸挥发性成分的变化,本次炮制炒至30 min,即麸炒白术已成焦黑状,取样结束,得到不同麸炒时间点蜜麸和白术样品。各取样时间点样品的外观性状、火候程度见表 1。
|
|
表 1 样品取样信息 Table 1 Sample information |
取不同麸炒时间点蜜麸粉末各0.5 g,精密称定,放入容量为20 mL的顶空进样瓶中,密封,置顶空进样器中进样。顶空进样参数:样品瓶加热温度120 ℃;样品环温度140 ℃;传输线温度160 ℃;样品瓶加热时间10 min;样品环平衡时间0.5 min;进样时间1 min。
2.3 GC-MS分析条件采用HP-5MS 5% Phenyl Methyl Siloxane (0.25 μm×30 m×0.25 mm)色谱柱,电离方式EI,离子源温度230 ℃,气化室温度260 ℃,接口温度270 ℃,程序升温(初始温度60 ℃,以每分钟20 ℃升温至140 ℃,保持5 min,再以每分钟4 ℃升温至240 ℃,最后以每分钟30 ℃升温至270 ℃),电子能量70 eV,扫描范围m/z 20~450。
2.4 Kováts保留指数RI的测定取正构烷烃C7~C30混合对照品,按照“2.2”和“2.3”项下条件分析。根据Van Den Dool与Kratz提出的公式[13]计算各待鉴定化合物的RI。RI=100(tx-tn)/(tn+1-tn),其中,tx为被分析组分的保留时间(min),tn、tn+1分别为碳原子数为n和n+1的正构烷烃的保留时间(min),且tn+1 > tx > tn。
3 结果GC-MS分析挥发油得到的原始TIC图谱中存在大量的重叠峰。AMDIS基于模型峰的算法,把形状与保留值完全相同的碎片峰重新组合,去除其他干扰峰,形成相对“纯净”的质谱图,从而准确对化合物进行定性[14-15]。
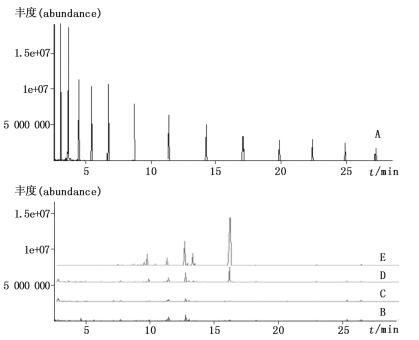
经GC-MS分析得到C7~C30混合对照品、蜜麸和白术挥发性成分的总离子流图,应用AMDIS对色谱峰纯化,再结合RI对化合物定性,面积归一化法对化合物定量,结果见图 1,表 2。
|
A. C7~C30混合对照品(C7~C30 mixed reference substances) B.蜜麸(bran) C.麸炒4min蜜麸(bran fried for 4 min) D.麸炒26 min蜜麸(bran fried for 26 min) E.净白术(Atractylodis Macrocephalae Rhizoma) 图 1 C7~C30混合对照品、蜜麸、白术挥发油GC-MS总离子流图 Figure 1 GC-MS total ion current(TIC)profiles of the volatile oil from C7~C30 mixed reference substances, bran and Atractylodis Macrocephalae Rhizoma |
|
|
表 2 蜜麸在麸炒过程中挥发性成分分析结果 Table 2 Analysis of volatile components from bran in the processing of Atractylodis Macrocephalae Rhizoma stir-fried with bran |
8个不同麸炒时间点蜜麸样品中共鉴定出49个化合物,分别占各自挥发油总量的96.41%、96.27%、98.01%、98.55%、97.95%、98.23%、98.27%、98.13%。蜜麸在麸炒过程中消失的的成分有7种,分别为糠醇、苯乙醛、2-乙酰基吡咯、芳樟醇、4-叔丁基苯丙酮、愈创木烯和N-甲基对甲苯磺酰胺;在麸炒过程中产生的新成分有14种,其中相对含量大于6.0%的成分有反式-2,4-庚二烯醛、壬醛、2-甲基3,5-二羟基-5,6-二氢-4H-吡喃-4-酮、5-羟甲基糠醛、石竹素、桉油烯醇和6-异丙烯基-4,8a-二甲基-1,2,3,5,6,7,8,8a-四氢-2-萘酚。
3.2 不同麸炒时间点蜜麸挥发性成分相对含量动态变化分析蜜麸生品中挥发性成分相对含量较高的化合物有糠醛(7.06%)、芳樟醇(4.45%)、8a-甲基-3,4,4a,5,8,8a-六氢-1(2H)-萘酮(4.20%)、γ-榄香烯(3.15%)、β-桉叶烯(14.57%)、α-杜松(17.21%)、7-乙炔基-1,4a-二甲基-4a,5,6,7,8,8a-六氢-2(1H)-萘酮(6.01%)、苍术酮(3.02%)等。在麸炒4~8 min时,这些成分的相对含量发生明显变化,之后变化较小,随麸炒时间延长至26~30 min,相对含量又发生明显变化。
4 结论与讨论 4.1 白术与蜜麸的相互吸附作用通过与白术麸炒过程中挥发性成分变化的比较发现,蜜麸在麸炒过程产生的新成分中,香树烯、(+)-瓦伦亚希、石竹素、桉油烯醇、(Z)-4-十六烯-6-炔和6-异丙烯基-4,8a-二甲基-1,2,3,5,6,7,8,8a-四氢-2-萘酚均来自白术中的挥发性成分;而白术在麸炒过程产生的新成分中,苯乙醛、2-乙酰基吡咯和6-(1,1-二甲基乙基)-3,4-二氢-1(2H)-萘酮均来自蜜麸中的挥发性成分,说明白术和蜜麸在麸炒过程中存在着相互吸附作用。
苍术酮具有燥性,为白术挥发油的主要成分,在麸炒过程中蜜麸大量吸附了白术中的苍术酮成分,这也许就是麸炒白术降低燥性,增强健脾止泻作用的主要原因,也符合麸炒白术“减酮增酯”的炮制原理。
分析发现,在麸炒4~8 min时蜜麸中挥发性成分在组成和含量上均发生明显变化,之后变化不明显,炒制20 min后,又出现明显变化,这可能是由于白术和蜜麸在开始炮制时立即发生相互吸附作用,导致成分在组成和含量上均发生明显变化,随麸炒时间延长,相互吸附作用逐渐达到饱和,而在炒制20 min以后,一些挥发性成分出现裂解或重组,导致成分再次发生明显变化,具体过程仍需进一步研究。白术和蜜麸在麸炒过程中挥发性成分的组成及其含量变化与白术不同饮片的功效变化及其药性改变密切相关,深入的研究尚需结合药效学以阐明麸炒白术的炮制机制。
4.2 AMDIS和RI的辅助定性保留时间为8.916 min的色谱峰,RI计算值为1 406,而NIST质谱库检索出最佳化合物的RI*为1231,匹配度高达87%,而匹配度为70%的的化合物八氢四甲基环戊并戊搭烯的RI*为1416,显然八氢四甲基环戊并戊搭烯为该色谱峰对应的化合物。保留时间为25.366min的色谱峰,经AMDIS提纯后对应的最佳匹配物是1-(4-甲氧基苯基)-4,6-二甲基-2(1H)-嘧啶酮,匹配率为73%,该点原始谱图对应的最佳匹配物还是1-(4-甲氧基苯基)-4,6-二甲基-2(1H)-嘧啶酮,但匹配率只有25%。可见,AMDIS和RI的应用可大大提高GC-MS定性的准确性。
| [1] |
贾天柱. 中药炮制学[M]. 上海: 上海科学技术出版社, 2008, 127. JIA TZ. The Processing of Chinese Materia Medica[M]. Shanhai: Shanghai Science and Technology Publishers, 2008, 127. |
| [2] |
孟莉, 陈缤, 贾天柱. 中药麸炒古今研究概述[J]. 中成药, 2006, 28(9): 1311. MENG L, CHEN B, JIA TZ. An overview of the study of ancient and modern Chinese medicine fried with bran[J]. Chin Tradit Pat Med, 2006, 28(9): 1311. |
| [3] |
吴慧, 单国顺, 赵文龙, 等. 不同麦麸对白术炮制品质量的影响[J]. 中国实验方剂学杂志, 2014, 20(6): 55. WU H, SHAN GS, ZHAO WL, et al. Effect of bran on the quality of processed products of Rhizoma Atractylodis Macrocephalae[J]. Chin J Exp Tradit Med Form, 2014, 20(6): 55. |
| [4] |
刘艳菊, 曾敏, 陈雯雯, 等. 气-质联用法分析苍术、麸炒苍术及其辅料麦麸的挥发性成分[J]. 中国医院药学杂志, 2012, 32(11): 847. LIU YJ, ZENG M, CHEN WW, et al. Analysis of volatile constituent of Rhizoma Atractylodis and processing product and auxiliary material by GC-MS[J]. Chin J Hosp Pharm, 2012, 32(11): 847. |
| [5] |
顾雪竹, 毛淑杰, 程立平, 等. 辅料麦麸炮制对枳壳成分的影响[J]. 中国实验方剂学杂志, 2008, 14(10): 26. GU XZ, MAO SJ, CHENG LP, et al. Effect of processing on the constituents of Fructus Aurantii bran accessories[J]. Chin J Exp Tradit Med Form, 2008, 14(10): 26. DOI:10.3969/j.issn.1005-9903.2008.10.011 |
| [6] |
陈鸿平, 刘友平, 刘承萍, 等. 不同土炒白术中白术内酯Ⅲ和白术多糖的含量比较[J]. 中国药房, 2010, 21(39): 3680. CHEN HP, LIU YP, LIU CP, et al. Content comparison of atractylenolide Ⅲ and soluble polysaccharide of Atractylodes macrocephala processed with different kinds of soils[J]. China Pharm, 2010, 21(39): 3680. |
| [7] |
中国药典2015年版. 一部[S]. 2015: 103. ChP 2015. Vol Ⅰ[S]. 2015:103 |
| [8] |
石晓, 黄艳萍. GC-MS分析白术炮制前后化学成分的变化[J]. 食品与药品, 2011, 13(1): 36. SHI X, HUANG YP. Analysis on the change of chemical compositions before and after Atractylodes macrocephala processing by GC-MS[J]. Food Drug, 2011, 13(1): 36. |
| [9] |
周爱珍, 程斌, 王和平. 炮制对白术的化学成分及药理作用的影响[J]. 中医药导报, 2010, 16(2): 79. ZHOU AZ, CHENG B, WANG HP. Effect of processing on the chemical composition and pharmacological effects of Atractylodes[J]. Guid J Tradit Chin Med Pharm, 2010, 16(2): 79. |
| [10] |
容穗华, 林海, 高妮. 白术炮制工艺及炮制原理的研究[J]. 中国中药杂志, 2011, 36(8): 1001. RONG SH, LIN H, GAO N. Study on processing technology and processing principles of Atractrylodis Macrocephalae Rhizoma[J]. China J Chin Mater Med, 2011, 36(8): 1001. |
| [11] |
郝延军. 白术的炮制原理研究[D]. 沈阳: 辽宁中医药大学, 2006. HAO YJ. Study on the Processing Principle of Atractylodes macrocephala[D]. Shenyang:Liaoning University of Traditional Chinese Medicine, 2006 http://cdmd.cnki.com.cn/Article/CDMD-10162-2006159168.htm |
| [12] |
赵文龙, 吴慧, 单国顺, 等. 麸炒白术"减酮减燥, 增酯增效"炮制理论的再印证[J]. 中国中药杂志, 2013, 38(20): 3493. ZHAO WL, WU H, SHAN GS, et al. Bran fried Atractylodes "reducing ketone ester dry, increase efficiency" verification of processing theory[J]. China J Chin Mater Med, 2013, 38(20): 3493. |
| [13] |
DOOL HVD, KRATZ PD. A generalization of the retention index system including linear temperature programmed gas-liquid partition chromatography[J]. J Chromatogr A, 1963, 11: 463. DOI:10.1016/S0021-9673(01)80947-X |
| [14] |
王坚, 陈鸿平, 刘友平, 等. 应用自动质谱退卷积定性系统拆分中药挥发油总离子流谱图中的重叠峰——以青皮为例[J]. 中国中药杂志, 2013, 38(10): 1564. WANG J, CHEN HP, LIU YP, et al. he application of automatic mass deconvolution qualitative system of volatile oil flow separation of the total ion spectrum of overlapping peaks in the green map as an example[J]. China J Chin Mater Med, 2013, 38(10): 1564. |
| [15] |
陈鸿平, 潘欢欢, 张鑫, 等. GC-MS结合AMDIS和保留指数研究不同炮制火候麸炒白术挥发性成分动态变化规律[J]. 中国中药杂志, 2016, 41(14): 2646. CHEN HP, PAN HH, ZHANG X, et al. GC-MS combined with AMDIS and Kofits retention index to investigate dynamic change rules of volatile components from Atractylodis Macrocephalae Rhizoma with different stir-baking degrees[J]. China J Chin Mater Med, 2016, 41(14): 2646. |
 2017, Vol. 37
2017, Vol. 37 
