2. 上海张江中药现代制剂技术工程研究中心, 上海 201203
2. Engineering Research Center of Modern Preparation Technology of Traditional Chinese Medicine of Zhangjiang Shanghai, Shanghai 201203, China
假马齿苋是玄参科匍匐草本植物假马齿苋Bacopa monnieri(L.)Wettst的全草,又名白花猪母菜;主要分布在台湾、福建、云南、广东等省区;其味微甘、淡,性寒,具有清热解毒、清肝明目的功效[1]。临床上还可用于治疗支气管炎、气喘等呼吸系统疾病[2]。主要含有三萜皂苷、苯乙醇苷、黄酮等成分[3]。研究表明假马齿苋对神经系统、血液循环系统、消化系统均有较好的补益作用,可以抗肿瘤、保护脑线粒体酶、保肝、松弛平滑肌等[4]。国外对其研究较多,焦点主要集中在具有促智活性三萜皂苷以及皂苷成分的神经药理活性上,其中的达玛烷型三萜皂苷,被认为可以通过调节一个合适的程度的先天免疫和吞噬作用,促进淀粉样蛋白减少,改善认知障碍,治疗阿尔兹海默症,已有相关制剂上市辅助治疗老年痴呆[5-8]。目前为止,假马齿苋在国内尚未被真正的开发利用,其多为野生,在质量控制方面的研究基础较薄弱,缺乏评价质量的成分研究。
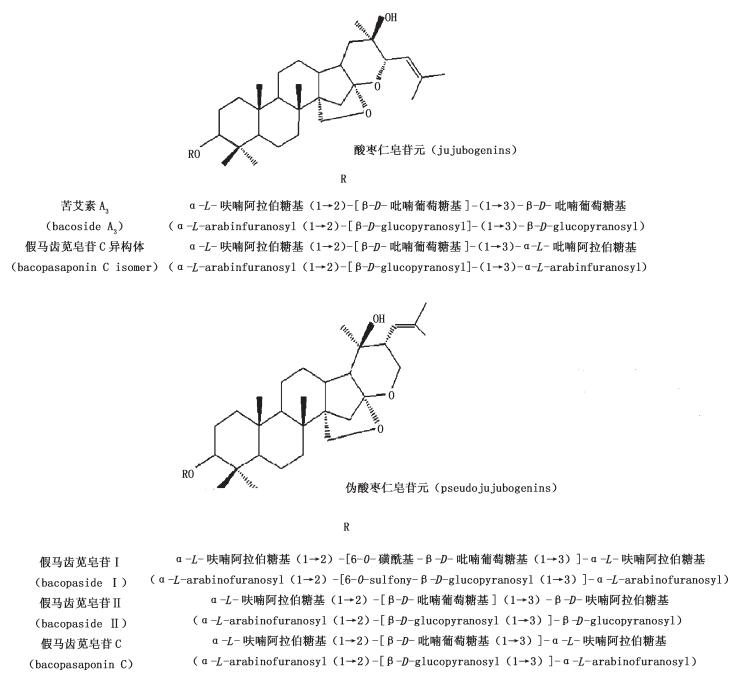
课题组前期发现假马齿苋中的原生皂苷主要有假马齿苋皂苷(bacopaside)Ⅰ和Ⅱ、苦艾素(bacoside)A3和假马齿苋皂苷(bacopasaponin)C以及假马齿苋皂苷C异构体(bacopasaponin C isomer),它们的化学结构见图 1。苷元以酸枣仁苷元(jujubogenin)或伪酸枣仁苷元(pseudojujubogenin)为主[9],本实验以此5个皂苷为指标,建立HPLC法同时测定这5个成分,并对福建漳州不同生长环境下栽培种植的假马齿苋进行测定和成分分析,为进一步完善其质量控制与品质评价提供依据,也将为该资源的综合利用提供参考。
|
中文注解 图 1 5个三萜皂苷的化学结构式 Figure 1 The chemical structure of five triterpenoid saponins |
Agilent 1200型高效液相色谱仪(四元泵、ALS、TCC、VWD和Chemstation工作站,Agilent公司),Agela公司Promsil C18色谱柱(4.6 mm×250 mm,5 μm;填料:十八烷基硅烷键合硅胶)。FA2104N型分析天平(0.1 mg,上海精密科学仪器有限公司),XP-205型分析天平(0.01 mg,梅特勒-托利多分析仪器有限公司)。
假马齿苋皂苷Ⅰ(bacopaside Ⅰ)对照品,批号ASB-00002002,纯度87.7%,购自上海迈瑞尔化学技术有限公司;苦艾素A3(bacoside A3)、假马齿苋皂苷Ⅱ(bacopasideⅡ)、假马齿苋皂苷C异构体(bacopasaponin C isomer)和假马齿苋皂苷C(bacopasaponin C)对照品为实验室自制,纯度分别为93.9%、92.9%、85.8%和93.3%。
无水乙醇、磷酸均为分析纯,乙腈为色谱纯。
采集10批假马齿苋(福建漳州各地),经第二军医大学药学院生药教研室张汉明教授鉴定为玄参科假马齿苋Bacopa monnieri,来源及采集地环境见表 1。
|
|
表 1 假马齿苋来源及采集地环境 Table 1 Habitats and environment of ten batches of Bacopa monnieri. |
Agela公司Promsil C18色谱柱(4.6 mm×250 mm,5 μm),流动相为乙腈-0.2%磷酸水溶液(氢氧化钠溶液调至pH 3.0)(32.5:67.5),流速1.0 mL·min-1,检测波长205 nm,柱温30 ℃,进样量10 μL。
2.2 混合对照品储备液的制备以甲醇制备假马齿苋皂苷Ⅰ 0.139 2 mg·mL-1、苦艾素A3 0.187 8 mg·mL-1、假马齿苋皂苷Ⅱ 0.148 6 mg·mL-1、假马齿苋皂苷C异构体0.171 6 mg·mL-1、假马齿苋皂苷C 0.130 6 mg·mL-1混合溶液,即得。
2.3 供试品溶液的制备精密称取剪碎的样品约0.5 g,加50%乙醇水溶液20 mL,称量,加热回流120 min,放冷,再称量,用50%乙醇水溶液补足减失的量,混匀,0.45 μm微孔滤膜滤过,取续滤液,即得。
2.4 方法学考察 2.4.1 线性关系考察取“2.2”项下各混合对照品储备液适量,以甲醇依次稀释成系列混合对照品溶液,分别吸取10 μL注入液相色谱仪,进行测定并记录,以各成分峰面积对对照品的进样质量(μg)进行线性回归,得到各对照品的回归方程和线性范围,见表 2。
|
|
表 2 5个化合物的线性关系 Table 2 Linearity of five triterpenoid saponins |
取同一供试品溶液(云霄船场村样品)10 μL,连续进样6次,结果假马齿苋皂苷Ⅰ、苦艾素A3、假马齿苋皂苷Ⅱ、假马齿苋皂苷C异构体和假马齿苋皂苷C峰面积的RSD分别为1.9%、0.7%、0.6%、0.5%和1.0%,表明本法日内精密度良好;取同一供试品溶液连续3 d每天进样2次,结果假马齿苋皂苷Ⅰ、苦艾素A3、假马齿苋皂苷Ⅱ、假马齿苋皂苷C异构体、假马齿苋皂苷C峰面积的RSD分别为2.8%、2.4%、1.9%、2.7%和2.5%,表明本法日间精密度良好[10]。
2.4.3 重复性试验取假马齿苋样品(产地3,云霄船场村)6份,精密称定,按“2.3”项下方法制备供试品溶液,按“2.1”项下条件进样分析;测得假马齿苋皂苷Ⅰ、苦艾素A3、假马齿苋皂苷Ⅱ、假马齿苋皂苷C异构体和假马齿苋皂苷C的平均含量分别为5.64、2.16、3.94、2.44和2.14 mg·g-1,RSD分别为0.5%、0.7%、0.6%、2.2%和0.5%,表明该方法重复性良好[11]。
2.4.4 稳定性试验取供试品溶液,分别于0、2、4、8、12和24 h进样10 μL进行测定;结果假马齿苋皂苷Ⅰ、苦艾素A3、假马齿苋皂苷Ⅱ、假马齿苋皂苷C异构体和假马齿苋皂苷C峰面积的RSD分别为1.7%、1.2%、1.4%、2.3%和2.1%,表明供试品溶液在制备后24 h内稳定。
2.4.5 加样回收率试验精密称取已知含量的假马齿苋样品(产地3)6份,每份0.25 g,精密加入各自对照溶液适量(相当于样品中各对照品原质量分数的100%)[12],按“2.3”项下方法制备供试溶液,进样测定并计算加样回收率,结果见表 3。
|
|
表 3 加样回收率试验结果(n=6) Table 3 Results of recovery tests |
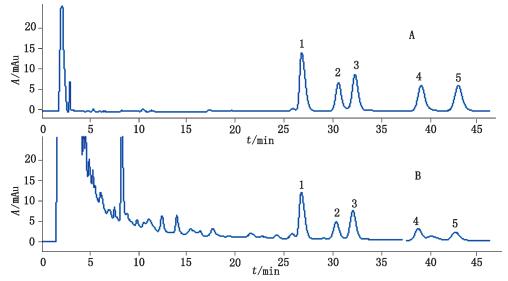
取10批假马齿苋样品,按“2.3”项下方法制备供试品溶液,精密吸取10 μL进样,HPLC分析测定,外标法计算含量,色谱图见图 2,测定结果见表 4。
|
1.假马齿苋皂苷Ⅰ(bacopaside Ⅰ)2.苦艾素A3(bacoside A3)3.假马齿苋皂苷Ⅱ(bacopasideⅡ)4.假马齿苋皂苷C异构体(bacopasaponin C isomer)5.假马齿苋皂苷C(bacopasaponin C)) 图 2 对照品(A)和样品(B编号3)的HPLC色谱图 Figure 2 HPLC chromatograms of reference substances(A) and sample (B No.3) |
|
|
表 4 样品中5个皂苷类成分的含量(mg·g-1,n=3) Table 4 Determination results of the contents of five triterpenoid saponins |
本文建立了假马齿苋中5个皂苷成分的同时测定方法,并进行了方法学验证,用于样品的测定。已有研究[13]仅针对成分假马齿苋皂苷Ⅰ和苦艾素A3同时检测,且图谱中2对异构体分离度较差,假马齿苋皂苷Ⅰ出峰靠后且与其他成分峰连在一起;而本分析方法中假马齿苋皂苷Ⅰ峰与其他峰能够达到完全分离,且2对异构体均达到基线分离,保证了含量测定结果更为准确可靠,方法简便,为多指标控制假马齿苋质量提供了实验基础。
液相色谱分离条件优化过程中,考察了乙腈-水、甲醇-水、乙腈-0.05%磷酸水、乙腈-0.2%磷酸水(氢氧化钠溶液分别调节pH至2.0、2.5、3.0、4.0和5.0)、乙腈-0.1%醋酸水、乙腈-0.1%甲酸水等不同比例的流动相体系,由于假马齿苋皂苷Ⅰ结构中含有磺酸基的缘故,发现其在中性水相中基本无保留,在磷酸盐pH小于3.0时,出峰较晚,而苦艾素A3和假马齿苋皂苷Ⅱ为同分异构体,在有机相比例大于33时,二者同时出峰,而采用醋酸或甲酸体系时,因紫外检测波长接近末端吸收,基线不平而导致无法准确定量,最终确定流动相为乙腈-0.2%磷酸水溶液(pH 3.0)混合体系时目标成分分离度最佳,且各峰的保留时间合适。对柱温考察时发现,当温度小于30 ℃时,假马齿苋皂苷Ⅰ峰与后面的苦艾素A3、假马齿苋皂苷Ⅱ峰始终难以达到基线分离,因此确定最佳柱温为30 ℃。另外,对Agela Promosil C18(4.6 mm×250 mm,5 μm)、Shiseido MP C18(4.6 mm×250 mm,5 μm)、Agilent(4.6 mm×250 mm,5 μm)等不同色谱柱进行对比研究,发现Agela Promosil C18色谱柱对5个指标性成分分离效果最为理想,峰形最佳。
采用本实验建立的色谱条件对产自不同生长环境下的10批假马齿苋进行含量测定。结果表明产自相同生长环境下的假马齿苋,其5个指标成分各自含量相差不多,而产自不同生长环境下的假马齿苋中各自含量差别较大。产于湿地的1、2、5批假马齿苋,假马齿苋皂苷Ⅰ、苦艾素A3、假马齿苋皂苷Ⅱ的含量明显高于潮湿地和旱地假马齿苋;产于旱地的4、9批假马齿苋,假马齿苋皂苷C异构体、假马齿苋皂苷C的含量明显高于潮湿地和湿地假马齿苋;而产于潮湿地的其他批假马齿苋,5个指标成分含量处于中间位置,且各个批次含量较为稳定。可见不同的生长环境,对假马齿苋样品中5种指标成分含量影响较大,另外假马齿苋中的皂苷成分含量,可能还与光照、温度、采集时间等有关,还需进一步研究加以确定。
采用本方法同时测定假马齿苋中的5个皂苷含量,简便可靠,但由于三萜皂苷类成分响应较低,各对照品需求较大且制备不易,下一步可尝试采用一测多评法,实现以假马齿苋皂苷Ⅰ为对照的多个成分的同时测定,为后续的植物标准化种植、质量控制和新药开发奠定基础。
| [1] |
郑国帅. 创新药物假马齿苋皂苷Ⅰ的制备及其代谢稳定性筛选研究[D]. 合肥: 安徽中医药大学, 2015. ZHENG GS. Preparation and Metabolic Stability Creening Studies of Innovative Drug Bacopaside Ⅰ[D]. Hefei:Anhui University of Traditional Chinese Medicine, 2015 |
| [2] |
张嫡群, 梅和珊, 石晓伟. 假马齿苋的生物活性及其临床研究[J]. 天然产物研究与开发, 2007, 19(3): 524. ZHANG DQ, MEI HS, SHI XW. Biological activity and clinical research of Bacopa monniera[J]. Nat Prod Res Dev, 2007, 19(3): 524. |
| [3] |
顾关云, 蒋昱. 假马齿苋的化学成分、药理作用及改善认知功能的临床应用[J]. 国外医药植物药分册, 2005, 20(1): 6. GU GY, JIANG Y. Chemical composition, pharmacological effects and clinical application of improving cognitive function of Bacopa monniera[J]. World Notes Plant Med, 2005, 20(1): 6. |
| [4] |
黄云秀, 阳明福. 假马齿苋的化学成分和药理作用研究进展[J]. 中国新药杂志, 2006, 15(9): 683. HUANG YX, YANG MF. Chemical constituents and pharmacological activities of Bacopa monniera[J]. Chin J New Drugs, 2006, 15(9): 683. |
| [5] |
SIDDIQUE YH, MUJTABA SF, FAISAL M, et al. The effect of Bacopa monnieri leaf extract on dietary supplementation in transgenic Drosophila model of Parkinson's disease[J]. Eur J Integr Med, 2014, 6(5): 571. |
| [6] |
JOSE S, SOWMYA S, CINU TA, et al. Surface modified PLGA nanoparticles for brain targeting of bacoside-A[J]. Eur J Pharm Sci, 2014, 63: 29. |
| [7] |
LE XT, NGUYET PHAM HT, VAN NGUYEN T, et al. Protective effects of Bacopa monnieri on ischemia-induced cognitive deficits in mice:the possible contribution of bacopaside Ⅰ and underlying mechanism[J]. J Ethnopharmacol, 2015, 164: 37. |
| [8] |
李元元. 假马齿苋皂苷Ⅰ治疗阿尔兹海默症的药效及作用机制研究[D]. 上海: 第二军医大学, 2014. LI YY. The Therapeutic Effect and Mechanism of Bacopaside Ⅰ Against Alzheimer's Disease[D]. Shanghai:The Second Military Medical University, 2014 |
| [9] |
周耘. 假马齿苋活性成分研究[D]. 上海: 上海医药工业研究院, 2005. ZHOU Y. Active Constituents of Bacopa monniera[D]. Shanghai:Shanghai Institute of Pharmaceutical Industry, 2005 |
| [10] |
张群群, 李慧芬, 张学兰, 等. HPLC-ELSD法同时测定不同产地白果药材中的4种萜内酯类成分[J]. 中成药, 2016, 38(1): 133. ZHANG QQ, LI HF, ZHANG XL, et al. Simultaneous determination of four terpene lactones in Ginkgo Semen from different growing areas by HPLC-ELSD[J]. Chin Tradit Pat Med, 2016, 38(1): 133. |
| [11] |
梁瑾, 刘小花, 任远, 等. HPLC-DAD-ELSD法同时测定黄芪中5个成分的含量[J]. 药物分析杂志, 2013, 33(2): 210. LIANG J, LIU XH, REN Y, et al. Simultaneous determination of five compounds in Radix Astragali by high-performance liquid chromatography coupled with diode array and evaporative light scattering detectors[J]. Chin J Pharm Anal, 2013, 33(2): 210. |
| [12] |
方诗琦, 瞿其扬, 仲欢欢, 等. 甘草中5种三萜皂苷的同时测定及主成分分析[J]. 中成药, 2016, 38(2): 336. FANG SQ, QU QY, ZHONG HH, et al. Simultaneous determination and principal component analysis of five triterpenoid saponins in licorice[J]. Chin Tradit Pat Med, 2016, 38(2): 336. |
| [13] |
PHROMPITTAYARAT W, WITTAYA AS, JETIYANON K, et al. Stability studies of saponins in Bacopa monnieri dried ethanolic extracts[J]. Planta Med, 2008, 74(14): 1756. |
 2017, Vol. 37
2017, Vol. 37 
