去水卫矛醇(dianhydrogalactitol)(图 1),又名卫康醇,是以卫矛科植物蜜花美登木(Maytenus confertiflorus J. Y. Luo ex X. X. Chen)中分离出的卫矛醇为原料,经溴化、消除反应而制得1,6-二溴卫矛醇的双环氧化物[1]。去水卫矛醇为广谱抗肿瘤药物,具有毒性小、易溶于水、抗肿瘤活性高等优点,早期临床试验表明,去水卫矛醇对慢性粒细胞白血病、肺癌、骨髓瘤、鼻咽癌、胃肠道肿瘤、原发性脑瘤、卵巢癌等均有抑制作用,同时,去水卫矛醇可以与某些周期特异性药物产生协同作用[2-5]。去水卫矛醇和注射用去水卫矛醇的国家药品标准中未收载有关物质项,含量测定项下均采用滴定法[6]77,112,文献报道[7]采用气相色谱法测定注射用去水卫矛醇含量。标准中使用的滴定法专属性差,并且由于去水卫矛醇具有双环氧结构,化学性质不稳定,气相色谱法测定时有降解的风险。
定量核磁共振(quantitative nuclear magnetic reson-ance,qNMR)技术作为一种日益成熟的仪器分析方法,具有传统方法不可比拟的优势,如操作简便、测定快速准确、无需待测物标准物质、不需要引进任何校正因子、不破坏样品等等,先后被美国药典、英国药典、欧洲药典、日本药局方和中国药典作为法定标准收录,该技术已应用于药物质量控制、新药研发、对照品研究、代谢组学以及聚合物组成分析等方面[8-13]。
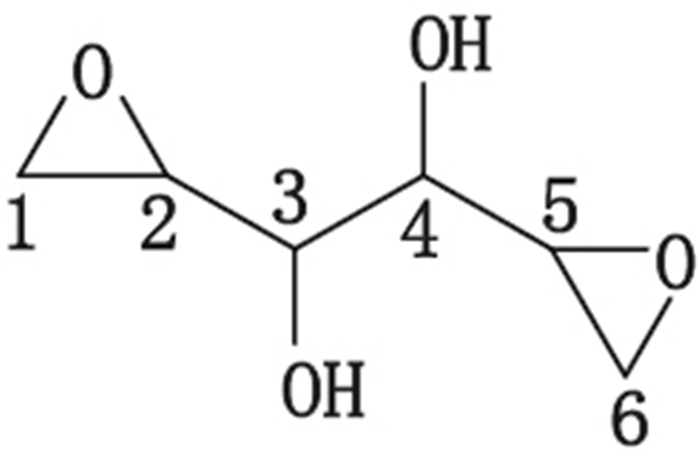
|
图 1 去水卫矛醇的化学结构 Figure 1 Chemical structure of dianhydrogalactitol |
本文通过研究选择适宜的核磁参数、内标物和溶剂,同时与质量平衡法测得的结果进行比较,探索去水卫矛醇的定量核磁共振含量测定方法。
1 仪器与试药Ascend-500型核磁共振波谱仪(Bruker公司);MSA 6.6S百万分之一电子天平(Sartorius公司);1260液相色谱仪(Agilent公司)。
去水卫矛醇(广西梧州制药(集团)股份有限公司,批号140401);氘代二甲基亚砜(DMSO-d6)(Sigma-Aldrich,纯度99.9%);甲酸(国药集团化学试剂有限公司,含量≥98.0%,批号20140321);甲醇(Fisher Scientific,含量99.9%,批号140400),对苯二甲酸二甲酯(中国食品药品检定研究院,含量99.9%,批号510052-201401)。
2 方法 2.1 供试品溶液制备精密称取去水卫矛醇样品约6 mg和内标物对苯二甲酸二甲酯约4 mg,加入DMSO-d6 1.0 mL,超声(35 kHz)使其完全溶解,再转入适量至5 mm核磁管中备用。
2.2 色谱条件采用Apollo C18(150 mm×4.6 mm,5 μm)色谱柱,0.05%甲酸水溶液与甲醇(90:10)为流动相等度洗脱,流速0.5 mL·min-1,雾化温度45 ℃,漂移管温度50 ℃,载气(氮气)流速1.5 L·min-1,进样器温度4 ℃,进样体积50 μL。
2.3 核磁仪器参数设置采用参数为90°脉冲,谱宽(SWH)7 500 Hz,采样时间(AQ)4.36 s,弛豫时间(D1)20 s,空扫次数(DS)16次,采样次数(NS)64次,核磁管不旋转,温度25 ℃。
2.4 qNMR结果计算对每个指定信号峰进行积分,积分次数不少于5次,取积分面积的平均值,根据下列公式(1)计算去水卫矛醇的含量[15]:
| ${P_x} = \frac{{{A_x}}}{{{A_{{\rm{std}}}}}}\frac{{{N_{{\rm{std}}}}}}{{{N_x}}}\frac{{{M_x}}}{{{M_{{\rm{std}}}}}}\frac{{{m_{{\rm{std}}}}}}{{{m_x}}}{P_{{\rm{std}}}}$ | (1) |
式中:Ax和Astd分别为待测样品与内标物定量峰的积分面积;Nx和Nstd分别为待测样品与内标物定量峰积分信号所包含的质子数;Mx和Mstd分别为待测样品与内标物的相对分子质量;mx和mstd分别为待测样品与内标物的质量;Pstd为内标物的质量百分含量。
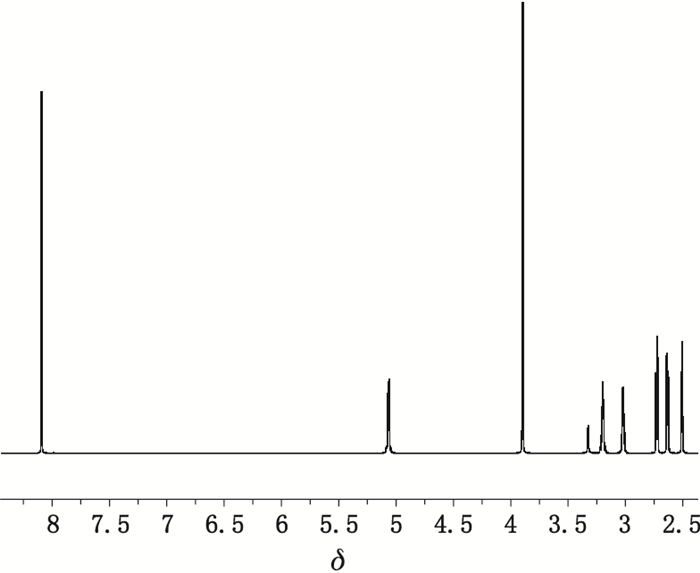
3 结果与讨论 3.1 内标物和溶剂的选择定量核磁共振法的内标物应该具有稳定的化学性质,不与待测样品发生化学反应,定量峰不与待测样品信号重叠,两者能溶于同一氘代溶剂中等性质。去水卫矛醇分子结构中含有双氧环,化学性质不稳定,对于内标物和氘代溶剂有一定要求。例如,内标物选择富马酸时,去水卫矛醇发生明显的降解,考虑可能样品在酸性溶液中稳定性降低,因此,选择中性内标物对苯二甲酸二甲酯,同时该内标物的定量峰(δ8.09)与样品峰分离良好(图 2)。选择的溶剂应能同时溶解样品和内标物,同时对两者的信号不产生干扰,因此选择DMSO-d6作为溶剂。
|
图 2 去水卫矛醇的1H NMR谱(溶剂:DMSO-d6) Figure 2 1H NMR spectrum of dianhydrogalactitol in DMSO-d6 |
通常选择与相邻峰无干扰的信号作为定量的特征峰。对去水卫矛醇进行定量分析前,已经通过一维和二维核磁共振谱对其1H-NMR信号进行归属。H-2(5)(δ3.02)与内标峰不重合(图 2),且附近无干扰峰,因此作为定量的特征峰。
3.3 仪器参数的选择弛豫延迟时间(D1)对NMR信号的积分值影响较大,定量实验中通常设定D1值不低于5倍的定量峰中最长的T1值[14]。通过翻转恢复试验对去水卫矛醇和内标物的定量峰的T1进行测试,发现两者定量峰(δ3.02和8.09)的T1值分别为2.27 s和2.39 s,为保证每次采样质子核磁共振信号得到充分的弛豫,并且不影响NMR信号积分值的测定,本次实验设定D1为20 s。
3.4 线性关系考察精密称取样品与内标物适量[样品(mg)/内标物(mg):2.266/4.260,4.076/4.390,6.110/3.950,12.118/4.214,16.332/4.284,21.978/4.282],分别加入DMSO-d6 1.0 mL配制成6份不同浓度溶液,进行线性考察,以样品定量峰面积与内标物定量峰面积的比值为纵坐标,以样品与内标物的质量比值为横坐标进行线性回归,回归方程:
Y=0.630 4X+0.016 3 r=0.999 9
表明样品与内标物质量比值在0.53~5.13范围内与两者定量峰面积比值呈良好的线性关系。
3.5 进样精密度试验取同一份供试品溶液,连续测定6次,以样品定量峰面积与内标物定量峰面积的比值计算RSD为0.038%。
3.6 重复性试验平行制备6份供试品溶液,在同一实验条件下测定,以样品定量峰面积与内标物定量峰面积的比值计算去水卫矛醇含量,重复性的RSD为0.55%。
3.7 稳定性试验取同一份供试品溶液,分别于0、2、4、6、8、10和12 h进行测定,计算样品定量峰与内标物定量峰面积比值,RSD为0.072%,表明供试品溶液室温放置12 h稳定。
3.8 样品定量核磁共振法测定结果平行制备6份供试品溶液进行测定,按照公式(1)计算去水卫矛醇的含量分别为96.31%、95.16%、95.18%、96.31%、96.07%和95.90%,平均含量为95.82%,RSD为0.55%。
3.9 定量核磁共振法与质量平衡法测定结果采用企业的高效液相色谱-蒸发光散射法(色谱条件见“2.2”项)测定去水卫矛醇色谱纯度为96.54%,卡尔-费休氏法测定水分为0.13%,气相色谱测定残留溶剂为0.20%,炽灼残渣未检出,根据质量平衡法[15],去水卫矛醇的含量(%)=(100%-水分含量-残留溶剂含量-炽灼残渣含量)×HPLC纯度=(100%-0.13%-0.20%-0)×96.54%=96.22%。质量平衡法测定去水卫矛醇的含量与定量核磁共振定法测定结果接近,表明定量核磁共振法测定结果准确。
4 结论本文建立了定量核磁共振法测定去水卫矛醇含量的方法,该方法简便快速、准确可靠,可用于去水卫矛醇的质量控制,也可用于其对照品的含量赋值。去水卫矛醇自身化学结构的特点,不具有紫外吸收和不稳定性,因此,定量核磁共振法测定其含量的方法是常规色谱含量测定方法的有效补充。
| [1] |
张慧玲, 王稼农, 梁霜, 等. 二去水卫矛醇对四种肿瘤细胞的体外抑制作用[J]. 广西科学, 2013, 20(1): 82. ZHANG HL, WANG JN, LIANG S, et al. Inhibitory effect of 1, 2:5, 6-dianhydrogalactitol on four different kinds of tumor cells in vitro[J]. Guangxi Sci, 2013, 20(1): 82. |
| [2] |
梁乔芳, 刘华钢, 谭强, 等. 二去水卫矛醇对人脑肿瘤细胞体外抑制作用[J]. 广西科学, 2015, 22(4): 454. LIANG QF, LIU HG, TAN Q, et al. Inhibitory effect of 1, 2:5, 6-dianhy-drogalctitol on human brain tumor cells in vitro[J]. Guangxi Sci, 2015, 22(4): 454. |
| [3] |
周莹, 刘华钢, 苏桂玉, 等. 二去水卫矛醇对人卵巢癌细胞的体外抑制作用[J]. 广西中医药大学学报, 2015, 18(4): 66. ZHOU Y, LIU HG, SU GY, et al. Inhibitory effect of 1, 2:5, 6-dianhydrogalactitol on human ovarian cancer cells in vitro[J]. J Guangxi Univ Chin Med, 2015, 18(4): 66. |
| [4] |
樊亦军, 韦焕英, 邢邦华, 等. 1, 2:5, 6-二去水卫矛醇抗肿瘤作用及毒性[J]. 华西药学杂志, 1987, 2(3): 161. FANG YJ, WEI HY, XIN BH, et al. Antitumor activity and toxicity of 1, 2:5, 6-dianhydrogalactitol[J]. West China J Pharm Sci, 1987, 2(3): 161. |
| [5] |
樊亦军, 韩锐, 周军, 等. 抗癌药1, 2:5, 6-二去水卫矛醇与长春新碱联合用药的实验研究[J]. 药学学报, 1987, 22(2): 98. FANG YJ, HAN R, ZHOU J, et al. Experimental studies on combination of vincristine and 1, 2:5, 6-dianhydrogalactitol[J]. Acta Pharm Sin, 1987, 22(2): 98. |
| [6] |
国家食品药品监督管理局. 国家药品标准[S]. 2003 China Food and Drug Administration. National Drug Standards. 2003 |
| [7] |
魏宁漪, 宁保明. 气相色谱法测定注射用去水卫矛醇的含量及有关物质[J]. 中国药师, 2011, 14(9): 1306. WEI NY, NING BM. Determination of dianhydrogalactitol for injection and related substances by GC[J]. China Pharm, 2011, 14(9): 1306. |
| [8] |
胡敏, 胡昌勤, 刘文英. 核磁共振波谱法测定药物基准物质的绝对含量[J]. 分析化学, 2004, 32(4): 451. HU M, HU CQ, LIU WY. Determination of drug reference substance content by 1H-nuclear magnetic resonance spectroscopy[J]. Chin J Anal Chem, 2004, 32(4): 451. |
| [9] |
禹珊, 郭强胜, 王会琳, 等. 定量核磁共振波谱法同时测定中药虎杖中白藜芦醇和虎杖苷的含量[J]. 分析化学, 2015, 43(1): 69. YU S, GUO QS, WANG HL, et al. Simultaneous determination of resveratrol and polydatin in polygonum cuspidatum by quantitative nuclear magnetic resonance spectroscopy[J]. Chin J Anal Chem, 2015, 43(1): 69. |
| [10] |
黄挺, 张伟, 全灿, 等. 定量核磁共振法研究进展[J]. 化学试剂, 2012, 34(4): 327. HUANG T, ZHANG W, QUAN C, et al. Review on quantitative nuclear magnetic resonance[J]. Chem Reagents, 2012, 34(4): 327. |
| [11] |
张芬芬, 蒋孟虹, 沈文斌, 等. 定量核磁共振(QNMR)技术及其在药学领域的应用进展[J]. 南京师范大学学报(工程技术版), 2014, 14(2): 8. ZHANG FF, JIANG MH, SHEN WB, et al. Progress in quantitative nuclear magnetic resonance technology in pharmaceutical applications[J]. J Nanjing Norm Univ(Eng Technol Ed), 2014, 14(2): 8. |
| [12] |
于小波, 沈文斌, 相秉仁. 定量核磁共振技术及其在药学领域中的应用进展[J]. 药学进展, 2010, 34(1): 17. YU XB, SHEN WB, XIANG BR. Advances in application of quantitative nuclear magnetic resonance technique in pharmaceutical field[J]. Prog Pharm Sci, 2010, 34(1): 17. |
| [13] |
林珊, 苏娟, 叶霁, 等. 定量核磁共振技术在中药分析中的应用进展[J]. 药学实践杂志, 2014, 32(2): 92. LIN S, SU J, YE J, et al. Application progress in quantitative NMR in analysis of traditional Chinese medicine[J]. J Pharm Pract, 2014, 32(2): 92. |
| [14] |
SHEN S, YAO J, SHI YQ. Quantitative proton nuclear magnetic resonance for the structural and quantitative analysis of atropine sulfate[J]. J Pharm Biomed Anal, 2014, 89: 118. DOI:10.1016/j.jpba.2013.10.036 |
| [15] |
张永权, 冯艳春, 李进, 等. 酮康唑相关杂质国家标准物质的研制[J]. 药物分析杂志, 2015, 35(3): 532. ZHANG YQ, FENG YC, LI J, et al. Establishment of national reference standards of ketoconazole impurities[J]. Chin J Pharm Anal, 2015, 35(3): 532. |
 2017, Vol. 37
2017, Vol. 37 
