柴黄颗粒由柴胡、黄芩提取物组成,具有清热消炎功效,用于上呼吸道感染、感冒发热等症状[1-2]。质量标准收载于卫生部药品标准(WS3-B-2009-95)[3]。柴胡皂苷是柴胡的主要化学成分,具有抗炎、抗病毒、抗过敏等药理活性[4]。黄芩苷是黄芩的主要有效成分之一,具有抑菌、清热、降压、镇静、利尿、利胆、抗炎、抗变态反应、解毒、抗癌等作用[5-6]。柴胡皂苷和黄芩苷的测定方法主要有HPLC法分别测定各皂苷或黄芩苷含量、分光光度法测定总皂苷或总黄酮含量[7-11]。对于柴黄颗粒的质量控制,只有采用薄层色谱法对柴胡、黄芩药材进行鉴别,采用红外光谱建立柴黄颗粒的指纹图谱[12],采用HPLC法测定黄芩苷含量[13-14]以及分光光度法测定柴胡总皂苷含量[15],未见柴黄颗粒中黄芩苷及柴胡皂苷含量的同时测定的文献报道。本文采用反相高效液相色谱法,对柴黄颗粒中柴胡皂苷a、b1、c、d以及黄芩苷同时进行测定,为评价和控制柴黄颗粒的质量提供了科学依据。
1 仪器与试药 1.1 仪器Agilent 1260高效液相色谱仪,配置DAD检测器(Agilent公司);Agilent ZORBAX SB-C18(4.6 mm×250 mm,5 μm;填料:二异丁基-十八烷基键合硅胶)色谱柱(Agilent公司);KQ2200B型超声波清洗仪(昆山市超声仪器有限公司),R-301旋转蒸发器(上海申顺生物科技有限公司),电子天平(北京赛多利斯仪器系统有限公司,d=0.01 mg),默克密理博Milli-Q超纯水机(美国默克密理博有限公司)。
1.2 试药柴胡皂苷a、b1、c、d对照品,批号141128、140621、140820、141220,含量均≥98%,成都普菲德生物技术有限公司;黄芩苷对照品,批号110715-201016,含量94.0%,中国食品药品检定研究院。乙腈、甲醇为色谱纯,水为实验室专用超纯水机制备的超纯水,磷酸、甲酸、氨水为分析纯。柴黄颗粒,批号z19993380,规格为3 g·袋-1,四川百利药业有限责任公司。
2 方法与结果 2.1 混合对照品储备液的制备精密称取对照品柴胡皂苷a 1.80 mg,柴胡皂苷b1 3.00 mg,柴胡皂苷c 4.20 mg,柴胡皂苷d 4.60 mg,黄芩苷5.00 mg,分别置于10 mL量瓶中,加甲醇约7 mL,振摇使之溶解,并用甲醇稀释至刻度,摇匀,制得柴胡皂苷a为0.180 mg·mL-1、柴胡皂苷b1为0.300 mg·mL-1、柴胡皂苷c为0.420 mg·mL-1、柴胡皂苷d为0.460 mg·mL-1,黄芩苷为0.500 mg·mL-1的5种对照品溶液;精密量取上述5种对照品溶液各8.0 mL,混合均匀,制成混合对照品储备液。
2.2 供试品溶液的制备称取样品细粉0.30 g,精密称定,加入5%浓氨甲醇溶液35 mL,密塞,超声处理(功率200 W,频率40 kHz)30 min,过滤,用甲醇20 mL分2次洗涤容器和药渣,洗液与滤液合并,减压旋蒸,残渣加甲醇约70 mL溶解并转移至100 mL量瓶中,加甲醇稀释至刻度,摇匀,用0.45 μm微孔滤膜滤过,取续滤液作为供试品溶液。
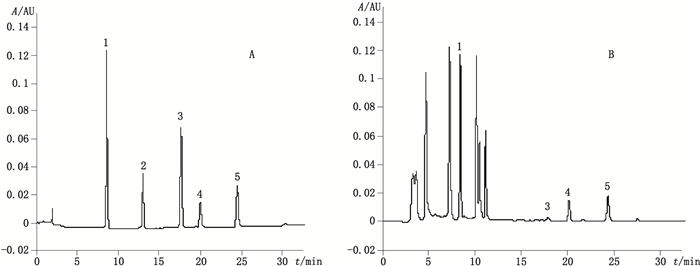
2.3 色谱条件色谱柱:Agilent ZORBAX SB-C18(4.6 mm×250 mm,5 μm);流动相:乙腈(A)-0.01%磷酸水溶液(B),梯度洗脱(0~30 min,30%A→60%A;30~35 min,60%A);流速:1.0 mL·min-1;柱温:常温(25℃);检测波长210 nm;进样量:10 μL;运行时间:35 min。在上述色谱条件下对照品及样品的色谱图见图 1。
|
1.黄芩苷(baicalin)2.柴胡皂苷c(saikosaponin c)3.柴胡皂苷a(saikosaponin a)4.柴胡皂苷b1(saikosaponin b1)5.柴胡皂苷d(saikosaponin d) 图 1 柴胡皂苷a、b1、c、d及黄芩苷对照品(A)和柴黄颗粒样品(B)的HPLC色谱图 Figure 1 HPLC chromatograms of saikosaponins a, b1, c and d, and baicalin(A)in Chaihuang granules(B) |
精密吸取上述混合对照品储备液1.0、2.0、4.0、6.0、8.0、10.0 mL,分别稀释定容于10 mL量瓶中,各取10 μL按上述色谱条件依次进样测定峰面积,以进样量X(μg)为横坐标,峰面积Y为纵坐标,绘制标准曲线,柴胡皂苷a、b1、c、d及黄芩苷的回归方程、线性范围和相关系数见表 1。
|
|
表 1 柴胡皂苷a、b1、c、d及黄芩苷的线性回归分析 Table 1 Regression analysis of saikosaponin a, saikosaponin b1, saikosaponin c, saikosaponin d and baicalin |
取供试品溶液,连续进样6次,测定峰面积。结果柴胡皂苷a、b1、d及黄芩苷峰面积的RSD分别为0.69%、0.78%、0.92%、0.77%,表明精密度良好。
2.6 稳定性试验取柴黄颗粒制成供试品溶液,按照“2.3”项下色谱条件分别于制备后0、2、4、6、8、10 h进样10 μL,测定柴胡皂苷a、b1、d及黄芩苷的峰面积;结果RSD分别为1.0%、1.2%、0.98%、0.97%,表明柴黄颗粒供试品溶液在10 h内稳定。
2.7 重复性试验按照“2.2”项平行制备6份柴黄颗粒供试品溶液,分别进样10 μL,结果样品中柴胡皂苷a、b1、d及黄芩苷含量平均值分别为1.562、7.574、9.221、11.648 mg·g-1,RSD分别为1.1%、0.82%、1.3%、0.99%。
2.8 回收率试验精密称取含有柴胡皂苷a 1.56 mg·g-1,柴胡皂苷b1 7.51 mg·g-1,柴胡皂苷d 9.36 mg·g-1及黄芩苷11.67 mg·g-1的柴黄颗粒样品6份,每份0.15 g,分别置于圆底烧瓶中,精密加入0.180 mg·mL-1的柴胡皂苷a对照品溶液1.0 mL和0.420 mg·mL-1的柴胡皂苷c对照品溶液1.0 mL,柴胡皂苷b1对照品1.18 mg和柴胡皂苷d对照品1.43 mg,黄芩苷对照品1.82 mg,按照“2.2”项方法进行操作,得到6份供试品溶液。分别吸取上述6份溶液各10 μL,注入液相色谱仪测定,进行加样回收率的考察;结果柴胡皂苷a、b1、c、d、黄芩苷平均回收率分别为97.5%、95.3%、99.7%、98.4%和95.1%,RSD分别为0.66%、0.93%、0.68%、0.74%和1.2%。
2.9 样品含量测定取3批柴黄颗粒,每批取3份,分别按照“2.2”项方法制备供试品溶液,按“2.3”项下色谱条件进样测定,以外标法计算含量,结果见表 2。
|
|
表 2 柴胡皂苷a、b1、c、d及黄芩苷的3批样品含量测定 Table 2 Contents of saikosaponins a, b1, c, d and baicalin in three batches of samples(mg·g-1, n=3) |
本研究考察了75%、85%、100%甲醇水溶液及5%浓氨甲醇溶液4种提取溶剂和回流提取、索氏提取、超声提取3种提取方法对提取率的影响。结果显示:5%浓氨甲醇试液超声提取时,提取效率最高;在超声时间考察时发现超声30 min以上时,提取效率基本不变,故选择超声时间为30 min。
3.2 检测波长的选择本研究考察了波长的影响。使用DAD二极管阵列检测器对5种对照品溶液在190~400 nm波长范围内进行全扫描。查看3D图谱发现:柴胡皂苷a、b1、c、d及黄芩苷在205 nm附近吸光系数均最大,但在此波长下基线漂移较大。综合考察检测灵敏度和基线漂移情况,本实验选择210 nm进行检测。
3.3 流动相的选择本研究考察了多种流动相系统。有机相分别为甲醇和乙腈,水相分别为水、磷酸水溶液(0.1%、0.05%、0.01%)、甲酸水溶液(0.1%、0.05%、0.01%)。实验结果表明,甲醇在210 nm的波长下吸收较大,基线漂移严重,所以有机相选定为乙腈。在水相中,使用甲酸水溶液为流动相时,基线明显向下漂移;使用0.1%和0.05%磷酸水溶液及0.1%和0.05%甲酸水溶液为流动相时,观察色谱图发现柴胡皂苷a、b1、c、d色谱峰均发生拖尾及分裂现象。使用水、0.01%磷酸水溶液及0.01%甲酸水溶液时色谱峰峰形好,但在以水为流动相时,黄芩苷酚羟基发生解离,使其在固定相表面有双重保留机制,峰形较差。综上所述,本实验选用乙腈-0.01%的磷酸水溶液为流动相。
3.4 小结本研究建立了同时测定柴黄颗粒中黄芩苷及柴胡皂苷a、b1、c、d的HPLC分析方法。经方法学验证,所建立的测定方法符合定量分析要求,该方法操作简单,结果准确、可靠,重现性好。可为柴黄颗粒定量控制指标的选择提供参考,为柴黄颗粒质量标准的建立提供一定的科学依据。
| [1] |
陈慧慧, 张敏, 虞慧娟, 等. 柴胡和黄芩配伍解热抗炎作用研究[J]. 中成药, 2011, 33(9): 1596. CHEN HH, ZHANG M, YU HJ, et al. The study of antipyretic and anti-inflammatory effects of Bupleurum and Scutellaria compatibility[J]. Chin Tradit Pat Med, 2011, 33(9): 1596. |
| [2] |
强立, 陈珍英. 柴黄颗粒治疗小儿反复呼吸道感染免疫功能及T细胞亚群的影响[J]. 中药药理与临床, 2014, 30(6): 170. QIANG L, CHEN ZY. Regulation of Chaihuang granules on immune function and T cell subsets of children with recurrent respiratory tract infections[J]. Pharmacol Clin Chin Mater Med, 2014, 30(6): 170. |
| [3] |
WS3-B-2009-95-2005柴黄颗粒质量标准[S]. 2005 WS3-B-2009-95-2005 Quality Standard of Chaihuang Granules[S]. 2005 |
| [4] |
黄伟, 孙蓉. 柴胡皂苷类成分化学与药理和毒理作用研究进展[J]. 中药药理与临床, 2010, 26(3): 71. HUANG W, SUN R. Research development on pharmacological and toxicity effects of saikosaponin constituents[J]. Pharmacol Clin Chin Mater Med, 2010, 26(3): 71. |
| [5] |
宋旦哥, 孟庆刚. 黄芩药理作用研究述评[J]. 中华中医药学刊, 2009, 27(8): 1619. SONG DG, MENG QG. Baicalin pharmacological effects commentary[J]. Chin Arch Tradit Chin Med, 2009, 27(8): 1619. |
| [6] |
吴莹, 金叶智, 吴珺, 等. 黄芩主要成分体外抗甲型流感病毒作用的研究[J]. 北京中医药大学学报, 2010, 33(8): 541. WU Y, JIN YZ, WU J, et al. Antiviral effects of major constituents of Huangqin(Radix Scutellariae)on influenza A virus(FM1) in vitro[J]. J Beijing Univ Tradit Chin Med, 2010, 33(8): 541. |
| [7] |
孟杰, 陈兴福, 杨文钰, 等. 柴胡主根与侧根中柴胡皂苷a及皂苷d含量测定[J]. 药物分析杂志, 2013, 33(7): 1218. MENG J, CHEN XF, YANG WY, et al. Determination of saikosaponin a and d in taproot and lateral root of Bupleurum chinense DC.[J]. Chin J Pharm Anal, 2013, 33(7): 1218. |
| [8] |
许磊, 田稷馨, 宋瑞, 等. 柴胡醋制前后柴胡皂苷a、b2、c、d的LC-MS/MS法测定及比较[J]. 中国药科大学学报, 2012, 43(4): 334. XU L, TIAN JX, SONG R, et al. LC-MS/MS determination and comparison of saikosaponin a, b2, c, d in crude and processed Radix Bupleuri by vinegar[J]. J Chin Pharm Univ, 2012, 43(4): 334. DOI:10.11665/j.issn.1000-5048.20120410 |
| [9] |
温华珍, 肖盛元, 王义明, 等. HPLC法测定不同规格并头黄芩的黄芩苷和汉黄芩苷含量[J]. 中草药, 2005, 36(4): 600. WEN HZ, XIAO SY, WANG YM, et al. Baicalin and wogonoside in different species of Scutellaria scordifolia by HPLC[J]. Chin Tradit Herb Drugs, 2005, 36(4): 600. |
| [10] |
谭玲玲, 蔡霞, 胡正海. 不同产地狭叶柴胡中柴胡皂苷含量的测定[J]. 时珍国医国药, 2010, 21(10): 2431. TAN LL, CAI X, HU ZH. Content determination of saikosaponin in Bupleurum scorzonerifolium Willd.from different areas[J]. Lishizhen Med Mater Med Res, 2010, 21(10): 2431. DOI:10.3969/j.issn.1008-0805.2010.10.005 |
| [11] |
伍蔚萍, 孙文基, 阎宏涛, 等. 分光光度法测定甘草中总黄酮的含量[J]. 药物分析杂志, 2005, 25(4): 469. WU WP, SUN WJ, YAN HT, et al. Determination of total flavone in Licorice by spectrophotometry[J]. Chin J Pharm Anal, 2005, 25(4): 469. |
| [12] |
杨莉丽, 秦旭华, 罗永静, 等. 柴黄颗粒的红外指纹图谱研究[J]. 河北省科学院学报, 2010, 27(4): 51. YANG LL, QIN XH, LUO YJ, et al. Study on the infrared fingerprint of Chaihuang granule[J]. J Hebei Acad Sci, 2010, 27(4): 51. |
| [13] |
申去非, 刘晓晖, 朱铁梁, 等. RP-HPLC法测定柴黄颗粒中黄芩苷含量[J]. 中医药信息, 2009, 26(3): 29. SHEN QF, LIU XH, ZHU TL, et al. Determination of baicalin in Chaihuang granules by RP-HPLC[J]. Inf Tradit Chin Med, 2009, 26(3): 29. |
| [14] |
黄妙婵. 高效液相色谱法测定柴黄颗粒中黄芩苷的含量[J]. 今日药学, 2009, 19(6): 43. HUANG MC. Determination of baicalin in Chaihuang granules by HPLC[J]. Pharm Today, 2009, 19(6): 43. |
| [15] |
索志荣, 吴楚棠, 刘林, 等. 柴黄颗粒中总皂苷含量的测定[J]. 西南科技大学学报, 2011, 26(3): 88. SUO ZR, WU CT, LIU L, et al. Contents determination of saikosaponins in Chaihuang granules[J]. J Southwest Univ Sci Technol, 2011, 26(3): 88. |
 2017, Vol. 37
2017, Vol. 37 
