肾康注射液具有通腑利湿和益气活血的功效,主要由大黄、丹参、黄芪、红花4味中药提取精制而成[1-3]。通过临床上不断的研究和探索,发现肾康注射液能降低肾小球硬化率,减轻肾脏病理损伤,对慢性肾衰竭及糖尿病肾病有突出的治疗作用,同时能改善患者的心、肾功能和肺功能,值得临床推广使用[4-5]。目前,关于肾康注射液中有效成分的测定已有文献报道,文献多采用HPLC-UV法对肾康注射液蒽醌类成分进行测定[6-9],未见对肾康注射液中其他有效成分测定的研究,难以全面控制其质量。而UPLC-MS/MS在中药多组分的测定中优于传统的HPLC-UV法[10-12],测定时间短,分离度好,可以排除复杂基质中性质相近的化学成分相互干扰,尤其适于复杂样品的定性和定量分析。并且UPLC-MS/MS检测的灵敏度高,不受化合物无生色团的限制,更适于样品中组分的测定[13-14]。本研究采用UPLC-MS/MS法同时测定肾康注射液中的丹参素、羟基红花黄色素A、毛蕊异黄酮、黄芪甲苷、大黄酸、丹参酮ⅡA、大黄素,为建立肾康注射液质量控制标准提供一定的参考。
1 仪器与试药 1.1 仪器Shimadzu 30A UPLC system超高效液相色谱系统,配有Shimadzu 30AD二元高压梯度泵、Shimadzu CTO30A柱温箱和Shimadzu SIL30AC自动进样器;Phenomenex Kinetex XB-C18(2.1 mm×50 mm,2.6 μm)色谱柱;Applied Biosystems公司AB Sciex Triple QuadTM 5500型串联四极杆线性离子阱质谱仪,配有Turbo V离子源和三重四极杆线性离子肼串联质量分析器。Analyst 1.6数据采集软件。北京赛多利斯仪器有限公司BP211D型分析天平。
1.2 试药对照品丹参素(批号ZA0809LA13)、羟基红花黄色素A(批号ZO1015BB14)、毛蕊异黄酮(批号20130425)、黄芪甲苷(批号CM0308QA14)、大黄酸(批号HS0905KA13)、丹参酮ⅡA(批号AJ0718LA14)、大黄素(批号SA0428XA14)均购自上海源叶生物科技有限公司,纯度均大于98%;甲醇、甲酸为色谱纯,水为娃哈哈纯净水。
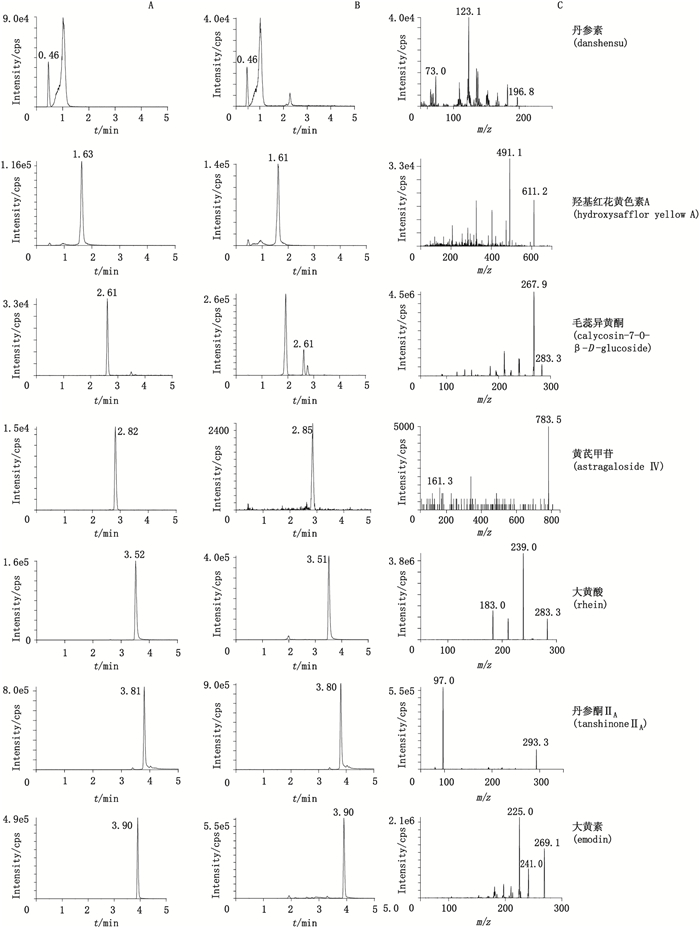
2 方法与结果 2.1 LC-MS条件 2.1.1 LC条件采用Phenomenex Kinetex XB-C18(2.1 mm×50 mm,2.6 μm)色谱柱,甲醇(A)-0.05%甲酸水(B),梯度洗脱(0~3 min,8%A→65%A;3~5 min,65%A→85%A),每针进样前平衡8 min,流速0.3 mL·min-1,柱温30 ℃,进样量20 μL。对照品和样品色谱图见图 1。
|
图 1 对照品(A)、肾康注射液(B)的多重反应监测色谱图和对照品二级质谱图(C) Figure 1 Representative extract ions chromatograms of multiple-reaction monitoring of standards(A), sample(B)and product ion scan spectra(C)of standards |
采用电喷雾离子源(ESI源),离子源温度为600 ℃,负离子监测模式,Turbo V离子源。源喷射电压为-4 500 V,雾化气(gas 1)和加热气(gas 2)分别为414和448 kPa,帘气为172 kPa,接口处加热,多反应监测模式(MRM)。丹参素、羟基红花黄色素A、毛蕊异黄酮、黄芪甲苷、大黄酸、丹参酮ⅡA、大黄素的MS参数见表 1,二级质谱图见图 1。
|
|
表 1 肾康注射液中7个成分的保留时间和主要质谱参数 Table 1 Retention time(tR)and main mass parameters of seven constituents in Shenkang injection |
分别精密称取丹参素、羟基红花黄色素A、毛蕊异黄酮、黄芪甲苷、大黄酸、丹参酮ⅡA和大黄素的对照品适量,加甲醇制成质量浓度分别为1.000、1.050、0.990 0、0.900 0、0.975 0、1.000和1.250 mg·mL-1的对照品储备液;分别取各对照品储备液适量,加甲醇制成适当浓度的混合对照品溶液(丹参素、羟基红花黄色素A、毛蕊异黄酮、黄芪甲苷、大黄酸、丹参酮ⅡA和大黄素的质量浓度分别为500.0、350.0、3.300、3 000、325.0、50.00和12.50 ng·mL-1),备用。
2.2.2 供试品溶液精密量取不同批次肾康注射液500 μL,分别置100 mL量瓶中,加甲醇稀释至刻度,用0.22 μm微孔滤膜过滤,取澄清的续滤液作为供试品溶液。
2.3 方法学考察 2.3.1 线性关系考察及检测限、定量限测定精密量取上述混合对照品溶液适量,采用倍数稀释法,用甲醇分别稀释0、2、4、8、16和32倍,制得6个不同浓度梯度的系列标准溶液,按“2.1”项下LC-MS条件进行分析,记录各个成分的峰面积。以质量浓度(X)为横坐标,峰面积(Y)为纵坐标,绘制标准曲线。回归方程、相关系数及线性范围见表 2。将混合对照品溶液逐步稀释,分别以信噪比S/N=3和S/N=10时各对照品溶液的质量浓度作为检测限和定量限,结果见表 2。
|
|
表 2 7个成分的回归方程、相关系数和线性范围、检测限和定量限 Table 2 Regression equations, correlation coefficients, linearity ranges, LODs and LOQs of the 7 constituents |
精密吸取混合对照品溶液,连续进样6次,计算各成分峰面积的RSD,7个组分的RSD分别为丹参素1.81%、羟基红花黄色素A 1.07%、毛蕊异黄酮0.94%、黄芪甲苷1.38%、大黄酸1.00%、丹参酮ⅡA 2.02%、大黄素1.51%,表明仪器精密度良好。
2.3.3 稳定性试验将样品(批号201504042)的供试品溶液在室温下放置0、2、4、6、8、12 h后分别进样,记录峰面积,计算各组分峰面积的RSD,结果依次为丹参素2.00%、羟基红花黄色素A 0.97%、毛蕊异黄酮0.49%、黄芪甲苷1.57%、大黄酸0.83%、丹参酮ⅡA 2.77%、大黄素1.78%,表明供试品溶液室温放置12 h稳定。
2.3.4 重复性试验按“2.2.2”项下方法制备样品(批号201504042)的供试品溶液,共6份,进样分析,样品中各成分平均含量及其RSD分别为丹参素15.01 μg·mL-1,1.33%;羟基红花黄色素A 11.22 μg·mL-1,1.17%;毛蕊异黄酮0.1018 μg·mL-1,0.81%;黄芪甲苷30.12 μg·mL-1,1.68%;大黄酸10.54 μg·mL-1,1.03%;丹参酮ⅡA 2.716 μg·mL-1,2.56%;大黄素0.3630 μg·mL-1,2.01%。结果表明该方法重复性良好。
2.3.5 回收率考察精密量取6份同一批样品(批号201504042)250 μL,分别置于100 mL量瓶中,分别精密加入7个被测组分的对照品储备液适量,并用甲醇稀释至刻度,摇匀,用0.22 μm微孔滤膜过滤,取澄清的续滤液进样测定分析,计算丹参素、羟基红花黄色素A、毛蕊异黄酮、黄芪甲苷、大黄酸、丹参酮ⅡA和大黄素的平均回收率,结果见表 3。
|
|
表 3 回收率测定结果(n=6) Table 3 Results of recovery of seven constituents in Shenkang injection |
取5批肾康注射液各3份,按照“2.2.2”项下的方法制备供试品溶液,按照“2.1”项下的LC-MS条件进样分析测定,记录7个被测物的色谱峰面积,代入各成分相应的回归方程分别计算丹参素、羟基红花黄色素A、毛蕊异黄酮、黄芪甲苷、大黄酸、丹参酮ⅡA和大黄素的含量,结果见表 4。
|
|
表 4 肾康注射液7种成分的含量(μg·mL-1,n=3,RSD < 2.5%) Table 4 The contents of the 7 compounds in Shenkang injection |
试验过程中,为选择最佳的化合物离子进行MRM模式的定量分析,分别配制纳克级的对照品溶液进入到质谱针泵进行打谱,在离子扫描中,羟基红花黄色素A、黄芪甲苷、大黄酸化合物在负离子模式下的响应值明显高于正离子模式下的响应值,丹参素、毛蕊异黄酮、丹参酮ⅡA和大黄素在正负离子模式下的响应值相差不大,因此选择用[M-H]-模式进行检测。每个化合物离子对的最优DP和CE列于表 1中。
通过将不同的电解质(醋酸铵、甲酸以及乙酸)加入流动相考察对各化合物峰形及响应值变化的影响,结果显示,甲酸优于乙酸和醋酸铵。进一步对甲酸在流动相中的比例进行考察,发现0.05%甲酸水溶液能使被测成分达到稳定的响应值和最佳的分离效果。同时对甲醇和乙腈进行了对比,结果都能得到良好的峰形和分离度,但乙腈毒性大,价格高[15],所以选择甲醇和0.05%甲酸水溶液作为流动相进行梯度洗脱。
本试验采用的是Phenomenex Kinetex XB-C18(2.1 mm×50 mm,2.6 μm)色谱柱,肾康注射液中的7个成分在5 min内被完全分离,时间短、效率高,并且减少了溶剂的消耗,可以达到快速分离的目的。
肾康注射液是由大黄、黄芪、红花和丹参4味药组成的中药注射液,自2005年上市以来,临床用于治疗糖尿病肾病,疗效良好[16-17],并能明显降低慢性肾功能衰竭患者尿素氮、血肌酐,可有效改善患者临床症状,延缓肾功能衰竭的进程[18],值得临床推广。中国药典目前还没有肾康注射液的质量规范,为全面有效控制肾康注射液的质量,本文采用UPLC-MS技术建立有效成分定量测定的方法,可在短时间内(5 min)准确、快速地分析测定肾康注射液中7个有效成分,为肾康注射液的质量控制提供了有效的检测手段。
| [1] |
叶烨, 丁邦晗, 王洁, 等. 肾康注射液临床应用真实世界研究[J]. 新中医, 2014, 46(10): 79. YE Y, DING BH, WANG J, et al. Clinical application of Shenkang injection in the real world[J]. J New Chin Med, 2014, 46(10): 79. |
| [2] |
宁泽琼, 乔逸, 白娟, 等. 肾康注射液治疗早期糖尿病肾病的Meta分析[J]. 陕西中医学院学报, 2015, 30(5): 595. NING ZQ, QIAO Y, BAI J, et al. Treatment of early diabetic nephropathy with Shenkang injection:a Meta-analysis[J]. J Shaanxi Coll Tradit Chin Med, 2015, 30(5): 595. |
| [3] |
廉江平, 韩珊, 方志远, 等. 肾康注射液治疗慢性肾衰竭的有效性和安全性[J]. 中成药, 2015, 37(8): 1677. LIAN JP, HAN S, FANG ZY, et al. Effects of Shenkang injection on chronic renal failure:a meta-analysis[J]. Chin Tradit Pat Med, 2015, 37(8): 1677. |
| [4] |
楚加元. 肾康注射液药理及临床研究进展综述[J]. 现代中药研究与实践, 2014, 28(2): 76. CHU JY. Review on the pharmacology and clinical research progress of Shenkang injection[J]. Res Pract Chin Med, 2014, 28(2): 76. |
| [5] |
王昱, 熊柱凤. 肾康注射液治疗老年早期糖尿病肾病的疗效及对患者免疫功能的影响[J]. 中国老年学杂志, 2015, 35(22): 6370. WANG Y, XIONG ZF. Therapeutic effect and immune function of Shenkang injection on senile patients with early diabetic nephropathy[J]. Chin J Gerontol, 2015, 35(22): 6370. DOI:10.3969/j.issn.1005-9202.2015.22.024 |
| [6] |
徐守竹, 谢艳华, 张晓卫, 等. RP-HPLC法同时测定肾康注射液中5种蒽醌类成分[J]. 中成药, 2013, 35(1): 90. XU SZ, XIE YH, ZHANG XW, et al. Simultaneous determination of five anthraquinones in Shenkang injection by RP-HPLC[J]. Chin Tradit Pat Med, 2013, 35(1): 90. |
| [7] |
万丽, 刘友平, 李明权. 肾康注射液中蒽醌类成分含量测定[J]. 时珍国医国药, 1999, 10(4): 244. WANG L, LIU YP, LI MQ. Determination of anthraquinones in Shenkang injection[J]. Lishizhen Med Mater Med Res, 1999, 10(4): 244. |
| [8] |
万丽, 刘友平, 李明权. 肾康注射液的薄层鉴别和大黄素含量测定[J]. 华西药学杂志, 1999, 14(1): 50. WANG L, LIU YP, LI MQ. TLC identification and content determination of emodin in Shenkang injection[J]. West China J Pharm Sci, 1999, 14(1): 50. |
| [9] |
汪世英, 曹成顺. HPLC法测定肾康注射液中原儿茶醛含量[J]. 药物分析杂志, 1999, 19(2): 121. WANG SY, CAO CS. Determination of protocatechuic aldehyde in Shenkang injection by HPLC[J]. Chin J Pharm Anal, 1999, 19(2): 121. |
| [10] |
刘珊, 杨涛, 刘成海. UPLC-MS/MS法同时测定扶正化瘀胶囊中12种成分[J]. 中草药, 2014, 45(2): 214. LIU S, YANG T, LIU CH. Simultaneous determination of 12 major components in Fuzheng Huayu capsules by UPLC-MS/MS[J]. Chin Tradit Herb Drugs, 2014, 45(2): 214. DOI:10.7501/j.issn.0253-2670.2014.02.012 |
| [11] |
刘杰, 许文, 李煌, 等. UPLC-MS/MS法同时测定白芍饮片中10种成分[J]. 药物分析杂志, 2015, 35(4): 635. LIU J, XU W, LI H, et al. Simultaneous determination of ten components in Radix Paeoniae Alba pieces by UPLC-MS/MS[J]. Chin J Pharm Anal, 2015, 35(4): 635. |
| [12] |
宋洋, 冯雪松. 无梗五加根化学成分的UPLC-MS/MS分析及与细柱五加、刺五加的比较[J]. 药物分析杂志, 2014, 34(6): 964. SONG Y, FENG XS. UPLC-MS/MS analysis of the constituents in the roots of A.sessiliflorus and comparison with A.gracilistylus and A.senticosus[J]. Chin J Pharm Anal, 2014, 34(6): 964. |
| [13] |
吴茵, 魏欣, 张黎媛, 等. HPLC-MS/MS法同时测定参麦注射液7种主要有效成分[J]. 中草药, 2014, 45(18): 2625. WU Y, WEI X, ZHANG LY, et al. Simultaneous determination of seven components in Shenmai injection by HPLC-MS/MS[J]. Chin Tradit Herb Drugs, 2014, 45(18): 2625. DOI:10.7501/j.issn.0253-2670.2014.18.010 |
| [14] |
陈安珍, 杨钊, 王尊文. UPLC-MS/MS法检测镇静安神类中药制剂及保健品中添加的化学药品[J]. 中国药事, 2010, 24(4): 383. CHEN AZ, YANG Z, WANG ZW. Detection of illegal mixture in traditional Chinese medicines preparation and health foods of phenobarbital by UPLC-MS/MS[J]. Chin Pharm Aff, 2010, 24(4): 383. |
| [15] |
刘灵改, 支旭然, 任非, 等. HPLC同时测定防芷鼻咽颗粒中的丹皮酚和木兰脂素[J]. 华西药学杂志, 2014, 29(3): 313. LIU LG, ZHI XR, REN F, et al. Simultaneous determination of paeonol and magnolin in Fangzhi nasopharyngeal granule by HPLC[J]. West China J Pharm Sci, 2014, 29(3): 313. |
| [16] |
高丽梅. 肾康注射液治疗2型糖尿病肾病的疗效和安全性[J]. 中国医学工程, 2011, 19(11): 134. GAO LM. Efficacy and safety of Shenkang injection in the treatment of type 2 diabetic nephropathy[J]. China Med Eng, 2011, 19(11): 134. |
| [17] |
谢欣颖, 张萌, 张莹莹, 等. 肾康注射液治疗Ⅲ期糖尿病肾病的Meta分析[J]. 中华中医药杂志, 2015, 30(10): 3676. XIE XY, ZHANG M, ZHANG YY, et al. Meta analysis on efficacy of Shenkang injection in treating stage Ⅲ diabetic nephropathy[J]. China J Tradit Chin Med Pharm, 2015, 30(10): 3676. |
| [18] |
张宇, 宋佳, 黄琳红, 等. 肾康注射液对高血压肾病大鼠肾脏的保护作用[J]. 西北药学杂志, 2014, 29(1): 42. ZHANG Y, SONG J, HUANG LH, et al. Protective effect of Shenkang injections on kidney function of hypertensive renal damage rats[J]. Northwest Pharm J, 2014, 29(1): 42. |
 2017, Vol. 37
2017, Vol. 37 
