文章信息
- 严绍裕
- YAN Shaoyu
- 供镁水平对杉木幼苗不同器官营养元素含量的影响
- Effect of different magnesium treatments on nutrient element content in different organs of Chinese fir (Cunninghamia lanceolata) seedlings
- 亚热带农业研究, 2018, 14(2): 116-121
- Subtropical Agriculture Research, 2018, 14(2): 116-121.
- DOI: 10.13321/j.cnki.subtrop.agric.res.2018.02.008
-
文章历史
- 收稿日期: 2018-04-17
镁是植物生长和发育所必需的营养元素, 作用仅次于氮、磷、钾[1], 是构成叶绿素的主要成分之一, 直接参与光合作用[2], 且对植物碳、氮的代谢具有重要作用[3]。我国镁资源丰富, 但土壤缺镁严重[4], 特别是南方地区, 随着酸沉降的加重, 土壤中镁不断风化、淋失, 导致其供镁能力下降, 从而影响植物的生长和发育, 降低植物的产量和品质[5]。目前, 国内外对植物镁元素的研究逐渐增多, 且多集中在镁对植物光合色素和光合特性影响等方面。适量镁肥有利于黄瓜生长量和光合生理指标的提高[6-7]; 镁过量处理可显著降低橘橙叶绿素含量[8]; 过量的镁添加会降低烟草的叶绿素含量[9]。N:P是衡量植物生长的限制性元素[10], 常作为植物养分限制因素的判断标准。但目前有关镁对植物器官养分元素含量影响的研究较少。
杉木[Cunninghamia lanceolata (Lamb.) Hook.]是我国南方重要的造林树种[11], 部分种植区域缺镁严重。当前有关镁对杉木养分元素、酶活性和生长发育等影响的研究鲜见报道。基于此, 本研究以1年生杉木无性系020为试材, 进行不同Mg浓度处理, 探讨不同器官(根、茎、叶)中营养元素的分布及N:P, 揭示杉木对不同浓度镁处理的响应, 以期为杉木更科学、合理的培育提供依据。
1 材料与方法 1.1 试验材料供试材料为1年生无性系020杉木幼苗, 由福建省顺昌县洋口国有林场提供。平均株高20.8 cm, 平均地径0.46 cm。
1.2 试验设计2017年3月选取长势一致且健康的1年生无性系020杉木幼苗, 采用体积比为3:1的沙与珍珠岩基质培养。选用上端内径12 cm、下端内径8 cm、高12 cm的塑料盆作为盆栽容器, 各塑料盆内填充2/3基质。每盆栽种1株幼苗, 置于温室内(温度27 ℃, 湿度65%)。在幼苗生长的1个月适应期内, 每隔2 d均匀浇灌100 mL营养液, 营养液配方参照文献[12]。
驯化1个月后(杉木开始抽梢)进行缺镁、高镁和正常供镁(对照, CK)处理。镁以MgSO4形态加入营养液, 施用量分别为0、3、1 mmol·L-1, 缺镁处理采用Na2SO4补充SO42-以维持离子浓度的平衡和避免S元素的缺乏。每个处理随机选取20株幼苗, 共60株, 并在抽梢处进行编号标记, 每隔2 d浇灌100 mL不同浓度MgSO4营养液, 每隔15 d用去离子水淋洗1次, 以防止基质中盐分积累。
1.3 样品采集不同浓度镁处理16周(当年生叶片发育成熟)后进行样品采集。每个处理取12株幼苗(平均株高19.85 cm, 平均地径0.41 cm), 每4株混合为1个重复, 共3个重复。按根、茎与叶分别取样, 选取新抽梢的成熟叶片为新叶, 茎为新茎; 取1年生叶片为老叶, 茎为老茎; 取已木质化(灰色)且直径>1 mm的根为老根, 未木质化(白色)且直径 < 1 mm的根为新根, 未木质化(白色)且直径>1 mm的根不进行取样。样品用去离子水洗净, 放入烘箱中105 ℃杀青30 min, 调节烘箱温度至75 ℃, 烘干至恒重, 粉碎后进行养分测定。
1.4 测定方法采用硫酸—高氯酸消煮[13]后, 根据ICP-AES法, 用Perkin ICP-MS 8000(美国Perkin Elmer公司)测定样品P、K和Mg含量。将已粉碎样品过0.149 mm筛, 采用全自动元素分析仪Vario Macro Cube(德国Elementar公司)测定N含量。
1.5 统计与分析采用SPSS 18.0和Excel 2003软件进行统计与分析。采用单因素方差分析检验各器官不同处理间的差异性。采用SPSS 18.0进行双因素方差分析。
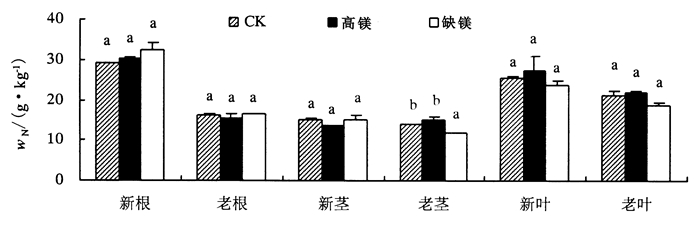
2 结果与分析 2.1 镁处理对杉木幼苗营养元素含量的影响 2.1.1 N含量如图 1所示, 新根、新叶和老叶中N含量均较高, 老根、新茎和老茎中较低。高镁处理不同器官N含量依次为:新根>新叶>老叶>老根>老茎>新茎; 缺镁与CK处理N含量依次为:新根>新叶>老叶>老根>新茎>老茎。不同镁处理下, 新根N含量依次为:缺镁>高镁>CK; 老根和新茎N含量依次为:缺镁>CK>高镁; 老茎、新叶和老叶N含量依次为:高镁>CK>缺镁。老茎缺镁处理N含量与高镁处理及CK差异达显著水平, 其他器官各处理间差异均不显著。
|
图 1 不同镁处理下杉木幼苗各器官N含量 Figure 1 The nitrogen (N) content in various organs of Chinese fir seedlings under different magnesium treatments |
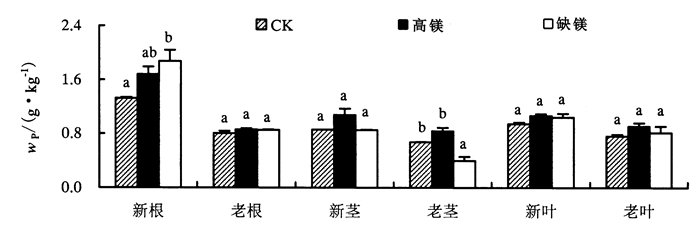
如图 2所示, 新根P含量较高, 其他器官较低。不同镁处理下, 新根P含量大小依次为:缺镁>高镁>CK; 老根P含量则表现为:高镁>缺镁>CK; 新茎、老茎、新叶和老叶P含量均为高镁处理最高, 其中新叶和老叶P含量依次为:高镁>缺镁>CK; 新茎和老茎P含量表现为:高镁>CK>缺镁, 且老茎缺镁处理P含量与高镁处理及CK差异达显著水平。
|
图 2 不同镁处理下杉木幼苗各器官P含量 Figure 2 The phosphorus (P) content in various organs of Chinese fir seedlings under different magnesium treatments |
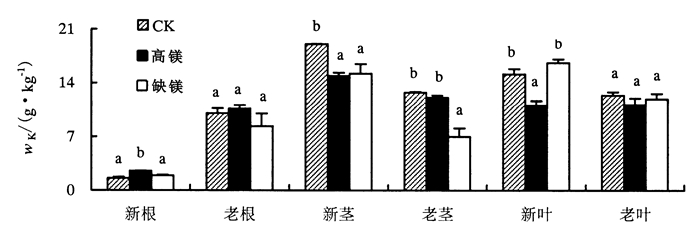
如图 3所示, 新根K含量较低, 其他器官均较高。CK处理中, 不同器官K含量表现为:新茎>新叶>老茎>老叶>老根>新根; 高镁处理则表现为:新茎>老茎>老叶>新叶>老根>新根; 缺镁处理表现为:新叶>新茎>老叶>老根>老茎>新根。
|
图 3 不同镁处理下杉木幼苗各器官K含量 Figure 3 The potassium (K) content in various organs of Chinese fir seedlings under different magnesium treatments |
不同镁处理下, 老根K含量表现为:高镁>CK>缺镁, 新根K含量则表现为:高镁>缺镁>CK, 其中新根高镁处理K含量与缺镁处理及CK差异达显著水平; 新叶和老叶K含量在缺镁中较高, 高镁较低, 其中新叶高镁处理K含量与缺镁处理及CK差异达显著水平; 新茎K含量依次为:CK>缺镁>高镁, 老茎K含量为:CK>高镁>缺镁, 其中, 新茎高镁处理、缺镁处理K含量与CK差异均达显著水平; 老茎缺镁处理K含量与高镁处理及CK差异均达显著水平。
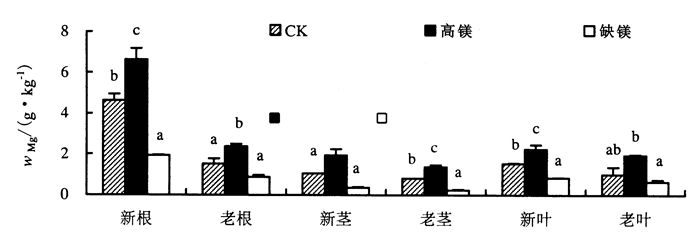
2.1.4 Mg含量如图 4所示, 新根中Mg含量较高, 其他器官则较低。CK与高镁处理中不同器官Mg含量表现为:新根>新叶>老根>新茎>老叶>老茎; 缺镁处理Mg含量依次为:新根>老根>新叶>老叶>新茎>老茎。
|
图 4 不同镁处理下杉木幼苗各器官Mg含量 Figure 4 The magnesium (Mg) content in various organs of Chinese fir seedlings under different magnesium treatments |
不同镁处理下, 各器官Mg含量均随Mg浓度的提高而上升, 即高镁>CK>缺镁。其中, 新根、新叶和老茎Mg含量各处理间差异达显著水平; 新茎和老根高镁处理Mg含量与缺镁处理及CK差异达显著水平; 老叶Mg含量在缺镁和高镁处理下差异显著, 而其他处理间差异未达显著水平。
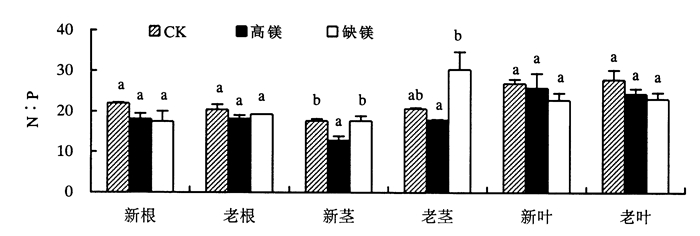
2.2 镁处理对杉木不同器官N:P的影响如图 5所示, 不同处理下杉木不同器官N:P变化特征不同。CK处理下各器官N:P均为:老叶>新叶>新根>老茎>老根>新茎; 高镁处理为:新叶>老叶>老根>新根>老茎>新茎; 缺镁处理为:老茎>老叶>新叶>老根>新茎>新根。
|
图 5 不同镁处理下杉木幼苗各器官N:P特征 Figure 5 The N:P ratio in various organs of Chinese fir seedling under different magnesium treatments |
不同镁处理下, 新叶、老叶和新根N:P表现出相似规律性, 即CK>高镁>缺镁; 新茎和老茎N:P均为:缺镁>CK>高镁, 其中新茎高镁处理N:P与缺镁处理及CK差异达显著水平; 老根N:P比则表现为:CK>缺镁>高镁。
2.3 不同镁处理和不同器官对杉木幼苗营养元素含量及N:P的差异性分析如表 1所示, 杉木N含量不同器官、不同处理以及不同器官和不同处理交互作用的离差平方和分别为1 440.99、6.49和51.52, 即杉木N含量的变异主要受不同器官的影响, 其次为不同器官和不同处理交互作用的影响, 受不同处理的影响最小。P、K含量和N:P比受不同器官的影响最大, 不同器官和不同处理交互作用的影响次之, 不同处理的影响最小。Mg含量主要受不同器官的影响, 其离差平方和为52.12, 其次为不同处理的影响, 离差平方和为23.83, 受不同器官和不同处理交互作用的影响最小。
| 参数 | 变异来源 | 离差平方和 | Df | 均方 | F | P |
| N | 器官 | 1 440.99 | 5 | 288.20 | 62.90 | 0.000 |
| 处理 | 6.49 | 2 | 3.24 | 0.71 | 0.504 | |
| 器官×处理 | 51.52 | 10 | 5.15 | 1.13 | 0.390 | |
| 误差 | 96.21 | 21 | 4.58 | - | - | |
| P | 器官 | 3.49 | 5 | 0.70 | 90.29 | 0.000 |
| 处理 | 0.20 | 2 | 0.10 | 12.97 | 0.000 | |
| 器官×处理 | 0.43 | 10 | 0.04 | 5.57 | 0.000 | |
| 误差 | 0.16 | 21 | 0.01 | - | - | |
| K | 器官 | 777.46 | 5 | 155.49 | 150.76 | 0.000 |
| 处理 | 20.58 | 2 | 10.29 | 9.98 | 0.000 | |
| 器官×处理 | 98.64 | 10 | 9.86 | 9.56 | 0.001 | |
| 误差 | 21.66 | 21 | 1.03 | - | - | |
| Mg | 器官 | 52.12 | 5 | 10.43 | 129.23 | 0.000 |
| 处理 | 23.83 | 2 | 11.91 | 147.68 | 0.000 | |
| 器官×处理 | 9.72 | 10 | 0.97 | 12.05 | 0.000 | |
| 误差 | 1.69 | 21 | 0.08 | - | - | |
| N:P | 器官 | 454.20 | 5 | 90.84 | 10.39 | 0.000 |
| 处理 | 62.71 | 2 | 31.36 | 3.59 | 0.046 | |
| 器官×处理 | 224.50 | 10 | 22.45 | 2.57 | 0.033 | |
| 误差 | 183.57 | 21 | 8.74 | - | - |
养分元素的积累和分配反映了一定生态环境下, 植物对某些养分元素的需求和吸收能力, 体现了植物与环境之间的关系[14-15]。N:P是衡量植物生长的限制因子[16]。本研究表明, 杉木不同器官N、P、K、Mg含量和N:P对不同浓度镁处理的响应机理不同。杉木各器官N、P、K含量和N:P在不同处理间的规律性特征不同, Mg含量均随Mg浓度的提高而上升。不同镁处理和不同器官对杉木N、P、K、Mg含量和N:P影响的方差分析表明, 杉木N、P、K含量及N:P的变异受不同器官的影响较大, 其次为不同器官和不同处理的交互影响, 受不同处理的影响较小; Mg含量主要受不同器官的影响, 其次为不同处理, 受不同器官和不同处理交互作用的影响最小。
植物不同器官养分元素含量的变化, 除受养分元素供给水平和外界环境影响外, 也与其生长节律和结构特性相关[17-18]本研究发现, 不同浓度镁处理下杉木各器官的养分元素含量存在差异, 但新根各处理下的N、P、K和Mg含量均高于其他器官, 老根各养分元素含量与其他器官相比均较低, 可能由于根是植物养分元素吸收和输送的通道[19], 且新根吸收能力高于老根。叶片是植物进行光合作用和吸收营养元素的主要器官, 新陈代谢旺盛[20]。本研究中, 新叶和老叶N、Mg含量均高于新茎和老茎, 且其含量均随Mg浓度的提高而上升; P、K含量与新茎基本一致, 其中, K含量随Mg浓度的提高而降低, 可能由于镁与钾之间既存在协同作用, 也存在拮抗作用[21]。Mg浓度的提高会抑制叶片对钾的吸收, 与Chapagain et al[22]对番茄的研究结果一致。茎是连接地下吸收器官和地上同化组织的传导器官, 作为养分传输通道, 茎中养分储存较少[23], 本研究中茎表现出K含量随Mg浓度的提高而降低, 其中老茎的表现更为明显。
本研究仅探讨不同供镁水平对杉木幼苗根、茎、叶营养元素及N:P的影响, 但镁对于杉木不同生长时期各器官营养元素及其N:P的影响, 以及各器官之间养分元素的分配机理有待进一步深入探讨。
| [1] | 李延, 刘星辉, 庄卫民. 植物Mg素营养生理的研究进展[J]. 福建农业大学学报, 2000, 29(1): 74–80. |
| [2] | WALKER C J, WEINSTEIN J D. Further characterization of the magnesium chelatase in isolated developing cucumber chloroplasts:substrate specificity, regulation, intactness, and ATP requirements[J]. Plant Physiology, 1991, 95(4): 1189–1196. DOI: 10.1104/pp.95.4.1189 |
| [3] | 刘雪琴, 石孝均, 詹风, 等. 浅谈营养元素镁[J]. 湖南农业科学, 2005(6): 41–43. |
| [4] | 朱帅. 镁对低温弱光下黄瓜光合作用的调控研究[D]. 泰安: 山东农业大学, 2014. |
| [5] | 李延, 刘星辉. 缺镁胁迫对龙眼叶片衰老的影响[J]. 应用生态学报, 2002, 13(3): 311–314. |
| [6] | 李泽, 谭晓风, 卢锟, 等. 供镁水平对油桐幼苗生长及光合特性的影响[J]. 生态学杂志, 2015, 34(9): 2440–2447. |
| [7] | HERMANS C, VERBRUGGEN N. Physiological characterization of Mg deficiency in Arabidopsis thaliana[J]. Journal of Experimental Botany, 2005, 56(418): 2153–2161. DOI: 10.1093/jxb/eri215 |
| [8] | 申燕, 肖家欣, 杨慧, 等. 镁胁迫对'春见'橘橙生长和矿质元素分布及叶片超微结构的影响[J]. 园艺学报, 2011, 38(5): 849–858. |
| [9] | 凌丽俐, 黄翼, 彭良志, 等. 镁缺乏和过量胁迫对纽荷尔脐橙叶绿素荧光特性的影响[J]. 生态学报, 2014, 34(7): 1672–1680. |
| [10] | AERTS R. Interspecific competition in natural plant communities:mechanisms, trade-offs and plant-soil feedbacks[J]. Journal of Experimental Botany, 1999, 50(330): 29–37. DOI: 10.1093/jxb/50.330.29 |
| [11] | 俞新妥. 杉木栽培学[M]. 福州: 福建科学技术出版社, 1997: 1-8. |
| [12] | PENG H Y, QI Y P, LEE J, et al. Proteomic analysis of Citrus sinensis roots and leaves in response to long-term magnesium-deficiency[J]. BMC Genomics, 2015, 16: 253. DOI: 10.1186/s12864-015-1462-z |
| [13] | 中国林业科学研究院林业研究所. 森林植物与森林枯枝落叶层全氮、磷、钾、钠、钙、镁的测定: LY/T 1271-1999[S]. 北京: 中国标准出版社, 1999. |
| [14] | 毛庆功, 鲁显楷, 陈浩, 等. 陆地生态系统植物多样性对矿质元素输入的响应[J]. 生态学报, 2015, 35(17): 5884–5897. |
| [15] | 金茜, 王瑞, 周向睿, 等. 水淹胁迫对紫穗槐生长及营养元素积累的影响[J]. 草业科学, 2013, 30(6): 904–909. |
| [16] | GÜSEWELL S. N:P ratios in terrestrial plants:variation and functional significance[J]. New Phytologist, 2004, 164(2): 243–266. DOI: 10.1111/j.1469-8137.2004.01192.x |
| [17] | HENDRICKSON O Q, CHATARPAUL L, BURGESS D. Nutrient cycling following whole-tree and conventional harvest in northern mixed forest[J]. Canadian Journal of Forest Research, 1989, 19(6): 725–735. DOI: 10.1139/x89-112 |
| [18] | BALDWIN D S, REES G N, MITCHELL A M, et al. The short-term effects of salinization on anaerobic nutrient cycling and microbial community structure in sediment from a freshwater wetland[J]. Wetlands, 2006, 26(2): 455–464. DOI: 10.1672/0277-5212(2006)26[455:TSEOSO]2.0.CO;2 |
| [19] | 赵亚芳, 徐福利, 王渭玲, 等. 华北落叶松根茎叶碳氮磷含量及其化学计量学特征的季节变化[J]. 植物学报, 2014, 49(5): 560–568. |
| [20] | 赵生龙, 曾凡江, 张波, 等. 不同干扰处理对骆驼刺茎、叶、刺器官化学计量特征的影响[J]. 干旱区研究, 2017, 34(4): 837–846. |
| [21] | 郑重禄. 缺镁胁迫对柑橘的影响研究综述(3)——缺镁对柑橘酶活性及其他生理生化的影响[J]. 浙江柑橘, 2015, 32(4): 4–9. |
| [22] | CHAPAGAIN B P, WIESMAN Z. Effect of potassium magnesium chloride in the fertigation solution as partial source of potassium on growth, yield and quality of greenhouse tomato[J]. Scientia Horticulturae, 2004, 99(3/4): 279–288. |
| [23] | 李合生. 现代植物生理学[M]. 3版. 北京: 高等教育出版社, 2012. |
 2018,Vol. 14
2018,Vol. 14

