文章信息
- 钱军, 陈侯鑫, 田蜜, 李敦禧, 郭霞
- QIAN Jun, CHEN Houxin, TIAN Mi, LI Dunxi, GUO Xia
- 超临界CO2萃取腺叶桂樱精油的工艺优化
- Optimization of supercritical CO2 extraction of essential oil from Laurocerasus phaeosticta
- 亚热带农业研究, 2018, 14(2): 73-77
- Subtropical Agriculture Research, 2018, 14(2): 73-77.
- DOI: 10.13321/j.cnki.subtrop.agric.res.2018.02.001
-
文章历史
- 收稿日期: 2018-03-20
腺叶桂樱(Laurocerasus phaeosticta)为蔷薇科(Rosaceae)桂樱属(Laurocerasus)常绿乔木, 别名腺叶野樱、墨点樱桃、腺叶稠李。我国主要分布在南方, 如湖南、广东、云南、海南等地。腺叶桂樱国内研究报道较少, 仅在植被调查中发现其为林下演替更新层树种[1-2]。该属植物可以选用组培、种子及扦插进行繁殖[3-5]。国外药理活性研究表明, 桂樱属植物富含酚类、黄酮类等物质[6-7], 有较好的消炎、镇痛[8]、抗氧化[9]和抑制胆碱酯酶活性等功效。
植物精油又称液体黄金, 是一些小分子、易挥发的油状物质[10]。植物精油在医药[11]、化妆品[12]、食品[13]和农业防治[14-15]等方面得到广泛的应用。植物精油常见的提取方法有水蒸气蒸馏法、溶剂提取法、超临界CO2流体萃取法等。因自动化程度高、操作程序化简单且精油回收直接, 超临界CO2流体萃取法得到广泛应用[16]。基于腺叶桂樱叶片具有一股浓烈的特殊气味, 推测该植物中富含精油。为了充分挖掘腺叶桂樱精油的应用价值, 本试验利用超临界CO2流体技术, 采用目前最常用的正交试验设计方法[17], 设计四因素三水平萃取其叶片中的精油, 优化提取工艺, 以期为腺叶桂樱的开发利用提供参考。
1 材料与方法 1.1 供试材料 1.1.1 供试原料腺叶桂樱叶片采自海南省枫木实验林场(北纬19°12′15.57″, 东经109°57′38.71″)。洗净、晾干、粉碎, 过60目筛, 备用。
1.1.2 试剂与仪器本试验使用超临界CO2萃取仪(SFT-100XW)、微型粉碎机(QE-700)和质量分数为99.99%的CO2进行腺叶桂樱叶片精油萃取。
1.2 供试方法 1.2.1 萃取流程将30 g腺叶桂樱叶片粉末装进物料袋中, 将物料袋放入萃取釜内。开通CO2去湿, 随后选择合适的萃取温度、萃取压力、CO2流量和萃取时间进行萃取。利用10 mL锥形试管接收精油, 并根据下式计算萃取率。
| $ {萃取率}/\% = \frac{精油质量}{腺叶桂樱叶片干粉质量} \times 100 $ | (1) |
单因素试验设置萃取温度(25、30、35、40、45、50 ℃), 萃取压力(10、15、20、25、30、35 MPa), CO2流量(6、9、12、15、18、21 mL·min-1), 萃取时间(15、25、35、45、55、65 min)共4个因素, 所有试验均重复3次。当改变单一因素则固定其他因素, 考察其对萃取率的影响。
1.2.3 正交试验设计在单因素试验的基础上, 优选出合适的萃取温度、萃取压力、CO2流量和萃取时间, 再根据四因素三水平设计正交试验。
1.3 数据分析对试验中单因素进行方差分析, 采用Duncan′s方法检验差异显著性。利用Excel软件绘图, 以及SPSS 20.0软件计算并分析试验结果。
2 结果与分析 2.1 单因素试验对萃取率的影响 2.1.1 萃取温度固定萃取压力为30 MPa、CO2流量为15 mL·min-1和萃取时间为55 min, 考察不同萃取温度(25、30、35、40、45、50 ℃)对萃取率的影响(图 1)。随着萃取温度升高, 萃取率先迅速提高, 之后降低。6个温度中, 30 ℃时萃取率最高(2.49%)。在其他因素固定的条件下, 随温度升高, 腺叶桂樱精油挥发性增强, 但CO2溶解精油的能力下降, 从而使得萃取温度与萃取率之间存在峰值关系。因此, 在30 ℃附近选择25、30、35 ℃作为正交试验的萃取温度。

|
图 1 萃取温度对腺叶桂樱叶片精油萃取率的影响 Figure 1 Effect of extraction temperature on the extraction rate of essential oil from L.phaeosticta |
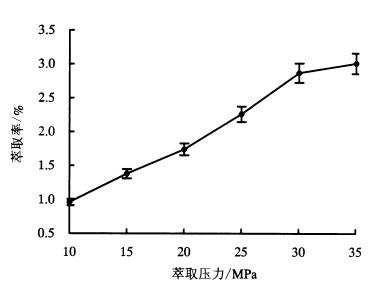
固定萃取温度为30 ℃、CO2流量为15 mL·min-1和萃取时间为55 min, 考察萃取压力(10、15、20、25、30、35 MPa)对萃取率的影响(图 2)。随着萃取压力增大, 萃取率不断提高。当萃取压力低于20 MPa时, 萃取率随压力增大而缓慢提高; 当30 MPa>萃取压力>20 MPa时, 萃取率随压力增大而迅速提高; 超过30 MPa时, 萃取率提高幅度则降低。以上说明, 增加压力, 则气体密度变大、气体液化, 有利于精油的提取; 当达到一定压力后, 气体饱和, 萃取率不再提高。因此, 选择20、25、30 MPa作为正交试验的萃取压力。
|
图 2 萃取压力对腺叶桂樱叶片精油萃取率的影响 Figure 2 Effect of extraction pressure on the extraction rate of essential oil from L.phaeosticta |
固定萃取温度为30 ℃、萃取压力为30 MPa和萃取时间为55 min, 考察CO2流量(6、9、12、15、18、21 mL·min-1)对萃取率的影响(图 3)。随着CO2流量升高, 萃取率先提高后降低。当CO2流量为15 mL·min-1时, 萃取率最高(2.43%)。由于CO2流量增加, 促进CO2与腺叶桂樱精油成分的亲和, 萃取率迅速提高; 达到饱和值后, 精油溢出降低, 导致萃取率下降。因此, 选择12、15、18 mL·min-1作为正交试验的CO2流量。

|
图 3 CO2流量对腺叶桂樱叶片精油萃取率的影响 Figure 3 Effect of CO2 flow rate on the extraction rate of essential oil from L.phaeosticta |
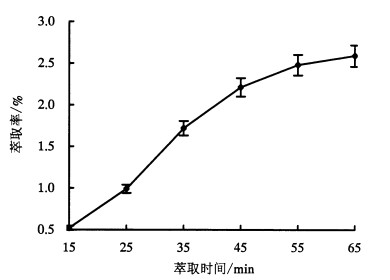
固定萃取温度为30 ℃、萃取压力为30 MPa和CO2流量为15 mL·min-1, 考察萃取时间(15、25、35、45、55、65 min)对萃取率的影响(图 4)。随着萃取时间的延长, 萃取率增幅加快; 达到55min时, 萃取率增幅减缓。随着萃取时间延长, 精油溢出可能由快变缓, 萃取率提高幅度则相应变小。因此, 选择35、45、55 min作为正交试验的萃取时间。
|
图 4 萃取时间对腺叶桂樱叶片精油萃取率的影响 Figure 4 Effect of extraction time on the extraction rate of essential oil from L.phaeosticta |
根据上述4个单因素试验的结果, 设计正交试验, 如表 1所示。
| 水平 | 因素1) | |||
| A/℃ | B/MPa | C/(mL·min-1) | D/min | |
| 1 | 25 | 20 | 12 | 35 |
| 2 | 30 | 25 | 15 | 45 |
| 3 | 35 | 30 | 18 | 55 |
| 1)A.萃取温度; B.萃取压力; C.CO2流量; D.萃取时间。 | ||||
根据四因素三水平设计, 选择L9(34)正交试验, 共设计9组试验。根据萃取率优化最佳工艺参数(表 2)。由表 2极差值(R)可知, 4个因素对萃取率的影响依次为:C>B>D>A, 即:CO2流量>萃取压力>萃取时间>萃取温度。根据各列k值大小可知, 最优组合为C3B3D3A2, 即:CO2流量18 mL·min-1、萃取时间55 min、萃取压力30 MPa和萃取温度30 ℃。在此条件下, 萃取率最理想。
| 编号 | A | B | C | D | 萃取率/% |
| 1 | 1(25) | 1(20) | 1(12) | 1(35) | 1.56 |
| 2 | 1 | 2(25) | 2(15) | 2(45) | 2.45 |
| 3 | 1 | 3(30) | 3(18) | 3(55) | 4.28 |
| 4 | 2(30) | 1 | 2 | 3 | 2.84 |
| 5 | 2 | 2 | 3 | 1 | 3.01 |
| 6 | 2 | 3 | 1 | 2 | 2.90 |
| 7 | 3(35) | 1 | 3 | 2 | 2.71 |
| 8 | 3 | 2 | 1 | 3 | 2.22 |
| 9 | 3 | 3 | 2 | 1 | 2.36 |
| k1 | 2.763 | 2.370 | 2.227 | 2.310 | |
| k2 | 2.917 | 2.560 | 2.550 | 2.687 | |
| k3 | 2.437 | 3.180 | 3.333 | 3.113 | |
| R | 0.371 | 1.077 | 1.943 | 0.969 | |
| 1)A.萃取温度; B.萃取压力; C.CO2流量; D.萃取时间。 | |||||
根据正交试验数据(表 2), 利用SPSS 20.0软件进行分析, 得到线性回归方程为:Y=0.317-0.167A+0.405B+0.553C+0.402D(N=8, P=0.024)。在最优组合C3B3D3A2条件下, 得到最优计算值为4.06%。
2.3 验证试验按照最优试验组合C3B3D3A2, 在萃取温度30 ℃、萃取压力30 MPa、CO2流量18 mL·min-1、萃取时间55 min条件下, 对30 g腺叶桂樱叶片粉末进行3次萃取, 得到平均萃取率为3.78%, 证明该优化工艺具有可靠性。
3 结论池庭飞等[18]对同属的大叶桂樱叶片进行了常压水蒸气蒸馏萃取, 得到精油的萃取率为0.15%, 远低于本试验采用的超临界CO2萃取方法的萃取率。由于易挥发的精油容易随水蒸气蒸出, 而难挥发的精油不易蒸馏出来; 精油在水中有部分溶解, 这两方面原因使得水蒸气蒸馏萃取法精油萃取率较低。超临界CO2萃取法利用超临界状态下的CO2为萃取溶剂, 辅助压力、温度等条件, 其萃取效率远高于水蒸气蒸馏, 因而萃取率较高。
本研究单因素试验中, 在其他条件不变情况下, CO2流量与萃取率的关系是先升后降, 与正交试验中CO2流量值趋势不一致。可能由于单因素试验中仅仅考虑了单个因素的变化, 而正交试验涉及4个因素同时变化, 故结果不一致。
本研究通过正交试验设计, 对萃取温度、萃取压力、CO2流量、萃取时间4个因素3个水平进行超临界CO2萃取工艺优化。结果显示, 最优组合为:CO2流量18 mL·min-1、萃取时间55 min、萃取压力30 MPa、萃取温度30 ℃。在该条件下, 得到腺叶桂樱叶的精油萃取率为3.78%。
| [1] | 姚金雨, 许娜子, 朱宁华, 等. 张家界国家森林公园生物多样性监测与森林可持续旅游对策[J]. 中南林业科技大学学报, 2011, 31(3): 191–196. |
| [2] | 许涵, 黄久香, 唐光大, 等. 南昆山观光木所在群落优势树种的种间联结性[J]. 华南农业大学学报, 2008, 29(1): 57–62. DOI: 10.7671/j.issn.1001-411X.2008.01.015 |
| [3] | 宣君华, 林夏珍. 大叶桂樱种子萌发特性试验[J]. 浙江林业科技, 2009, 29(3): 77–79. |
| [4] | 胡译文, 王瑞辉, 贺竹梅, 等. 柔毛大叶桂樱的组织培养初探[J]. 湖南林业科技, 2009, 36(6): 15–16, 21. |
| [5] | 宿静, 潘健, 汤庚国. 大叶桂樱的扦插繁殖试验[J]. 林业科技开发, 2006, 20(5): 79–80. |
| [6] | AKKOL E K, KIRMIZIBEKMEZ H, KÜÇÜKBOYACI N, et al. Isolation of active constituents from cherry laurel (Laurocerasus officinalis Roem.) leaves through bioassay-guided procedures[J]. Journal of Ethnopharmacology, 2012, 139(2): 527–532. DOI: 10.1016/j.jep.2011.11.043 |
| [7] | ORHAN I E, AKKOL E K. Estimation of neuroprotective effects of Laurocerasus officinalis Roem. (cherry laurel) by in vitro methods[J]. Food Research International, 2011, 44(3): 818–822. DOI: 10.1016/j.foodres.2011.01.037 |
| [8] | KARABEGOVIĆ I T, STOJIČEVIĆ S S, VELIČKOVIĆ D T, et al. The effect of different extraction techniques on the composition and antioxidant activity of cherry laurel (Prunus laurocerasus) leaf and fruit extracts[J]. Industrial Crops and Products, 2014, 54: 142–148. DOI: 10.1016/j.indcrop.2013.12.047 |
| [9] | KARABEGOVIĆ I T, STOJIČEVIĆ S S, VELIČKOVIĆ D T, et al. Optimization of microwave-assisted extraction and characterization of phenolic compounds in cherry laurel (Prunus laurocerasus) leaves[J]. Separation and Purification Technology, 2013, 120: 429–436. DOI: 10.1016/j.seppur.2013.10.021 |
| [10] | LIU H Y, ZHANG Y Q. Rose oil composition from the flowers of Rosa rugosa Thunb. growing in different locations of China[J]. Agricultural Science & Technology, 2012, 13(6): 1260–1262. |
| [11] | LOW P, CLARK A M, CHOU T C, et al. Immunomodulatory activity of Melaleuca alternifolia concentrate (MAC):Inhibition of LPS-induced NF-κB activation and cytokine production in myeloid cell lines[J]. International Immunopharmacology, 2015, 26(1): 257–264. DOI: 10.1016/j.intimp.2015.03.034 |
| [12] | 袁敏之. 几种植物精油的提取及其在化妆品中的应用[J]. 日用化学品科学, 1996(5): 39–41. |
| [13] | ATARÉS L, CHIRALT A. Essential oils as additives in biodegradable films and coatings for active food packaging[J]. Trends in Food Science & Technology, 2016, 48: 51–62. |
| [14] | POLATOǦLU K, KARAKOÇ Ö C, YÜCEL Y Y, et al. Insecticidal activity of Salvia veneris Hedge:essential oil against coleopteran stored product insects and Spodoptera exigua (Lepidoptera)[J]. Industrial Crops and Products, 2017, 97: 93–100. DOI: 10.1016/j.indcrop.2016.12.012 |
| [15] | 叶征美. 千层金精油的提取、成分分析、抗氧化及抗菌活性的研究[D]. 福州: 福建农林大学, 2014. |
| [16] | 戴琳, 单银花, 王志祥, 等. 超临界CO2萃取玫瑰精油的工艺优化[J]. 食品工业科技, 2015, 26(3): 266–269, 274. |
| [17] | 刘瑞江, 张业旺, 闻崇炜, 等. 正交试验设计和分析方法研究[J]. 实验技术与管理, 2010, 27(9): 52–55. |
| [18] | 池庭飞, 施小芳, 黄儒珠, 等. 大叶桂樱叶精油的化学成分初步研究[J]. 植物学通报, 1986, 4(1/2): 44–45, 78. |
 2018,Vol. 14
2018,Vol. 14

