文章信息
- 李彩霞, 郑冬梅, 林碧英, 陈艺群, 黄碧阳, 杨玉凯, 庄团达
- LI Caixia, ZHENG Dongmei, LIN Biying, CHEN Yiqun, HUANG Biyang, YANG Yukai, ZHUANG Tuanda
- 盐胁迫下外源激素对苦瓜幼苗抗逆性的影响
- Effects of exogenous hormone on stress tolerance of Momordica charantia L. seedlings under salt stress
- 亚热带农业研究, 2017, 13(3): 171-176
- Subtropical Agriculture Research, 2017, 13(3): 171-176.
- DOI: 10.13321/j.cnki.subtrop.agric.res.2017.03.006
-
文章历史
- 收稿日期: 2017-03-23
2. 福建省中科生物股份有限公司, 福建 厦门 361000
2. Fujian Zhongke Biological Limited by Share Ltd., Xiamen, Fujian 361000, China
设施蔬菜栽培采用特殊的覆盖结构进行常年生产,设施内复种指数高,施肥、灌溉及耕作频率大,因此盐分极易聚集,造成设施内土壤不同程度的次生盐渍化。盐胁迫严重影响植物生长并导致农作物减产, 近年来通过传统杂交育种、海水灌溉筛选育种、转基因获得抗盐品种,但仍未培育出大面积推广的抗盐品种[1]。研究表明,1 mmol·L-1水杨酸(salicylic acid, SA)能提高番茄抗盐能力[2];0.05 mmol·L-1脱落酸(abscisic acid, ABA)可减轻环境胁迫对番茄的伤害[3];50 mg·L-1赤霉素(gibberellin, GA3)可缓解盐胁迫对大豆根系的伤害[4]。而对ABA、SA与GA3缓解盐胁迫程度进行比较的相关报道较少。
苦瓜(Momordica charantia L.)属于葫芦科苦瓜属1年生攀缘草本植物,原产于亚洲热带地区,广泛分布于热带、温带及亚热带地区。苦瓜具有促进食欲、利尿活血、消炎退热、解疲劳、清心明目的功效[5-7]。近年来设施种植面积逐年扩大,针对设施生产上返盐现象严重,本研究通过研究喷施ABA、SA和GA3对盐胁迫下苦瓜幼苗形态及生理生化的影响,以期筛选出缓解盐胁迫的最佳外源激素种类及浓度,为利用外源激素缓解盐分胁迫提供依据,提高盐渍土地的利用效率。
1 材料与方法 1.1 试验材料供试品种为佳美苦瓜,由福州市农福种苗有限公司提供。
1.2 试验设计试验于2016年10月—2017年1月在福建农林大学温室及蔬菜生理生化实验室中进行。将苦瓜种子在55 ℃温水中浸种20 min后,置清水中浸泡12 h,之后放入28 ℃恒温箱中催芽,待70%以上露白后,播到72孔穴盘中。待幼苗长至两叶一心时,选取长势均匀一致的苦瓜苗移栽于装有混合基质(草炭:蛭石:珍珠岩=3:1:1) 的营养钵(8 cm×10 cm)中,待苗长至四叶一心时进行盐胁迫处理。
盐胁迫即在第1天浇灌50 mL 40 mmol·L-1 NaCl,第4天浇灌50 mL 75 mmol·L-1 NaCl,第7天浇灌50 mL 100 mmol·L-1 NaCl,之后每3天浇灌50 mL 100 mmol·L-1 NaCl。在盐胁迫浓度达到100 mmol·L-1之后,第3、6、9天喷施3种外源激素,早晚各喷1次,喷施程度以叶面均匀布满雾状水滴为宜。即处理1:100 mmol·L-1 NaCl+0.05 mmol·L-1 ABA(A1);处理2:100 mmol·L-1 NaCl+1 mmol·L-1 SA(A2);处理3:100 mmol·L-1 NaCl+50 mg·L-1 GA3(A3),本试验设2个对照:清水处理(CK1)、100 mmol·L-1 NaCl处理(CK2)。激素处理结束后第7、14、21天进行形态、生理生化指标的测定,每个处理15盆,每盆1株。
1.3 测定方法 1.3.1 形态指标随机选取长势一致的植株,分别在外源激素处理后第7、14、21天测量地上、地下鲜重。壮苗指数=(茎粗/株高)×全株干重。
1.3.2 生理生化指标丙二醛(malondialdehyde, MDA)含量测定采用硫代巴比妥酸法;可溶性糖含量的测定采用蒽酮比色法;可溶性蛋白质含量的测定采用考马斯亮蓝G-250法;叶绿素采用丙酮乙醇浸提液提取法;脯氨酸的测定采用磺基水杨酸法[8]。
1.4 统计与分析采用DPS 7.05软件进行方差分析,用Duncan新复极差法进行差异显著性分析。
2 结果与分析 2.1 盐胁迫下外源激素对苦瓜幼苗形态指标的影响 2.1.1 壮苗指数从表 1可见,喷施外源激素7 d,CK2壮苗指数与各处理没有显著性差异;随着胁迫时间的延长,第14天A1、A2、A3处理间无显著性差异,而与CK1差异性显著;第21天A3与其他处理间差异显著,A3壮苗指数最大(0.060),比CK2高0.020,比CK1低0.044。以上说明,盐胁迫条件下幼苗长势较弱,A3处理缓解盐胁迫效果较明显。
| 处理 | 壮苗指数 | ||
| 7 d | 14 d | 21 d | |
| A1 | 0.091±0.009a | 0.069±0.014bc | 0.053±0.002c |
| A2 | 0.063±0.009b | 0.052±0.007c | 0.048±0.003c |
| A3 | 0.067±0.013b | 0.062±0.002bc | 0.060±0.004b |
| CK1 | 0.093±0.017a | 0.091±0.014a | 0.104±0.007a |
| CK2 | 0.075±0.011ab | 0.074±0.007ab | 0.040±0.001d |
| 1)A1.100 mmol·L-1 NaCl+0.05 mmol·L-1 ABA; A2.100 mmol·L-1 NaCl+1 mmol·L-1 SA; A3.100 mmol·L-1 NaCl+50 mg·L-1 GA3; CK1.清水; CK2.100 mmol·L-1 NaCl。同列数值后附不同小写字母者表示差异达0.05显著水平。 | |||
从表 2可见, 在整个生长过程中CK2地上鲜重明显低于CK1,随着盐胁迫时间的延长,地上部分受抑制程度明显增加,地上物质积累减少, 第7、14、21天CK2分别比CK1低0.333、0.350、0.440 g。第21天,A1、A2、A3处理地上鲜重大于CK2,其大小依次为:A3>CK1>A1>A2>CK2。在整个处理期间,A3地上鲜重显著高于CK1。以上说明,喷施外源激素在不同程度上缓解了盐害对苦瓜的胁迫作用,喷施GA3明显促进苦瓜幼苗茎叶的生长,同时对苦瓜的生长具有重要调控作用。在喷施外源激素第7天,除了A2处理,CK2地下鲜重显著低于其他处理,分别比CK1、A1、A2、A3低0.251、0.230、0.090、0.147 g。随着盐胁迫时间的延长, 地下鲜重各处理间差异不显著,由此推测苦瓜幼苗根对短期盐胁迫响应不灵敏。
| g | |||||||
| 处理 | 地上鲜重 | 地下鲜重 | |||||
| 7 d | 14 d | 21 d | 7 d | 14 d | 21 d | ||
| A1 | 2.143±0.068c | 2.190±0.020c | 2.517±0.070c | 0.730±0.079ab | 1.141±0.434a | 1.237±0.325a | |
| A2 | 2.087±0.124c | 2.167±0.081c | 2.403±0.06cd | 0.590±0.056cd | 0.934±0.496a | 0.940±0.380a | |
| A3 | 2.510±0.044a | 2.760±0.108a | 3.237±0.142a | 0.647±0.038bc | 0.980±0.151a | 1.012±0.516a | |
| CK1 | 2.320±0.090b | 2.497±0.099b | 2.713±0.025b | 0.751±0.056a | 1.216±0.365a | 1.152±0.416a | |
| CK2 | 1.987±0.120c | 2.147±0.049c | 2.273±0.032d | 0.500±0.018d | 0.551±0.018a | 0.703±0.209a | |
| 1)A1.100 mmol·L-1 NaCl+0.05 mmol·L-1 ABA; A2.100 mmol·L-1 NaCl+1 mmol·L-1 SA; A3.100 mmol·L-1 NaCl+50 mg·L-1 GA3; CK1.清水; CK2.100 mmol·L-1 NaCl。同列数值后附不同小写字母者表示差异达0.05显著水平。 | |||||||
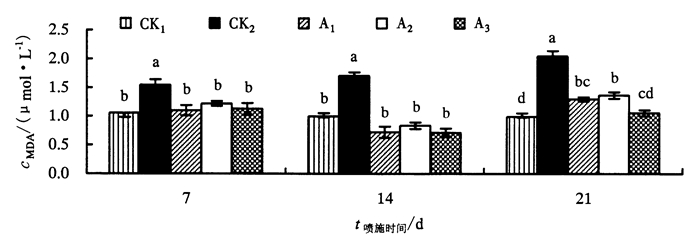
MDA含量通常作为脂质过氧化指标,表示细胞膜脂过氧化程度和植物对逆境条件反应的强弱[9]。由图 1可见, 随着盐胁迫时间的延长,CK1变化趋势较平缓,CK2明显高于CK1且差异显著,在第7、14、21天分别高0.490、0.710、1.059 μmol·L-1,并呈现逐渐递增的变化趋势。喷施ABA、SA、GA3后,苦瓜叶片MDA含量低于CK2而高于CK1,A1、A2、A3处理在第7、14天与CK1差异不显著,,A1、A2处理在第21天与CK2有显著差异,而A3比CK1高0.062 μmol·L-1,但差异不显著。处理期间,A1、A2、A3变化趋势基本一致且呈先降低后上升的变化趋势。以上说明,在一定的盐胁迫条件下,苦瓜幼苗植株有一定的抗盐害能力,能够自身调节膜脂过氧化程度;喷施ABA、SA、GA3可降低苦瓜幼苗的膜脂过氧化程度, 维持膜的稳定性。
|
图 1 外源激素对盐胁迫下苦瓜幼苗MDA含量的影响 Figure 1 Effect of exogenous hormones on MDA content of M.charantia seedlings under salt stress |
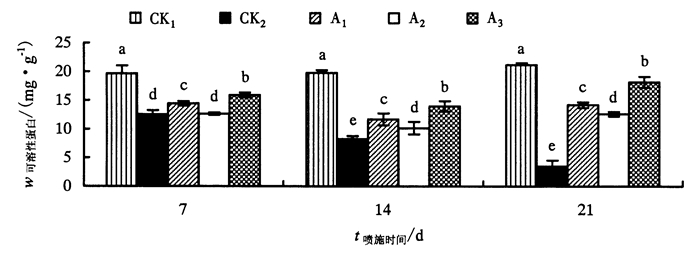
由图 2、3可知,可溶性蛋白、可溶性糖含量变化趋势相似。CK1可溶性蛋白、可溶性糖含量变化较为稳定;随着盐胁迫时间的延长,CK2可溶性蛋白、可溶性糖含量呈现逐渐降低的变化趋势。处理第7天,CK2与A2差异不显著,而与A1、A3有显著性差异;处理第14天,A1、A2、A3可溶性蛋白含量高于CK2,分别高3.432、1.902、5.705 mg·g-1; 处理第21天,A1、A2、A3可溶性糖、可溶性蛋白含量均高于CK2,可溶性糖分别高0.827、0.953、1.106 mg·g-1,可溶性蛋白分别高10.721、9.137、14.678 mg·g-1,呈先降低后上升的变化趋势。以上说明,盐胁迫条件下,苦瓜幼苗生长受抑制,喷施ABA、SA、GA3提高了苦瓜幼苗的渗透调节能力。
|
图 2 外源激素对盐胁迫下苦瓜幼苗可溶性蛋白含量的影响 Figure 2 Effect of exogenous hormones on soluble protein of M.charantia seedlings under salt stress |

|
图 3 外源激素对盐胁迫下苦瓜幼苗可溶性糖含量的影响 Figure 3 Effect of exogenous hormones on soluble sugar content of M.charantia seedlings under salt stress |
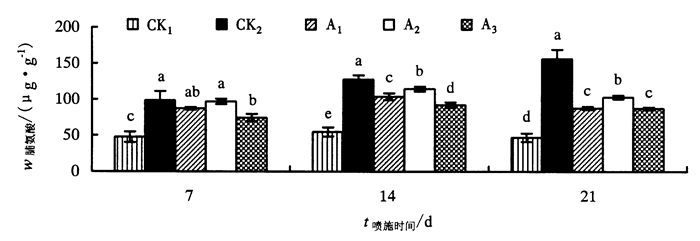
脯氨酸含量能够反映植物的抗逆性。由图 4可知,CK1脯氨酸含量最低,且随着苦瓜幼苗的生长其含量变化不明显;随着盐胁迫时间的延长,CK2脯氨酸含量显著增加并呈上升趋势,处理A1、A2、A3均低于CK2,分别低68.469、53.454、69.069 μg·g-1。处理第21天,脯氨酸含量依次为:CK2>A2>A1>A3>CK1。以上说明,苦瓜幼苗体内游离脯氨酸含量随着盐胁迫的增强而增加,喷施ABA、SA、GA3可缓解盐害对苦瓜幼苗的胁迫作用, 提高植株的抗盐害能力。
|
图 4 外源激素对盐胁迫下苦瓜幼苗脯氨酸含量的影响 Figure 4 Effect of exogenous hormones on proline content of M.charantia seedlings under salt stress |
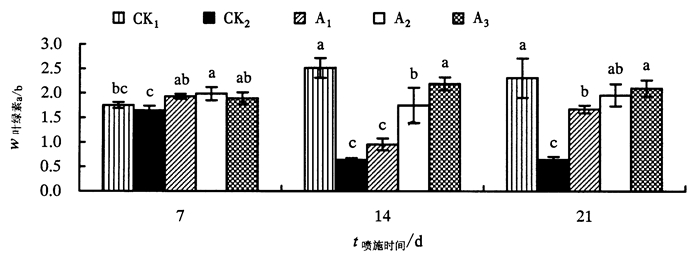
叶绿素是捕获光能的物质基础,一定程度上反映了植物光合作用的强弱及衡量植物同化物质的能力[10-12]。从图 5、6可以看出,A1、A2、A3、CK2叶绿素含量显著低于CK1,CK2叶绿素a/b值持续降低。处理第21天,A1、A2、A3叶绿素含量高于CK2,分别高0.401、0.315、0.647 mg·g-1,A1、A2、A3叶绿素含量、叶绿素a/b值均低于CK1,叶绿素a/b值依次为:CK1>A3>A2>A1>CK2。以上说明,盐胁迫可以促进叶绿素酶的活性,加速叶绿素的降解,进而影响植物光合作用及光合产物的制造能力,其中喷施GA3缓解盐胁迫的效果最好。

|
图 5 外源激素对盐胁迫下苦瓜幼苗叶绿素含量的影响 Figure 5 Effect of exogenous hormones on chlorophyll content of M.charantia seedlings under salt stress |
|
图 6 外源激素对盐胁迫下苦瓜幼苗叶绿素a/b的影响 Figure 6 Effect of exogenous hormones on chlorophyll a/b of M.charantia seedlings under salt stress |
喷施外源激素可调控植物的形态,增加植物木质部的含水量[13-15]。本研究表明,盐胁迫明显抑制苦瓜幼苗地上部分的增长,且降低了壮苗指数。喷施ABA、SA、GA3能够缓解盐胁迫对植株生长的抑制作用。与CK1相比,喷施GA3能显著促进植株茎叶的生长,而短期盐胁迫对苦瓜幼苗根系生长量影响不太明显,A3壮苗指数最接近CK1,抗盐胁迫能力较强。
3.2 盐胁迫下外源激素对苦瓜生理生化特性的影响盐胁迫下植物细胞会发生膜脂过氧化作用, 导致质膜的透性增大[16-18]。本研究表明,CK2脯氨酸、MDA含量明显高于CK1。与CK2相比, 喷施外源激素ABA、SA、GA3明显]降低了苦瓜幼苗MDA、脯氨酸含量,缓解了盐胁迫的伤害,降低了细胞内膜脂氧化损伤程度且保持了膜系统的完整性,增强了植株的抗逆性。
在胁迫条件下植物会进行自身渗透势的调节[19-21]。本研究表明,在盐胁迫下苦瓜幼苗体内渗透调节物质(可溶性蛋白与可溶性糖)含量降低,且呈持续下降的趋势。由此推测, 随着盐胁迫时间的延长,超过植物渗透调节的限量会导致植株死亡。而喷施外源激素ABA、SA、GA3可提高可溶性蛋白和可溶性糖的积累,进而调节渗透势,其中以喷施50 mg·L-1 GA3缓解盐胁迫效果最为显著。
叶绿素是植物进行光合作用的主要色素,植物光合性能的好坏直接影响其生长量、产量的高低[22-24]。本研究表明,随着盐胁迫时间的延长,苦瓜幼苗叶绿素含量显著降低,而各处理叶绿素a/b值大于CK2。喷施GA3, 叶绿素含量、叶绿素a/b值最接近CK1,缓解盐胁迫的效果最好。
综上所述,在盐胁迫条件下,喷施外源激素ABA、SA、GA3可缓解苦瓜幼苗的盐胁迫作用,喷施50 mg·L-1 GA3缓解盐胁迫的效果最好。有关缓解盐胁迫的机理仍有待深入研究。
| [1] | 钟新榕. 外源ABA及GA3对NaCl胁迫下黄瓜幼苗的影响[D]. 兰州: 甘肃农业大学, 2005: 4-7. |
| [2] | 张林青. 水杨酸对盐胁迫下番茄幼苗生理指标的影响[J]. 北方园艺, 2011(21): 36–38. |
| [3] | 赵许朋, 杨立, 杨双燕, 等. ABA对盐胁迫下番茄幼苗生理特性的影响[J]. 安徽农业科学, 2010, 38(27): 14833–14835. DOI: 10.3969/j.issn.0517-6611.2010.27.005 |
| [4] | 李欣欣, 廖红, 赵静. GA3、ABA和6-BA对大豆根系生长的影响[J]. 华南农业大学学报, 2014, 35(3): 35–40. DOI: 10.7671/j.issn.1001-411X.2014.03.007 |
| [5] | 刘斌, 周延, 王景燕, 等. 不同品种苦瓜水培幼苗耐盐碱性研究初探[J]. 河南农业科学, 2010(8): 96–100. |
| [6] | 于爽, 任玉兰, 王晶晶, 等. NaCl对苦瓜幼苗生理特性的影响[J]. 东北农业大学学报, 2010, 41(3): 43–47. |
| [7] | 赵秀娟, 宋建文, 胡开林. 苦瓜种质遗传多样性的SRAP标记分析[J]. 植物遗传资源学报, 2013, 14(1): 78–84. |
| [8] | 王学奎. 植物生理生化实验原理和技术[M]. 北京: 高等教育出版社, 2011: 190-280. |
| [9] | 高俊凤. 植物生理学实验指导[M]. 北京: 高等教育出版社, 2012: 228-230. |
| [10] | 徐锴, 金芳. 外源激素对盐胁迫下草莓光合性能的影响[J]. 甘肃农业大学学报, 2006, 41(2): 31–34. |
| [11] | 朱进, 别之龙, 李娅娜. 盐胁迫对不同基因型黄瓜幼苗生长和光合作用的影响[J]. 沈阳农业大学学报, 2006, 37(3): 476–478. |
| [12] | 张彦. 外源水杨酸对盐胁迫下番茄幼苗生理特性的影响[J]. 北方园艺, 2013(12): 8–11. |
| [13] | 刘拴成, 曹兴明, 穆俊祥, 等. 外源激素对盐胁迫下番茄种子萌发及幼苗生长的影响[J]. 种子, 2016, 35(12): 94–98. DOI: 10.3969/j.issn.1005-2690.2016.12.072 |
| [14] | 赖杭桂, 李瑞梅, 符少萍, 等. 盐胁迫对植物形态结构影响的研究进展[J]. 广东农业科学, 2011, 38(12): 55–57. DOI: 10.3969/j.issn.1004-874X.2011.12.021 |
| [15] | 李萍, 华春, 周泉澄, 等. 外源赤霉素对盐胁迫下盐角草种子萌发及幼苗生长的影响[J]. 安徽农业科学, 2011, 39(9): 5119–5121, 5237. |
| [16] | HUANGY Q, CAIS G, YEL Z, et al. The effects of GA and ABA treatments on metabolite profile of germinating barley[J]. Food Chemistry, 2016, 192: 928–933. DOI: 10.1016/j.foodchem.2015.07.090 |
| [17] | 尚娜, 李景富, 吴明臣. 盐胁迫下番茄幼苗对赤霉素处理的响应[J]. 基因组学与应用生物学, 2017, 36(7): 2965–2972. |
| [18] | 韩志平, 张海霞, 周凤. 盐胁迫对植物的影响及植物对盐胁迫的适应性[J]. 山西大同大学学报(自然科学版), 2015, 31(3): 59–62. |
| [19] | LEE S A, JANGS, YOONE K, et al. Interplay between ABA and GA modulates the timing of asymmetric cell divisions in the Arabidopsis root ground tissue[J]. Molecular Plant, 2016, 9(6): 870–884. DOI: 10.1016/j.molp.2016.02.009 |
| [20] | 赵秀娟, 韩雅楠, 蔡禄. 盐胁迫对植物生理生化特性的影响[J]. 湖北农业科学, 2011, 50(19): 3897–3899. DOI: 10.3969/j.issn.0439-8114.2011.19.003 |
| [21] | 覃杰明, 何含杰, 张党权, 等. 6-BA和GA3对盐胁迫下红杆铁皮石斛幼苗生理生化影响[J]. 亚热带植物科学, 2016, 45(1): 27–31. |
| [22] | 王宝增, 张一名, 张江丽, 等. 水杨酸对盐胁迫下沙打旺幼苗生长的影响[J]. 草业学报, 2016, 25(8): 74–80. DOI: 10.11686/cyxb2016085 |
| [23] | 芦建国, 仲玉婷. 外源GA3和SA对德国鸢尾耐盐性的影响[J]. 江西农业学报, 2011, 23(4): 49–52, 56. |
| [24] | 郭春爱, 刘芳, 许晓明. 叶绿素b缺失与植物的光合作用[J]. 植物生理学通讯, 2006, 42(5): 967–973. |
 2017,Vol. 13
2017,Vol. 13


