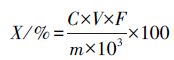文章信息
- 林庆景, 王志江, 杨旭, 姚闽娜
- LIN Qingjing, WANG Zhijiang, YANG Xu, YAO Minna
- 超声波辅助提取木棉花黄酮工艺
- Ultrasound-assisted extraction of flavonoids from kapok flowers
- 亚热带农业研究, 2016, 12(3): 192-198
- Subtropical Agriculture Research, 2016, 12(3): 192-198.
- DOI: 10.13321/j.cnki.subtrop.agric.res.2016.03.010
-
文章历史
- 收稿日期: 2016-03-22
2. 福建农林大学食品科学学院, 福建 福州 350002
2. College of Food Science, Fujian Agriculture and Forestry University, Fuzhou, Fujian 350002, China
木棉(Bombax ceiba)又名攀枝花、英雄花、斑芝花等,是木棉科(Malvaceae)木棉属(Bombax)植物,喜温,多分布于我国广东、广西、福建、台湾、海南等地区。木棉花含有多种功能活性成分[1-2],如黄酮、多酚、多糖、花青素以及矿物质元素,具有抗炎、抗菌、抗癌等功效。其中,天然黄酮化合物具有抑菌、抗辐射、抗氧化和美白等功效,可在清除皮肤自由基的同时减少自由基对人体细胞的伤害,减少色素的沉着,达到显著美白和润泽肌肤的效果。木棉花黄酮将有望作为化妆品添加剂和天然保鲜剂进行研发[3]。
黄酮类化合物存在于植物植株的不同部位,提取黄酮应根据其所在部位,结合存在形式选择适合的提取方式。常见的提取方式包括有机溶剂提取法、索氏提取法等传统提取方法以及微波提取法、超声波提取法、酶解提取法、超临界流体萃取法等现代高新技术提取方法[4-9]。本文借鉴梁云贞等[10]对木棉花总黄酮的提取工艺,采用超声波提取法,以超声功率、温度、料液比和提取时间为变量,木棉花总黄酮提取率为目标函数进行单因素试验,并通过响应面优化得到最佳水提法工艺[11-12]。木棉花是南方特有植物,其数量繁多,运用新技术制备木棉花黄酮化合物产品,有利于提高木棉花的资源利用和产品附加值。
1 材料与方法 1.1 试验材料 1.1.1 材料与试剂木棉落花(采自福建农林大学后山);芦丁(购自中国药品生物制品检定所)、无水乙醇、甲醇、NaNO2、NaOH、Al(NO3)3等试剂,均为国产分析纯。
1.1.2 仪器2601紫外可见光分光光度计(北京瑞利分析仪器公司),KQ-500DE超声波清洗器(昆山市超声仪器有限公司),RE-52AA旋转蒸发仪(上海亚荣生化仪器厂),A11碾磨机(德国IKA集团),FW80高速万能粉碎机(天津市泰斯特仪器有限公司),SHB-Ⅲ真空泵(郑州长城仪器公司),SC-3612台式低速离心机(科大创新股份有限公司中佳分公司)。
1.2 试验方法 1.2.1 单因素试验分别以不同浓度的乙醇或甲醇(0.10、0.25、0.40、0.55、0.70、0.85 mg·mL-1)、超声时间(10、20、30、40、50、60、70 min)、超声温度(20、30、40、50、60、70 ℃)、料液比(1:10、1:15、1:20、1:30、1:35、1:40、1:50)、超声功率(200、250、300、350、400、450、500 W)及提取次数(1、2、3、4、5次)为单因素。考察各单因素对提取液中黄酮含量的影响。
1.2.2 总黄酮提取工艺的优化设计在单因素试验基础上,采用Design-Expert.V8.0.6 中Box-Benhnken模块对料液比、乙醇浓度、超声功率3个主要因素进行响应面优化设计。
1.2.3 NaNO2-Al(NO3)3比色法测定黄酮含量(1)标准曲线的制定。以芦丁为标准品。准确称取10.0 mg干燥充分的芦丁,置于50 mL容量瓶中,加入0.75 mg·mL-1乙醇,置于温水中加热溶解;冷却至室温后定容,得到0.2 mg·mL-1的芦丁标准品溶液。准确吸取0.2 mg·mL-1芦丁对照品溶液0、2.0、4.0、6.0、8.0、10.0、12.0 mL分别置于50 mL容量瓶中,加入0.75 mg·mL-1乙醇至12 mL;加入2 mL 0.05 mg·mL-1 NaNO2后混匀,静置6 min;加入2 mL 0.10 mg·mL-1 Al(NO3)3后摇匀,静置6 min;再加入20 mL 0.043 mg·mL-1 NaOH后用0.75 mg·mL-1乙醇定容至50 mL,静置15 min。以空白液为对照,于510 nm波长下测定各浓度标准样品的光密度(D510 nm),以芦丁对照品溶液浓度为横坐标,D510 nm为纵坐标,绘制标准曲线[13],如图 1所示。得到标准曲线的回归方程:y=10.773x+0.008 1(R2=0.999 4),其中,x为芦丁标准溶液浓度/(mg·mL-1),y为光密度,在所取浓度范围内其浓度与光密度具有良好的线性关系。
|
图 1 总黄酮的标准曲线 Figure 1 Standard curve of total flavonoids |
(2)提取液中黄酮含量的检测。将样品置于超声波清洗器,在一定的功率和温度下进行一定时间的处理,并移取处理过的样品上清液进行离心。取适量上清液,用0.75 mg·mL-1乙醇稀释10倍,在510 nm波长下测定其光密度,再根据标准曲线得到样品中总黄酮的含量。
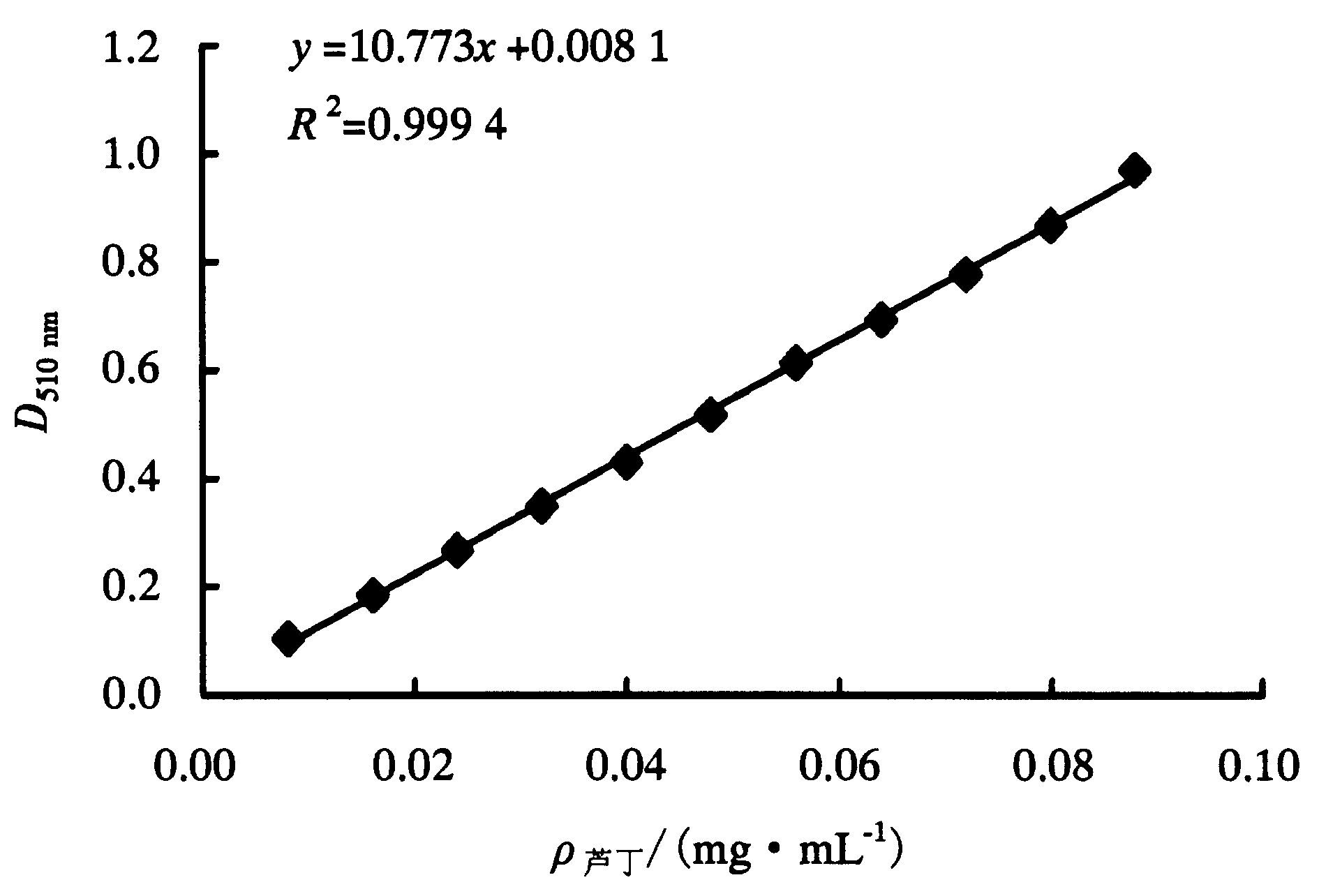
1.2.4 总黄酮提取率式中,X为木棉提取液中总黄酮含量/%;C为木棉提取液稀释液中的黄酮浓度/(mg·mL-1);m为样品质量/g;F为稀释倍数;V为待测液的总体积/mL。
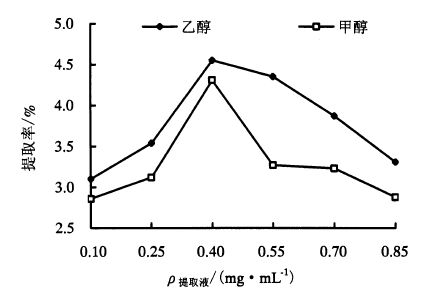
2 结果与分析 2.1 单因素试验对木棉花总黄酮提取率的影响 2.1.1 提取浓度在超声温度50 ℃、超声功率300 W、料液比1:30、超声时间30 min、提取次数1次的条件下,分析不同浓度的乙醇和甲醇对木棉花总黄酮提取率的影响(图 2)。由图 2可知,分别以不同浓度的甲醇和乙醇作为提取剂,木棉花总黄酮提取率均先增加后减少,总体来说,乙醇浸提效果稍好于甲醇。主要由于乙醇极性较甲醇小,且考虑到甲醇有毒,因此,提取剂应选择乙醇。同时,随着乙醇浓度的逐渐增加,样品中木棉花总黄酮提取量也逐渐增加。乙醇浓度达到0.40 mg·mL-1时,提取率最大,为4.55%;当乙醇浓度继续升高时,提取率反而下降。因此,乙醇浓度宜选择0.40 mg·mL-1左右。
|
图 2 乙醇和甲醇浓度对木棉花总黄酮提取率的影响 Figure 2 Effect of ethanol and methanol concentration on flavonoid extraction rate |
在超声温度50 ℃、超声功率300 W、乙醇浓度0.75 mg·mL-1、超声时间30 min、提取次数1次的条件下,考察不同料液比对木棉花总黄酮提取率的影响(图 3)。由图 3可知,料液比在1:10~1:30对总黄酮的提取率有显著影响,即提取率从2.04%提高到3.88%;当料液比达到1:30后,总黄酮提取率呈下降趋势。因此,料液比宜选择在1:30左右。

|
图 3 料液比对木棉花总黄酮提取率的影响 Figure 3 Effect of solid-liquid ratio on flavonoidextraction rate |
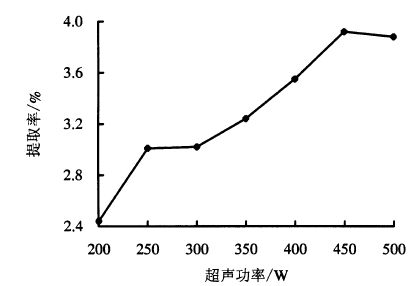
在超声温度50 ℃、料液比1:30、乙醇浓度0.75 mg·mL-1、超声时间30 min、提取次数1次的条件下,考察不同超声功率对木棉花总黄酮提取率的影响(图 4)。由图 4可知,总黄酮提取率随着超声功率的提高呈先增加后减少的趋势;当超声功率为200 W时,提取率仅为2.44 %,当功率增加到450 W时,提取率上升到3.92%;继续升高超声功率,提取率反而下降。因此,最佳超声功率宜选择450 W左右。
|
图 4 超声功率对木棉花总黄酮提取率的影响 Figure 4 Effect of ultrasonic poweron flavonoid extraction rate |
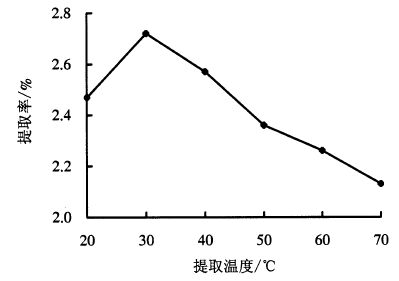
在超声功率300 W、乙醇浓度0.75 mg·mL-1、料液比1:30、超声时间30 min、提取次数1次的条件下,考察提取温度对木棉花总黄酮提取率的影响(图 5)。由图 5可知,总黄酮提取率随着提取温度的升高呈先增加后减少的趋势;30 ℃时提取率最高,当超过30 ℃时,提取率则开始下降。因此,超声温度宜选择30 ℃左右。
|
图 5 提取温度对木棉花总黄酮提取率的影响 Figure 5 Effect of temperature on flavonoid extraction rate |
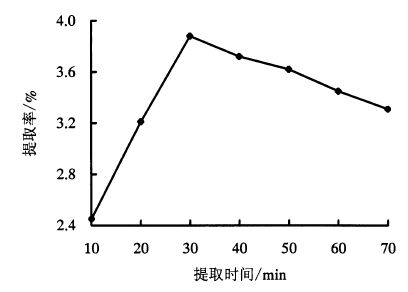
在超声功率300 W、乙醇浓度0.75 mg·mL-1、超声温度30 ℃、料液比1:30、提取次数1次的条件下,考察提取时间对木棉花总黄酮提取率的影响(图 6)。由图 6可知,在10~30 min内,随着提取时间的延长,总黄酮提取率逐渐增加,30 min时,提取率为3.88%,达到最大;进一步延长提取时间,则呈下降趋势。因此,提取时间应选择30 min左右为宜。
|
图 6 提取时间对木棉花总黄酮提取率的影响 Figure 6 Effect of extraction duration on flavonoid extraction rate |
在超声功率300 W、料液比1:30、超声温度30 ℃、乙醇浓度0.75 mg·mL-1、超声时间30 min的条件下,考察提取次数对木棉花总黄酮提取率的影响(图 7)。由图 7可知,总黄酮提取率分别为0.81%、1.10%、1.15%、1.18%、1.21%,即提取率随着提取次数的增加而逐渐提高。随着提取次数的增多,总黄酮提取量虽增加,但增加的幅度不高,考虑实际操作和提取成本,选择提取1次为宜。

|
图 7 提取次数对木棉花总黄酮提取率的影响 Figure 7 Effect of number of extraction on flavonoid extraction rate |
| 编码水平 | 因素 | ||
| X1 | X2/(mg·mL-1) | X3/W | |
| -1 | 1:25 | 0.25 | 400 |
| 0 | 1:30 | 0.40 | 450 |
| 1 | 1:35 | 0.55 | 500 |
| 1)X1.料液比;X2.乙醇浓度;X3.超声功率。 | |||
根据Box-Benhnken中心组合设计试验,综合单因素试验结果,选择3个对木棉花总黄酮提取率影响较大的因素,即料液比(X1)、乙醇浓度(X2)、超声功率(X3)进行3水平3因素的响应面分析试验,并对17个试验点加以效应分析。试验因素与水平设计见表 1。每组试验重复3次,取其平均值。在单因素试验的基础上,Box-Benhnken试验设计及试验结果见表 2,回归模型方差分析见表 3。
将表 2试验结果输入SAS软件,建立的数学模型为:
Y=4.35+0.023X1+0.034X2+0.13X3-0.025X1X2+0.005X1X3-0.023X2X3-0.11X12-0.14X22-0.17X32。
| 试验号 | 因素 | Y/% | ||
| X1 | X2 | X3 | ||
| 1 | -1 | 0 | 1 | 4.15 |
| 2 | 1 | 0 | -1 | 3.99 |
| 3 | 0 | 1 | 1 | 4.20 |
| 4 | 0 | -1 | -1 | 3.84 |
| 5 | -1 | 0 | -1 | 3.95 |
| 6 | 0 | 0 | 0 | 4.33 |
| 7 | 0 | -1 | 1 | 4.20 |
| 8 | -1 | 1 | 0 | 4.15 |
| 9 | -1 | -1 | 0 | 4.01 |
| 10 | 0 | 0 | 0 | 4.35 |
| 11 | 0 | 0 | 0 | 4.38 |
| 12 | 0 | 0 | 0 | 4.34 |
| 13 | 0 | 1 | -1 | 3.93 |
| 14 | 1 | 0 | 1 | 4.21 |
| 15 | 1 | 1 | 0 | 4.14 |
| 16 | 1 | -1 | 0 | 4.10 |
| 17 | 0 | 0 | 0 | 4.36 |
| 1)X1.料液比;X2.乙醇浓度;X3.超声功率;Y.提取率。 | ||||
| 变异来源 | 自由度 | 平方和 | 均方 | F值 | P值 |
| 模型 | 9 | 0.440 0 | 0.049 0 | 42.29 | <0.000 1 |
|
| 1 | 0.000 4 | 0.000 4 | 3.52 | 0.102 8 |
| X2 | 1 | 0.000 9 | 0.000 9 | 7.92 | 0.026 0 |
| X3 | 1 | 0.140 0 | 0.140 0 | 119.76 | <0.000 1 |
| X1X2 | 1 | 0.000 3 | 0.000 3 | 2.17 | 0.184 0 |
| X1X3 | 1 | 0.000 0 | 0.000 0 | 0.09 | 0.776 7 |
| X2X3 | 1 | 0.000 2 | 0.000 2 | 1.76 | 0.226 3 |
| X12 | 1 | 0.051 0 | 0.051 0 | 44.07 | 0.000 3 |
| X22 | 1 | 0.085 0 | 0.085 0 | 74.04 | <0.000 1 |
| X32 | 1 | 0.120 0 | 0.120 0 | 102.35 | <0.000 1 |
| 残差 | 7 | 0.000 8 | 0.000 1 | ||
| 失拟性 | 3 | 0.000 7 | 0.000 2 | 5.92 | 0.059 3 |
| 纯误差 | 4 | 0.000 1 | 0.000 4 | ||
| 总变异 | 16 | 0.450 0 | |||
| 1)X1.料液比;X2.乙醇浓度;X3.超声功率。 | |||||
从表 3的方差分析结果可以看出,P值<0.01,表明二次方程数学模型高度显著;F值为5.92,说明失拟项相对于绝对误差是不显著的,因此,失拟项是可取的;该方程的相关系数RAdj2=0.981 9和校正决定系数R2=0.958 7,均接近于1,表明该响应面优化结果的回归方程拟合情况良好,试验误差小。因此,用该回归方程可以准确模拟不同提取条件对木棉花总黄酮提取率的影响并进行预测,可以准确预测木棉花总黄酮的最佳提取工艺。此外,料液比的P值>0.05,表明其对总黄酮提取率的影响不显著;乙醇浓度P值<0.05,表明其对总黄酮提取率的影响显著;超声功率P值<0.01,表明其对总黄酮提取率的影响极显著。
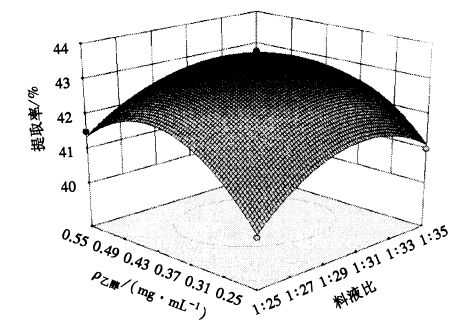
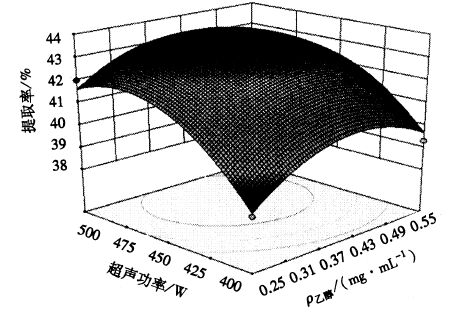
2.2.2 因素之间的交互作用根据多元线性回归方程,用计算机模拟分析软件分析各提取因素的相互关系,其交互项的交互作用如图 8~10所示。从图中可以直观地反映各因素对响应值的影响,由响应面可以看出存在极值的条件明显,结合回归方程的结果,根据二次回归数学模型的优化分析,得到木棉总黄酮最佳提取工艺为:料液比为1:30.51、乙醇浓度为0.411 7 mg·mL-1、超声波功率为469.45 W,在此条件下木棉花总黄酮提取率预测值为4.38%。
|
图 8 乙醇浓度与料液比对木棉花总黄酮提取率的交互影响 Figure 8 Mutual effects of ethanol concentration and solid-liquid ratio on flavonoid extraction rate |
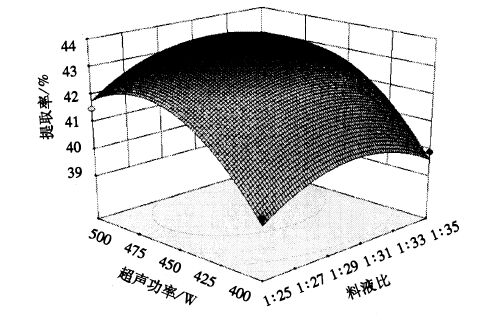
|
图 9 超声功率与料液比对木棉花总黄酮提取率的交互影响 Figure 9 Mutual effects of ultrasonic power and solid-liquid ratio on flavonoid extraction rate |
|
图 10 超声功率与乙醇浓度对木棉花总黄酮提取率的交互影响 Figure 10 Mutual effects of ultrasonic power and ethanol concentration on flavonoid extraction rate |
由于试验条件限制,故将模型预测条件优化为:超声温度30 ℃,乙醇浓度0.41 mg·mL-1、料液比1:31、超声功率470 W,提取时间30 min。对模型试验预测的结果进行验证,重复3次,测得木棉花总黄酮提取率平均值为4.35%,与模型预测值吻合良好。
3 小结本文采用微波辅助法提取木棉花总黄酮,探究相同条件下乙醇和甲醇对木棉花总黄酮提取率的影响。结果表明,乙醇提取效果较甲醇好,考虑到安全性问题,选择乙醇作为提取剂。通过单因素试验研究乙醇浓度、料液比、超声波功率、提取温度、提取时间和提取次数对木棉花总黄酮提取率的影响。再利用响应面法优化木棉花总黄酮提取工艺,得出最佳提取条件:(1)提取剂乙醇浓度为0.41 mg·mL-1;(2)料液比为1:31;(3)超声功率为470 W。在此条件下进行验证试验,得到木棉花总黄酮提取率为4.35%。
| [1] | 叶斯琴, 王翀梅, 王辉. 木棉花红色素的提取及其应用研究[J]. 广州食品工业科技, 2004, 20(4): 90–91. |
| [2] | 刘成伦, 唐德容. 黄酮类化合物抗氧化性质的研究进展[J]. 食品研究与开发, 2006, 27(5): 158–160. |
| [3] | HE G Q, XIONG H P, CHEN Q H, et al. Optimization of conditions for supercritical fluid extraction of flavonoids from hops (Humulus lupulus L[J]. Zhejiang University Journal Science B: International Biomedicine & Biotechnology Journal, 2005, 6(10): 999–1004. |
| [4] | 张佳赫, 韩丽琴. 不同提取方式对葛根总黄酮抗氧化反应的影响[J]. 安徽农业科学, 2010, 38(24): 13032–13033. |
| [5] | 陈伟, 刘青梅, 杨性民, 等. 微波技术在杜仲黄酮提取工艺中的应用研究[J]. 食品科学, 2006, 27(10): 285–288. |
| [6] | 张尊听, 杨伯伦, 刘谦光, 等. 野葛根异黄酮成分的超声萃取及抗氧化作用[J]. 食品科学, 2002, 23(5): 31–33. |
| [7] | 张赟彬, 李彩侠, 李军, 等. 荷叶黄酮提取工艺研究[J]. 食品研究与开发, 2005, 26(5): 92–94. |
| [8] | 林敬明, 夏平光, 吴忠. 木棉花CO2超临界萃取物的GC-MS分析[J]. 广东药学院学报, 2001, 17(2): 111–112. |
| [9] | 何琦, 及元乔, 丁立生, 等. D140大孔吸附树脂银杏黄酮提取纯化性能研究[J]. 天然产物研究与开发, 2001, 13(1): 56–59. |
| [10] | 梁云贞, 彭金云, 李怡, 等. 微波辅助提取木棉花中总黄酮的工艺研究[J]. 安徽农业科学, 2010, 38(24): 13064–13066. |
| [11] | 罗兰, 曾茂贵, 饶雪娥, 等. 应用响应面分析优化酶法辅助超声提取余甘子多糖工艺[J]. 亚热带农业研究, 2014(4): 264–268. |
| [12] | 伊恒杰, 许明, 翁武斌, 等. 响应面法优化红肉火龙果茎多糖的超声波辅助提取工艺[J]. 亚热带农业研究, 2016, 12(1): 56–61. |
| [13] | 吕萍, 刘景圣, 蔡丹, 等. 超声波法提取绿豆中的黄酮的最佳工艺研究[J]. 粮油加工, 2010(9): 117–119. |
 2016,Vol. 12
2016,Vol. 12