文章信息
- 伊恒杰, 许明, 翁武斌, 杨志坚, 廖素凤
- YI Hengjie, XU Ming, WENG Wubin, YANG Zhijian, LIAO Sufeng
- 响应面法优化红肉火龙果茎多糖的超声波辅助提取工艺
- Optimization of ultrasonic-assisted extraction of polysaccharides from red pulp pitaya stem by response surface method
- 亚热带农业研究, 2016, 12(01): 56-61
- JOURNAL OF AERONAUTICAL MATERIALS, 2016, 12(01): 56-61.
- DOI: 10.13321/j.cnki.subtrop.agric.res.2016.01.009
-
文章历史
- 收稿日期:2015-07-31
2. 福建省文德堡食品有限责任公司,福建 平潭 350400
2. Fujian Wendebao Foods Co., Ltd, Pingtan, Fujian 350400, China
火龙果(Hylocerus undatus),又名仙蜜果、红龙果等,是一种高营养保健价值的热带水果[1, 2],具有助消化、降血压与血糖、抗氧化等多种保健功能,深受消费者喜爱[3]。目前在广西、广东、海南、福建、云南和贵州等省(区)有较大种植面积[4]。火龙果栽培品种主要有白肉和红肉两种,其中红肉品种在甜度、风味品质等方面优于白肉[5, 6],市场价格也较高,发展潜力大。红肉火龙果栽培中常需要修枝整形以提高产量,修剪后的茎富含植物多糖等活性成分[7],对其茎多糖进行提取利用,可以提高红肉火龙果的附加值。
超声波提取法利用超声波的空化效应、机械效应和热效应促进有效成分溶出,加速提取物扩散[8],具有提取时间较短、提取率较高且产品易纯化等优点[9],被广泛应用于天然产物有效成分的提取[10, 11, 12, 13, 14]。本研究探讨超声波对红肉火龙果茎多糖提取率的影响,并应用响应面法(response surface analysis,RSA)对其超声波辅助提取工艺进行优化,以期为进一步开发利用红肉火龙果多糖提供依据。
1 材料与方法 1.1 材料和仪器 1.1.1 材料与试剂红肉火龙果果茎,由福建省文德堡食品有限责任公司提供。浓硫酸、苯酚、葡萄糖、三氯甲烷、无水乙醇、丙酮和乙醚等试剂均为分析纯。
1.1.2 仪器设备KQ-500DE数控超声波清洗器(昆山市超声仪器有限公司);3K30冷冻离心机(德国Sigma公司);HB10 Basic旋转蒸发仪(德国IKA公司);UV-754紫外—可见分光光度计(北京普析通用仪器有限责任公司);BDA2202S-CW电子天平(赛多利斯科学仪器有限公司);LGJ-10普通型真空冷冻干燥机(北京松源华兴科技发展有限公司)。
1.2 方法 1.2.1 粗多糖的提取新鲜红肉火龙果茎除刺去皮后用清水洗净,切成细丝。每次取20 g,按设定料液比加入纯水,放入搅拌机中打至糊状,然后按设定的功率、时间和温度进行超声提取。提取液在4 500 r·min-1下离心15 min,取上清,浓缩至原体积的1/4,用Sevag法[15]去除蛋白,按体积1:4的比例加入95%乙醇,低温静置12 h,4 500 r·min-1离心15 min,沉淀先用无水乙醇洗涤1遍,随后用丙酮洗涤1遍,最后用乙醚洗涤1遍,所得沉淀经冷冻干燥后即为多糖粗品。
1.2.2 多糖含量的测定采用苯酚—硫酸法[16],测得的光密度值通过葡萄糖标准曲线换算成葡萄糖质量,计算粗多糖提取率[17]。多糖提取率/%=粗多糖质量/火龙果茎质量×100。
1.2.3 单因素试验分别以不同液料比(10:1、15:1、20:1、25:1、30:1)、超声功率(200、250、300、350、400 W)、浸提时间(6、8、10、12、14 min)和浸提温度(40、50、60、70、80 ℃)为单因素,考察各单因素对多糖提取率的影响。每组试验重复3次,取平均值。
1.2.4 响应面试验(RSM)设计及优化根据单因素试验结果和Box-Behnken 设计原则,选取对红肉火龙果茎多糖提取率影响显著的因素为自交量,以多糖提取率为响应值,通过响应曲面分析进行提取条件的优化。
2 结果与讨论 2.1 单因素试验对多糖提取率的影响 2.1.1 液料比在浸提温度60 ℃、浸提时间10 min、超声功率300 W的提取条件下,分别选取5种液料比(10:1、15:1、20:1、25:1、30:1),按照1.2.1 的方法提取多糖。结果显示,随着液料比的增加,多糖提取率先升高后降低(图 1)。由于起始时先增加水,可以使多糖充分溶解,损失减少,在15:1时达到最大值。但随着液料比的增加,反应产物浓度降低,多糖提取率不升反降。故选择15:1为最佳液料比。
 |
图 1 液料比对红肉火龙果茎多糖提取率的影响 Figure 1 Effect of water/dry weight ratio on the polysaccharides extraction rate |
从图 2可以看出,在液料比为1:20、浸提温度60 ℃、浸提时间10 min的提取条件下,随着超声功率的增加,多糖提取率先升高后降低。超声功率在200~250 W之间,多糖提取率平稳上升;当超声功率在250~400 W之间时,提取率逐步降低;当超声功率为250 W时,多糖提取率最高,故超声功率以250 W时最佳。
 |
图 2 超声功率对红肉火龙果茎多糖提取率的影响 Figure 2 Effect of ultrasonic power on the polysaccharides extraction rate |
从图 3可以看出,在设定液料比为20:1、浸提温度60 ℃、超声功率300 W的提取条件下,随着浸提时间的延长,多糖提取率呈先升高后降低的趋势。浸提时间为8 min时,多糖提取率最高,故浸提时间以8 min时最佳。
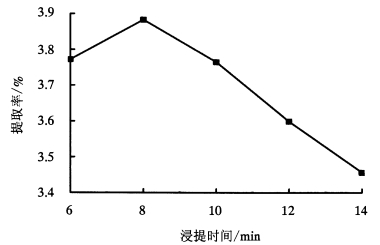 |
图 3 浸提时间对红肉火龙果茎多糖提取率的影响 Figure 3 Effect of extraction time on the polysaccharides extraction rate |
从图 4可以看出,在选取液料比为20:1、浸提时间为 10 min、超声功率300 W的提取条件下,当浸提温度从40 ℃升至50 ℃,多糖提取率显著提高,50 ℃之后,随着浸提温度的增加,多糖提取率呈不断下降趋势。因此,选取50 ℃为最佳浸提温度。
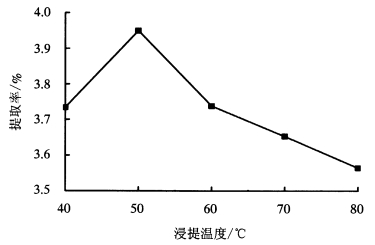 |
图 4 浸提温度对红肉火龙果茎多糖提取率的影响 Figure 4 Effect of extraction temperature on the polysaccharides extraction rate |
根据Box-Benhnken中心组合试验设计原则[18],在单因素试验结果的基础上,选取液料比、超声功率、浸提时间、浸提温度为自变量,通过四因素三水平的响应面分析方法对试验因素进行优化。试验因素与水平设计见表 1 。
| 水平与编码 | 因素 | |||
| X1 | X2/W | X3/min | X4/℃ | |
| 1)X1.液料比;X2.超声功率;X3.浸提时间;X4.浸提温度。 | ||||
| -1 | 10 | 200 | 6 | 40 |
| 0 | 15 | 250 | 8 | 50 |
| 1 | 20 | 300 | 10 | 60 |
对液料比(X1)、超声功率(X2)、浸提时间(X3)和浸提温度(X4)做如下变换:X1=(z-15)/5,X2=(W-250)/50,X3=(t-8)/2,X4=(T-50)/10,以3次试验所得多糖提取率的平均值为响应值(Y),所设计的试验方案及试验结果见表 2。
| 序号 | X1 | X2 | X3 | X4 | Y/% | 序号 | X1 | X2 | X3 | X4 | Y/% |
| 1)X1.液料比;X2.超声功率;X3.浸提时间;X4.浸提温度;Y.多糖提取率。 | |||||||||||
| 1 | 0.00 | 0.00 | 0.00 | 0.00 | 2.511 | 16 | 0.00 | -1.00 | 0.00 | 1.00 | 0.772 |
| 2 | 0.00 | -1.00 | 1.00 | 0.00 | 0.424 | 17 | -1.00 | 0.00 | 0.00 | 1.00 | 0.916 |
| 3 | 1.00 | 0.00 | 1.00 | 0.00 | 1.508 | 18 | 1.00 | -1.00 | 0.00 | 0.00 | 0.365 |
| 4 | 0.00 | 0.00 | 1.00 | 1.00 | 2.279 | 19 | 0.00 | 1.00 | -1.00 | 0.00 | 0.766 |
| 5 | 0.00 | 0.00 | 0.00 | 0.00 | 2.899 | 20 | -1.00 | 0.00 | 0.00 | -1.00 | 0.685 |
| 6 | -1.00 | 0.00 | -1.00 | 0.00 | 0.951 | 21 | 0.00 | 1.00 | 0.00 | 1.00 | 2.389 |
| 7 | 1.00 | 0.00 | 0.00 | -1.00 | 1.184 | 22 | 1.00 | 1.00 | 0.00 | 0.00 | 2.111 |
| 8 | 1.00 | 0.00 | 0.00 | 1.00 | 1.624 | 23 | 0.00 | 0.00 | 0.00 | 0.00 | 2.911 |
| 9 | -1.00 | -1.00 | 0.00 | 0.00 | 1.562 | 24 | 0.00 | 0.00 | -1.00 | 1.00 | 1.560 |
| 10 | 0.00 | 1.00 | 0.00 | -1.00 | 0.760 | 25 | -1.00 | 1.00 | 0.00 | 0.00 | 0.831 |
| 11 | 0.00 | -1.00 | 0.00 | -1.00 | 0.424 | 26 | 1.00 | 0.00 | -1.00 | 0.00 | 1.694 |
| 12 | 0.00 | 0.00 | -1.00 | -1.00 | 0.830 | 27 | 0.00 | 0.00 | 0.00 | 0.00 | 2.766 |
| 13 | -1.00 | 0.00 | 1.00 | 0.00 | 0.959 | 28 | 0.00 | -1.00 | -1.00 | 0.00 | 0.992 |
| 14 | 0.00 | 1.00 | 1.00 | 0.00 | 1.404 | 29 | 0.00 | 0.00 | 1.00 | -1.00 | 0.737 |
| 15 | 0.00 | 0.00 | 0.00 | 0.00 | 2.566 | ||||||
将表 2试验结果输入SAS软件,进行响应面回归分析,得出各因素与红肉火龙果茎多糖提取率之间的回归方程为:
Y=2.731+0.215X1+0.310X2+0.043X3+0.410X4+0.619X1X2-0.049X1X3+0.052X1X4+0.302X2X3+0.320X2X4+0.203X3X4-0.722X12-0.921X22-0.758X32-0.751X42
从表 3的显著性检验和方差分析可以看出,所建立的回归方程模型的差异是极显著的。模型一次项X1(液料比)、X2(超声功率)、X3(浸提温度),交互项X1X2(液料比与超声功率的交互作用),以及二次项X12、X22、X32、X42均极显著,说明该模型拟合度良好。
| 方差来源 | 平方和 | 自由度 | 均方 | F值 | P值 | ||||||
| 1)X1.液料比;X2.超声功率;X3.浸提时间;X4.浸提温度。 | |||||||||||
| 模型 | 16.71 | 14 | 1.19 | 12.42 | <0.000 1 | ||||||
| X1 | 0.56 | 1 | 0.56 | 5.78 | 0.030 6 | ||||||
| X2 | 1.15 | 1 | 1.15 | 12.01 | 0.003 8 | ||||||
| X3 | 0.02 | 1 | 0.02 | 0.23 | 0.637 0 | ||||||
| X4 | 2.02 | 1 | 2.02 | 20.99 | 0.000 4 | ||||||
| X1X2 | 1.53 | 1 | 1.53 | 15.96 | 0.001 3 | ||||||
| X1X3 | 25.54 | 1 | 25.54 | 0.10 | 0.759 0 | ||||||
| X1X4 | 0.01 | 1 | 0.01 | 0.11 | 0.741 0 | ||||||
| X2X3 | 0.36 | 1 | 0.36 | 3.78 | 0.072 1 | ||||||
| X2X4 | 0.41 | 1 | 0.41 | 4.27 | 0.057 8 | ||||||
| X3X4 | 0.16 | 1 | 0.16 | 1.72 | 0.211 4 | ||||||
| X12 | 3.38 | 1 | 3.38 | 35.17 | <0.000 1 | ||||||
| X22 | 5.50 | 1 | 5.50 | 57.21 | <0.000 1 | ||||||
| X32 | 3.72 | 1 | 3.72 | 38.74 | <0.000 1 | ||||||
| X42 | 3.65 | 1 | 3.65 | 38.03 | <0.000 1 | ||||||
| 残差 | 1.35 | 14 | 0.10 | ||||||||
| 失拟值 | 1.21 | 10 | 0.12 | 3.51 | 0.118 6 | ||||||
| 纯误差 | 0.14 | 4 | 0.03 | ||||||||
| 总差 | 18.05 | 28 | |||||||||
根据回归分析结果绘制响应面图形。液料比、超声功率、浸提时间和浸提温度4个因素中,选取任意两因素为0水平,其余两因素对红肉火龙果茎多糖提取率的影响见图 5~10。 从图 5可以看出,当液料比处于恒定时,随着超声功率的增加,多糖提取率先增加后降低,最佳超声功率在260~280 W之间。当超声功率处于恒定时,随着液料比增加,多糖提取率也先增加后降低,最佳液料比在15:1~18:1之间,说明液料比和超声功率存在较为显著的交互作用。图 6~10也全部开口向下,且随着各个因素值的增加,其响应值均先增加后减小,均能取得一个较优值。
 |
图 5 液料比与超声功率对红肉火龙果茎多糖提取率的影响 Figure 5 Effects of water/dry weight ratio and ultrasonic power on the polysaccharides extraction rate of red pulp pitaya stems |
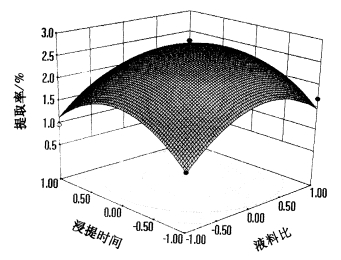 |
图 6 液料比与浸提时间对红肉火龙果茎多糖提取率的影响 Figure 6 Effects of water/dry weight ratio and extraction time on the polysaccharides extraction rate of red pulp pitaya stems |
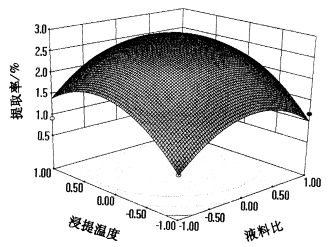 |
图 7 液料比与浸提温度对红肉火龙果茎多糖提取率的影响 Figure 7 Effects of water/dry weight ratio and extraction temperature on the polysaccharides extraction rate of red pulp pitaya stems |
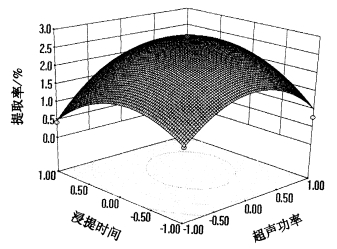 |
图 8 超声功率与浸提时间对红肉火龙果茎多糖提取率的影响 Figure 8 Effects of ultrasonic power and extraction time on the polysaccharides extraction rate of red pulp pitaya stems |
 |
图 9 超声功率与浸提温度对红肉火龙果茎多糖提取率的影响 Figure 9 Effects of ultrasonic power and extraction temperature on the polysaccharides extraction rate of red pulp pitaya stems |
 |
图 10 浸提时间与浸提温度对红肉火龙果茎多糖提取率的影响 Figure 10 Effects of extraction time and extraction temperature on the polysaccharides extraction rate of red pulp pitaya stems |
利用Design-Exepert 软件对试验参数进行拟合,得出最佳条件为: 液料比16.55:1,超声功率268 W,浸提时间8.28 min(取8 min),浸提温度为53.8 ℃(取54 ℃)。
2.2.3 最佳条件的试验验证为了检测响应面法试验结果的可靠性,采用上述最优条件进行超声波辅助提取红肉火龙果茎多糖的验证试验。设3次重复,取其平均值,得到红肉火龙果茎多糖的平均提取率为2.755%,与回归模型预测的提取率理论值(2.902%)相对误差为5.07%,说明回归方程能够比较真实地反映各因素对多糖提取率的影响,使用响应面法优化所得到的参数准确可信。
3 小结本研究通过超声辅助提取法从红肉火龙果茎中提取多糖,并利用响应面法对其提取因素进行了优化。结果表明,超声波提取的最佳条件为: 液料比16.55:1、超声功率268 W、浸提时间8 min、浸提温度54 ℃。在此条件下多糖提取率为2.755%,与预测值(2.902%)基本一致。本研究结果可为红肉火龙果茎多糖的开发利用提供参考。
| [1] | 许伟东, 廖剑锹, 刘加建, 等.火龙果引种初报[J].中国南方果树, 2002, 31(1):33-34. |
| [2] | 赵志平, 杨春霞.火龙果的开发与发展前景[J].中国种业, 2006(2):13-14. |
| [3] | 王壮, 王立娟, 蔡永强, 等.火龙果营养成分及功能性物质研究进展[J].中国南方果树, 2014, 43(5):25-29. |
| [4] | 郑文武, 刘永华.我国火龙果生产现状及发展前景[J].中国热带农业, 2008(3):17. |
| [5] | 蔡永强, 向青云, 陈家龙, 等.火龙果的营养成分分析[J].经济林研究, 2008, 26(4):53-56. |
| [6] | 陈丽娜, 陈石, 李润唐, 等.红肉火龙果与白肉火龙果品质分析[J].中国南方果树, 2011, 40(4):69-70. |
| [7] | 周丽屏, 郭璇华.火龙果茎的生物活性成分及其开发应用前景[J].食品研究与开发, 2007, 28(7):169-172. |
| [8] | 邬方宁.超声提取技术在现代中药中的应用[J].中草药, 2007, 38(2):315-316. |
| [9] | 兰冬梅, 许平, 林晓岚, 等.超声波辅助渗透脱水预处理的农产品干制研究进展[J].亚热带农业研究, 2015, 11(2):133-138. |
| [10] | 蒲彪, 岳金玫, 陈安均, 等.响应面法优化块菌多糖的超声波辅助提取工艺[J].核农学报, 2013, 27(7):996-1002. |
| [11] | 鲁轮, 郑少燕, 赵晓勤, 等.响应面法优化超声辅助提取南板蓝根多糖工艺[J].广州中医药大学学报, 2015, 32(3):508-512. |
| [12] | 黄诚, 喻晓梅, 尹红.超声波提取黄秋葵多糖的工艺条件研究[J].现代农业科技, 2015(11):299-301. |
| [13] | 王桓, 潘杨, 敬思群.超声强化提取喀什小枣多糖的工艺研究[J].食品研究与开发, 2009, 30(11):40-43. |
| [14] | 黄礼德, 郭立强, 潘廷啟, 等.正交设计优化土人参多糖的超声提取工艺[J].中国酿造, 2012, 31(3):105-107. |
| [15] | 盛家荣, 曾令辉, 陈超球, 等.多糖的提取、分离及结构分析[J].广西师范学院学报(自然科学版), 1999, 16(4):49-54. |
| [16] | 张青, 张天民.苯酚——硫酸比色法测定多糖含量[J].山东食品科技, 2004(7):17-18. |
| [17] | 洪小君, 林端权, 王春莲, 等.应用响应面法优化复合酶提取绣球菌多糖工艺[J].亚热带农业研究, 2015, 11(1):40-45. |
| [18] | 吴有炜.试验设计与数据处理[M].苏州:苏州大学出版社, 2002:115-154. |
 2016, Vol. 12
2016, Vol. 12


