文章信息
- 沈立明, 钟惠, 朱雅婷, 赵亚梅, 吴沙沙, 翟俊文
- HEN Liming, ZHONG Hui, ZHU Yating, ZHAO Yamei, WU Shasha, ZHAI Junwen
- 温度胁迫下4种广义虾脊兰属植物的光合特性
- Photosynthetic characteristics of four Calanthe s. l. species under temperature stress
- 森林与环境学报,2021, 41(1): 60-65.
- Journal of Forest and Environment,2021, 41(1): 60-65.
- http://dx.doi.org/10.13324/j.cnki.jfcf.2021.01.008
-
文章历史
- 收稿日期: 2020-10-17
- 修回日期: 2020-11-22
2. 兰科植物保护与利用国家林业和草原局重点实验室, 福建 福州 350002
2. Key Laboratory of National Forestry and Grassland Administration for Orchid Conservation and Utilization, Fuzhou, Fujian 350002, China
广义虾脊兰属(Calanthe s. l.)植物是国内外兰花爱好者青睐的兰科(Orchidaceae)花卉,主要分布在亚洲东部的亚热带及南部的部分热带、非洲的热带、美洲中部及大洋洲东部等地区[1]。虾脊兰属内三褶虾脊兰[Calanthe triplicata(Willemet) Ames]、虾脊兰(Calanthe discolor Lindl.)及剑叶虾脊兰(Calanthe davidii Franch.)等多个物种的根部和假鳞茎均可入药,用于活血、散瘀、清热、止痛,是应用非常广泛的传统中药[2]。据记载,中国有50多种虾脊兰属植物,超过20种为特有种[1]。尽管中国的广义虾脊兰属野生资源较为丰富,但由于人们的长期采挖和生境变化,其野外居群数量逐年缩减, 加之该属植物自然繁殖率低,种质资源相关的研究尚处于起步阶段,大量广义虾脊兰属植物正濒临灭绝的风险[3-4]。因此,研究广义虾脊兰属植物的生物学特性,了解其生长发育规律,提高该属植物的生产栽培技术,进而满足市场需求,对于广义虾脊兰属植物种质资源的保护和开发利用具有重要意义。
目前,对植物光合特性的研究已经成为鉴定评价植物抗逆能力最常用的手段之一,在生产实践上有十分重要的意义,特别是在不同温度逆境中植物光合特性方面,其它植物已有相关研究[5-7],但广义虾脊兰属植物的研究滞后。植物光合作用在环境温度短时间或者小范围偏离植物最适温度时虽会受到抑制,却能在温度恢复之后恢复光合效率[8]。因此,本研究以避免植株受损伤为前提,通过人工智能气候箱设定低温、室温和高温3种温度条件,对淡红离翅兰[Preptanthe rubens (Ridl.)Ridl.]、银带虾脊兰(Calanthe argenteostriata C. Z. Tang & S. J. Cheng)、三褶虾脊兰及长距虾脊兰[Calanthe sylvatica (Thou.)Lindl.]共4种广义虾脊兰属植物的光合-光响应曲线进行了测定,并利用直角双曲线修正模型[9]拟合出光合生理参数,探讨短期温度胁迫下这4种植物光响应特征参数的变化规律,为广义虾脊兰属植物的引种、育种和规模化栽培提供理论依据。
1 材料与方法 1.1 试验材料供试材料为淡红离翅兰(花期为11月—次年1月)、银带虾脊兰(花期为4—5月)、三褶虾脊兰(花期为4—5月)及长距虾脊兰(花期为4—9月),于2017年春季引种至福建农林大学森林兰苑(26°05′20″N,119°13′45″E)[1]。该区冬冷夏热,年平均气温为16~20 ℃,相对湿度约77%。选用长势基本一致且生长状态健康的植株(植株已开过花,但未授粉结果,并于花谢后剪掉花枝),每种植物测定4株,每株测定1片完全成熟的叶片,测定时避开主叶脉且靠近叶片中部位置。
1.2 试验方法2018年9月,在人工智能气候箱(相对湿度为70%,光照度为2 000 lx)中进行试验,设置低温(10 ℃)、室温(25 ℃,CK)和高温(35 ℃)3个温度处理。将4种广义虾脊兰属植物分别放进人工智能气候箱进行1 h的环境温度处理,并将待测叶片置于饱和光(1 000 μmol·m-2·s-1)下照射30 min,使其充分适应。利用LI-6400XT便携式光合测定系统(LR-COR,美国)对叶片进行光合作用净光合速率(net photosynthesis rate,Pn)、气孔导度(stomatal conductance,Gs)、蒸腾速率(transpiration rate,Tr)测定,测定时控制叶室CO2浓度为400 mmol·mol-1,光照强度(photosynthetically active radiation, PAR)设定梯度为1 200、1 000、800、600、500、400、300、200、150、100、50、25、0 μmol·m-2·s-1,由LI-6400XT LED红蓝光源提供。启动仪器,预热后按照温度由低到高的顺序进行测定,进入自动测量程序,随PAR由高到低顺序进行测量,最大等待时间为300 s,最小等待时间为120 s,获得Pn、Gs及Tr,并筛选出3组有效数据。
1.3 数据处理利用光合计算4.1软件中的直角双曲线修正模型[9]对3组有效数据进行拟合,获得暗呼吸速率(dark respiration rate, Rd)、初始量子效率、光补偿点(light compensation point,LCP)、光饱和点(light saturation point,LSP)、最大净光合速率(Pnmax),利用Excel 2016软件将测定的数据绘制成Pn-PAR响应曲线及PAR为400 μmol·m-2·s-1时的Gs、Tr柱状图,并使用SPSS 19.0统计软件的Duncan法对光合参数进行多重比较。
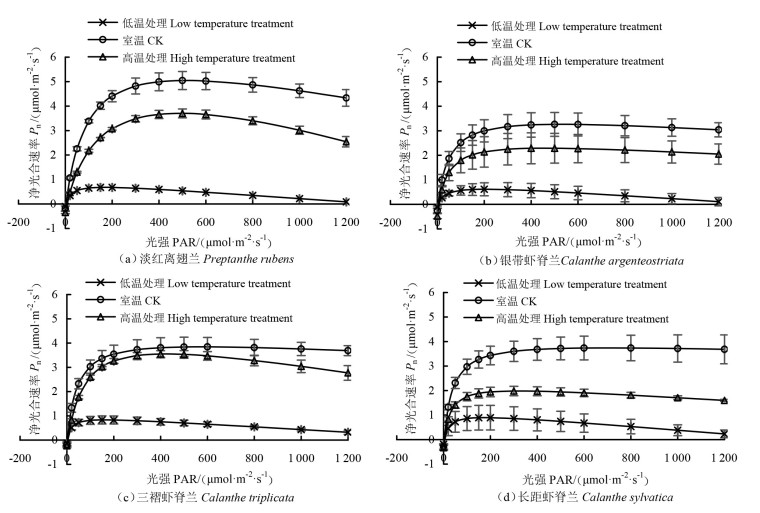
2 结果与分析 2.1 温度胁迫对植株叶片光合-光响应曲线的影响使用光合计算4.1软件中的直角双曲线修正模型[9]对4种广义虾脊兰属植物在低温、室温、高温处理下的光响应曲线进行拟合,得到的方程系数(R2):淡红离翅兰为0.932、0.993、0.992;银带虾脊兰为0.924、0.984、0.990;三褶虾脊兰为0.914、0.988、0.992;长距虾脊兰为0.924、0.976、0.992。在3种温度处理下,4种广义虾脊兰属植物的Pn均随PAR的增加而呈现先上升后下降的趋势,各自出现了不同程度的光抑制现象,相比于室温、高温胁迫,4种植物均在低温胁迫下先出现明显的光抑制现象;除了银带虾脊兰外,高温胁迫下淡红离翅兰、三褶虾脊兰和长距虾脊兰的光抑制现象相比于各自室温状态发生的光抑制现象更为明显;室温下,淡红离翅兰的光抑制现象在4种植物中表现最为明显,而三褶虾脊兰与长距虾脊兰均未出现明显的光抑制现象,淡红离翅兰和三褶虾脊兰在高温胁迫下的光抑制现象明显于银带虾脊兰和长距虾脊兰(图 1)。
|
图 1 4种广义虾脊兰属植物的叶片光合-光响应曲线 Fig. 1 Leaf photosynthesis-light response curve of photosynthetic rate of four Calanthe s. l. species |
由表 1可知,淡红离翅兰、三褶虾脊兰在3种温度处理下各自的初始量子效率无显著差异;银带虾脊兰在低温胁迫下,其初始量子效率最低,且在高温胁迫与室温下的无显著差异;3种温度处理下长距虾脊兰在低温胁迫的初始量子效率和在室温下的差异显著,低温胁迫下的最低,室温下的最高,高温胁迫下的则居中。4种广义虾脊兰属植物在低温胁迫下的Pnmax均最低;三褶虾脊兰在低温胁迫下的Pnmax与高温胁迫及室温下的差异显著,而在高温胁迫下的与室温下的无显著差异;此外,淡红离翅兰、银带虾脊兰和长距虾脊兰在3种温度处理下,各自的Pnmax间差异显著,均为室温下的最高,高温胁迫下的次之,低温胁迫下的最低。淡红离翅兰及银带虾脊兰在低温胁迫下的LSP均最低,与高温胁迫及室温下的差异显著,且在高温胁迫下的与室温下的无显著差异;三褶虾脊兰在3种温度处理下的LSP差异显著,表现为室温下的最高,高温胁迫下的次之,低温胁迫下的最低;长距虾脊兰在室温下的LSP最高,与高温胁迫及低温胁迫下的均差异显著,其中高温胁迫下的与低温胁迫下的无显著差异。淡红离翅兰、银带虾脊兰及三褶虾脊兰各自的LCP均表现为在高温胁迫下最高,与低温胁迫及室温下的差异显著,且低温胁迫下的与室温下的无显著差异;长距虾脊兰在3种温度处理下的LCP无显著差异。淡红离翅兰、三褶虾脊兰及长距虾脊兰在3种温度处理下各自的Rd间无显著差异;银带虾脊兰在高温胁迫下的Rd最高,与室温及低温胁迫下的均差异显著,其中室温与低温胁迫下的Rd无显著差异。
| 物种 Species |
处理 Treatment |
初始量子效率 Initial quantum efficiency /(μmol·μmol-1) |
最大净光合速率Pnmax /(μmol·m-2·s-1) |
光饱和点LSP /(μmol·m-2·s-1) |
光补偿点LCP /(μmol·m-2·s-1) |
暗呼吸速率Rd /(μmol·m-2·s-1) |
| 淡红离翅兰 | 低温Low temperature | 0.041±0.013a | 0.680±0.155c | 170.761±10.146b | 2.830±0.163b | 0.103±0.032a |
| Preptanthe rubens | 室温CK | 0.077±0.013a | 5.050±0.369a | 527.702±57.147a | 2.344±1.088b | 0.183±0.102a |
| 高温High temperature | 0.048±0.026a | 3.816±0.416b | 484.074±186.436a | 7.803±1.028a | 0.345±0.180a | |
| 银带虾脊兰 | 低温Low temperature | 0.038±0.016b | 0.626±0.269c | 186.543±75.084b | 3.542±0.589b | 0.116±0.051b |
| Calanthe | 室温CK | 0.091±0.029a | 3.280±0.463a | 608.002±256.369a | 2.972±1.293b | 0.248±0.098b |
| argenteostriata | 高温High temperature | 0.081±0.014a | 2.318±0.629b | 589.776±225.088a | 6.950±0.392a | 0.480±0.102a |
| 三褶虾脊兰 | 低温Low temperature | 0.074±0.016a | 0.833±0.167b | 163.740±4.276c | 1.862±0.259b | 0.120±0.009a |
| Calanthe triplicata | 室温CK | 0.119±0.041a | 3.854±0.394a | 631.017±127.123a | 1.610±0.509b | 0.193±0.122a |
| 高温High temperature | 0.067±0.003a | 3.552±0.143a | 423.362±30.343b | 3.655±0.496a | 0.233±0.023a | |
| 长距虾脊兰 | 低温Low temperature | 0.065±0.033b | 0.897±0.504c | 178.571±14.875b | 4.859±3.649a | 0.193±0.014a |
| Calanthe sylvatica | 室温CK | 0.126±0.018a | 3.755±0.498a | 770.379±231.117a | 2.299±0.693a | 0.278±0.109a |
| 高温High temperature | 0.103±0.010ab | 1.983±0.191b | 323.528±24.175b | 3.754±1.370a | 0.332±0.101a | |
| 注:同列数据后不同的小写字母表示同一种不同温度处理间差异达0.05显著水平。Note: different small letters of the same species between different temperatures indicate a significant difference at the 0.05 level. | ||||||
由图 2(a)可知,在短期温度胁迫下,4种虾脊兰属植物的Gs均有显著变化。低温胁迫使得4种广义虾脊兰属植物的Gs显著降低;高温胁迫下,淡红离翅兰和银带虾脊兰的Gs与室温相比,表现为显著上升,而三褶虾脊兰和长距虾脊兰的则表现出显著下降。4种广义虾脊兰属植物在高温胁迫下的Gs均显著大于低温胁迫下的。由图 2(b)可知,低温胁迫使得4种广义虾脊兰属植物的Tr显著降低,低于室温及高温胁迫下的。高温胁迫下,除长距虾脊兰的Tr较室温的没有表现出显著提升外,其余3种广义虾脊兰属植物的Tr均表现出显著提升。

|
注:不同小写字母表示同一种不同温度处理间差异达0.05显著水平。Note: different small letters of the same species between different temperatures indicate a significant difference at the 0.05 level. 图 2 4种广义虾脊兰属植物叶片的气孔导度与蒸腾速率 Fig. 2 Leaf Gs and Tr of four Calanthe s. l. species |
光合作用作为一个易受环境影响的重要生理过程,对温度的变化极为敏感[10]。研究表明,低温使植物光合酶的活性和光合电子传递速率降低,降低植物对光能的利用能力[11]。此外,高温同样会导致植物光合速率降低[12]。兰科被认为是与环境高度适应的类群,对环境变化的响应具有敏感性[13-14]。研究发现, 墨兰[Cymbidium sinense (Jacks. ex Andrews) Willd.]对温度升高极为敏感[15],文心兰(Oncidium Sw.)光合作用受夏季高温和冬季寒潮的影响大[6],高温胁迫对白及[Bletilla striata (Thunb.)Rchb. f.]的Pn产生的影响相比于干旱胁迫更明显[5]。本研究显示,短期的低温胁迫显著限制了4种广义虾脊兰属植物的Pn,除三褶虾脊兰在高温胁迫下的Pnmax与室温下的无显著差异外,短期高温胁迫显著限制了其余3种广义虾脊兰属植物的Pn,且低温胁迫对植株Pn的限制作用较高温胁迫更大。
当植物光合作用所需的光能过剩时会引起光合效率降低,出现光抑制现象,特别是在环境胁迫下植物更易发生光抑制[16-17]。本研究发现,短期温度胁迫会增加4种广义虾脊兰属植物光合作用对光强的敏感性,使得植株容易出现光抑制现象,并且,相比于高温胁迫,低温胁迫促使光抑制现象发生的作用更为明显。初始量子效率表现植物光合机构对光能的最大转化能力[18],本研究中短期温度胁迫对淡红离翅兰与三褶虾脊兰的光能利用能力没有显著影响。此外,对于银带虾脊兰和长距虾脊兰,低温胁迫导致其光能利用能力出现了较为明显的减弱。
LSP和LCP被认为是能够体现植物耐阴性强弱的两个指标[19-20]。本研究结果显示,室温下,4种广义虾脊兰属植物的LSP均高于卡特兰(Cattleya×hybrida)和蝴蝶兰(Phalaenopsis Aphrodite Rchb. f.)(130~180 μmol·m-2·s-1)[21],与同属的虾脊兰(867.678 μmol·m-2·s-1)[22]相近。4种广义虾脊兰属植物的LCP均与虾脊兰(2.209 μmol·m-2·s-1)[22]相近,而低于春兰[Cymbidium goeringii (Rchb. f.) Rchb. f.](55 μmol·m-2·s-1)[23]。由此可见,这4种广义虾脊兰属植物均具有良好的弱光利用能力,耐阴性强。相比于室温,短期低温胁迫下,4种广义虾脊兰属植物的LCP无显著变化,而LSP均显著降低,说明低温胁迫对植株利用弱光的能力无影响,而对强光的适应力变弱。另一方面,短期高温胁迫虽然对淡红离翅兰与银带虾脊兰的LSP无明显影响,却使其LCP显著升高,导致其弱光利用能力减弱。对于三褶虾脊兰来说,高温胁迫使得其LSP显著降低,LCP显著升高,该物种的弱光及强光适应力同时减弱,光照适应范围显著缩小。长距虾脊兰的LSP受高温胁迫影响显著降低,对强光的适应力减弱,而其LCP受到高温胁迫的影响并不明显,即短期高温胁迫对其利用弱光的能力无明显影响。此外,本研究中短期温度胁迫对淡红离翅兰、三褶虾脊兰及长距虾脊兰的Rd无明显影响。而银带虾脊兰在高温胁迫下的Rd表现高于室温及低温胁迫下的,其高温下呼吸作用消耗有机物的程度增大。4种广义虾脊兰属植物常见于高海拔山地的林下阴湿处,最高海拔可达3 500 m[1],处于弱光的生长环境下。因此,在生产栽培中应适当进行遮阴,以维持其光合作用反应条件的稳定,特别是存在环境温度胁迫时更应避免植株受到强光伤害。
气孔的开放状况深刻影响着植物光合作用所进行的物质交换,其开放状况能够通过Gs来反映;蒸腾作用是植物进行物质交换的一种途径,可以带走植物体内多余的热量,维持植物进行生理反应所需条件的稳定[24-25]。影响植物光合效率的因素有气孔及非气孔因素,非气孔因素很多,如叶绿体内部组成结构、植物膜系统、光合电子传递系统、光合色素及光合酶的活性[26-27]。通过本研究的分析结果来看,低温胁迫使得4种广义虾脊兰属植物的Gs与Tr显著降低,导致光合作用所需的气体交换受限制,进而降低了植物的Pn,与郝平安[7]对蝴蝶兰的研究结果基本一致。然而,高温胁迫抑制植物光合作用的机制尚有争论:一种理论认为植物受到高温胁迫Gs降低,使得光合机构的CO2供应受限,进而降低了光合最大羧化效率,植物光合作用受到抑制;另一理论则认为高温胁迫降低了光合电子传递及核酮糖-1, 5-二磷酸羧化酶/加氧酶的活性, 从而抑制了植物的光合作用[28-29]。本研究中,高温胁迫使淡红离翅兰和银带虾脊兰的Gs、Tr均表现为显著上升,可能是因为其尚未发生光抑制,植株通过增强蒸腾作用来散去多余热量以保护光合机构,但因高温抑制了光合电子传递及Rubiso酶的活性使得其Pn下降,更为符合后者的理论。高温胁迫下长距虾脊兰Gs、Tr与Pn均显著降低,可能是高温导致其Gs降低,使得进行光合作用所需的CO2供应受限,与前者的理论较为符合。对于高温胁迫下三褶虾脊兰的Gs表现出显著下降,Tr显著上升,而Pn未出现明显下降,其原因可能是由不同虾脊兰属物种的适应性等有所差异,以致不同物种对Gs和蒸腾作用的响应不同,最终对植物光合作用等生理反应产生影响[30]。
综上所述,短期低温胁迫的存在降低了此4种广义虾脊兰属植物的Pnmax、LSP,植株光合能力显著减弱,对光强的敏感性增强,容易出现光抑制现象。受短期高温胁迫影响,除长距虾脊兰外的3种植物LCP升高,弱光利用能力明显减弱;三褶虾脊兰和长距虾脊兰的LSP降低,对强光的适应力减弱,夏季高温时适当遮阴将有利于植株进行光合作用。此外,不同广义虾脊兰属物种叶片的Gs和蒸腾作用对温度胁迫的响应机制存在差异。温度作为植物发生光合作用的基础反应条件之一,往往决定着植物体的生长发育。在全球变暖,极端天气频发的现状下,研究温度胁迫对广义虾脊兰属植物光合作用的影响可为该属植物的引种、育种和规模化栽培提供理论依据,对该属植物的保护及后续开发利用来说具有极其重要的意义。
| [1] |
陈心启, 吉占和, 郎楷永, 等. 中国植物志:第18卷[M]. 北京: 科学出版社, 1999.
|
| [2] |
国家中医药管理局《中华本草》编委会. 中华本草-7[M]. 上海: 上海科学技术出版社, 1999.
|
| [3] |
苏文君, 龙波, 刘飞虎. 虾脊兰属植物研究现状[J]. 北方园艺, 2012(16): 190-193. |
| [4] |
汪松, 解焱. 中国物种红色名录:第一卷:红色名录[M]. 北京: 高等教育出版社, 2004.
|
| [5] |
王莹博, 许申平, 马杰, 等. 高温干旱胁迫对白及光合特性及叶绿素荧光参数的影响[J]. 河南农业大学学报, 2018, 52(2): 199-205. |
| [6] |
孔倩倩.高温胁迫下文心兰对外源水杨酸的生理响应及WRKY基因的克隆[D].福州: 福建农林大学, 2017.
|
| [7] |
郝平安.蝴蝶兰对低温胁迫的生理响应及相关基因表达特性研究[D].郑州: 河南农业大学, 2019.
|
| [8] |
SLAYTER R O, MORROW P A. Altitudinal variation in the photosynthetic characteristics of snow gum, Eucalyptus pauciflora Sieb. ex Spreng.Ⅰ.Seasonal changes under field conditions in the Snowy Mountains area of south-eastern Australia[J]. Australian Journal of Botany, 1977, 25(1): 1-20. DOI:10.1071/BT9770001 |
| [9] |
叶子飘, 王建林. 植物光合-光响应模型的比较分析[J]. 井冈山学院学报(自然科学版), 2009, 30(2): 9-13. DOI:10.3969/j.issn.1674-8085.2009.02.002 |
| [10] |
SZYMA SKA R, LESAK I, ORZECHOWSKA A, et al. Physiological and biochemical responses to high light and temperature stress in plants[J]. Environmental and Experimental Botany, 2017, 139: 165-177. DOI:10.1016/j.envexpbot.2017.05.002 |
| [11] |
朱玲, 张旭, 张姣佼, 等. 石蒜光合特性比较及其对温度胁迫的响应[J]. 分子植物育种, 2020, 18(18): 6. |
| [12] |
付豪, 朱宁华, 段润梅, 等. 温度与光照强度对红心杉幼苗光合特性的影响[J]. 中南林业科技大学学报, 2020, 40(7): 73-78. |
| [13] |
ROBERTS D L, DIXON K W. Orchids[J]. Current Biology, 2008, 18(8): R325-R329. DOI:10.1016/j.cub.2008.02.026 |
| [14] |
刘仲健, 陈心启, 陈利君, 等. 中国兜兰属植物[M]. 北京: 科学出版社, 2009.
|
| [15] |
刘仲健, 陈利君, 刘可为, 等. 气候变暖致使墨兰(Cymbidium sinense)野外种群趋向灭绝[J]. 生态学报, 2009, 29(7): 3 443-3 455. |
| [16] |
王玉萍, 郜春晓, 王盛祥, 等. 低温弱光胁迫下芸豆叶片光抑制与类囊体膜脂构成变化[J]. 草业学报, 2020, 29(8): 116-125. |
| [17] |
GOH C H, KO S M, KOH S, et al. Photosynthesis and environments:photoinhibition and repair mechanisms in plants[J]. Journal of Plant Biology, 2012, 55(2): 93-101. DOI:10.1007/s12374-011-9195-2 |
| [18] |
叶子飘, 胡文海, 闫小红, 等. 基于光响应机理模型的不同植物光合特性[J]. 生态学杂志, 2016, 35(9): 2 544-2 552. |
| [19] |
VALLADARES F, NⅡNEMETS V. Shade tolerance, a key plant feature of complex nature and consequences[J]. Annual Review of Ecology, Evolution, and Systematics, 2008, 39: 237-257. DOI:10.1146/annurev.ecolsys.39.110707.173506 |
| [20] |
汪小飞, 靳文文. 扇脉杓兰耐阴性的测定与分析[J]. 南京林业大学学报(自然科学版), 2014, 38(S1): 57-61. |
| [21] |
吴根良, 何勇, 王永传, 等. 不同光照强度下卡特兰和蝴蝶兰光合作用和叶绿素荧光参数日变化[J]. 浙江林学院学报, 2008, 25(6): 733-738. |
| [22] |
冯巧, 权秋梅, 皮华强, 等. 虾脊兰光合-光响应曲线的拟合及分析[J]. 西华师范大学学报(自然科学版), 2014, 35(4): 333-338. |
| [23] |
宋军阳. 秦岭野生春兰光合特性研究[J]. 林业科技通讯, 2019(12): 59-62. |
| [24] |
杜久军, 左力辉, 梁海永, 等. 5种榆树光合特性对比[J]. 分子植物育种, 2018, 16(7): 2 348-2 357. |
| [25] |
PAPANATSIOU M, PETERSEN J, HENDERSON L, et al. Optogenetic manipulation of stomatal kinetics improves carbon assimilation, water use, and growth[J]. Science, 2019, 363(6 434): 1 456-1 459. |
| [26] |
DRAKE J E, POWER S A, DUURSMA R A, et al. Stomatal and non-stomatal limitations of photosynthesis for four tree species under drought:a comparison of model formulations[J]. Agricultural and Forest Meteorology, 2017, 247: 454-466. |
| [27] |
叶子飘, 谢志亮, 段世华, 等. 设施栽培条件下三叶青叶片光合的气孔和非气孔限制[J]. 植物生理学报, 2020, 56(1): 41-48. |
| [28] |
杜尧东, 李键陵, 王华, 等. 高温胁迫对水稻剑叶光合和叶绿素荧光特征的影响[J]. 生态学杂志, 2012, 31(10): 2 541-2 548. |
| [29] |
MAKINO A, SAGE R F. Temperature response of photosynthesis in transgenic rice transformed with 'sense' or 'antisense' rbcS[J]. Plant and Cell Physiology, 2007, 48(10): 1 472-1 483. |
| [30] |
李玉凤, 黄婧, 马姜明, 等.桂林喀斯特石山50种常见植物叶片光合特性研究[J/OL].生态学报, 2020(23):1-11[2020-11-20].http://kns.cnki.net/kcms/detail/11.2031.Q.20201029.1134.052.html.
|

 2021, Vol. 41
2021, Vol. 41


