文章信息
- 郑钰铟, 胡素萍, 陈辉, 郑国华, 张桃香, 陈俊杰
- ZHENG Yuyin, HU Suping, CHEN Hui, ZHENG Guohua, ZHANG Taoxiang, CHEN Junjie
- 油茶饼粕生物炭和有机肥对土壤酶活性的影响
- Effects of Camellia cake biochar and organic fertilizer on soil enzymatic activities
- 森林与环境学报,2018, 38(3): 348-354.
- Journal of Forest and Environment,2018, 38(3): 348-354.
- http://dx.doi.org/10.13324/j.cnki.jfcf.2018.03.014
-
文章历史
- 收稿日期: 2017-09-21
- 修回日期: 2018-01-15
福建省油茶(Camellia oleifera Abel.)林以红壤和紫色土为主,但是红壤和紫色土的强酸性和营养元素有效性低等特点导致油茶产量较低。近年来,国家越来越重视油料产业的发展,普遍推广“上改树、下改土”的低产林改造措施,因此土壤改良成为低产林改造中的一项必要措施[1]。
油茶饼粕是油茶榨油后的残渣,含有丰富的多糖、纤维素、皂素和蛋白质等[2]。我国油茶资源丰富,每年油茶籽消耗量为1.07×107 t,油茶饼粕占6.83×106 t[3]。查钱慧等[4]研究表明施用油茶饼粕发酵的有机肥可以促进番茄(Lycopersicon esculentum Mill.)的生长。有机肥是一种缓效肥料,养分全面,有机质含量丰富,有利于改善土壤和微生物群落结构[5-6]。梁元振等[7]研究表明有机肥容易腐熟分解,有利于增加土壤温度,为微生物创造良好的环境, 改善土壤孔隙结构,使土壤疏松,保水保肥。生物炭是一类高度芳香化、难溶解的固态物质,是生物质在完全或部分缺氧条件下热解、炭化产生的[8]。国际生物炭协会(International Biochar Initiative)指出生物炭施加到土壤中具有巨大的农业应用价值。目前生物炭在针对土壤的强酸性和营养元素有效性低等方面展现出巨大的应用修复潜力[9]。陈心想等[10]研究表明施用生物炭可以提高土壤有效磷、速效钾和矿质氮含量。尚杰等[11]研究表明施用生物炭可以显著提高糜子(Panicum miliaceum L.)产量。
土壤酶活性的高低反映了土壤微生物活性的高低,是土壤养分转化和运移能力强弱的表征[12],土壤酶活性的变化能够调控作物吸收养分的有效性[11],是土壤质量的潜在敏感指标和评价土壤肥力的重要指标[12-13]。因此,研究土壤酶活性的变化可以更好地解释施用生物炭对土壤微生态的影响。周震峰等[14]研究表明添加花生壳生物炭对土壤脲酶和蔗糖酶有显著促进作用。贾俊香等[15]研究表明添加秸秆生物炭和有机肥对土壤脲酶、蔗糖酶、过氧化氢酶和碱性磷酸酶均有促进作用。
目前关于油茶饼粕生物炭和有机肥对土壤酶活性影响的研究还鲜见报道。因此,本研究以油茶林红壤和紫色土为研究对象,以油茶饼粕为原料制备生物炭和发酵有机肥。设置单独添加生物炭和有机肥、混合添加生物炭和有机肥等不同处理,进行室内培养,研究施加生物炭和有机肥后土壤酶活性的动态变化,旨在开启油茶饼粕新用途,为施用生物炭和有机肥对于改善油茶林土壤微生态提供一定的科学依据。
1 材料与方法 1.1 供试材料供试土壤:取自福建省闽侯县桐口林场油茶林红壤和福建省三明市宁化县田背村油茶林紫色土0~20 cm表层土壤。自然风干后除去碎石、杂根,研磨过2 mm土筛。
生物炭的制备:以油茶饼粕为原料,粉碎过2 mm筛。采用CHUN et al[16]生物炭制备方法。将原料放于坩埚中置马弗炉300及600 ℃炭化2 h,冷却至室温后取出。
有机肥的制备:以油茶饼粕为原料,粉碎过2 mm筛。将油茶饼粕放置在80 ℃以上的热水浸泡2 h后过滤,除去水分,盖上透明薄膜发酵,定期揭开加入适量的蒸馏水并搅动,直到油茶饼粕无异味,发酵完毕[4],放入冰箱4 ℃保存备用。
| 土壤类型 Soil type |
pH值 pH value |
有机质含量 SOM/(g·kg-1) |
全碳含量 TC/(g·kg-1) |
全氮含量 TN/(g·kg-1) |
全磷含量 TP/(g·kg-1) |
砂粒含量 Sand/% |
粉粒含量 Silt/% |
黏粒含量 Clay/% |
| 红壤Red soil | 4.48 | 13.99 | 8.53 | 0.97 | 0.12 | 63.55 | 7.40 | 29.05 |
| 紫色土Purple soil | 4.83 | 17.53 | 7.67 | 1.07 | 0.13 | 85.86 | 4.26 | 9.88 |
| Note:SOM indicates soil organic matter, TC indicates total carbon, TN indicates total nitrogen, TP indicates total phosphorus. | ||||||||
| 肥料类型 Fertilizer Type |
pH值 pH value |
全碳含量 TC/(g·kg-1) |
全氮含量 TN/(g·kg-1) |
全磷含量 TP/(g·kg-1) |
灰分含量 Ash content/% |
产率 Productive rate/% |
比表面积 BET surface area/(cm2·g-1) |
| 300 ℃生物炭Biochar 300 ℃ | 5.80 | 562.933 | 14.267 | 2.749 | 3.00 | 54.77 | 66.195 |
| 600 ℃生物炭Biochar 600 ℃ | 10.00 | 250.500 | 11.667 | 5.353 | 28.33 | 28.06 | 47.420 |
| 有机肥Organic fertilizer | 6.84 | 437.267 | 10.500 | 1.450 | 6.00 |
试验共设12个处理:红壤(RS)空白对照、红壤+300 ℃生物炭(RS+B300 ℃)、红壤+600 ℃生物炭(RS+B600 ℃)、红壤+有机肥(RS+OF)、红壤+300 ℃生物炭+有机肥(RS+B300 ℃+OF)、红壤+600 ℃生物炭+有机肥(RS+B600 ℃+OF)、紫色土(PS)空白对照、紫色土+300 ℃生物炭(PS+B300 ℃)、紫色土+600 ℃生物炭(PS+B600 ℃)、紫色土+有机肥(PS+OF)、紫色土+300 ℃生物炭+有机肥(PS+B300 ℃+OF)、紫色土+600 ℃生物炭+有机肥(PS+B600 ℃+OF)。具体方法:称取1 200 g干土于240 mm×340 mm自封袋中,调节土壤含水量至田间持水量的70%,放置在培养箱25 ℃条件下培养。
每个处理设3个重复,生物炭和有机肥添加量为干土重的3%(混合添加时生物炭和有机肥各为干土重的1.5%)。培养开始后,分别于第5、10、15、30天取样测定脲酶、蔗糖酶、酸性磷酸酶。培养期间每隔2 d采用称重法来保持土壤含水量。
1.3 测定指标及方法脲酶、酸性磷酸酶参考CANG et al[17]的方法测定,蔗糖酶参考关松荫[18]的方法进行测定。脲酶以24 h后1 g土壤中NH4+-N的质量(mg)表示酶活性。蔗糖酶以24 h后1 g土壤中葡萄糖的质量(mg)表示酶活性。酸性磷酸酶以2 h后1 g土壤中释放的酚质量(mg)表示酶活性。
pH值采用电位法(水土比例为2.5:1,水与生物炭或有机肥比为10:1)测定;土壤、生物炭和有机肥全碳(total carbon, TC)、全氮(total nitrogen, TN)含量采用碳氮元素分析仪(Elementar Vario EL Ⅲ,德国)测定;全磷(total phosphorus, TP)通过酸融提取,其含量采用ICP元素分析仪(ICP-MS,日本)测定;有机质(soil organic matter, SOM)含量采用水合热重洛酸钾氧化-比色法[19]测定;土壤可溶性有机碳(dissolved organic carbon, DOC)和可溶性有机氮(dissolved organic nitrogen, DON)含量采用TOC总氮分析仪(TOC-L,日本)测定(水土比为5:1);土壤机械组成采用比重计法[19]测定;产量测定——称量油茶饼粕原料干重,计算不同温度生物炭的产率,产率(%)= (M1/M2) ×100(其中:M1为热解后的样品质量,g; M2为油茶饼粕的干重,g);灰分测定——将原生物炭平铺于陶瓷坩埚,750 ℃炭化6 h,冷却称重,计算公式为:CA(%)=(M1-M2/M)×100(其中:CA为灰分含量,M1为灰分和坩埚质量,g; M2为坩埚质量,g; M为生物炭质量,g);比表面积采用全自动比表面积仪测定,采用Brunauer-Emmettv Teller(BET)公式计算。
1.4 数据处理运用Excel 2007软件对不同处理的土壤的酶活性指标进行处理并绘图,误差线为平均数±标准差;用SPSS 19.0软件对不同土壤酶与各养分进行单因素分析和相关分析。
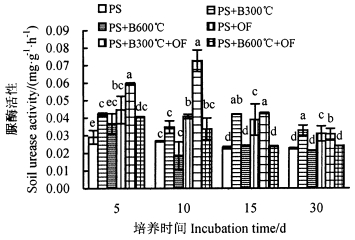
2 结果与分析 2.1 施肥处理对土壤脲酶活性的影响由图 1和图 2可知,整个培养期间,添加不同温度生物炭和有机肥均对土壤中脲酶活性有较强的促进作用,红壤和紫色土中脲酶活性随培养时间先升高后降低。培养初期,各施肥处理对土壤中的脲酶活性有一定的激发促进效应,且红壤强于紫色土。红壤和紫色土中大部分处理的脲酶活性在5 d后达到最大值。但是红壤中单独添加300 ℃生物炭处理与紫色土中混合添加300 ℃生物炭和有机肥处理的脲酶活性在培养第10天达到最高值,分别为对照的2.39和2.72倍,与其他处理的差异显著(P < 0.05)。随后红壤和紫色土中激发效应逐渐减弱,脲酶活性开始缓慢降低,在培养第30天达到最低值。培养结束后,各个处理相比对照的差异性降低,但单独添加300 ℃生物炭与混合添加300 ℃生物炭和有机肥的土壤脲酶活性均显著高于对照(P < 0.05),单独添加600 ℃生物炭处理与混合添加600 ℃生物炭和有机肥与对照差异不显著。单独添加有机肥与红壤对照的差异不显著,但要显著高于紫色土对照。

|
图 1 不同处理对红壤脲酶活性的影响 Fig. 1 Effects of treatments on red soil urease activity |
|
图 2 不同处理对紫色土脲酶活性的影响 Fig. 2 Effects of treatments on puple soil urease activity |
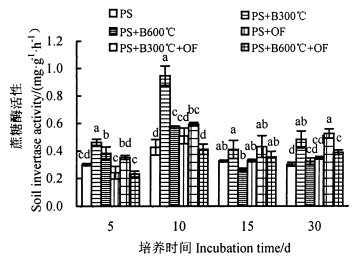
由图 3和图 4可知,红壤和紫色土中不同施肥处理的蔗糖酶活性存在显著差异。除单独添加300 ℃生物炭与混合添加300 ℃生物炭和有机肥对红壤蔗糖酶有显著的促进作用外,其余处理对红壤蔗糖酶活性的影响较小,且在培养期间变化较小。各施肥处理对紫色土蔗糖酶活性均呈先上升后下降趋势。单独添加300 ℃生物炭对红壤和紫色土蔗糖酶活性的激发效应均在第10天达到最大值,分别为对照的7.99和2.22倍,与其他处理均呈显著差异关系(P < 0.05)。培养10 d后,对红壤的促进一直保持着较高水平,但是对紫色土酶活性的促进作用显著减小,培养结束后,红壤中单独添加300 ℃生物炭与混合添加300 ℃生物炭和有机肥对蔗糖酶活性的促进作用显著,为对照的7.04和4.48倍。其余处理与对照差异不大,单独添加600 ℃生物炭对红壤蔗糖酶有轻微抑制作用。紫色土中各施肥处理的蔗糖酶活性差异较小,但均高于对照。

|
图 3 不同处理对红壤蔗糖酶活性的影响 Fig. 3 Effects of treatments on red soil invertase activity |
|
图 4 不同处理对紫色土蔗糖酶活性的影响 Fig. 4 Effects of treatments on purple soil invertase activity |
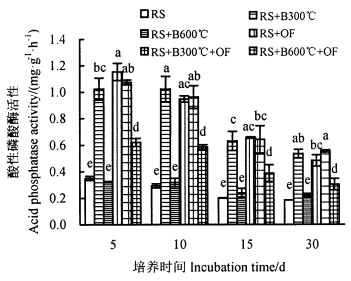
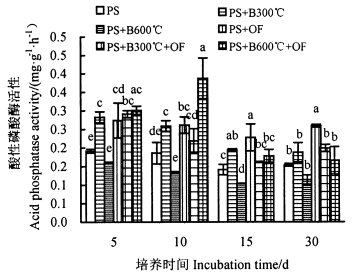
由图 5和图 6可知,在整个培养期间,不同施肥处理的红壤酸性磷酸酶活性均随培养时间呈下降趋势,添加300 ℃生物炭和有机肥的土壤酸性磷酸酶活性差异较小,且显著高于添加600 ℃生物炭处理(P < 0.05)。紫色土中大部分施肥处理的酸性磷酸酶活性在培养15 d后降至最小值,之后小幅度上升。混合添加600 ℃生物炭和有机肥处理在培养前10 d酶活性不断升高直至最大,最大值为对照的2.08倍,之后酶活性显著下降。单独添加600 ℃生物炭处理始终低于对照。培养结束后,各处理间酶活性的差异减小,红壤中各处理酸性磷酸酶活性均高于对照,添加300 ℃生物炭和有机肥处理效果优于添加600 ℃生物炭处理。紫色土中单独添加有机肥对酸性磷酸酶活性的促进作用显著高于其他处理(P < 0.05),添加600 ℃生物炭的酸性磷酸酶活性低于对照,为对照的73.9%。
|
图 5 不同处理对红壤酸性磷酸酶活性的影响 Fig. 5 Effects of treatments on red soil acid phosphatase activity |
|
图 6 不同处理对紫色土酸性磷酸酶活性的影响 Fig. 6 Effects of treatments on purple soil acid phosphatase activity |
由表 3和表 4可知,施用生物炭和有机肥均可不同程度地改善红壤和紫色土的化学性状,主要表现在:施用生物炭和有机肥都明显提高了土壤pH值,变化幅度随生物炭烧制温度的升高而增加,而单独添加有机肥对红壤pH值的影响小于添加生物炭,且对紫色土pH值的影响不显著。生物炭和有机肥的施用也显著地改变了红壤和紫色土的养分状况,与有机肥相比,施用生物炭对提高土壤养分元素含量的作用更强,其中全碳、全氮、全磷含量随生物炭烧制温度的升高其含量均显著增加,而有机质和可溶性有机碳含量随生物炭烧制温度的升高其贡献率减少。
| 处理 Treatment |
pH值 pH value |
有机质含量 SOM/(g·kg-1) |
全碳含量 TC/(g·kg-1) |
全氮含量 TN/(g·kg-1) |
全磷含量 TP/(g·kg-1) |
可溶性有机碳含量 DOC/(mg·kg-1) |
可溶性有机氮含量 DON/(mg·kg-1) |
| RS | 4.42f | 14.88e | 8.03f | 0.97e | 0.10c | 5.00d | 27.59d |
| RS+300 ℃ | 4.95b | 26.69a | 23.75b | 1.30cg | 0.12c | 17.09a | 5.09e |
| RS+B600 ℃ | 5.06a | 15.78e | 34.37a | 1.50ag | 0.19a | 6.22cd | 30.86c |
| RS+OF | 4.59e | 23.93b | 13.53e | 1.17ec | 0.18c | 7.69ce | 42.56a |
| RS+B300 ℃+OF | 4.72d | 23.68bc | 18.13d | 1.30dc | 0.12c | 10.66b | 27.15d |
| RS+B600 ℃+OF | 4.82c | 20.46d | 22.27c | 1.37bc | 0.13bc | 6.79de | 37.93b |
| 注:同列数据后不同小写字母示表示差异达显著水平(P < 0.05)。Note: different lowercase letters within the same column indicate significant different between treatments at P < 0.05 level. | |||||||
| 处理 Treatment |
pH值 pH value |
有机质含量 SOM/(g·kg-1) |
全碳含量 TC/(g·kg-1) |
全氮含量 TN/(g·kg-1) |
全磷含量 TP/(g·kg-1) |
可溶性有机碳含量 DOC/(mg·kg-1) |
可溶性有机氮含量 DON/(mg·kg-1) |
| PS | 4.86d | 17.74d | 7.50e | 1.07e | 0.13c | 6.33e | 0.83e |
| PS+300 ℃ | 4.96c | 28.83a | 18.15c | 1.53ab | 0.16b | 18.05a | 1.77ab |
| PS+B600 ℃ | 5.27a | 15.79e | 26.20a | 1.53a | 0.19a | 6.38e | 1.91a |
| PS+OF | 4.89d | 22.79c | 11.80ed | 1.27d | 0.08fg | 9.34c | 0.94e |
| PS+B300 ℃+OF | 4.92cd | 25.11b | 15.43dc | 1.37cd | 0.09eg | 12.16b | 1.30d |
| PS+B600 ℃+OF | 5.18b | 17.30d | 18.50bc | 1.35ad | 0.10dg | 8.41cd | 1.61bc |
| 注:同列数据后不同小写字母表示差异达显著水平(P < 0.05)。Note: different lowercase letters within the same column indicate significant different between treatments at P < 0.05 level. | |||||||
由表 5可知,红壤脲酶、蔗糖酶和酸性磷酸酶与土壤有机质和可溶性有机碳均呈极显著正相关,与可溶性有机氮呈极显著负相关。由表 6可知,紫色土脲酶与有机质呈极显著正相关,与可溶性有机碳呈显著正相关,蔗糖酶与有机质呈显著正相关,酸性磷酸酶与有机质和可溶性有机碳呈显著正相关。
| 酶活性 Enzymatic activity |
pH值 pH value |
有机质 SOM |
全碳 TC |
全氮 TN |
全磷 TP |
可溶性有机碳 DOC |
可溶性有机氮 DON |
| 脲酶Urease activity | 0.343 | 0.709** | -0.058 | 0.049 | 0.051 | 0.800** | -0.778** |
| 蔗糖酶Invertase activity | 0.096 | 0.775** | 0.103 | 0.268 | -0.183 | 0.578** | -0.694** |
| 酸性磷酸酶Acid phosphatase activity | 0.239 | 0.568** | -0.182 | -0.064 | 0.020 | 0.667** | -0.533** |
| 注:*代表 0.05水平上显著相关,**代表 0.01水平上显著相关。Note:*represents significant correlation at P < 0.05, **represents significant correlation at P < 0.01. | |||||||
| 酶活性Enzymatic activity | pH值pH value | 有机质SOM | 全碳TC | 全氮TN | 全磷TP | 可溶性有机碳DOC | 可溶性有机氮DON |
| 脲酶Urease activity | -0.068 | 0.630** | -0.146 | -0.015 | 0.353 | 0.498* | 0.091 |
| 蔗糖酶Invertase activity | -0.065 | 0.474* | 0.234 | 0.315 | 0.166 | 0.342 | 0.098 |
| 酸性磷酸酶Acid phosphatase activity | -0.076 | 0.411* | -0.126 | 0.019 | 0.353 | 0.408* | 0.194 |
| 注:*代表 0.05水平上显著相关,**代表 0.01水平上显著相关。Note:*represents significant correlation at P < 0.05, **represents significant correlation at P < 0.01. | |||||||
土壤酶活性表征土壤微生物活性水平、有机质积累和土壤水肥转化和迁移能力, 而土壤养分含量和孔隙结构是影响土壤酶活性的重要因素[20]。本文通过室内培养试验发现:300 ℃生物炭比600 ℃生物炭对土壤酶活性的促进作用更强。由表 2可得,和600 ℃生物炭相比,300 ℃生物炭拥有更丰富的碳氮含量和较大比表面积,施入土壤后可以快速提高土壤的肥力[21],且其疏松多孔的结构特点对土壤养分的吸附性较强,能够为土壤微生物提供栖息繁殖的微环境,增加土壤中微生物数量和活性,间接提高红壤和紫色土的酶活性[14]。同时生物炭灰分含量随着热解温度升高而增加(表 2),钾、镁、钙等元素以氧化物或碳酸盐形式储存于灰分中, 使生物炭表面碱度随温度升高而升高[21],因此施加600 ℃生物炭的土壤pH值高于300 ℃生物炭,乔继杰等[22]研究表明土壤蔗糖酶和磷酸酶与pH值呈显著负相关,所以pH值可能是导致300 ℃生物炭对土壤酶活性的促进作用高于600 ℃生物炭的一个主要因素。本研究结果显示添加有机肥对土壤酶活性的提升幅度小于300 ℃生物炭处理,但高于600 ℃生物炭处理。在紫色土中,相比其他处理,添加有机肥对酸性磷酸酶的促进作用明显较强。添加有机肥可以提高土壤中碳和氮的含量,改变土壤微生物区系,刺激微生物活动,间接提高土壤酶活性[23]。另外有机肥中丰富的胶体物质,以及有机质与土壤的交互作用有利于改善土壤生态环境,新的碳源和氮源促使土壤微生物区系组成发生变化,进而提高土壤酶活性[24]。红壤和紫色土均为酸性土,土壤中的铁、铝活性较高,易与土壤中的磷结合形成铁磷和铝磷[25]。本试验中,添加生物炭和有机肥对红壤pH值和有机质的促进效果更强,有机质能够分解有机酸,从而活化土壤中的磷元素[26]。土壤pH值的提高又可以降低土壤中铁、铝活性,提高磷的有效性[21],而土壤磷元素与土壤磷酸酶活性关系密切[10]。另一方面可能是因为红壤本身养分含量较低,生物炭和有机肥本身含有的养分含量可以成为肥料从而提高红壤的肥力[27]。
统计分析结果表明:红壤和紫色土中脲酶、蔗糖酶和酸性磷酸酶的活性均与土壤有机质呈显著正相关。土壤有机质为土壤微生物提供碳源和氮源,且有机质可以促进土壤中大小孔隙的形成,为微生物提供充足的氧气和水分,大量研究已经证明了有机质对土壤中酶的活性具有促进作用[28]。本研究中施用生物炭和有机肥均能有效提高土壤的有机质含量,且添加300 ℃生物炭对土壤有机质的贡献率高于添加600 ℃生物炭,这是因为高温热解条件下生物炭的碳损失较高,而300 ℃生物炭较高的碳氮含量为土壤微生物生长提供充足的营养物质,从而保持较高的微生物活性, 更有效地提高土壤中各类酶的含量。红壤中3种酶活性与紫色土中脲酶和酸性磷酸酶均与土壤可溶性有机碳呈显著正相关。KALBITZ et al[29]认为外加碳源和土壤中的微生物均可以成为土壤中可溶性有机碳的来源,且土壤中的可溶性有机碳具有水溶性和分子量小的特点,可以为土壤微生物的新陈代谢提供能量、碳源和氮源,活跃微生物,提高土壤酶活性[30-31]。试验结果表明添加300 ℃生物炭对土壤中可溶性有机碳含量的促进作用显著高于添加600 ℃生物炭的土壤,这可能是添加300 ℃生物炭对土壤酶活性的促进作用更强的一个主要因素。
4 结论与有机肥相比,添加生物炭更好地提高了土壤全碳、全氮、全磷含量和pH值,并且高温生物炭的促进作用更明显。培养结束后,各施肥处理对红壤酶活性的促进作用普遍高于紫色土。施加300 ℃生物炭和有机肥对酶活性的促进作用优于施加600 ℃生物炭。有机质和可溶性有机碳是影响红壤和紫色土酶活性的主要影响因子。
| [1] | 张乃燕, 陈国臣, 江泽鹏, 等. 油茶低产林综合改造效果分析[J]. 林业科技开发, 2009, 23(1): 103–105. |
| [2] | 李静, 李燕, 党培育. 茶皂素的提取及纯化研究[J]. 食品科学, 2008, 29(11): 154–156. DOI:10.3321/j.issn:1002-6630.2008.11.030 |
| [3] | 王斌, 王开良, 董洁杰, 等. 我国油茶产业现状及发展对策[J]. 林业科技开发, 2011, 25(2): 11–15. |
| [4] | 查钱慧, 洪文泓, 谭莎, 等. 油茶饼粕有机肥对番茄生长表观及生理指标的影响[J]. 安徽农业大学学报, 2015, 42(3): 458–462. |
| [5] | 徐明岗, 李冬初, 李菊梅, 等. 化肥有机肥配施对水稻养分吸收和产量的影响[J]. 中国农业科学, 2008, 41(10): 3133–3139. DOI:10.3864/j.issn.0578-1752.2008.10.029 |
| [6] | ZHANG H, XU M, ZHANG F. Long-term effects of manure application on grain yield under different cropping systems and ecological conditions in China[J]. The Journal of Agricultural Science, 2009, 147(1): 31–42. DOI:10.1017/S0021859608008265 |
| [7] | 梁元振, 赵京考, 吴德亮, 等. 秋施有机肥对土壤生物学理化性状及玉米产量的影响[J]. 水土保持研究, 2017, 24(3): 113–118. |
| [8] | ANTAL M J, GRØNLI M. The art, science, and technology of charcoal production[J]. Industrial Engineering Chemistry Research, 2003, 42(8): 1619–1640. DOI:10.1021/ie0207919 |
| [9] | 何钢, 袁德义, 刘贤桂, 等. 油茶低产林土壤改良对土壤养分及土壤酶活的影响[J]. 中南林业科技大学学报(自然科学版), 2011, 31(3): 76–80. |
| [10] | 陈心想, 耿增超, 王森, 等. 施用生物炭后塿土土壤微生物及酶活性变化特征[J]. 农业环境科学学报, 2014, 33(4): 751–758. DOI:10.11654/jaes.2014.04.019 |
| [11] | 尚杰, 耿增超, 陈心想, 等. 生物炭对土壤酶活性和糜子产量的影响[J]. 干旱地区农业研究, 2015, 33(2): 146–151, 158. |
| [12] | 刘世平, 聂新涛, 张洪程, 等. 稻麦两熟条件下不同土壤耕作方式与秸秆还田效用分析[J]. 农业工程学报, 2006, 22(7): 48–51. |
| [13] | 武志杰, 张海军, 许广山, 等. 玉米秸秆还田培肥土壤的效果[J]. 应用生态学报, 2002, 13(5): 539–542. |
| [14] | 周震峰, 王建超, 饶潇潇. 添加生物炭对土壤酶活性的影响[J]. 江西农业学报, 2015, 27(6): 110–112. |
| [15] | 贾俊香, 谢英荷. 生物炭对采煤塌陷复垦区土壤养分与酶活性的影响[J]. 灌溉排水学报, 2016, 35(11): 88–91. |
| [16] | CHUN Y, SHENG G Y, CHIOU C T, et al. Compositions and sorptive properties of crop residue-derived chars[J]. Environmental Science & Technology, 2004, 38(17): 4649–4655. |
| [17] | CANG L, ZHOU D M, WANG Q Y, et al. Effects of electrokinetic treatment of a heavy metal contaminated soil on soil enzyme activities[J]. Journal of Hazardous Materials, 2009, 172(2/3): 1602–1607. |
| [18] | 关松荫. 土壤酶及其研究法[M]. 北京: 农业出版社, 1986: 338-339. |
| [19] | 鲁如珅. 土壤农业化学分析方法[M]. 北京: 农业科技出版社, 2000: 282-286. |
| [20] | DICK R P. A review:Long-term effects of agricultural systems on soil biochemical and microbial parameters[J]. Agriculture Ecosystems & Environmentv, 1992, 40. |
| [21] | NOVAK J M, BUSSCIHER W J, LATRD D L, et al. Impact of biochar amendment on fertility of a southeasterm coastal in Nanjing, China[J]. Soil Science and Plant Nutrition, 2012, 58: 91–103. DOI:10.1080/00380768.2011.644510 |
| [22] | 乔继杰, 马振朝, 王玮, 等. 河北低平原夏玉米高产田土壤酶与肥力特征[J]. 江苏农业科学, 2016, 44(12): 484–487. |
| [23] | 刘术新, 丁枫华, 陈伟祥, 等. 有机肥对长豇豆连作土壤养分及酶活性的影响[J]. 浙江农业学报, 2014, 26(3): 770–774. |
| [24] | JOSHI D, HOODA K S, BHATT J C, et al. Suppressive effects of composts on soil-borne and foliar diseases of French bean in the field in the western Indian Himalayas[J]. Crop Protection, 2009, 28(7): 608–615. DOI:10.1016/j.cropro.2009.03.009 |
| [25] | 张祥, 王典, 姜存仓, 等. 生物炭对我国南方红壤和黄棕壤理化性质的影响[J]. 中国生态农业学报, 2013, 21(8): 979–984. |
| [26] | CUI H J, WANG M K, FU M L, et al. Enhancing phosphorus availability in phosphorus-fertilized zones by reducing phosphate adsorbed on ferrihydrite using rice straw-derived biochar[J]. Journal of Soils and Sediments, 2011, 11(7): 1135–1141. DOI:10.1007/s11368-011-0405-9 |
| [27] | 张阿凤, 潘根兴, 李恋卿. 生物黑炭及其增汇减排与改良土壤意义[J]. 农业环境科学学报, 2009, 28(12): 2459–2463. DOI:10.3321/j.issn:1672-2043.2009.12.004 |
| [28] | 周礼恺, 张志明, 曹承绵. 土壤酶活性的总体在评价土壤肥力水平中的作用[J]. 土壤学报, 1983, 20(4): 413–417. |
| [29] | KALBITZ K, SOLINGER S, PARK J H, et al. Controls on the dynamics of dissolved organic matter in soils:a review[J]. Soil Science, 2000, 165(4): 277–304. DOI:10.1097/00010694-200004000-00001 |
| [30] | 梁斌, 周建斌, 杨学云, 等. 栽培和施肥模式对黄土区旱地土壤微生物量及可溶性有机碳、氮的影响[J]. 水土保持学报, 2009, 23(2): 132–137, 142. |
| [31] | 韩琳, 张玉龙, 金烁, 等. 灌溉模式对保护地土壤可溶性有机碳与微生物量碳的影响[J]. 中国农业科学, 2010, 43(8): 1625–1633. DOI:10.3864/j.issn.0578-1752.2010.08.011 |

 2018, Vol. 38
2018, Vol. 38


