文章信息
- 刘垚, 韦廷舟, 龙治坚, 徐刚, 胡尚连, 胡勇
- LIU Yao, WEI Tingzhou, LONG Zhijian, XU Gang, HU Shanglian, HU Yong
- 温度和水分对梁山慈竹生态化学计量学特征的影响
- Effects of temperature and different moisture on ecological stoichiometry of Dendrocalamus farinosus
- 森林与环境学报,2018, 38(2): 209-215.
- Journal of Forest and Environment,2018, 38(2): 209-215.
- http://dx.doi.org/10.13324/j.cnki.jfcf.2018.02.013
-
文章历史
- 收稿日期: 2017-10-12
- 修回日期: 2018-01-26
2. 四川省生物质资源利用与改性工程技术研究中心, 四川 绵阳 621010;
3. 四川省西龙生物质材料科技有限公司, 四川 青神 620460
2. Engineering Research Center for Biomass Resource Utilizaiton and Modification of Sichuan Province, Mianyang, Sichuan 621010, China;
3. Sichuan Xilong Biomass Material Science and Technology Co., Ltd, Qingshen, Sichuan 620460, China
生态化学计量学是研究生命系统中能量平衡和多重化学元素平衡的科学,而有机体的C、N、P、S等元素含量及其比值是该学研究的主要方向[1-4]。N和P是生态化学计量学中研究较多的营养元素,N/P临界值是判断植物生长是受N限制还是P限制或二者共同限制的重要依据[5];而S元素的生态化学计量学特征研究甚少,N/S作为判断植物是否处于S元素缺乏状态的指标[6-9]。在高等植物体内,不同器官以及同种器官不同年龄之间元素含量均存在差别[1, 10-11], 而植株营养的分配则取决于各器官生物量的分配[12]。植物生物量分配格局受外界环境因子影响较大,温度或水分会改变植物生长所需资源的分布格局,从而改变植物生物量分配,引起植物不同器官营养格局的变化。
政府间气候变化专门委员会(Intergovernmental Panel on Climate Change,IPCC)于2001年报道夏季热浪平均气温将比正常气温高出5 ℃,甚至更多,且平均高温天气持续5~7 d[13]。温度的升高常伴随着严重干旱的发生[14]。21世纪西南地区的年平均气温变化趋势为每100 a上升2.30~4.66 ℃,年降水趋势为每100 a增加6.8%~13.1%[12], 这势必会引起植物对夏季气温和降雨的交互响应。梁山慈竹[Dendrocalamus farinousus (Keng et kengf.) Chia et HL Fung]是我国西南地区的大型丛生竹之一,是优良的笋材两用竹,多用于建筑和造纸[15]。目前,关于温度和不同水分对梁山慈竹的生长、发育以及对元素的摄取和营养的分配等方面的研究尚未见报道。基于此,文中研究温度和不同水分对梁山慈竹生长发育的影响,分析根、茎、叶中C、N、P和S生态化学计量学特征及生理变化,并用生态化学计量学理论解释其适应特征,旨在为梁山慈竹应对可能的气候变化在栽培管理方面提供一定的理论指导。
1 材料与方法 1.1 研究材料与研究地点供试材料均为“五叶一心”的梁山慈竹实生植株,株高为15 cm。试验在四川省绵阳市西南科技大学玻璃温室中进行,该地位于北纬31°32′6″,东经104°02′05″,处在四川省绵阳市涪城区,属于亚热带湿润季风气候,年平均气温16.3 ℃,年平均日照时间1 298.1 h,年平均无霜期272 d,年平均降雨量963.2 mm,年平均相对湿度79%,年平均雾日51 d。
1.2 试验方法2016年3月15日至2016年7月1日为梁山慈竹幼苗为处理前的培育时间。供试材料共设置8个处理,分别为常温(26.56±2.96) ℃下的CK、30R、60R、HR和增温(32.22±3.88) ℃下的ZW-CK、ZW-30R、ZW-60R、ZW-HR。其中CK为正常水分量280 mL·次-1,30R为30%的浇水量,60R为60%的浇水量,HR为150%的浇水量。每个处理15盆,共120盆,而所选植株生长良好、长势一致。每组供试植株15丛,共120丛。盆底部直径为30 cm,顶部直径为40 cm,每盆盛有混匀的土壤基质14 kg。土壤容重(1.47±0.21) g·cm-3,pH值为6.2±0.84,有机质含量(18.25±1.76) g·kg-1,有机碳含量(5.81±0.48) g·kg-1,全氮含量(0.47±0.09) g·kg-1,全磷含量(30.25±4.43) g·kg-1,全硫含量(320.26±18.26) mg·kg-1。
将2 000 W远红外碳纤维加热管装置悬挂于高出植株主要叶片分层1.8 m处增温,每隔7 d增温1次,每次7 d(10:00—18:00)。增温时间段为2016年7月1日—9月30日。处理组的平均温度为(32.22±3.88) ℃,对照组的为(26.56±2.96) ℃,试验组较对照组高5.66 ℃,增幅为21.31%。用温湿度记录器(TP-2200,中国上海发泰精密仪器仪表有限公司)记录相应的温、湿度。不同水分则根据四川绵阳市年平均降雨量,设置4个梯度,每周浇水3次。浇水量:CK为280 mL·次-1、30R为84 mL·次-1、60R为168 mL·次-1和HR为420 mL·次-1。为防止因浇水而造成土壤营养流失,每个盆外套黑色塑料袋并不定期清理袋中积水,保证植物正常生长。选择晴朗天气,每次处理后在第2天9:00—11:00,利用便携式光合测定仪(LI-6400型,美国LI-COR公司)测定每组植株从顶端向下第5片完全展开叶的净光合速率(net photosynthetic rate,Pn),光合测定仪的流速设定为500 μmol·s-1,叶室温度设定为25 ℃。
1.3 样品处理与化学分析方法试验结束后,采用全收获式采样, 清洗植株后分离根、茎和叶,70 ℃烘干至恒重并记录。采用可变速高速旋转粉碎机(Pulverisette 14型,德国Fritsch公司生产)粉碎干样,用元素分析仪(Vario Micro型,德国Elementar公司)测量植物各器官C、N、P和S元素含量。
1.4 数据处理采用SPSS 19.0软件对梁山慈竹根、茎、叶中C/N、C/P、N/P、C/S、N/S以及P/S生态化学计量学特征等数据进行单因素方差分析和多因素方差分析,并利用Tukey检验法检验数据之间的显著性。
2 结果与分析 2.1 梁山慈竹不同器官干重以及叶片净光合速率由表 1可知,增温、不同水分及其交互作用均对梁山慈竹根、茎和叶的干重有极显著的影响。在ZW-HR处理下,根、茎、叶干重显著高于ZW-30R和ZW-60R处理;与ZW-CK相比,茎干重显著升高。在常温状态不同水分处理下,CK的根、茎和叶干重均高于其他水分处理。同时,增温、不同水分及其交互作用也对梁山慈竹的根茎干重比有显著影响,其中在ZW-HR处理下的根茎干重比值较ZW-CK、ZW-30R和ZW-60R处理显著增加。增温、不同水分及其交互作用也对梁山慈竹的根叶干重比有显著影响,而对茎叶干重比和叶片净光合速率没有产生显著影响。
| 处理 Treatment | 根干重 Dry root weight/g | 茎干重 Dry stem weight/g | 叶干重 Dry leaf weight/g | 根茎干重比 Dry root to stem ratio | 根叶干重比 Dry root to leaf ratio | 茎叶干重比 Dry stem to leaf ratio | 净光合速率 Net photosynthetic rate/(μmol·m2·s-1) |
| CK | 1.25±0.45b | 1.80±0.14a | 1.2±0.55b | 0.69±0.01a | 1.04±0.07a | 1.50±0.13a | 5.21±0.29a |
| 30R | 0.30±0.22b | 0.88±0.34b | 0.35±0.33b | 0.34±0.14a | 0.86±0.04b | 2.51±0.99a | 3.75±0.67a |
| 60R | 0.53±0.34ab | 1.12±0.52ab | 0.60±0.38ab | 0.47±0.23a | 0.88±0.04b | 1.87±1.49a | 4.75±0.73a |
| HR | 0.97±0.43ab | 1.55±0.29ab | 1.05±0.46ab | 0.63±0.16a | 0.92±0.02b | 1.48±0.40a | 5.81±0.29a |
| ZW-CK | 0.48±0.11a | 1.07±0.43b | 0.47±0.19a | 0.45±0.16b | 1.02±0.26a | 2.28±1.34a | 4.85±0.18a |
| ZW-30R | 0.28±0.08b | 0.68±0.17b | 0.32±0.10b | 0.29±0.11b | 0.88±0.09a | 2.13±0.51a | 3.51±1.11a |
| ZW-60R | 0.85±0.20b | 1.47±0.13b | 0.89±0.31b | 0.58±0.11b | 0.96±0.13a | 1.65±0.39a | 5.05±0.19a |
| ZW-HR | 3.74±0.69a | 3.53±0.78a | 3.65±0.66a | 1.06±0.07a | 1.02±0.06a | 0.97±0.03a | 6.34±0.24a |
| P(T) | *** | *** | *** | * | * | ns | ns |
| P(R) | *** | *** | *** | *** | ns | ns | ns |
| P(R×T) | *** | *** | *** | ** | ns | ns | ns |
| 注:P(T)表示增温处理的影响,P(R)表示水分处理的影响,P(R×T)表示水分与增温交互作用的影响;表中数据均为平均值±标准差;在多因素方差分析中ns表示无显著相关,*表示在0.05水平上显著相关,**表示在0.01水平上显著相关,***表示在0.001水平上显著相关。Note:P(T) indicates the influence of warming treatment,P(R) indicating the effect of rainfall,P(R×T) indicates the interaction between rainfall and warming; the data in the table are average value ± standard deviation;ns in the table indicates no significant correlation;* in the table indicates significant correlation at 0.05 level;** in the table indicates significant correlation at 0.01 level;*** in the table indicates significant correlation at 0.001 level. | |||||||
由表 2可知,随着水分的增加,根的C/N呈下降趋势,不同水分水平之间的差异显著,ZW-HR处理与ZW-CK、ZW-30R和ZW-60R处理相比,根的C/N显著下降。同时,不同水分及其与增温相互作用也影响梁山慈竹根系的C/P,与CK相比,其在HR处理下显著下降,而在ZW-HR处理下与ZW-CK相比也显著下降。梁山慈竹在不同水分和增温相互作用下根的N/P变化显著。此外,所有处理都对梁山慈竹根的C/S、N/S和P/S有所影响,其中增温处理导致根的C/S、N/S和P/S显著下降;随着水分的增加,根的C/S、N/S和P/S呈上升趋势;二者互作时,ZW-HR处理下根的C/S、N/S和P/S均高于ZW-CK处理的且差异显著。
| 器官 Organ | 处理 Treatment | C/N | C/P | N/P | C/S | N/S | P/S |
| 根 Root | CK | 33.70±1.02a | 383.66±4.42b | 11.39±0.25a | 51.32±2.37b | 1.52±0.09b | 0.13±0.01b |
| 30R | 34.64±0.50a | 407.24±25.73ab | 11.75±0.66a | 45.97±2.15bc | 1.33±0.08b | 0.11±0.01bc | |
| 60R | 34.21±0.78a | 448.37±7.54a | 13.11±0.10a | 42.69±0.95c | 1.25±0.06b | 0.10±0.003c | |
| HR | 30.80±4.74a | 334.37±16.05c | 11.10±2.38a | 73.71±3.37a | 2.43±0.42a | 0.22±0.01a | |
| ZW-CK | 34.81±0.99a | 448.95±34.77a | 12.92±1.32a | 12.73±0.42d | 0.37±0.02c | 0.03±0.002c | |
| ZW-30R | 34.71±0.36a | 377.95±29.89b | 10.89±0.96a | 31.64±4.05b | 0.91±0.12b | 0.08±0.01b | |
| ZW-60R | 32.67±1.34a | 350.49±6.97b | 10.74±0.54a | 42.57±1.18a | 1.30±0.05a | 0.12±0.01a | |
| ZW-HR | 29.00±1.71b | 337.63±16.95b | 11.64±0.10a | 22.62±0.96c | 0.78±0.06b | 0.07±0.005b | |
| P(T) | ns | ns | ns | *** | *** | *** | |
| P(R) | ** | *** | ns | *** | *** | *** | |
| P(R×T) | ns | *** | * | *** | *** | *** | |
| 茎 Stem | CK | 24.15±4.18a | 280.75±5.01ab | 11.84±1.89a | 76.75±3.19a | 3.23±0.46a | 0.27±0.02a |
| 30R | 25.33±3.20a | 296.55±16.22a | 11.85±1.86a | 25.07±1.74c | 1.00±0.18b | 0.08±0.009ab | |
| 60R | 23.17±0.75a | 247.92±11.49b | 10.70±0.32a | 67.53±4.58b | 2.91±0.15a | 0.27±0.02a | |
| HR | 21.79±0.66a | 306.790±16.84a | 14.10±1.11a | 24.00±0.69c | 1.10±0.03b | 0.08±0.004a | |
| ZW-CK | 22.65±0.58b | 281.74±19.51c | 12.45±1.13b | 37.59±3.19a | 1.66±0.17a | 0.13±0.003a | |
| ZW-30R | 26.75±1.50a | 311.19±6.15bc | 11.66±1.00b | 35.78±4.75a | 1.34±0.17a | 0.11±0.01a | |
| ZW-60R | 24.54±2.17ab | 345.56±1.33ab | 14.14±1.09b | 19.68±1.64b | 0.81±0.14b | 0.06±0.006c | |
| ZW-HR | 21.94±0.98b | 389.36±27.29a | 17.76±1.29a | 34.78±4.23a | 1.58±0.14a | 0.09±0.01b | |
| P(T) | ns | *** | ** | *** | *** | *** | |
| P(R) | * | *** | *** | *** | *** | *** | |
| PP(R×T) | ns | *** | * | *** | *** | *** | |
| 叶 Leaf | CK | 14.41±0.51ab | 264.22±1.81a | 18.35±0.67a | 49.38±1.45a | 3.43±0.03a | 0.19±0.006a |
| 30R | 12.96±0.54b | 221.21±7.94c | 17.07±0.23a | 14.26±0.22d | 1.10±0.04d | 0.06±0.002c | |
| 60R | 14.80±0.75a | 247.85±1.88b | 16.77±0.89a | 25.72±2.11c | 1.74±0.14c | 0.10±0.01b | |
| HR | 13.17±0.82ab | 220.23±4.98c | 16.74±0.70a | 39.43±3.67b | 2.99±0.16b | 0.18±0.01a | |
| ZW-HR | 14.51±0.62a | 236.11±10.60b | 16.27±0.06c | 48.81±0.22a | 3.37±0.13a | 0.21±0.01a | |
| ZW-30R | 13.94±0.23ab | 245.44±11.13b | 17.61±0.62c | 22.16±0.41c | 1.59±0.04c | 0.09±0.003c | |
| ZW-30R | 14.84±0.30a | 309.23±12.90a | 20.85±1.19b | 44.44±2.44b | 2.72±0.12b | 0.13±0.01b | |
| ZW-HR | 13.33±0.18b | 317.11±14.93a | 23.79±1.17a | 17.15±0.93d | 1.29±0.07d | 0.05±0.001d | |
| P(T) | ns | *** | *** | ns | ns | *** | |
| P(R) | *** | *** | *** | *** | *** | *** | |
| P(R×T) | ns | *** | *** | *** | *** | *** | |
| 注:P(T)表示增温处理的影响,P(R)表示水分处理的影响,P(R×T)表示水分与增温交互作用的影响;表中数据均为平均值±标准差;在多因素方差分析中ns表示无显著相关,*表示在0.05水平上显著相关,**表示在0.01水平上显著相关,***表示在0.001水平上显著相关。Note:P(T) indicates the influence of warming treatment,P(R) indicating the effect of rainfall,P(R×T) indicates the interaction between rainfall and warming; the data in the table are average value ± standard deviation;ns in the table indicates no significant correlation;* in the table indicates significant correlation at 0.05 level;** in the table indicates significant correlation at 0.01 level;*** in the table indicates significant correlation at 0.001 level. | |||||||
由表 2可知,增温处理下,随着水分的增加,茎的C/N呈下降趋势,不同水分水平之间的差异显著。增温、不同水分以及二者交互作用对梁山慈竹茎的C/P、N/P、C/S、N/S和P/S的影响均达到了显著水平,其中增温处理导致茎的C/P、N/P显著上升而C/S、N/S和P/S显著下降,HR处理与CK相比,茎的C/P、N/P增加而C/S、N/S和P/S下降,ZW-HR处理与ZW-CK相比,茎的C/P、N/P增加而C/S、N/S和P/S下降。
2.4 不同处理下梁山慈竹叶生态化学计量学特征由表 2可知,不同水分对梁山慈竹叶的C/N影响显著,所有处理对叶的C/P、N/P影响均达到极显著。其中,增温处理导致叶的C/P、N/P显著增加;而HR处理与CK相比,叶的C/P、N/P降低,但ZW-HR处理与ZW-CK相比,叶的C/P、N/P增加。而对于叶的C/S、N/S,不同水分及其与增温交互作用对其影响极显著。其中HR处理与CK相比,叶的C/S、N/S显著下降,而ZW-HR处理与ZW-CK相比,叶的C/S、N/S显著下降。增温、不同水分及其与增温交互作用对叶的P/S影响极显著。
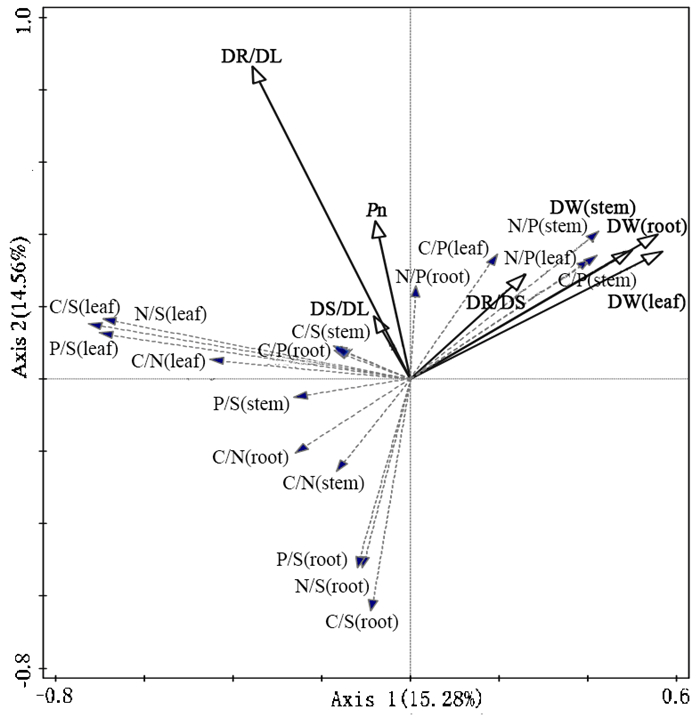
2.5 冗余分析和偏相关分析对根、茎、叶各元素比值进行除趋势对应分析(detrended correspondence analysis,DCA),结果显示,最大的梯度长度为0.20,小于3。因此,选择对梁山慈竹净光合速率、根、茎、叶干重及比值与根、茎、叶各元素比值进行冗余分析。结果表明,前两个轴的特征值分别为0.152 8和0.145 6,解释了元素比值变化的29.84%(图 1)。根叶干重比(解释百分数为12.9%,P=0.014)和根干重(解释百分数为9.2%,P=0.03)对元素比值的贡献作用最大,且达到了显著水平(P<0.05)。偏相关分析表明,根的C/N和C/P、茎的C/P和N/P、叶的C/P和N/P对梁山慈竹根、茎、叶干重的相关程度达到显著水平(表 3),其中根C/N、C/P与根、茎、叶干重以及根茎干重比表现为负相关,而茎的C/P和N/P、叶的C/P和N/P则表现为正相关。对于根叶干重比,根的C/S、N/S、P/S以及叶的C/S与其呈显著相关性,其中根的C/S、N/S、P/S表现为负相关,而叶的C/S表现为正相关。
|
图 1 生理指标与元素比值的冗余分析 Fig. 1 Redundancy analysis of physiological indexes and element ratios |
| 皮尔森相关意义 Pearson correlation significance | 根干重 Dry root weight | 茎干重 Dry steam dry weight | 叶干重 Dry leaf dry weight | 根茎干重比 Dry root to steam ratios | 根叶干重比 Dry root to leaf ratios | 茎叶干重比 Dry steam to leaf ratios | 净光合速率 Net photosynthetic rate |
| 根C/N | -0.578** | -0.510* | -0.568** | -0.598** | -0.038 | 0.428* | 0.314 |
| 根C/P | -0.513* | -0.479* | -0.524** | -0.594** | 0.155 | 0.660** | 0.619** |
| 根N/P | -0.160 | -0.190 | -0.179 | -0.231 | 0.194 | 0.422* | 0.456* |
| 根C/S | -0.240 | -0.215 | -0.211 | -0.110 | -0.477* | -0.183 | -0.327 |
| 根N/S | -0.162 | -0.146 | -0.136 | -0.030 | -0.421* | -0.227 | -0.345 |
| 根P/S | -0.139 | -0.116 | -0.111 | -0.004 | -0.421* | -0.267 | -0.384 |
| 茎C/N | -0.228 | -0.174 | -0.234 | -0.212 | -0.060 | 0.059 | -0.005 |
| 茎C/P | 0.710** | 0.674** | 0.690** | 0.598** | 0.163 | -0.358 | -0.212 |
| 茎N/P | 0.709** | 0.648** | 0.696** | 0.615** | 0.161 | -0.334 | -0.179 |
| 茎C/S | -0.024 | -0.017 | -0.045 | 0.036 | 0.114 | 0.020 | 0.053 |
| 茎N/S | 0.012 | 0.008 | -0.006 | 0.073 | 0.108 | 0.002 | 0.042 |
| 茎P/S | -0.161 | -0.154 | -0.174 | -0.074 | 0.039 | 0.068 | 0.064 |
| 叶C/N | -0.261 | -0.181 | -0.276 | -0.218 | 0.265 | 0.169 | 0.177 |
| 叶C/P | 0.611** | 0.851** | 0.593** | 0.579** | 0.210 | -0.366 | -0.218 |
| 叶N/P | 0.762** | 0.696** | 0.750** | 0.707** | 0.109 | -0.453* | -0.298 |
| 叶C/S | -0.283 | -0.258 | -0.295 | -0.068 | 0.406* | 0.003 | 0.052 |
| 叶N/S | -0.264 | -0.246 | -0.273 | -0.038 | 0.382 | -0.033 | 0.015 |
| 叶P/S | -0.366 | -0.344 | -0.373 | -0.156 | 0.356 | 0.066 | 0.090 |
| 注:*表示在0.05水平上显著相关,**表示在0.01水平上显著相关。Notes:* in the table indicates significant correlation at 0.05 level, and * * indicates significant correlation at 0.01 level. | |||||||
温度和水分是影响植物生长的两大环境因子。在文中,ZW-CK与CK相比,根、茎、叶干重显著降低,这证明了植株遭受了胁迫;而在不同水分处理下,根、茎、叶干重的下降表明了植株在水分胁迫时不利于生长。光合作用是植物的重要的生理过程,它不仅与植物的生存环境密切相关,还影响植物的生长、发育[16-22]。有研究表明[22-24], 净光合速率与空气相对湿度有线性相关关系,但是与空气温度无显著相关。而文中的结果发现,增温、不同水分以及交互作用均对净光合速率没有显著影响。这和前人的研究[22-24]有一定的相似之处。
植物不同器官大宗元素C、N、P和S比值可用于衡量各器官中营养元素的分配和利用效率,而植物改变自身各器官间营养的分配是应对外界环境变化的表现之一[25-26]。文中发现,不同水分处理除了对根的N/P没有产生显著影响外,对其他部分的C/N、C/P、N/P、C/S、N/S和P/S均产生显著效应。而增温和不同水分的交互作用除对C/N没有显著影响外,对根、茎、叶的C/P、N/P、C/S、N/S和P/S均有显著影响。以上结果同时也表明,温度和水分对S元素参与的计量比值均有显著差异。但是,不同器官的C/S、N/S和P/S应对温度和水分变化时参与调节各器官的元素分配具有差异。温度处理使C/S、N/S和P/S在根中显著上升,而在茎和叶中有不同程度的下降。
具体而言,梁山慈竹各器官S元素分配对水分变化敏感。在HR和30R处理下,叶和茎的C/S、N/S和P/S均不同程度的下降。充足水分和极度干旱的土壤,均导致叶片C元素含量积累减少,S元素的增加,致使C/P、C/S和N/S显著减少。增温对植物的影响大多是消极的[27],而S元素在植物的抗逆境生理中起着重要的作用[28-30]。植物所需的S元素需从土壤中吸收,从土壤中吸收的S元素经同化形成的半胱氨酸作为前体形成甲硫氨酸、谷胱甘肽、类谷胱甘肽以及植物螯合剂[28]。温度参与下的不同水分处理,同样使叶和茎的C/S、N/S和P/S均显著较少。表明叶和茎中S元素含量对温度和水分的叠加效应敏感,特别是在HR和30R处理下表现尤为明显。梁山慈竹S元素含量显著变化,极有可能是梁山慈竹在抗逆生境下表现出来的一种调节机制。梁山慈竹在温度和水分胁迫下S元素参与的抗逆的调节机制,对生产实践具有重要的指导意义。
植物不同器官的C/N和C/P在应对温度和不同水分时结果具有差异。30R、HR、ZW-30R和ZW-HR处理使梁山慈竹叶的C/N和C/P显著下降,这与研究人员[31-32]的研究结果一致。极端干旱和充足的水分抑制植物叶片的碳同化能力,为使叶片具有较高的同化能力,植物根系运送更多的N和P元素至叶片,使之保持较高的同化能力来维持梁山慈竹的存活。梁山慈竹根和茎应对温度和水分的变化则有所不同。极度干旱胁迫使根和茎中C/N和C/P增加,这是因为严重干旱引起的碳同化减弱,根和茎中结构性碳含量较少,同时,为保持叶片更多的光合作用,根和茎中的N和P元素运输至叶片,参与光合作用。温度处理下,根C/N和C/P比值降低,而茎中C/N和C/P比却增加。这个结果表明温度胁迫需要根吸收更多的N和P元素,来弥补低效的光合作用。
温度-植物生理学假说认为,植物叶片N和P的调节机制是温度敏感型[33],N/P随气温的增加而降低。文中叶的N/P支持温度-植物生理学假说。N/P可作为鉴定植物的生长是否受到N或者P的限制的指标,N/P < 10通常(并不总是)表示植物的生长受到了N的限制[5],N/P>20表示受到P的限制。文中梁山慈竹叶N/P多数值小于20,说明梁山慈竹的生长受到了N的限制。ZW-HR处理下,N/P(23.97)大于20,表明梁山慈竹在高温高湿的条件下受到了P的限制。高碳叶植物通常有较低的N和P,且与N和P呈显著负相关[33]。高温高湿环境是梁山慈竹叶C增加与P限制,表明梁山慈竹更适应于短时间高温天气和高湿的生长环境。
| [1] | 曾德慧, 陈广生. 生态化学计量学:复杂生命系统奥秘的探索[J]. 植物生态学报, 2005, 29(6): 1007–1019. |
| [2] | 贺金生, 韩兴国. 生态化学计量学:探索从个体到生态系统的统一化理论[J]. 植物生态学报, 2010, 34(1): 2–6. |
| [3] | DA SILVA J J R F, WILLIAMS R J P. The biological chemistry of the elements:the inorganic chemistry of life[M]. Oxford: Oxford University Press, 2001. |
| [4] | FROST P C, EVANS-WHITE M A, FINKEL Z V, et al. Are you what you eat? Physiological constraints on organismal stoichiometry in an elementally imbalanced world[J]. Oikos, 2005, 109(1): 18–28. DOI:10.1111/oik.2005.109.issue-1 |
| [5] | GÜSEWELL S. N:P ratios in terrestrial plants:variation and functional significance[J]. The New Phytologist, 2004, 164(2): 243–266. DOI:10.1111/j.1469-8137.2004.01192.x |
| [6] | BLAKE-KALFF M M A, HAWKESFORD M J, ZHAO F J, et al. Diagnosing sulfur deficiency in field-grown oilseed rape (Brassica napus L.) and wheat (Triticum aestivum L.)[J]. Plant and Soil, 2000, 225(1/2): 95–107. DOI:10.1023/A:1026503812267 |
| [7] | DIVITO G A, ECHEVERRÍA H E, ANDRADE F H, et al. Diagnosis of S deficiency in soybean crops:performance of S and N:S determinations in leaf, shoot and seed[J]. Field Crops Research, 2015, 180: 167–175. DOI:10.1016/j.fcr.2015.06.006 |
| [8] | SALVAGIOTTI F, FERRARIS G, QUIROGA A, et al. Identifying sulfur deficient fields by using sulfur content; N:S ratio and nutrient stoichiometric relationships in soybean seeds[J]. Field Crops Research, 2012, 135: 107–115. DOI:10.1016/j.fcr.2012.07.011 |
| [9] | REUSSI N, ECHEVERRÍA H, ROZAS H S. Diagnosing sulfur deficiency in spring red wheat:plant analysis[J]. Journal of Plant Nutrition, 2011, 34(4): 573–589. DOI:10.1080/01904167.2011.538118 |
| [10] | CHEN X G, ZHANG X Q, ZHANG Y P, et al. Changes of carbon stocks in bamboo stands in China during 100 years[J]. Forest Ecology and Management, 2009, 258(7): 1489–1496. DOI:10.1016/j.foreco.2009.06.051 |
| [11] | HESSEN D O, ELSER J J, STERNER R W, et al. Ecological stoichiometry:an elementary approach using basic principles[J]. Limnology and Oceanography, 2013, 58(6): 2219–2236. DOI:10.4319/lo.2013.58.6.2219 |
| [12] | 刘晓冉, 程炳岩, 杨茜, 等. 我国西南地区21世纪气候变化的情景预估分析[J]. 西南大学学报(自然科学版), 2012, 34(9): 82–89. |
| [13] | RENNENBERG H, LORETO F, POLLE A, et al. Physiological responses of forest trees to heat and drought[J]. Plant Biology, 2006, 8(5): 556–571. DOI:10.1055/s-2006-924084 |
| [14] | CHEN H P, SUN J Q. Drought response to air temperature change over China on the centennial scale[J]. Atmospheric and Oceanic Science Letters, 2015, 8(3): 113–119. DOI:10.1080/16742834.2015.11447247 |
| [15] | 周振华, 胡尚连, 徐刚, 等. 梁山慈竹体细胞突变体特性及分子水平变化[J]. 森林与环境学报, 2015, 35(1): 67–73. |
| [16] | SCHAPENDONK A H C M, VAN OIJEN M, DIJKSTRA P, et al. Effects of elevated CO2 concentration on photosynthetic acclimation and productivity of two potato cultivars grown in open-top chambers[J]. Australian Journal of Plant Physiology, 2000, 27(12): 1119–1130. |
| [17] | PRITCHARD S G, JU Z L, VAN SANTEN E, et al. The influence of elevated CO2 on the activities of antioxidative enzymes in two soybean genotypes[J]. Australian Journal of Plant Physiology, 2000, 27(11): 1061–1068. |
| [18] | LEE T D, BARROTT S H, REICH P B. Photosynthetic responses of 13 grassland species across 11 years of free-air CO2 enrichment is modest, consistent and independent of N supply[J]. Global Change Biology, 2011, 17(9): 2893–2904. DOI:10.1111/gcb.v17.9 |
| [19] | 江世高, 尚振艳, 牛得草, 等. 贺兰山西坡草地植物多样性与其叶片C:N:P计量比的关系[J]. 干旱区研究, 2014, 31(3): 523–529. |
| [20] | WILLIAM HAMILTON Ⅲ E, HECKATHORN S A, JOSHI P, et al. Interactive effects of elevated CO2 and growth temperature on the tolerance of photosynthesis to acute heat stress in C3 and C4species[J]. Journal of Integrative Plant Biology, 2008, 50(11): 1357–1387. |
| [21] | BROWN R H, RADCLIFFE D E. A comparison of apparent photosynthesis in sericea lespedeza and alfalfa[J]. Crop Science, 1986, 26(6): 1208–1211. DOI:10.2135/cropsci1986.0011183X002600060027x |
| [22] | 王冉, 李素英, 任丽娟, 等. 锡林浩特草原区27种植物净光合速率影响因素的多因子分析[J]. 干旱区研究, 2015, 32(2): 272–278. |
| [23] | GUTIÉRREZ-RODR ÍGUEZ M, REYNOLDS M P, LARQUÉ-SAAVEDRA A. Photosynthesis of wheat in a warm, irrigated environment:Ⅱ. Traits associated with genetic gains in yield[J]. Field Crops Research, 2000, 66(1): 51–62. DOI:10.1016/S0378-4290(99)00078-7 |
| [24] | ALLEN D J, ORT D R. Impacts of chilling temperatures on photosynthesis in warm-climate plants[J]. Trends in Plant Science, 2001, 6(1): 36–42. DOI:10.1016/S1360-1385(00)01808-2 |
| [25] | PREGITZER K S, KING J S. Effects of soil temperature on nutrient uptake[M]//BASSIRIRAD H. Nutrient Acquisition by Plants. Berlin: Springer, 2005. |
| [26] | CORTINA J, VALLEJO V R. Effects of clearfelling on forest floor accumulation and litter decomposition in a radiata pine plantation[J]. Forest Ecology and Management, 1994, 70(1/2/3): 299–310. |
| [27] | LARKINDALE J, MISHKIND M, VIERLING E. Plant responses to high temperature[M]//JENKS M A, HASEGAWA P M. Plant Abiotic Stress. Oxford: Blackwell Publishing Ltd, 2007. |
| [28] | ANJUM N A, GILL R, KAUSHIK M, et al. ATP-sulfurylase, sulfur-compounds, and plant stress tolerance[J]. Frontiers in Plant Science, 2015, 6: 210. |
| [29] | NA G N, SALT D E. The role of sulfur assimilation and sulfur-containing compounds in trace element homeostasis in plants[J]. Environmental and Experimental Botany, 2011, 72(1): 18–25. DOI:10.1016/j.envexpbot.2010.04.004 |
| [30] | KHAN N A, KHAN M I R, ASGHER M, et al. Salinity tolerance in plants:revisiting the role of sulfur metabolites[J]. Journal of Plant Biochemistry and Physiology, 2014, 2: 120. |
| [31] | 羊留冬, 杨燕, 王根绪, 等. 短期增温对贡嘎山峨眉冷杉幼苗生长及其CNP化学计量学特征的影响[J]. 生态学报, 2011, 31(13): 3668–3676. |
| [32] | 黄菊莹, 余海龙, 袁志友, 等. 氮、磷和水分供给对羊草枯叶分解质量的影响[J]. 植物生态学报, 2011, 35(8): 808–815. |
| [33] | WRIGHT I J, REICH P B, WESTOBY M, et al. The worldwide leaf economics spectrum[J]. Nature, 2004, 428(6985): 821–827. DOI:10.1038/nature02403 |

 2018, Vol. 38
2018, Vol. 38


