文章信息
- 张炎, 左丹丹, 陈宇, 熊升, 王珍, 林思祖
- ZHANG Yan, ZUO Dandan, CHEN Yu, XIONG Sheng, WANG Zhen, LIN Sizu
- 杉木胚珠的解剖学观察
- Anatomical observation of ovule of Cunninghamia lanceolata
- 森林与环境学报,2017, 37(2): 142-147.
- Journal of Forest and Environment,2017, 37(2): 142-147.
- http://dx.doi.org/10.13324/j.cnki.jfcf.2017.02.003
-
文章历史
- 收稿日期: 2016-12-28
- 修回日期: 2017-03-06
2. 国家林业局杉木工程技术研究中心, 福建 福州 350002;
3. 福建农林大学林学院, 福建 福州 350002
2. State Forestry Administration Engineering Research Center of Chinese Fir, Fuzhou, Fujian 350002, China;
3. College of Forestry, Fujian Agriculture and Forestry University, Fuzhou, Fujian 350002, China
杉木[Cunninghamia lanceolata (Lamb.) Hook.]是我国南方重要的优良造材树种,分布面积广,栽培历史悠久,具有重要的经济价值。在杉木种子发育过程中,会受各种因素的影响而出现败育。刘志敏[1]曾报道在雌配子体的发育、传粉、受精、胚和胚乳的发育等每一环节都有可能败育。这种败育现象严重影响杉木种子后期萌发,对杉木人工林的可持续发展极为不利。
一般杉木涩籽率达到50%~60%,种子园的杉木涩籽率相对较低,但也达到30%左右[2]。高涩籽率是杉木种子发芽率低的主要原因,严重地影响种子园的产量和质量。目前,对杉木种子的研究多集中在杉木种子萌发、激素、蛋白和基因方面[3-8],此外也有关于杉木胚胎发育过程的形态变化、涩粒物质的研究[9-11]。但这些针对杉木涩籽的研究也多集中在胚的败育过程,而对在受精前就已经发生败育的杉木胚珠,其败育过程的研究相对较少,且研究方法仅局限于常规制片法,此方法往往存在染色不易控制、分辨率低、不利于观察等问题。鉴于此,采用清晰度和分辨率较优的半薄切片法,在超微结构上对杉木胚珠进行观察,以杉木健籽胚珠为对照,与在受精前就已经发生败育的杉木胚珠的形态结构进行比较分析,可为杉木种子生产中降低涩籽率提供科学依据。
1 材料与方法 1.1 材料的采集与保存杉木胚珠采自福建省三明市尤溪县林木良种基地,该林场杉木从2009年开始采种。2013年5月初至6月中旬,定期采集同种家系的杉木球果若干枚,用福尔马林-乙酸-乙醇 (formalin-aceto-alcohol, FAA) 固定液 (浓度70%的酒精、冰醋酸和甲醛以18:1:1的比例配制) 固定带回,放到4 ℃冰箱保存,备用。
1.2 杉木胚珠的外部形态观察将杉木胚珠置于解剖镜下用解剖针除去种翅,操作时胚珠不能离开FAA固定液过久,避免胚珠干燥变形,且针头不能划破胚珠,以免影响形态观察结果。将解剖好的胚珠按不同采集时间分别在体视解剖镜下观察并拍照。
1.3 杉木胚珠的内部结构特征观察观察种子内部结构主要采用半薄切片法,将除去种翅的杉木胚珠用Epon 812环氧树脂包埋剂渗透、包埋。其主要步骤为漂洗、脱水、丙酮置换、渗透、聚合,在切片机上分别切片,在显微镜下观察、照相。
1.3.1 取材取每个时期的杉木胚珠各30粒左右,剥去种翅,放FAA固定液里,作好标记。
1.3.2 漂洗和脱水将处理后的胚珠用1xPBS洗2次,每次30 min,然后用乙醇进行脱水:分别在体积分数为30%、50%、70%、80%、90%的乙醇中逐级脱水各20 min,然后在体积分数为95%的乙醇中脱水30 min,体积分数为100%的乙醇中脱水3次, 各30 min。
1.3.3 丙酮置换把1.3.2处理后的材料放入等体积无水乙醇和无水丙酮的混合液中30 min,再转入无水丙酮中过夜。
1.3.4 渗透将1.3.3处理后的材料依次放入体积比分别为3:1和1:1的丙酮和Epon 812包埋液中3 h,然后转入纯Epon 812包埋液中2次, 各12 h,各级处理温度都为30 ℃。
1.3.5 聚合将1.3.4处理后的材料挑入包埋树胶板的胶囊内,待放好位置后,填满新配的Epon 812包埋液,先置于40 ℃温度下12 h,然后转入60 ℃温度下3 d,待包埋液干燥后取出包埋小块。
1.3.6 半薄切片根据材料在固定块中的位置和方向,修整样品块 (在保证样品完整的情况下, 与切刀的接触面尽可能小,周边光滑平整),然后把包埋小块固定到固定台上进行切片,切片厚度为2~4 μm。
1.3.7 展片及粘片将铁丝的一端拧成一个小圆圈,用来捞水槽中的切片,然后将切片小心地放在干净的载玻片上,放在40 ℃干燥台上干燥。
1.3.8 染色和观察在切片上均匀地滴上甲苯胺蓝,3 min后用吸水纸吸掉多余的染色液,在显微镜下观察并拍照。
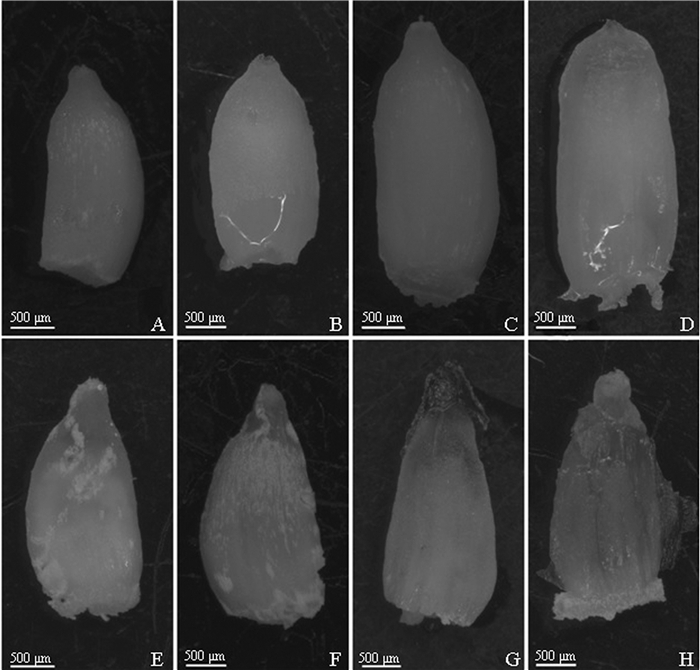
2 结果与分析 2.1 杉木胚珠的外部形态杉木胚珠外形多种多样,外侧有翅,将种翅剖开后会发现正常发育的胚珠呈乳白色,败育胚珠呈灰黄色,但在形成初期从外形上无法辨认。杉木可育胚珠的形态如图 1A~D所示,败育胚珠的形态如图 1E~H所示。从图 1A~D中可以看出,可育胚珠颜色呈乳白色,籽粒饱满,到5月下旬 (图 1C),胚珠迅速膨大;由图 1E~H可以看出,败育胚珠表面色泽较暗,籽粒干瘪,败育初期的胚珠仅珠孔端颜色较深呈灰黑色,后期胚珠表面全都变成灰黑色。
|
图 1 杉木胚珠显微图 Fig. 1 Micrograph of ovules of C. lanceolata 注:A~D为可育胚珠显微图;E~H为败育胚珠显微图。 Note: A~D indicate micrograph of fertile ovule. E~H indicate micrograph of abortive ovule. |
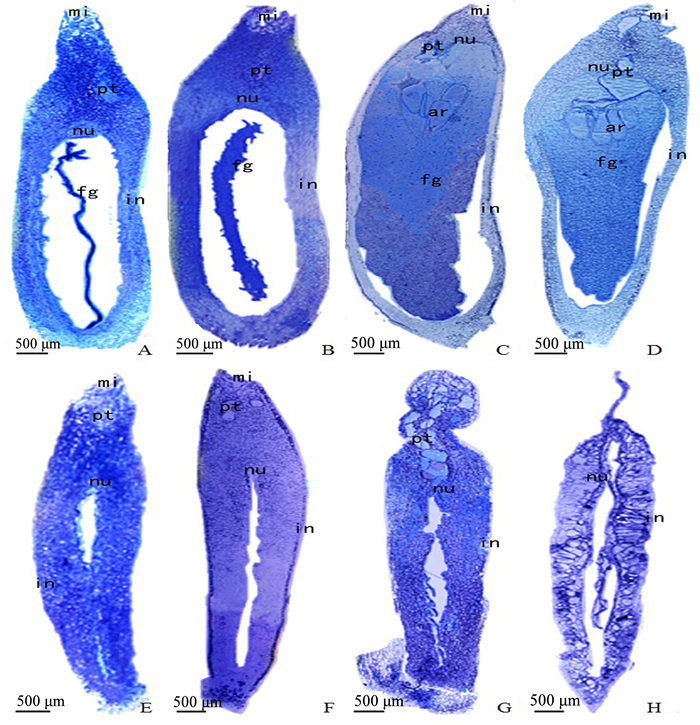
图 2A~D分别为5月10日、20日、30日和6月10日的可育胚珠纵切显微图。从图 2A可以观察到胚珠顶端的珠孔、花粉管,而在胚珠中央的珠心组织内刚发育形成雌配子体。5月10—30日是雌配子体快速发育的时期,珠心组织大部分被分解吸收,仅顶端还残留纸帽形状的薄层,颈卵器已经形成,花粉管向颈卵器方向延伸。到6月10日 (图 2D),花粉管伸长至颈卵器内。
|
图 2 杉木胚珠的纵切显微结构 Fig. 2 Longitudinal section of ovule of C. lanceolata 注:A~D为可育胚珠纵切显微图;E~H为败育胚珠纵切显微图;mi为珠孔;pt为花粉管;nu为珠心组织;in为珠被;fg为雌配子体;ar为颈卵器。 Note: A~D indicate longitudinal section micrograph of fertile ovule in early May and June; E~H indicate longitudinal section micrograph of abortive ovules in early May and June; mi indicate micropyle; pt indicate pollen tube; nu indicate nucellus; in indicate integument; fg indicate female gametophyte; ar indicate archegonium. |
图 2E~H分别为5月10日、20日、30日和6月10日的败育胚珠纵切显微图。5月10日 (图 2E) 胚珠刚出现败育的现象,胚珠瘦小,顶端有珠孔、花粉管,珠心组织萎缩且内部未形成雌配子体。到5月30日 (图 2G),珠孔退化消失,近珠孔部分明显收缩,花粉管伸长到珠心内部,雌配子体仍没有发育。到6月10日 (图 2H),部分珠心组织解体,胚珠内部组织松散。
综上所述,胚珠败育在正常授粉后不能形成健全的雌配子体完成受精,它与健全的胚珠结构变化有很大区别。此外,与可育胚珠相比,败育胚珠发育较快,如5月30日时可育胚珠刚形成颈卵器时,败育胚珠花粉管已经延伸到胚珠内部,到6月10日可育胚珠花粉管伸长至胚珠内部的颈卵器时,败育胚珠的内部结构已基本定型。
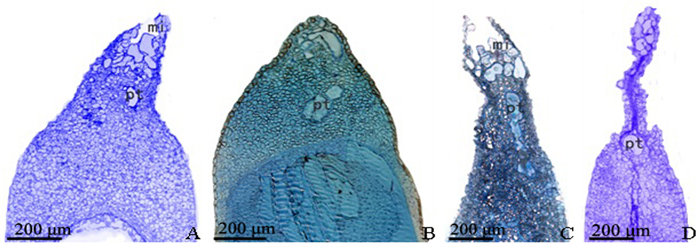
2.3 可育与败育胚珠的内部结构 2.3.1 可育与败育胚珠的顶端结构图 3为胚珠珠孔端的纵切显微图。杉木的雄配子体即花粉粒,经珠孔直接进入到胚珠,在珠心上方萌发,形成花粉管进入胚囊,将由生殖细胞所产生的精子送到颈卵器内。可育和败育胚珠均能正常形成珠孔,花粉都会萌发形成花粉管,且无论是健全还是败育的胚珠,其花粉管都能够向珠心组织内部延伸,为受精活动做准备。
|
图 3 杉木胚珠珠孔端的纵切显微图 Fig. 3 Longitudinal section of the micropylar end of ovule of C. lanceolata 注:A~B为5月上旬和6月上旬可育胚珠的珠孔端纵切显微图;C~D为5月上旬和6月上旬败育胚珠的珠孔端纵切显微图;mi为珠孔;pt为花粉管。 Note: A~B indicate longitudinal section micrograph of fertile ovule bead in early May and June; C~D indicate longitudinal section micrograph of abortive ovules center in early May and June; mi indicate micropyle; pt indicate pollen tube. |
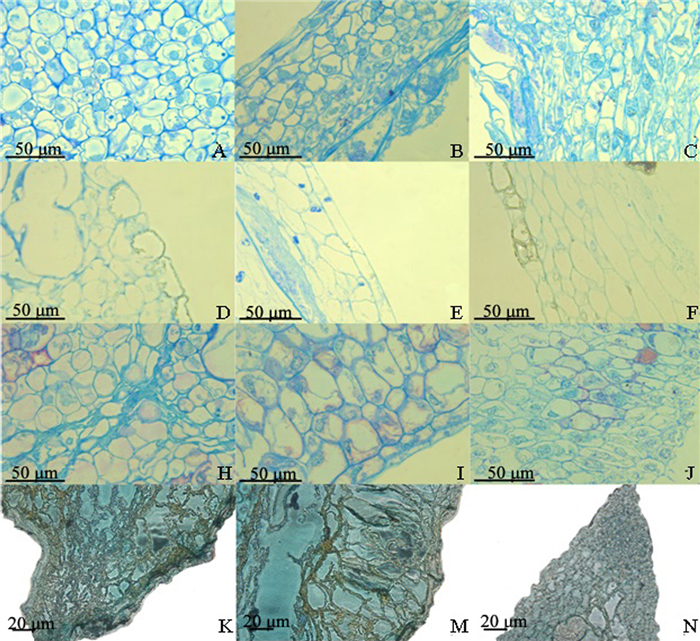
图 4A~C和图 4H~J分别为可育和败育胚珠5月10日的珠孔端、两侧和底端结构的放大图。可育胚珠内部细胞轮廓清晰,排列紧密,可清楚观察到细胞核结构。在败育胚珠的珠孔端,大多数细胞坏死,细胞核消失,少数细胞会解体退化,细胞间存在间隙;与珠孔端相比,两侧和底端的细胞保持较好,轮廓清晰,细胞未出现解体现象,细胞核明显。
|
图 4 杉木胚珠的珠孔端、两侧和底端的结构放大图 Fig. 4 Enlarged structure views at the ovule hole ends, both sides and the bottom of ovule of C. lanceolata 注:A~C为5月10日可育胚珠的珠孔端、两侧和底端纵切显微图;D~F为6月10日可育胚珠的珠孔端、两侧和底端纵切显微图;H~J为5月10日败育胚珠的珠孔端、两侧和底端纵切显微图;K~N为6月10日败育胚珠的珠孔端、两侧和底端纵切显微图。 Note: A~C indicate longitudinal section micrograph of sound ovules at the ovule hole ends, both sides and the bottom on May 10; D~F indicate longitudinal section micrograph of sound ovules at the ovule hole ends, both sides and the bottom on June 10; H~J indicate longitudinal section micrograph of abortive ovules at the ovule hole ends, on both sides and the bottom on May 10; K~N indicate longitudinal section micrograph of abortive ovules at the ovule hole ends, both sides and the bottom on June 10. |
图 4D~F和图 4K~N为可育和败育胚珠6月10日的珠孔端、两侧和底端结构放大图。可育胚珠内部细胞分层排列,结构清晰。败育胚珠萎缩较严重已经看不到完整细胞结构,内部组织解体退化,仅留下组织残痕,胚珠内部充满灰褐色物质。
与可育胚珠的内部正常形成的完整细胞形态和结构相比较而言,在败育胚珠的内部,细胞会发生解体,未解体的细胞会被灰褐色物质填充,细胞解体最先出现在胚珠的珠孔端。
3 结论与讨论在可育和败育胚珠珠心内,花粉都能萌发,形成的花粉管能持续向胚珠内部延伸。在败育胚珠内花粉萌发,形成花粉管向着珠心内部延伸。裸子植物中普遍存在受精延迟现象,太白红杉 (Larix chinensis Beissn)[12]、白豆杉 (Pseudotaxus chienii Cheng)[13]从传粉到受精大约需要一个月,在授粉后不久,花粉就开始从珠孔端向下生长,而此时胚珠还没有出现败育现象。另外汤红明等[14]研究表明花粉萌发离不开矿质元素和植物生长激素。这些说明胚珠尚未败育时,花粉已经萌发,而在败育初期,胚珠的结构功能未完全消失,仍然能为花粉的萌发提供所需营养物质。
可育胚珠的珠心组织中央会形成健全的雌配子体,而败育胚珠的珠心组织较瘦弱,其内未形成健全雌配子体。5月10日时在可育胚珠的珠心组织内,雌配子体开始发育,到6月10日时雌配子体发育成熟,其近珠孔端形成颈卵器结构,而同时期的败育胚珠,其珠心组织较弱小,珠心内部未形成雌配子体。苏建英等[15]、贾桂霞等[16]认为雌配子体从周围的珠心组织中吸收营养,另外史忠礼[17]也认为杉木胚的败育是因为雌配子体 (胚乳) 营养不充足造成的。故杉木胚珠的败育可能是珠心组织较瘦小,无法为雌配子体的发育提供充足营养。
在败育胚珠的珠孔端,最先出现细胞坏死和解体,导致珠孔端的组织变得松散,组织间出现涩粒物质,然后胚珠中下端逐渐开始出现这种现象, 说明胚珠败育时珠孔端先出现涩粒物质,然后向下蔓延。
雌配子体从其周围的珠心组织内吸收营养,体积快速增大,败育胚珠内部无雌配子体形成,内部主要是被涩粒物质填充的珠心组织。刘成运、苏建英等认为珠心组织主要是为雌配子体的发育提供营养, 而因败育胚珠内部未能形成雌配子体,珠心组织得以保留,后期败育胚珠的内部主要是珠心组织。
| [1] | 刘志敏. 香榧雌配子体的发育过程和败育研究[D]. 临安: 浙江农林大学, 2015. |
| [2] | 高智慧, 史忠礼, 许月明, 等. 杉木种子发育生理、涩籽成因及降低败育措施的研究[J]. 林业科学研究, 2000, 13(6): 659–666. |
| [3] | ZHEN Y, JI S S, ZHAO Z Z, et al. Proteomic analysis of seed development in Chinese fir (Cunninghamia lanceolata)[J]. Russian Journal of Plant Physiology, 2010, 57(4): 560–567. |
| [4] | ZHAO G W, ZHONG T L. Influence of exogenous IAA and GA on seed germination, vigor and their endogenous levels in Cunninghamia lanceolata[J]. Scandinavian Journal of Forest Research, 2013, 28(6): 511–517. |
| [5] | SHI J S, ZHEN Y, ZHENG R H. Proteome profiling of early seed development in Cunninghamia lanceolata (Lamb.) Hook.[J]. Journal of Experimental Botany, 2010, 61(9): 2367–2381. |
| [6] | WAN L C, WANG F, GUO X Q, et al. Identification and characterization of small non-coding RNAs from Chinese fir by high throughput sequencing[J]. BMC Plant Biology, 2012, 12(1): 146. |
| [7] | 许小丽, 崔朋辉, 林思祖, 等. 铝胁迫下杉木幼苗体内几种矿质元素含量变化及其相关性[J]. 福建农业学报, 2015, 30(12): 1178–1183. DOI:10.3969/j.issn.1008-0384.2015.12.009 |
| [8] | 方禄明. 低温、NaCl和PEG胁迫对杉木种子萌发及幼苗生长的影响[J]. 中国农学通报, 2016, 32(10): 1–6. DOI:10.11923/j.issn.2095-4050.cjas16040023 |
| [9] | 叶培忠, 陈岳武, 蒋恕, 等. 杉木种子生活力变异的研究[J]. 南京林业大学学报, 1981, 5(3): 22–32. |
| [10] | 余象煜, 李平, 顾建英, 等. 杉木的胚胎发育及淀粉动态[J]. 杭州大学学报, 1984, 11(1): 110–115. |
| [11] | 余象煜, 李平, 何福基, 等. 杉木败育种子及其涩粒物质的研究[J]. 西北植物学报, 1989, 9(4): 252–256. |
| [12] | 俞晓敏. 太白红杉胚胎学及其遗传多样性研究[D]. 西安: 西北大学, 2004. |
| [13] | 陈祖铿, 王伏雄. 白豆杉的配子体发育和受精作用[J]. 植物学报, 1979, 21(1): 19–29. |
| [14] | 汤红明, 徐冬青, 徐根娣, 等. 植物花粉萌发的研究进展[J]. 安徽农业科学, 2006, 34(24): 6436–6438, 6440. DOI:10.3969/j.issn.0517-6611.2006.24.014 |
| [15] | 苏建英, 王黎元. 白杄两性孢子叶球的胚胎学研究[J]. 阴山学刊, 1999, 15(6): 49–56. |
| [16] | 贾桂霞, 李凤兰, 沈熙环. 华北落叶松雌雄配子体的形成及胚胎发育[J]. 北京林业大学学报, 1994, 16(2): 10–14. |
| [17] | 史忠礼. 杉木涩籽的成因及降低措施[J]. 浙江林业, 1998(1): 23. |
| [18] | 刘成运. 云南油杉受精过程中新细胞质及蛋白泡的动态观察[J]. 植物学报, 1985, 27(3): 233–238. |

 2017, Vol. 37
2017, Vol. 37


