文章信息
- 郭晓申, 李涛洪, 梁坚坤, 王辉, 杜官本
- GUO Xiaoshen, LI Taohong, LIANG Jiankun, WANG Hui, DU Guanben
- 初始碱酸阶段摩尔比对脲醛树脂结构的影响
- Effects of molar ratio at initial alkaline and acid reaction stage on the structure of urea-formaldehyde resin
- 森林与环境学报,2016, 36(4): 494-499.
- Journal of Forest and Environment,2016, 36(4): 494-499.
- http://dx.doi.org/10.13324/j.cnki.jfcf.2016.04.019
-
文章历史
- 收稿日期: 2015-11-17
- 修回日期: 2016-01-06
脲醛(urea formaldehyde, UF)树脂以其成本低廉、性价比高、原料来源充足等一系列优势,被广泛地应用于木材工业领域[1-3]。但是,UF树脂也存在一些致命的缺点,如水解稳定性差、甲醛释放量高等,导致这些缺点的主要原因是树脂分子中一系列不稳定结构如亚甲基醚键(-CH2-O-CH2)的水解[4-7]。因此,在合成过程中尽可能减少醚键的生成,是对UF树脂结构及性能进行优化的主要研究方向之一。
在UF树脂的传统合成工艺中,普遍认为碱性阶段主要发生尿素与甲醛的加成反应,生成一系列的羟甲基化合物,同时羟甲基化产物间会发生一定程度的缩聚,生成小分子量的初聚物[8]。由于一些学者[3, 8]认为碱性条件下缩聚反应程度低,对后期UF树脂的最终结构影响不大,因此这方面的研究被多数学者所忽略。在酸性反应阶段,通常认为主要发生羟甲基化合物之间的缩聚反应,树脂分子量在此阶段急剧增加[8-12],宏观表现为树脂液的粘度不断增大。虽然在起始碱性反应阶段生成的一部分醚键在此阶段会水解重排为更为稳定的亚甲基桥键(-NR-CH2-NR-),但到达反应终点时仍有一部分醚键会残留在树脂最终结构中,因此通过改变工艺条件来降低此阶段醚键的含量是降低树脂最终结构中醚键含量的另一种有效措施。
由于在酸性条件下,甲醛与尿素的摩尔比(F/U)一般仍为2/1甚至更高,体系中仍然存在大量的二羟甲基脲以及三羟甲基脲,因此在醚键向桥键不断转化时仍然会有醚键不断生成,只不过醚键水解的速率大于生成的速率,总体表现为醚键的不断水解。若此时向反应体系内引入一定量的-NH2,那么从理论上来讲,体系中大量的羟甲基会与游离氨基碰撞生成桥键,桥键的生成会再次与醚键的生成形成明显的竞争,从而提高此阶段亚甲基桥键的生成量。
为了探索起始碱性阶段以及酸性阶段F/U的摩尔比对树脂最终结构的影响,对UF树脂合成工艺进行优化,使最终树脂结构中醚键含量处于较低水平。本研究将运用定量13C-NMR技术分别对传统工艺以及降低起始F/U摩尔比后合成出的UF树脂和降低酸性反应阶段时的UF树脂进行结构上的分析,以考察相应的树脂结构变化,进而阐述UF树脂起始碱性以及酸性阶段摩尔比对最终树脂结构的影响机制。
1 实验部分 1.1 实验原料尿素,分析纯,国药集团化学试剂有限公司生产;甲醛,分析纯,质量分数37%-40%,国药集团化学试剂有限公司生产;甲酸、NaOH均为分析纯,质量分数15%。
1.2 实验仪器数显恒温水浴锅,HH-2型;增力电动搅拌器(JJ1),常州澳华仪器有限公司生产;电子天平(0.01 g),JJ-200型,常熟双杰测试仪器厂生产;普通三口烧瓶(250 mL),带有回流冷凝装置以及温度计;精密pH试纸;烧杯,玻璃棒等常用器皿。
1.3 UF树脂的合成 1.3.1 基于传统工艺下UF树脂的合成UF系列树脂的合成,详细操作过程参照文献[9]所述。
UF-A1:保持F : U1=2.0(摩尔比,下同),在pH为8.0-8.5,温度为90 ℃条件下,保温反应40 min;之后用甲酸溶液调节反应液pH为5.0-5.5,反应至目标粘度,降温至60 ℃并调节pH=8.0,加入第2批尿素U2,使F : (U1+U2)=1.2,冷却出料,取少量合成树脂迅速冷却后放置冰箱中冷藏备用(下同)。
UF-A2:保持F : U1=2.0,90 ℃条件下保温反应40 min;之后用甲酸溶液调节反应液pH为5.0-5.5,反应0.5 h后加入第2批尿素U2使反应体系摩尔比为1.5:1,反应到达终点后降温至60 ℃并调节pH=8.0,加入U3使得F: (U1+U2+U3)=1.2,继续反应10-15 min后冷却出料。
UF-A3 :工艺及反应参数与UF-A2大致相同,不同处为U2的加入是在酸性反应阶段后期。
1.3.2 低起始摩尔比UF树脂的合成UF-B1:保持F1 : U1=1.0,在pH为8.0-8.5,温度为90 ℃条件下,保温反应40 min,补加甲醛,使(F1+F2) : U1=2.0,之后调节pH为5.0-5.5,反应至目标粘度后,调节pH=8.0,加入U2,同样使(F1+F2) : (U1+U2)=1.2,冷却出料。
UF-B2:保持F1 : U1=1.0,90 ℃条件下保温反应40 min;之后加入F2,使(F1+F2) : U1=2.0,调节pH为5.0-5.5,反应0.5 h后加入尿素U2使(F1+F2) : (U1+U2)=1.5:1,反应至目标粘度后,降温至60 ℃并调节pH=8.0,加入尿素U3,使摩尔比(F1+F2) : (U1+U2+U3)=1.2,继续反应10-15 min后冷却出料。
UF-B3 :尿素分3批加入,U2的加入是在酸性反应阶段后期,其它参数与UF-B2所用工艺参数相同。
1.4 13C-NMR测定仪器:瑞士布鲁克公司(Brucker Advance Ⅲ 600MHz)生产的高分辨超导核磁共振仪。
样品处理:用氘代二甲基亚砜(DMSO-d6)作为溶剂,样品与溶剂各取300 μL注入核磁管中溶解摇匀。
测定参数:脉冲序列为反门控去耦(zgig),弛豫延迟时间6 s,内标为DMSO-d6,累加次数500-800次,测量谱宽39 062.5 Hz,数据点64 k。
谱峰归属参见文献[6, 10-12],各类型含亚甲基碳结构峰值归属见表 1。
| 结构Structure | 化学位移Chemical shift (δ) | UF-A1 | UF-A2 | UF-A3 | UF-B1 | UF-B2 | UF-B3 |
| -NH-CH2-NH-(Ⅰ) | 46-48 | 15.34 | 20.64 | 19.89 | 14.73 | 21.03 | 20.16 |
| -NH-CH2-N=(Ⅱ) | 53-55 | 14.72 | 19.08 | 18.88 | 18.90 | 22.69 | 17.41 |
| =N-CH2-N=(Ⅲ) | 60-61 | - | 0.72 | 0.73 | - | 0.78 | - |
| 总计Total | 30.06 | 40.44 | 39.50 | 33.63 | 44.50 | 37.57 | |
| -NH-CH2OCH2NH-(Ⅰ) | 68-70 | 8.18 | 7.43 | 8.50 | 5.60 | 6.26 | 7.61 |
| -NH-CH2OCH2N=(Ⅱ)/Uron | 75-77 | 4.09 | 1.93 | 1.62 | 0.35 | 0.57 | 0.60 |
| =N-CH2OCH2N=(Ⅲ)/Uron | 78-80 | 5.60 | 2.32 | 3.94 | 0.80 | 1.22 | 0.58 |
| 总计Total | 17.87 | 11.68 | 14.06 | 6.75 | 8.05 | 8.79 | |
| -NH-CH2OH(Ⅰ) | 64-66 | 45.80 | 37.97 | 36.87 | 48.89 | 35.03 | 45.02 |
| -NH(-CH2 )-CH2OH(Ⅱ) | 71-72 | 1.97 | 2.66 | 3.05 | 5.23 | 0.42 | 3.08 |
| 总计Total | 47.77 | 40.63 | 39.92 | 54.12 | 35.45 | 48.10 | |
| HO-CH2-OH | 83-84 | 0.35 | 0.47 | 0.04 | 0.86 | 0.69 | 0.46 |
| HOCH2-O-CH2-OCH2OH | 86-87 | 0.29 | 0.26 | 0.33 | 0.82 | 0.52 | 0.35 |
| HOCH2-O-CH2-OCH2OH | 90-91 | 0.32 | 0.71 | 0.39 | 0.72 | 0.92 | 0.41 |
| H(CH2O)nOCH2OCH3 | 94-95 | - | 0.27 | 0.28 | 0.32 | 0.25 | - |
| 总计Total | 0.96 | 1.71 | 1.04 | 2.72 | 2.38 | 1.22 | |
| -NH-CH2-O-CH3 | 72-73 | 3.35 | 5.55 | 5.49 | 2.77 | 5.88 | 4.31 |
| NH2-CO-NH2 | 163-164 | 20.66 | 10.35 | 14.46 | 26.51 | 16.52 | 14.27 |
| NH2-CO-NH- | 161-162 | 34.02 | 31.85 | 31.68 | 24.81 | 22.15 | 29.63 |
| -NH-CO-N-/-NH-CO-N= | 159-161 | 41.10 | 55.10 | 50.69 | 47.85 | 60.69 | 55.49 |
| Uron | 154-158 | 4.22 | 2.71 | 3.18 | 0.83 | 0.65 | 0.62 |
定量分析:以δ=83处甲二醇为基准峰,对所有峰进行积分。然后对所有亚甲基碳积分面积求和,即δ=100以下所有谱峰的积分面积之和(δ=50处甲醇以及δ=56处甲氧醚除外)。不同类型化学键积分值与总亚甲基碳积分值的比值为各类型亚甲基碳的百分含量[12]。另外对所有羰基碳积分面积求和,即对δ位于150-165区域内谱峰面积求和,此区域中不同结构类型所对应的羰基碳的积分值与总羰基碳积分值的比值为各类型羰基碳结构的百分含量。各工艺UF树脂最终结构所对应化学位移与定量分析结果见表 1。
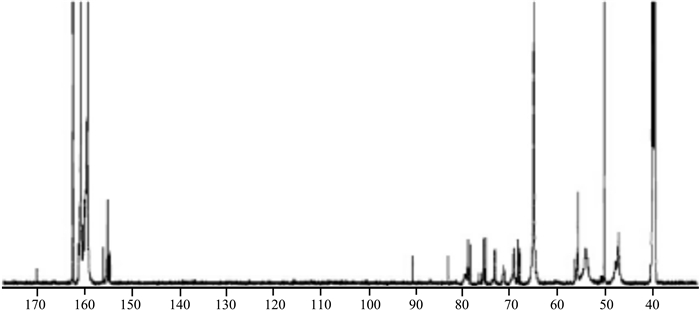
2 结果与讨论 2.1 碱性阶段低起始摩尔比对树脂结构的影响UF-A1与UF-B1的谱图分别见图 1和图 2。各化学位移归属与百分含量见表 1。当降低碱性阶段摩尔比后树脂中醚键含量由17.87%降低至6.75%,说明在碱性阶段降低起始摩尔比是一种降低最终树脂结构中醚键含量的非常有效的手段。值得注意的是,在δ位于154-158区域内,对应于Uron环结构羰基碳的化学位移,而Uron环结构中亚甲基醚键亚甲基碳的化学位移也会出现在δ位于75-80区域内,它们可能对应Uron环被羟甲基化或者发生了一定程度的取代,一般在UF树脂的谱图中δ位于75-80区域内的谱峰与δ位于154-158区域的谱峰是相伴随出现的,因此δ位于75-80区域内的醚键与Uron结构会发生重叠。在UF-A1中δ位于75-80区域内醚键的总含量为9.69%,而Uron环结构的含量为4.22%;同样在UF-B1中δ位于75-80区域内醚键的总含量为1.15%,而Uron环结构的含量为0.83%,这说明δ位于75-80区域内醚键中的相当一部分是由Uron环结构所贡献的。也就是说降低碱性阶段摩尔比后醚键含量的降低大部分来源于树脂中Uron结构的降低,线性醚键降低的比例相对较小。另外,UF-A1桥键含量为30.06%,而UF-B1桥键含量为33.63%,二者桥键含量基本相当。
|
图 1 UF-A1的13C-NMR谱图 Fig. 1 13C-NMR spectrum of UF-A1 |

|
图 2 UF-B1的13C-NMR谱图 Fig. 2 13C-NMR spectrum of UF-B1 |
虽然通过降低起始甲醛与尿素的摩尔比可以有效地降低树脂中醚键的含量,但也带来了一些负面的影响。UF-B1工艺虽然醚键含量较低,但是羟甲基含量较UF-A1工艺高7%左右,而游离甲醛总量也较UF-A1工艺高2%,造成这种现象的主要原因是醚键的分解使得最终树脂结构中羟甲基含量较高,而没有转化为比较稳定的亚甲基桥键,另外酸性过程中醚键大量水解的同时会伴随甲醛的释放。
2.2 酸性阶段前期降低摩尔比对UF树脂结构的影响为了适当降低最终树脂中羟甲基的含量同时增加树脂的缩聚度,在UF-A1与UF-B1工艺基础上,再在其酸性阶段反应前期30 min时和酸性阶段反应后期加入了第2批尿素,使酸性阶段的甲醛与尿素的摩尔比降低至1.5:1。由表 1可知,总体上UF-B系列树脂相对于UF-A系列工艺,醚键含量普遍偏低,这是由于低摩尔比工艺在碱性阶段时醚键即处于一个较低的水平,因此最终树脂中醚键的含量也相对较低。其中,2种工艺在I型醚键含量上的差异并不明显,而主要差异在于δ位于75-80区域内醚键,即Uron环结构的差异,因为2种工艺起始甲醛与尿素的摩尔比不同,因此最终结构中Uron结构含量有一定的差异。
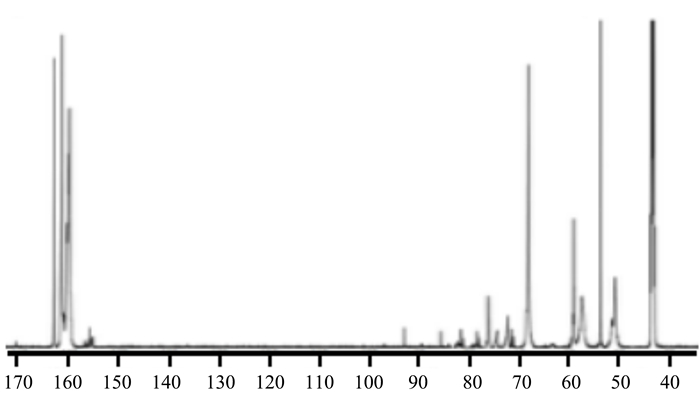
UF-A2与UF-B2谱图分别见图 3和图 4。UF-A2在桥键含量上比UF-A1约增加了10%,同时羟甲基含量也出现了一定幅度的降低,这种趋势在UF-B2工艺中也有一定的体现。总体看来,不管是传统工艺还是低起始摩尔比工艺,在酸性反应阶段前期添加尿素都会使亚甲基桥键的含量明显增加,同时羟甲基含量也出现了明显的降低。对比UF-A2与UF-A1样品中基团含量变化可知,羟甲基的含量大约减少了7%,而亚甲基桥键的含量则大约增加了10%。证明尿素加入后,主要与游离羟甲基反应生成亚甲基桥键,在UF-B1到UF-B2也呈现出相同的趋势。
|
图 3 UF-A2的13C-NMR谱图 Fig. 3 13C-NMR spectrum of UF-A2 |
|
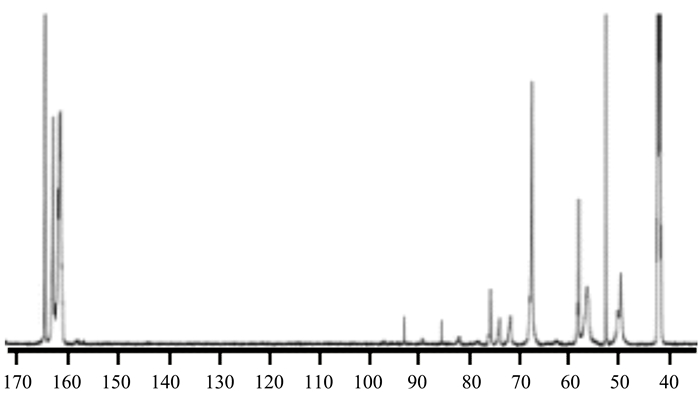
图 4 UF-B2的13C-NMR谱图 Fig. 4 13C-NMR spectrum of UF-B2 |
将UF-A2与UF-A1对比,当在传统工艺酸性反应阶段前期加入尿素后,树脂最终结构中亚甲基醚键含量从17.87%变为11.68%,即醚键的含量出现明显降低的趋势,这是由于酸性阶段前期加入尿素时,体系中羟甲基含量仍处于较高水平,加入的尿素会立刻与羟甲基反应生成亚甲基桥键,即反应效率较率较低,因此最终树脂中醚键含量出现降低的趋势。而出人意料的是在UF-B系列工艺中,对比UF-B2与UF-B1醚键的含量高,而羟甲基之间反应生成醚键的效可以发现当酸性阶段加入尿素后醚键含量并没有下降,反而醚键含量增加了3%,这是由于UF-B2树脂第2批加入的甲醛在酸性阶段前期仍部分存在于反应体系中,在此时加入的尿素将首先与甲醛发生反应生成羟甲基化合物,羟甲基化合物之间缩聚形成了醚键,虽然醚键会随后发生水解,但是酸性阶段生成了一部分醚键会导致醚键的峰值变大,因此反应结束后出现UF-B2中醚键含量稍有升高的现象。
对比表 1中UF-B2与UF-B1的数据可以发现,它们最终的游离甲醛含量基本相当,这说明了尿素的加入并没有改变游离甲醛在反应体系内存在的平衡;而从UF-A1到UF-A2,游离甲醛的含量反而从0.96%增加到1.71%,这是由于在传统工艺酸性阶段加入尿素后,醚键含量出现降低,醚键的水解必然伴随游离甲醛的释放,因此UF-A2工艺出现游离甲醛增加的现象。
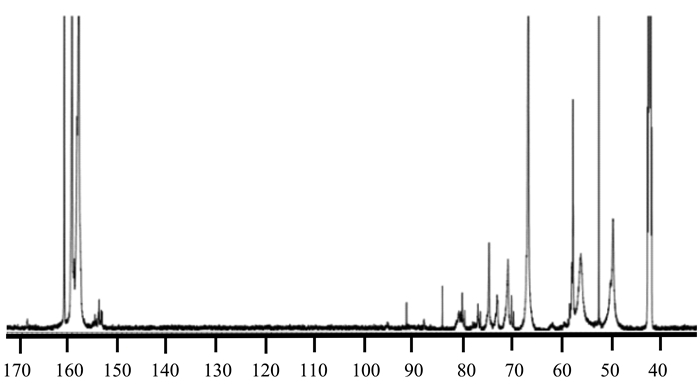
2.3 酸性阶段后期降低摩尔比对UF树脂结构的影响样品UF-A3与UF-B3的核磁谱图分别见图 5和图 6。由表 1中可知,当在酸性阶段后期加入尿素后各结构的变化与酸性阶段前期加入尿素的变化相似,均出现羟甲基含量减少,桥键含量增加的现象。而在UF-B3工艺中,醚键含量也有所增加,这是由于酸性阶段后期树脂中醚键水解产生了大量的游离甲醛,此时加入的尿素会首先发生羟甲基化,随后生成醚键,因此会出现醚键含量的升高。
|
图 5 UF-A3的13C-NMR谱图 Fig. 5 13C-NMR spectrum of UF-A3 |

|
图 6 UF-B3的13C-NMR谱图 Fig. 6 13C-NMR spectrum of UF-B3 |
对比UF-A3与UF-A2可以看出2组数据在各种化学结构含量上的差异非常小,最终树脂各结构含量上相差最大的不超过3%。这说明不管酸性阶段前期向反应体系内加入尿素还是后期加入,最终树脂结构并不会有太大的差异。
而对比表 1中UF-B3与UF-B2结构的数据可以看出对于低起始摩尔比工艺来讲,酸性阶段尿素的加入时间对最终树脂结构造成了明显的差异,UF-B2中亚甲基桥键含量为44.50%,而UF-B3中亚甲基桥键含量为37.57%,二者相差较大,分析UF-B2工艺是在进入酸性阶段后又加入了第2批甲醛,因此在酸性阶段30 min时体系中仍存在大量的羟甲基化合物,此时加入尿素后大量羟甲基必然会被尿素消耗生成桥键;而在酸性阶段后期,树脂结构中羟甲基之间的缩聚已趋于平衡,因此,此时羟甲基的含量已接近酸性阶段的最低值,而在此时加入尿素后与之反应的羟甲基数量也非常有限,因此桥键的生成也比较有限。
另外值得注意的是,无论是UF-A3还是UF-B3工艺,最终制成的树脂中游离甲醛的含量都是几组工艺中最小的,说明在酸性阶段后期向体系中加入尿素对游离甲醛的吸收是有一定促进作用的。由于酸性后期反应体系内醚键的水解趋势已经非常微弱,而体系中的游离甲醛也呈现比较稳定的趋势并且其含量也较高,因此加入尿素的一部分会与游离甲醛反应,起到提前吸收游离甲醛的作用。
对比UF-B系列工艺所得最终树脂的结构,酸性前期加入尿素后桥键的增长要高于后期加入尿素后桥键的增长,这是由于在酸性反应阶段后期,聚合物结构已经基本形成,尿素的加入主要会与甲醛反应生成羟甲基,羟甲基之间的缩聚导致聚合度的增加;而在酸性阶段前期加入尿素时,体系内存在着大量的羟甲基,因此桥键的提升要更为明显。
3 结论通过研究, 可以得出以下一些结论: (1)降低碱性阶段起始F/U摩尔比后, 可以有效降低最终树脂结构中醚键的含量,特别是Uron环含量差异较大。然而,由于醚键分解所生成的羟甲基未有效参与亚甲基桥键的生成,因此,最终树脂中羟甲基与游离甲醛含量较高。(2)无论在酸性反应阶段前期还是后期降低F/U摩尔比,都可以提高树脂最终结构中亚甲基桥键含量,同时羟甲基含量减少,主要原因是加入尿素的游离氨基与体系内存在的羟甲基反应生成亚甲基桥键的效率比较高。(3)由于树脂酸性阶段反应后期聚合物结构已经基本形成,而酸性阶段前期反应体系内仍存在大量的羟甲基,因此在酸性阶段前期加入尿素后桥键含量的提升更为明显。
| [1] | 顾继友. 胶粘剂与涂料[M]. 北京: 中国林业出版社, 1999 . |
| [2] | 李东光. 脲醛树脂胶粘剂[M]. 北京: 化学工业出版社, 2002 . |
| [3] | DUNKY M. Adhesives based on formaldehyde condensation resins[J]. Macromolecular Symposia, 2004, 217(1): 417–430. |
| [4] | 赵临五, 王春鹏. 脲醛树脂胶黏剂[M]. 北京: 化学工业出版社, 2005 . |
| [5] | MEYER B, HERMANNS K, SMITH D C. Formaldehyde release from urea-formaldehyde bonded wood products[J]. The Journal of Adhesion, 1985, 17(4): 297–308. |
| [6] | KIM M G, AMOS L W. Quantitative carbon-13 NMR study of urea-formaldehyde resins in relation to the formaldehyde emission levels[J]. Industrial & Engineering Chemistry Research, 1990, 29(2): 208–212. |
| [7] | FERG E E, PIZZI A, LEVENDIS D C. 13C NMR analysis method for urea-formaldehyde resin strength and formaldehyde emission[J]. Journal of Applied Polymer Science, 1993, 50(5): 907–915. |
| [8] | DUNKY M. Urea-formaldehyde (UF) adhesive resins for wood[J]. International Journal of Adhesion and Adhesives, 1998, 18(2): 95–107. |
| [9] | 郭晓申, 李涛洪, 梁坚坤, 等. 碱性阶段起始F/U配比对UF最终结构影响的13C-NMR研究[J]. 中国胶粘剂, 2014, 23(11): 1–6. |
| [10] | CHRISTJANSON P, PEHK T, SIIMER K. Structure formation in urea-formaldehyde resin synthesis[J]. Proceedings of the Estonian Academy of Sciences, Chemistry, 2006, 55(4): 212–225. |
| [11] | CHUANG I S, MACIEL G E. NMR study of the stabilities of urea-formaldehyde resin components toward hydrolytic treatments[J]. Journal of Applied Polymer Science, 1994, 52(11): 1637–1651. |
| [12] | 杜官本. 酸性环境下脲醛树脂结构形成特征[J]. 西南林学院学报, 1999, 19(2): 126–130. |

 2016, Vol. 36
2016, Vol. 36


