文章信息
- 林宝平, 林思祖, 何宗明, 林宇, 郜士垒, 董强
- LIN Baoping, LIN Sizu, HE Zongming, LIN Yu, GAO Shilei, DONG Qiang
- 不同碳输入方式对沿海防护林土壤氮库的影响
- Effects of different carbon input methods on soil nitrogen pool of coastal shelter forest
- 森林与环境学报,2016, 36(4): 385-391.
- Journal of Forest and Environment,2016, 36(4): 385-391.
- http://dx.doi.org/10.13324/j.cnki.jfcf.2016.04.001
-
文章历史
- 收稿日期: 2016-04-11
- 修回日期: 2016-05-10
2. 国家林业局杉木工程技术研究中心, 福建 福州 350002;
3. 福建省长乐大鹤国有防护林场, 福建 长乐 350212
2. State Forestry Administration Engineering Research Center of Chinese Fir, Fuzhou, Fujian 350002, China;
3. Changle Dahe State-Owned Protection Forest Farm of Fujian Province, Changle, Fujian 350212, China
土壤氮素通常占整个森林生态系统氮储量的90%以上[1],森林土壤氮素的转化与循环是森林生态系统氮素循环中最重要和最活跃的部分,影响土壤的质量和森林生态系统的生产力,其微小的变化都会改变整个森林生态系统的氮素平衡。森林土壤氮素主要来自于生物固氮、凋落物归还、人为施肥、氮沉降等,而氮素的输出途径主要有氮挥发、氮淋溶损失、植物根系吸收等,其中,根系和凋落物是植物体影响土壤氮素循环的最主要途径。通过凋落物的添加和去除(detritus input and removal treatments, DIRT)试验来探究植物根系和凋落物对土壤氮素的影响,根系去除处理阻断了植物对氮素的吸收,对壕沟小区内土壤氮素循环影响较大,地上凋落物的移除对氮循环影响较小[2]。然而,HOLUB et al[3]认为凋落物和根系处理对土壤氮循环的影响均不显著。此外,大气氮沉降也是影响DIRT试验的重要因素。土壤中的氮主要以有机氮和无机氮(以硝态氮和铵态氮为主)2种形式存在,其中硝态氮(NO3 --N)和铵态氮(NH4 +-N)是植物从土壤中吸收氮源的主要形态,可溶性有机氮(dissolved organic nitrogen, DON)和土壤微生物量氮(microbial biomass nitrogen, MBN)是土壤氮素活性组分,影响土壤养分的有效性和流动性[4],同时能够反映土壤有机氮的矿化能力,可以作为反映土壤矿化和固持能力的指标。
氮素是植物生长的必要元素,但过量的氮素会导致森林生态系统的氮饱和现象,亚热带地区是氮沉降最严重的地区,有研究表明氮素不再是该地区植物生长的限制性因子,但目前对亚热带地区氮素循环的研究多集中于内陆森林土壤,对滨海沙地人工林土壤氮素循环的认识还十分有限,亚热带滨海沙地雨热同期,多台风强降雨天气,同时砂质土壤渗透性极强,不利于氮素的固持,夏季高强度的降雨容易造成土壤氮素淋溶损失,在严重氮沉降和氮淋溶背景下滨海沙地土壤氮素循环特征还未可知,因此探究亚热带滨海地区人工林土壤氮素保持机制的影响因子至关重要。土壤凋落物和根系是植物体影响土壤氮素循环的主要途径,改变地上、地下碳输入是探究植物体对土壤氮素影响的有效方法。为此,以3种典型沿海防护林树种尾巨桉(Eucalyptus urophylla×E.grandis, Euc)、纹荚相思(Acacia aulacocarpa Benth., Aca)、木麻黄(Casuarina equisetifolia J R Forst & G.Forst., Cas)人工林为研究对象,通过设置切断根系、去除地表凋落物处理来探究滨海沙地人工林土壤氮素特征,探究根系和凋落物在土壤氮素循环中所扮演的角色,以期为中国沿海防护林土壤氮素循环提供理论依据。
1 材料与方法 1.1 试验地概况试验地位于福建省东南部长乐大鹤国有防护林场,北纬25°96′,东经119°68′,东临东海,属南亚热带海洋性季风气候,温和多雨,年降水量达1 196-1 771 mm,年平均气温19.2 ℃,最高气温35 ℃,最低气温0 ℃,年积温7 400-7 700 ℃。试验地土壤均为滨海风积砂土,砂层6-10 m,保水能力低,土壤极度贫瘠,有机质聚集于0-10 cm表层。该地沿海防护林为人工纯林,林下植被稀少,常见零星植被有大蓟(Cirsium japonicum Fisch.ex DC.)、马樱丹(Lantana camara Linn.)、茅莓(Rubus parvifolius L.),一点红[Emilia sonchifolia (L.)DC.]等。尾巨桉、纹荚相思、木麻黄均为2003年春在湿地松(Pinus elliottii Engelm.)采伐迹地上营造的,林分的生物量和土壤基本理化性质见表 1。其中,年凋落物量采用凋落物框收集法获得,收集时间为2014年9月至2015年8月每月下旬。2015年1月对各林分进行每木检尺,调查其生长量;土壤容重采用200 cm3环刀测定;使用酸度计测定土壤pH值,水土比为2.5 : 1。
| 林分类型 Forest types | 平均胸径 DBH /cm | 平均树高 Tree height /m | 密度 Density /(tree·hm-2) | 容重 Bulk density /(g·cm-3) | 土壤全碳 Soil total C /(g·kg-1) | 土壤全氮 Soil total N /(g·kg-1) | 土壤碳氮比 Soil C/N rate | 年凋落物量 Litter biomass /(t·hm-2·a-1) | pH |
| Euc | 14.63 (0.28) | 19.28 (0.23) | 1 250 | 1.32 (0.03) | 3.65 (0.43) | 0.35 (0.05) | 10.41 (1.19) | 9.88 | 5.48 (0.14) |
| Aca | 10.61 (0.68) | 10.60 (0.26) | 1 500 | 1.47 (0.03) | 4.13 (0.44) | 0.40 (0.04) | 10.62 (1.35) | 8.53 | 4.96 (0.04) |
| Cas | 11.61 (0.56) | 11.32 (0.46) | 1 903 | 1.24 (0.08) | 4.42 (0.39) | 0.47 (0.01) | 9.51 (0.52) | 16.76 | 5.06 (0.04) |
| 1)括号中数据为标准误(n=4)。Note : figures in brackets indicate standard errors. | |||||||||
2014年7月,在3种人工林内分别设置4个20 m×20 m样地,每个样地内随机布设3个2 m×2 m的小区。采用完全随机区组设计方法分别在小区内设置3种处理:(1)去除凋落物层,将地上部分枯枝落叶清除后,在小区上方1 m高处用网框截留枯枝落叶;(2)切断根系,沿小区四周挖1 m深壕沟,并埋入尼龙网隔断新的根系进入;(3)对照,不做人为干扰,保持天然状态下的凋落物和根系输入。
1.2 样品采集与测定2015年7月,在每个处理内随机选取3个点,使用内径2.5 cm土钻取各点0-10 cm土层土壤,去除残留的凋落物、可见根系,充分混匀后立即冷藏带回室内。在室内取部分样品过2 mm筛后置于4 ℃冰箱中,用氯仿—熏蒸浸提法测定MBN[5],冷水浸提方法测定土壤DON[6]。使用2 mol · L-1的KCl溶液(土: KCl=1 : 4)浸提土壤中的矿质氮(NH4 +-N 、NO3 --N),并采用全自动连续流动分析仪测定。另取部分土样自然风干后过0.149 mm筛,采用碳氮元素分析仪测定土壤全碳和全氮含量。
1.3 数据处理与分析所有的数据统计与分析均基于SPSS Statistics 17.0和Excel 2003软件,相关图表在Excel 2003中完成。采用单因素方差分析(One-way ANOVA)和多重比较(least-significant difference,LSD)法对比同一树种不同处理间以及不同树种相同处理间各氮素成分的差异显著性。显著性水平设置为P=0.05。采用相关分析方法分析土壤各氮素指标之间的相关性。
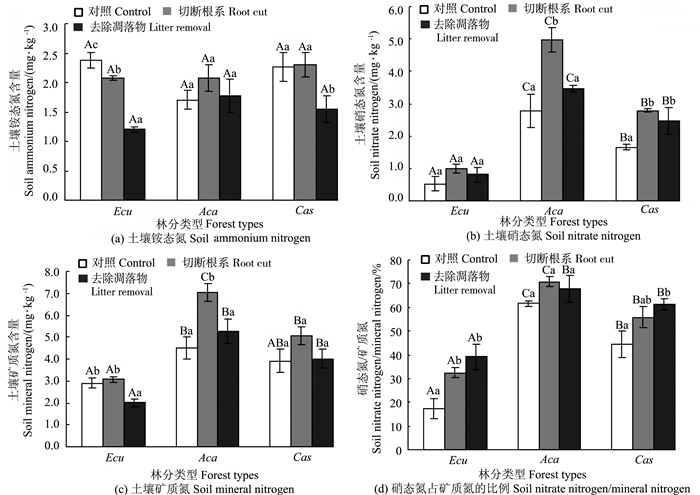
2 结果与分析 2.1 不同处理下土壤矿质氮含量特征对照处理下3种人工林土壤矿质氮含量表现为纹荚相思>木麻黄>尾巨桉,其中尾巨桉与纹荚相思土壤矿质氮含量差异显著(P < 0.05),3种人工林土壤NH4 +-N含量差异不显著,但NO3 --N含量差异显著(P < 0.05),表现为纹荚相思>木麻黄>尾巨桉。切断根系和去除凋落物处理均显著降低尾巨桉土壤NH4 +-N含量(P < 0.05),去除凋落物处理显著降低了木麻黄土壤NH4 +-N含量(P < 0.05),对纹荚相思土壤NH4 +-N影响不显著[图 1(a)];切断根系或去除凋落物1 a后,3种人工林土壤NO3 --N含量均升高,其中,切断根系处理对纹荚相思和木麻黄的影响达到显著水平(P < 0.05)[图 1(b)]。
|
图 1 3种人工林不同处理下土壤矿质氮含量 Fig. 1 Content of mineral nitrogen under different treatments of three plantations 注:图中横条为标准误(n=4),同一树种不同处理间未出现相同小写字母表示差异显著(P < 0.05),相同处理不同树种间未出现相同大写字母表示差异显著(P < 0.05)。 Note : bars indicate standard error(n=4), figures lack of a same lowercase letter in the same species under different treatments indicated significant differences between the different treatments, figures lack of a same lowercase letter in the same treatment under different species indicated significant differences between the different species (P < 0.05). |
切断根系处理均提高土壤矿质氮含量,这与土壤NO3 --N含量对该处理的响应一致,去除地表枯枝落叶层后,尾巨桉土壤矿质氮含量显著降低(P < 0.05),对其余2种树种的影响并不一致[图 1(c)]。NO3 --N含量占矿质氮含量的比重可以反映土壤硝化作用的强弱,切断根系和凋落物均提高了NO3 --N在矿质氮中的比重,其中,对尾巨桉的影响均达显著水平(P < 0.05)[图 1(d)],说明去除凋落物或切断根系处理后土壤硝化作用增强。
2.2 不同处理对DON 、MBN的影响尾巨桉人工林土壤DON含量显著低于纹荚相思和木麻黄人工林,除木麻黄DON含量在去除凋落物后有所降低外,切断根系或去除凋落物后人工林土壤DON含量均高于对照组。与可溶性有机氮对切断根系和去除凋落物的响应相反,切断根系或去除凋落物后3种人工林土壤微生物量氮均低于对照组,其中对尾巨桉和纹荚相思的影响达显著水平(P < 0.05)。切断根系或去除凋落物后,尾巨桉和纹荚相思人工林的土壤MBN/TN均显著低于对照组(P < 0.05)(表 2)。
| 林分类型 Forest types | 处理 Treatment | 可溶性有机氮含量 DON content/(mg·kg-1) | 微生物量氮含量 MBN content/(mg·kg-1) | 微生物量氮:全氮 MBN:TN/% |
| Ecu | 对照Control | 0.64 (0.04)Aa | 19.70 (1.11)Bb | 5.77 (0.79)Bb |
| 切断根系Root cut | 0.92 (0.12)Aa | 7.18 (0.31)Ba | 1.88 (0.13)Ba | |
| 去除凋落物Litter removal | 0.72 (0.03)Aa | 8.24 (0.86)Ba | 2.17 (0.35)Ba | |
| Aca | 对照Control | 2.70 (0.25)Ba | 5.04 (0.43)Ab | 1.30 (0.14)Ab |
| 切断根系Root cut | 5.44 (0.10)Cb | 2.91 (0.35)Aa | 0.76 (0.12)Aa | |
| 去除凋落物Litter removal | 4.31 (0.15)Cc | 2.85 (0.20)Aa | 0.83 (0.06)Aa | |
| Cas | 对照Control | 1.99 (0.30)Ba | 7.44 (0.71)Ab | 1.62 (0.19)Aab |
| 切断根系Root cut | 3.42 (0.19)Bb | 8.96 (0.37)Cb | 2.09 (0.10)Bb | |
| 去除凋落物Litter removal | 1.43 (0.23)Ba | 4.30 (0.96)Aa | 1.10 (0.29)Aa | |
| 1)括号中数据为标准误(n=4),未出现相同小写字母表示同一树种不同处理间的差异显著(P < 0.05),相同处理不同树种间未出现相同大写字母表示差异显著(P < 0.05)。Note : figures in brackets indicate standard errors(n=4), figures lack of a same lowercase letter in the same species under different treatments indicated significant differences between the different treatments(P < 0.05), figures lack of a same capital letter in the same treatment under different species indicated significant differences between the different species (P < 0.05). | ||||
项目 Items | 全碳 Total C | 全氮 Total N | 土壤碳氮比 Soil C/N rate | 硝态氮 NO3--N | 铵态氮 NH4+-N | 可溶性有 机碳DOC | 可溶性有 机氮DON | 微生物量 碳MBC | 微生物 量氮MBN | 土壤pH Soil pH |
| 全碳 Total C | 1 | |||||||||
| 全氮 Total N | 0.771** | 1 | ||||||||
| 土壤碳氮比 Soil C/N rate | 0.776** | 0.213 | 1 | |||||||
| 硝态氮 NO3--N | -0.106 | 0.056 | -0.248 | 1 | ||||||
| 铵态氮 NH4+-N | 0.367 | 0.332 | 0.240 | 0.074 | 1 | |||||
| 可溶性有机碳 DOC | 0.534** | 0.282 | 0.556** | -0.413* | 0.461** | 1 | ||||
| 可溶性有机氮 DON | -0.058 | 0.017 | -0.146 | 0.900** | 0.138 | -0.203 | 1 | |||
| 微生物量碳 MBC | 0.219 | 0.010 | 0.341* | -0.258 | 0.203 | 0.488** | -0.210 | 1 | ||
| 微生物量氮 MBN | 0.187 | -0.059 | 0.380* | -0.671** | 0.264 | 0.437** | -0.552** | 0.491** | 1 | |
| 土壤pH Soil pH | -0.050 | -0.197 | 0.115 | -0.739** | -0.145 | 0.074 | -0.748** | 0.181 | 0.571** | 1 |
| 1)*表示在0.05水平(双侧)上显著相关,* *表示在0.01水平(双侧)上显著相关。Note : * two tailed correlation to P < 0.05 significant level, * * two tailed correlation to P < 0.01 significant level. | ||||||||||
相关分析表明,土壤NO3 --N与DON之间存在极显著正相关(P < 0.01),与MBN存在极显著负相关(P < 0.01)。与DON和MBN相对应的可溶性有机碳(dissolved organic carbon, DOC)和微生物量碳(microbial biomass carbon, MBC)可同时表征土壤状况,对碳输入的改变具有敏感响应。土壤DOC与NO3 --N 、NH4 +-N分别具有显著的负相关和极显著的正相关,DON与MBN之间也呈极显著负相关关系(P < 0.01)。NH4 +-N与NO3 --N 、DON 、MBN均之间相关性均不显著。土壤pH与NO3 --N 、DON均存在极显著负相关(P < 0.01),与MBN存在极显著正相关(P < 0.01)。
3 结论与讨论 3.1 滨海沙地不同人工林土壤矿质氮特征3种人工林对照组的土壤矿质氮含量范围为2.91-4.49 mg · kg-1,与陈书信等[7]对中国滨海沙地土壤的研究结果相近,但远低于内陆森林土壤(北京九龙山棕壤[8] 、福建九龙岭赤红壤[9] 、福建中部山地红壤[10])。滨海沙地土壤养分贫瘠,可参与矿化作用的底物较少,同时土壤砂粒含量大,难以形成团粒结构,导致土壤渗透性强,保水能力弱,并且滨海地区降水丰富,土壤NO3 --N在这种环境下极易被淋溶而损失。气候和土壤质地可能是造成滨海沙地土壤矿质氮含量远低于内陆森林土壤的主要原因。
林分组成是决定土壤氮素组分的重要因素,对照组尾巨桉、纹荚相思、木麻黄土壤NO3 --N含量占矿质氮含量比重分别为17% 、62% 、44%,该比值是土壤矿化作用输入、硝化与反硝化作用、植物根系吸收、硝态氮淋溶损失等综合作用的结果,在一定程度上反映了土壤硝化作用的强弱。通气状况良好的土壤有利于硝化作用的进行,NO3 --N可能成为植物吸收的主要氮源[11]。尾巨桉是速生树种,对土壤速效养分的需求量大,可能是导致其土壤NO3 --N含量显著低于纹荚相思和木麻黄的主要原因。
3.2 切断根系处理对土壤矿质氮的影响土壤中的矿质氮是有机质矿化作用的产物,又通过硝化作用、反硝化作用、动植物和微生物吸收利用、淋溶损失等途径从土壤中输出,其输入、输出速率和氮素形态之间的相互转换决定了土壤中矿质氮的含量。切断根系处理后3种人工林土壤矿质氮含量均高于对照,其中土壤NO3 --N含量的贡献大于NH4 +-N,且切断根系显著提高了土壤NO3 --N在矿质氮中的比重。这与ROSS et al[12]对19年生杉木林做切断根系处理后得出的结果相似。通常,根系分泌的酚类物质和有机酸能够抑制硝化作用的进行,切断根系后解除了该抑制,硝化作用增强;同时,根系是植物吸收氮的主要器官,切断根系后阻断了土壤NO3 --N在根系上的输出;当植物吸收氮的途径被切断后,土壤微生物会产生过量的NH4 +和NO3 -[13]。但同时根系分泌的有机物质和根凋落物容易被微生物利用矿化成矿质氮,是土壤矿质氮的来源之一,这一来源仅占土壤中氮的1%-2%[14]。因此,由植物根系引起的矿质氮输出大于由根系输入的矿质氮来源是切断根系后土壤矿质氮含量高于对照的主要原因。
3.3 去除凋落物处理对土壤矿质氮的影响凋落物是生态系统中土壤氮素的重要输入,是调控土壤氮素平衡的重要途径,能够决定土壤有机质氮库的大小。有关去除凋落物对土壤矿质氮的影响研究表明:森林凋落物中含有的水溶性物质和碳水化合物可以作为土壤矿物层氮素的源和库,凋落物可以促进氮矿化和提高硝化速率[15]。但也有研究表明凋落物对土壤氮素无显著影响[3]。本研究结果显示,不同树种土壤矿质氮含量对去除凋落物的响应不同,去除凋落物处理后纹荚相思和木麻黄人工林土壤矿质氮含量高于对照,但去除凋落物后尾巨桉土壤NH4 +-N含量显著降低,从而降低了尾巨桉土壤矿质氮含量。这与马红亮等[16]研究结果相似。凋落物是土壤矿质氮的重要来源,去除凋落物后土壤NH4 +-N含量降低可能与失去来自凋落物中的氮源有关。但同时,由于不同树种凋落物的质和量不同导致其分解速率不同,所分解得到的氮素成分与含量存在差异,导致不同树种对去除凋落物处理的响应不一致。此外,日益严重的大气氮沉降所增加的外源氮可能掩盖由去除凋落物所损失的那部分氮,干扰了处理对氮素的影响。去除凋落物后3种人工林土壤NO3 --N在矿质氮中的比重均升高,表明硝化作用增强。通气状况良好的土壤有利于硝化作用的进行。去除凋落物后增加了表层土壤与大气的接触,能够为硝化作用提供充足的氧气,可能是导致土壤硝化作用增强的原因。
3.4 土壤DON与MBN在土壤氮素循环中的作用去除凋落物和切断根系后尾巨桉和纹荚相思人工林土壤MBN含量均显著低于对照组,这与SAYER et al[17] 、LI et al[18]的研究结果一致。微生物是土壤养分转化与循环的驱动力,其数量和活跃程度与土壤中的有机碳密切相关,切断根系和去除凋落物限制了地上、地下有机碳的输入,可能是导致这一结果的主要原因。土壤DON含量对切断根系和去除凋落物的响应与MBN相反。土壤DON可直接或转化后被植物根系吸收,切断根系处理后原先预被根系吸收的那部分DON在土壤中积累导致其含量升高。这可能是切断根系后3种人工林土壤DON含量均高于对照的原因。同时,DON具有很强的移动性,易发生径流或淋溶损失,去除凋落物后表层土壤直接被雨水冲刷,易导致DON的损失,但本试验结果表明,去除凋落物后尾巨桉和纹荚相思土壤DON含量均高于对照,这可能与凋落物在被微生物分解过程中需要以DON为底物有关。凋落物一方面通过在其分解过程中消耗DON,一方面通过覆盖地表保护DON不受淋溶损失,是综合作用的结果。
3.5 土壤碳氮各组分之间的相关性土壤氮素的固定、转化与损失与土壤微生物的数量和活性密切相关,而土壤微生物量碳、氮可以反映土壤微生物的数量,有研究表明,土壤矿质氮主要来自于微生物对氮的释放[19],土壤微生物量碳氮之间、微生物量氮与土壤矿质氮具有正相关关系[20],但本研究相关分析表明,土壤MBN与NO3 --N含量极显著负相关(P < 0.01),这与以往的研究结果相反,土壤中反硝化微生物能够将NO3 --N还原成N2O和N2,造成土壤氮素损失,可能是MBN与NO3 --N存在极显著负相关的原因之一,同时,土壤pH值与NO3 --N极显著负相关,与MBN极显著正相关,该地区酸性土壤能够抑制硝化作用的进行,而反硝化作用在pH值为3.5-11.2的环境中均可进行,因此,在反硝化微生物作用下NO3 --N被还原成N2O和N2而损失。土壤DOC与NO3 --N和NH4 +-N均具有显著的相关性,说明对土壤中不同方式的碳源输入可能通过改变土壤中的碳素成分或含量来影响矿质态氮含量,土壤矿质态氮含量的变化受到DOC的控制。
| [1] | KAYE J P, BINKLEY D, RHOADES C. Stable soil nitrogen accumulation and flexible organic matter stoichiometry during primary floodplain succession[J]. Biogeochemistry, 2003, 63(1): 1–22. |
| [2] | NADELHOFFER K J, BOONE R D, BOWDEN R D, et al. The DIRT experiment:litter and root influences on forest soil organic matter stocks and function[M]//FOSTER D R, ABER J D. Forests in Time:the Environmental Consequences of 1000 Years of Change in New England. New Haven:Yale University Press, 2004:300-315. |
| [3] | HOLUB S M, LAJTHA K, SPEARS J D H, et al. Organic matter manipulations have little effect on gross and net nitrogen transformations in two temperate forest mineral soils in the USA and central Europe[J]. Forest Ecology and Management, 2005, 214(1/2/3): 320–330. |
| [4] | 张彪, 高人, 杨玉盛, 等. 万木林自然保护区不同林分土壤可溶性有机氮含量[J]. 应用生态学报, 2010, 21(7): 1635–1640. |
| [5] | HUANG Z Q, WAN X H, HE Z M, et al. Soil microbial biomass, community composition and soil nitrogen cycling in relation to tree species in subtropical China[J]. Soil Biology and Biochemistry, 2013, 62(5): 68–75. |
| [6] | CURTIN D, WRIGHT C E, BEARE M H, et al. Hot water-extractable nitrogen as an indicator of soil nitrogen availability[J]. Soil Science Society of America Journal, 2006, 70(5): 1512–1521. |
| [7] | 陈书信, 王国兵, 阮宏华, 等. 苏北沿海不同土地利用方式冬季土壤氮矿化速率比较[J]. 南京林业大学学报(自然科学版), 2014, 38(1): 41–46. |
| [8] | 张连金, 赖光辉, 孙长忠, 等. 北京九龙山土壤质量综合评价[J]. 森林与环境学报, 2016, 36(1): 22–29. |
| [9] | 王纪杰, 王炳南, 李宝福, 等. 不同林龄巨尾桉人工林土壤养分变化[J]. 森林与环境学报, 2016, 36(1): 8–14. |
| [10] | 陈爱玲, 林德喜, 张国防, 等. 杉木施肥17年后土壤养分的变化[J]. 福建林学院学报, 2000, 20(3): 265–268. |
| [11] | 霍常富, 孙海龙, 范志强, 等. 根系氮吸收过程及其主要调节因子[J]. 应用生态学报, 2007, 18(6): 1356–1364. |
| [12] | ROSS D J, SCOTT N A, TATE K R, et al. Root effects on soil carbon and nitrogen cycling in a Pinus radiata D. Don plantation on a coastal sand[J]. Australian Journal of Soil Research, 2001, 39(5): 1027–1039. |
| [13] | DAHLGREN R A, DRISCOLL C T. The effects of whole-tree clear-cutting on soil processes at the Hubbard Brook experimental forest, New Hampshire, USA[J]. Plant and Soil, 1994, 158(2): 239–262. |
| [14] | USELMAN S M, QUALLS R G, THOMAS R B. A test of a potential short cut in the nitrogen cycle:the role of exudation of symbiotically fixed nitrogen from the roots of a N-fixing tree and the effects of increased atmospheric CO2 and temperature[J]. Plant and Soil, 1999, 210(1): 21–32. |
| [15] | TAN X, CHANG S X. Soil compaction and forest litter amendment affect carbon and net nitrogen mineralization in a boreal forest soil[J]. Soil and Tillage Research, 2007, 93(1): 77–86. |
| [16] | 马红亮, 闫聪微, 高人, 等. 林下凋落物去除与施氮对针叶林和阔叶林土壤氮的影响[J]. 环境科学研究, 2013, 26(12): 1316–1324. |
| [17] | SAYER E J, HEARD M S, GRANT H K, et al. Soil carbon release enhanced by increased tropical forest litterfall[J]. Nature Climate Change, 2011, 1(6): 304–307. |
| [18] | LI Y Q, XU M, ZOU X M, et al. Soil CO2 efflux and fungal and bacterial biomass in a plantation and a secondary forest in wet tropics in Puerto Rico[J]. Plant and Soil, 2005, 268(1): 151–160. |
| [19] | BONDE T A, SCHNVRER J, ROSSWALL T. Microbial biomass as a fraction of potentially mineralizable nitrogen in soils from long-term field experiments[J]. Soil Biology and Biochemistry, 1988, 20(4): 447–452. |
| [20] | 王淑平, 周广胜, 孙长占, 等. 土壤微生物量氮的动态及其生物有效性研究[J]. 植物营养与肥料学报, 2003, 9(1): 87–90. |

 2016, Vol. 36
2016, Vol. 36


