恢复沉水植物是水生态修复的关键环节,影响沉水植物生长的因素都可能影响生态修复的成败[1]。在诸多影响因素中,除草剂和重金属的影响尤为突出。随着工农业发展和排入环境的污染物种类增多,复合污染问题越来越突出,其中重金属-农药的复合污染在农村水体中较为常见[2]。
草甘膦是一种有机磷除草剂,效果好、使用范围广。但草甘膦的大量和不科学使用,使其未能作用于植物就随水循环进入水体。朱国念等[3]研究表明草甘膦进入水体后,会首先向沉水植物体内迁移并在细胞内累积,影响植物萌发与生长。含Cu2+杀菌剂的使用、工业废水的排放使水体Cu2+含量较20世纪有所上升。Cu2+具有难降解性、生物累积性,严重影响人类健康及生态环境[4]。Cu2+是沉水植物生长必需微量元素,利用沉水植物可修复低浓度Cu2+污染,但Cu2+浓度过高会对其生长产生抑制甚至导致枯萎死亡[5]。目前已有学者开始关注草甘膦与Cu2+复合污染的危害,李培林[6]发现Cu2+与草甘膦毒性有加和作用,复合污染中菱形藻生物量明显低于单一污染。LIU等[7]研究了草甘膦与Cu2+的共同污染对水生生态环境的危害,发现高浓度复合污染对槐叶萍有协同作用,加剧了Cu2+和草甘膦在水中的毒性。
狐尾藻(Myriophyllum verticillatum L.)是水体初级生产者之一,也是生态修复工程中常用的沉水植物,能预防与修复富营养化水体[8]。在修复工程中需定期收割维护以减轻水体生物量负荷过大和自然死亡腐烂带来的二次污染。因此,收割植物的资源化利用也一直倍受关注。
生物炭是由生物有机质制成的稳定的多孔固体,因其价格低、二次污染小等特点在环保领域被广泛利用,在水体治理方面主要用来吸附水体中N、P营养盐和重金属、有机物等污染物。目前植物生物碳的研究包括农业废弃物、林业废弃物和水生植物残体,对于水生植物的研究主要集中在美人蕉和芦苇等挺水植物基生物炭[9],而对沉水植物生物炭的研究较少,特别是使用其去除水体Cu2+和草甘膦单一及复合污染鲜见报道。本文使用收割的狐尾藻植株废弃物制成生物炭,研究吸附法去除水中草甘膦和Cu2+污染,结果可为生态修复条件改善和废弃物资源化利用提供参考。
1 材料与方法 1.1 实验材料及药品狐尾藻(Myriophyllum verticillatum)来源于上海海洋大学金山基地。将预处理制得的过60目筛的狐尾藻粉置于马弗炉中,按5 ℃/min的速率升温至450 ℃炭化2 h。冷却后研磨过100目标准筛,密封保存。所得狐尾藻基生物炭记为HW450。
使用草甘膦试剂(德国,DR.E)配制1 000 mg/L草甘膦储备液。使用分析纯CuCl2·2H2O(国药集团)配制1 000 mg/L Cu2+储备液。
1.2 实验方法 1.2.1 单一污染吸附实验取100 mL一定浓度的草甘膦或Cu2+单一污染试液于聚乙烯瓶中,加适量HW450,调节pH,在25 ℃、180 r/min条件下于恒温摇床中振荡一定时间后,取2 mL试液,用0.22 μm针头滤膜过滤稀释后测定草甘膦或Cu2+浓度。选择吸附时间、初始浓度、pH和生物炭投加量为单因素变量,分别研究其对HW450吸附草甘膦或Cu2+效果的影响,每组实验3个平行。
1.2.2 复合污染吸附实验设置5、25、50、75 mg/L 4个草甘膦(Cu2+)浓度组,每组分别添加0、1、5、25、50 mg/L Cu2+(草甘膦),调节pH为5,以保证Cu2+和草甘膦的较大去除率。100 mL复合污染试液和0.05 g HW450混合后置于聚乙烯瓶中,在25 ℃、180 r/min条件下于恒温摇床中振荡48 h,取2 mL试液,用0.22 μm针头滤膜过滤稀释后测定草甘膦(或Cu2+)浓度。
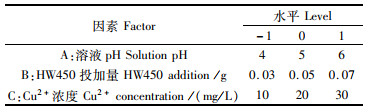
1.2.3 响应面优化吸附条件实验根据前期单一污染吸附实验及复合污染影响实验结果,选取对草甘膦及Cu2+去除率均影响显著的pH、HW450投加量、Cu2+浓度为影响因子,记为因素A、B、C,草甘膦去除率和Cu2+去除率为响应值,记为Y1和Y2。按照Box-Behnken实验方法设计3因素3水平实验,如表 1。控制混合溶液体积为100 mL,草甘膦浓度为25 mg/L,在25 ℃、180 r/min条件下于恒温摇床中振荡48 h,取2 mL试液,用0.22 μm针头滤膜过滤稀释后测定草甘膦(或Cu2+)浓度。
|
表 1 实验因素与水平表 Tab.1 Factors and levels of experiment |
草甘膦准确浓度参照《水质草甘膦的测定高效液相色谱法(征求意见稿)》测定(日本,岛津)。Cu2+准确浓度用石墨炉原子吸收光谱法测定(北京,普析通用)。
1.4 数据处理污染物去除率(η)和生物炭吸附量(Q)可用来描述吸附效果,计算如下:
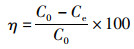 (1)
(1)
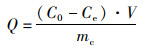 (2)
(2)
式中:η为污染物去除率,%;Q为生物炭吸附量,mg/g;C0为吸附前污染物浓度,mg/L;Ce为吸附平衡时污染物浓度,mg/L;V为溶液体积,L;mc为加入生物炭质量,g。
使用SPSS、Origin 9、Design Expert 8.05处理数据、绘制曲线、响应面拟合及方差分析。
2 结果与分析 2.1 单一污染物吸附效果的单因素影响 2.1.1 吸附时间的影响在0~48 h内HW450对草甘膦或Cu2+的吸附去除率随时间变化如图 1所示,48 h Cu2+去除率为100%,草甘膦去除率为85.35%。可分成快速吸附阶段、缓慢吸附阶段和吸附平衡阶段。HW450对Cu2+的快速吸附阶段历时短、速率快,30 min内去除率达87%;缓慢吸附阶段较短;约6 h达到吸附平衡,去除率为100%。HW450对草甘膦的快速吸附阶段约为1 h,吸附速率低于HW450对Cu2+的快速吸附;但缓慢吸附阶段较长,直到36 h才基本平衡。

|
图 1 吸附时间对去除率的影响 Fig. 1 Effect of time on removal rate |
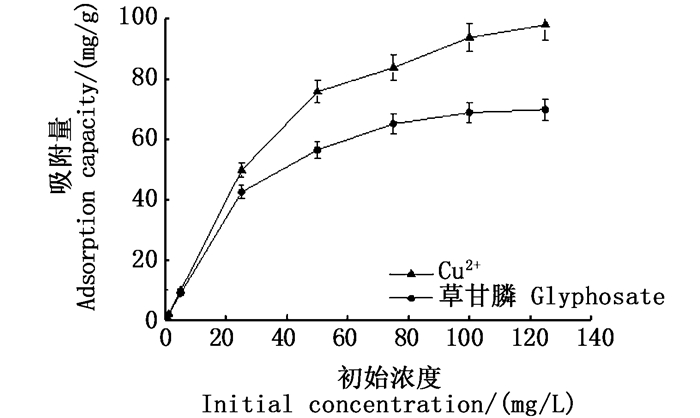
HW450对两污染物吸附量受初始浓度变化影响显著(P < 0.05),如图 2所示,生物炭的吸附量均随初始浓度增加而增加。其中Cu2+吸附量变化表现为增速先快后慢;对草甘膦的吸附低浓度增速较快,高浓度(>100 mg/L)后生物炭吸附量逐渐稳定,生物炭的活性位点达到吸附饱和状态。HW450对Cu2+和草甘膦的最大吸附量分别为98.16和70.04 mg/g。
|
图 2 污染物初始浓度对吸附量的影响 Fig. 2 Effect of initial pollutant concentration on adsorption capacity |
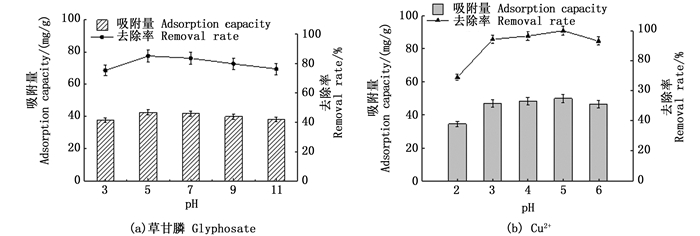
如图 3所示,由于Cu2+在pH > 7时会生成Cu(OH)2沉淀,因此Cu2+溶液pH范围为2~6,草甘膦溶液pH范围为3~11。可以看出,Cu2+吸附效果受pH变化影响较大(P < 0.01)。随着pH值增大,生物炭吸附量及Cu2+去除率均呈现先增大后减小的趋势,pH=5时吸附效果最好,此时Cu2+去除率为100%、HW450吸附量为50 mg/g。随着pH增大,草甘膦生物炭吸附量及去除率先增加后减小,但变化幅度较Cu2+小(P < 0.05),pH=5时草甘膦去除率为85.35%、HW450吸附量为42.68 mg/g,去除效果最优。
|
图 3 pH对吸附效果的影响 Fig. 3 Effect of pH on adsorption |
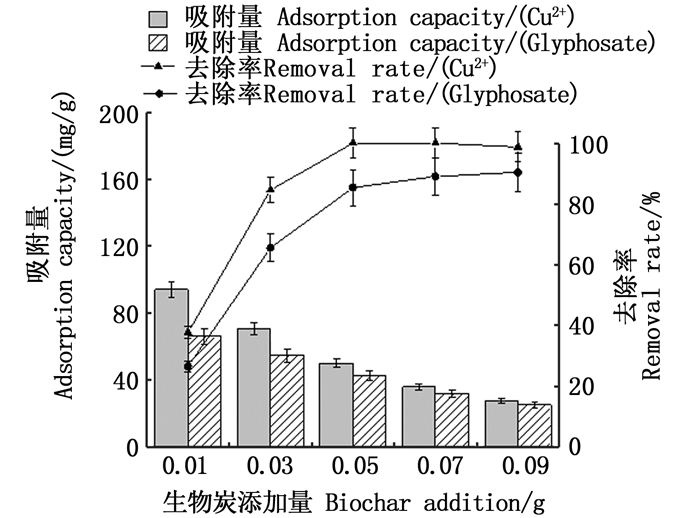
如图 4所示,随着投加量增加,草甘膦和Cu2+的去除率先明显增加,而后增加变缓,最后趋于稳定(P < 0.05)。HW450投加量为0.05 g时,Cu2+去除率已达100%,草甘膦去除率增加变缓;投加量0.09 g时,草甘膦去除率为90.4%。HW450吸附量则表现为随生物炭添加量的增加而降低,且降低速率渐小,最后趋于稳定。
|
图 4 生物炭投加量对吸附效果的影响 Fig. 4 Effect of biochar dosage on adsorption |
图 5a为复合污染体系中Cu2+浓度对草甘膦去除率的影响,Cu2+浓度对复合水体中草甘膦去除率的影响显著(P < 0.05),Cu2+对去除草甘膦有一定促进作用,草甘膦去除率随Cu2+浓度增加而增大。图 5b为草甘膦浓度对Cu2+去除率的影响,草甘膦浓度对复合水体中Cu2+去除率的影响显著性较差(P>0.05),高浓度的草甘膦对低浓度的Cu2+去除率有轻微抑制作用,但高浓度的Cu2+受草甘膦影响较小。

|
图 5 草甘膦和Cu2+的相互影响 Fig. 5 The interaction between glyphosate and Cu2+ |
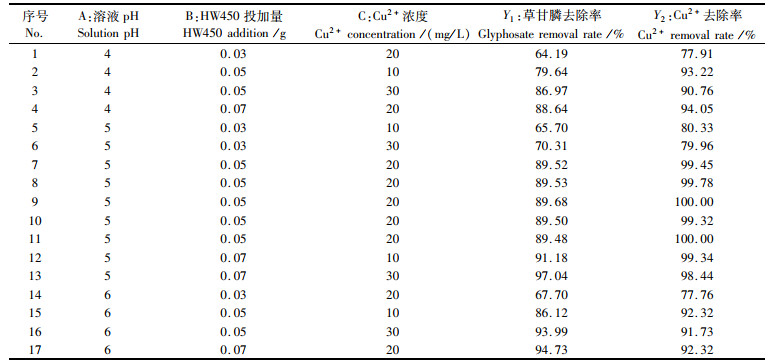
响应面优化吸附条件实验结果如表 2所示。
|
表 2 响应面设计及结果 Tab.2 Response surface design and results |
运用Design Expert 8.05软件对实验结果进行分析,得出三个影响因子的多元回归方程(公式3和公式4):
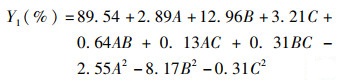 (3)
(3)
 (4)
(4)
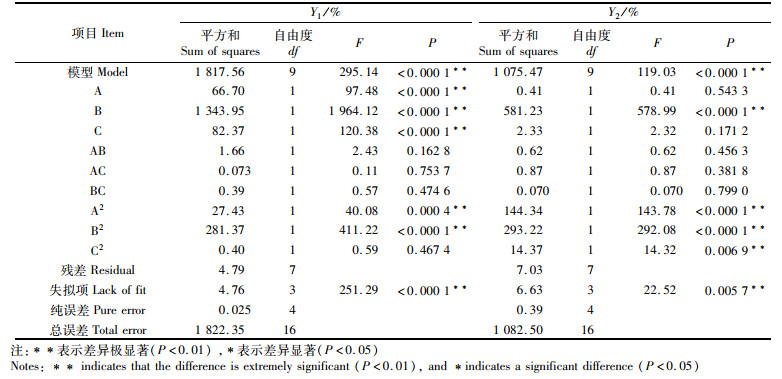
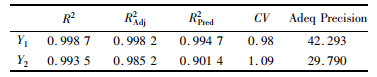
为检验拟合模型的合理性,对其进行统计分析。表 3和表 4分别为响应面的方差分析和可行度分析。在对Y1草甘膦去除率和Y2 Cu2+去除率的响应面分析中,模型的F值分别为295.14、119.03,P值都小于0.000 1,说明两个模型都具有良好的显著性。相关系数R2为0.998 7、0.993 5,调整相关系数RAdj2为0.998 2、0.985 2,均接近1,表明模型中99.87%的Y1响应变化和99.35%的Y2响应变化可以被解释,99.82%和98.52%的调整在模型中可以分别被解释,说明模型稳定性好,并且各因素和应变量间相关性高。Y1和Y2模型精密度分别为42.293、29.790,远大于4,表明两模型数据精密度较高。变异系数分别为0.98%、1.09%,远小于30%,表明变异数据少。综合来看,该响应面拟合能很好的反应各因素的变化对结果的影响,并对条件进行最优化预测。
|
表 3 方差分析 Tab.3 Variance analysis |
|
表 4 可信度分析 Tab.4 Credibility analysis |
表 3中的A、B、C项F值表明三个因素对响应值变化的影响程度大小。三因素对Y1草甘膦去除率和Y2 Cu2+去除率影响大小排序相同,均为B:HW450投加量>C:Cu2+浓度>A:pH。
固定一个因素为中间值不变,剩余两个因素的响应面分析图如图 6所示。

|
图 6 响应面分析图 Fig. 6 Response surface analysis diagram |
从图 6中可以看出,在拟合范围内,草甘膦的去除率随着HW450投加量增加先快速增长后逐渐平稳,该因素影响较大;随着pH增加有小幅度的先增后减趋势;随Cu2+浓度增长而缓慢增加。从等高线来看,在实验范围内HW450投加量对草甘膦的去除率最显著。Cu2+的去除率随着HW450投加量明显增加,在pH同时为中值时可取最值点;pH在范围内增加使得去除率先增后减;在10~30 mg/L的浓度范围内对Cu2+的去除率影响较小。从等高线可以看出,对于Cu2+去除率来说,HW450和pH的交互性显著;pH和Cu2+浓度则交互性较差,两者交互对Cu2+去除率影响小。
2.3.4 响应面优化吸附条件验证使用模型拟合分析后得出,当pH为5.21,HW450投加量为0.06 g,Cu2+浓度为27.23 mg/L时,可以得到草甘膦最大去除率为97.44%,Cu2+最大去除率100%。为验证拟合模型的可靠度及准确度,使用拟合最优条件进行验证实验。设置3组平行,测量实验结束后的草甘膦及Cu2+去除率。实验结果如表 5所示,3组实验中草甘膦和Cu2+的实际去除率与优化预测值相差不大,说明结果与实际相符。在3组实验中草甘膦和Cu2+去除率均在95%以上,表明在该条件下草甘膦和Cu2+复合污染水体的修复效果较好。

|
表 5 优化吸附条件验证 Tab.5 Verification of optimized adsorption conditions |
本实验中草甘膦和Cu2+的去除率增速先快后慢,实验初期生物炭活性位点较多,因此高浓度的污染物可以迅速吸附[10]。随着时间推移生物炭表面位点减少,溶液浓度降低,吸附速度变缓。当生物炭达到该条件下最大吸附量时,吸附达到平衡状态。
初始浓度增加导致吸附量增加,主要是因为高浓度的污染物液体使得溶液中固液驱动增强,污染物与生物炭的运动增多,导致草甘膦分子或Cu2+与生物炭的有效碰撞次数增加,更有利于生物炭表面活性位点与生物炭的结合[11]。当吸附位点饱和后,则污染物不再吸附,浓度变化不再引起吸附量的变化。本实验中HW450对Cu2+和草甘膦最大吸附量分别为98.16和70.04 mg/g,Cu2+比草甘膦更容易吸附去除。
溶液初始pH能影响污染物溶解度、生物炭表面电荷[12],是影响吸附效果的重要因素,影响程度与生物炭性质及吸附污染物有关。当pH过小时,H+和Cu2+存在竞争关系,且大量H+使生物炭质子化程度提高,表面带正电[13],与Cu2+发生静电斥力,吸附量较低。随着pH增加,生物炭表面正电荷减少,H+和Cu2+竞争减弱,更容易产生吸附[14]。有研究表明草甘膦在溶液中一般从pH 4.5开始带负电[11, 15],因此在pH < 4.5及pH>7区间内,草甘膦带电电荷分别为正电荷及负电荷与H+及OH-相同,因此存在竞争离子及静电斥力,吸附效果较差。实验最优pH为5,处于4.5~7区间,符合理论结果。但江鲜英[16]发现在pH=4时改性棕榈生物炭对草甘膦吸附最大,可能是化学药品造成生物炭表面官能团变化影响反应进行。
生物炭投加量的增加使得草甘膦和Cu2+的去除率增加是因为溶液浓度相同时,生物炭的投入增加了系统内吸附剂活性位点的总量[17],促进更多的草甘膦或Cu2+吸附。但当投加量多于一定值时,去除率增加变缓或不变,一方面是因为生物炭过量容易互相影响、叠加遮蔽了部分有效孔隙和位点[18],另一方面是系统内的吸附质已全部去除。由于溶液浓度不变,生物炭投加量增加,因此生物炭的吸附量与溶液污染物的去除率变化相反。在实际应用中,考虑到经济性、节能等因素,生物炭的投加量应根据污染物的性质跟浓度,适量添加。
3.2 HW450对复合吸附系统中草甘膦及Cu2+吸附从HW450吸附草甘膦和Cu2+单一污染可以看出,与草甘膦相比,HW450对Cu2+的吸附速率更快、吸附量更大。Cu2+浓度对草甘膦污染去除的促进作用可能是HW450对Cu2+的吸附性能比草甘膦更强,因此Cu2+更容易优先吸附,草甘膦容易跟二价金属离子形成络合物,在生物炭表面表现为生物炭—Cu2+—草甘膦结构,Cu2+起到了“纽带”作用[16]。JULIA等[19]发现铜和草甘膦在水针铁矿表面会形成三元表面复合物,复合物的量主要由Cu2+含量决定,这与本实验结果一致。草甘膦对HW450吸附Cu2+影响较小,只有在Cu2+低浓度时高浓度的草甘膦会产生抑制作用,因为溶液中的草甘膦浓度过高,会与Cu2+竞争吸附位点。陈鑫等[20]发现Cu2+和氧氟沙星复合体系中,低浓度的Cu2+能促进氧氟沙星吸附,而高浓度导致其饱和吸附量降低,该结果与本实验结果相似,进一步验证了在金属离子与其他物质的复合污染中,金属离子更易被生物炭吸附。
目前响应面分析法在生物炭方面的应用集中于生物炭的制备及改性[21-22],生物炭吸附污染物方面响应面法仅有少量研究,多以单因素实验和正交实验确定最优吸附条件,如汤嘉雯等[23]用正交法确定Cd2+最优去除条件。正交实验的最优条件局限于实验方案的具体取值,而响应面分析法能够在合适范围内使用数据建立回归方程,拟合最优结果[23]。本实验由单因素对单一污染吸附效果的影响以及复合污染体系中草甘膦和Cu2+的相互影响确定pH、HW450投加量、Cu2+浓度三因素对两种污染物去除率均有显著影响,使用响应面拟合后确定最优吸附条件为pH=5.21、HW450投加量=0.06 g、Cu2+浓度=27.23 mg/L,且模型准确性好,拟合结果与实际吸附结果差异小。该结果对于草甘膦及Cu2+复合体系染污物的去除有一定参考作用。
3.3 HW450的应用意义狐尾藻废弃物来源于沉水植物收割,价格低廉、分布广,在450 ℃下炭化2 h后制成的生物炭性能优异。崔孝强[24]使用美人蕉、芦苇等22种湿地植物在500 ℃下制备生物炭,果木等林业废弃物所需炭化温度更高、炭化时间更长,与其相比狐尾藻生物炭制备耗能低。通过超声法、微波法等生物炭可以再生利用,胡晓虹[25]发现再生5次的竹炭对Cu2+的去除率高达92.4%,仅比首次使用降低约6%。由此可见生物炭循环利用率高,能降低生产成本。
HW450因其吸附性能优异、成本低、绿色环保的特点,可用于水污染处理。首先工业含铜废水、农田退水、养殖废水等,可以将污染水体集中收集,通过改变生物炭投加量、水体pH等达到最优吸附条件,高效去除草甘膦、Cu2+污染,最终达标排放或者水体循环利用,使用的HW450也能够收集处理再利用[26]。HW450也可用于自然水体的草甘膦、Cu2+吸附,相较污水集中处理而言,自然水体的限制因素更多,在处理过程中可以调节可控因素如投加量、吸附时间,借助水体pH的自然变化规律等,以达到最优去除效果。此外天然水体使用中,可以采用制粒、磁改性等手段以增加生物炭回收率。
综上所述,使用废弃狐尾藻制作生物炭,既能协助生态修复系统的维护管理,又能有效利用沉水植物废弃物资源,变废为宝,具有一定应用价值。研究其对草甘膦及Cu2+的吸附,能去除沉水植物生长胁迫因素,对水污染处理有一定参考作用。
4 结论(1) 狐尾藻基生物炭对草甘膦或Cu2+的吸附效果受多因素影响,其中包括吸附时间、初始污染物浓度、溶液pH和HW450投加量。
(2) 在草甘膦与Cu2+混合系统中,草甘膦的浓度对Cu2+污染物去除率影响较小,但Cu2+能在一定程度上促进草甘膦被吸附。响应面拟合得出最优吸附条件为pH=5.21、HW450投加量=0.06 g、Cu2+浓度=27.23 mg/L,该条件复合污染水体中草甘膦去除率为97.44%,Cu2+为100%。
| [1] |
卓帅, 何文辉, 彭自然, 等. 椭圆萝卜螺对3种沉水植物的牧食特性实验[J]. 上海海洋大学学报, 2020, 29(3): 339-345. ZHUO S, HE W H, PENG Z R, et al. Experimental study on the grazing characteristics of three kinds of submerged plants for Radix swinhoei(H. Adams)[J]. Journal of Shanghai Ocean University, 2020, 29(3): 339-345. |
| [2] |
周垂帆.重金属和草甘膦复合污染生态毒理研究[D].南京: 南京林业大学, 2013. ZHOU C F. Study of the ecology toxic effects of single and combined pollution between heavy metal and glyphosate[D]. Nanjing: Nanjing Forestry University, 2013. |
| [3] |
朱国念, 郭江峰, 孙锦荷. 应用14C核素研究草甘膦在水域生态系中的迁移、生物富集与消失动态[J]. 核农学报, 2002, 16(3): 185-190. ZHU G N, GUO J F, SUN J H. Studies on transfer, bioaccumulation and disappearance of glyphosate in the aquatic ecosystem by utilizing 14C tracer technique[J]. Journal of Nuclear Agricultural Sciences, 2002, 16(3): 185-190. |
| [4] |
HU B F, SHAO S, FU Z Y, et al. Identifying heavy metal pollution hot spots in soil-rice systems:A case study in South of Yangtze River Delta, China[J]. Science of the Total Environment, 2019, 656: 614-625. |
| [5] |
陈璐, 李威, 王敏, 等. 刺苦草对铜胁迫的耐受性及其恢复能力研究[J]. 水生态学杂志, 2018, 39(5): 104-110. CHEN L, LI W, WANG M, et al. Tolerance and recovery capability of Vallisneria spinulosa exposed to copper[J]. Journal of Hydroecology, 2018, 39(5): 104-110. |
| [6] |
李培林.草甘膦与Cu2+对菱形藻的单一与复合胁迫研究[D].贵阳: 贵州师范大学, 2016. LI P L. Study of toxic effects of singleand combined pollution of glyphosate and Cu2+ to Nizschiapalea[D].Guiyang: Guizhou Normal University, 2016. |
| [7] |
LIU N, ZHONG G D, ZHOU J N, et al. Separate and combined effects of glyphosate and copper on growth and antioxidative enzymes in Salvinianatans(L.) All[J]. Science of the Total Environment, 2019, 655: 1448-1456. DOI:10.1016/j.scitotenv.2018.11.213 |
| [8] |
张晓姣, 朱金格, 刘鑫. 浅水湖泊沉水植物调控技术研究进展[J]. 净水技术, 2018, 37(12): 46-51. ZHANG X J, ZHU J G, LIU X. Research development in controlling technology for submerged aquatic plants in shallow lakes[J]. Water Purification Technology, 2018, 37(12): 46-51. |
| [9] |
何琦.挺水植物基生物炭去除硫丹的效果与机理研究[D].北京: 中国环境科学研究院, 2018. HE Q. Removal mechanism of endosulfan by biochars derived from emergent plants[D]. Beijing: Chinese Research Academy of Environmental Sciences, 2018. |
| [10] |
程扬, 沈启斌, 刘子丹, 等. 两种生物炭的制备及其对水溶液中四环素去除的影响因素[J]. 环境科学, 2019, 40(3): 1328-1336. CHENG Y, SHEN Q B, LIU Z D, et al. Preparation of two kinds of biochar and its influencing factors on tetracycline removal from aqueous solution[J]. Environmental Science, 2019, 40(3): 1328-1336. |
| [11] |
HERATH G A D, PÖH L S, NG W J. Statistical optimization of glyphosate adsorption by biochar and activated carbon with response surface methodology[J]. Chemosphere, 2019, 227: 533-540. DOI:10.1016/j.chemosphere.2019.04.078 |
| [12] |
LIU J W, JIANG J G, MENG Y, et al. Preparation, environmental application and prospect of biochar-supported metal nanoparticles:A review[J]. Journal of Hazardous Materials, 2020, 388: 1-22. |
| [13] |
林美珊, 陈玉, 陈婷. 稻壳灰对水体中Cu2+的吸附性能[J]. 武汉工程大学学报, 2020, 42(1): 38-44. LIN M S, CHEN Y, CHEN T. Adsorptive performance and mechanism of Cu2+ on rice husk ash[J]. Journal of Wuhan Institute of Technology, 2020, 42(1): 38-44. |
| [14] |
左海强, 刘艳, 张彦博, 等. 稻壳灰吸附剂对重金属铜离子的吸附性能研究[J]. 工业用水与废水, 2012, 43(4): 58-61. ZUO H Q, LIU Y, ZHANG Y B, et al. Adsorption capability of rice husk ash adsorbent on Cu2+[J]. Industrial Water & Wastewater, 2012, 43(4): 58-61. |
| [15] |
崔凯飞. NH2-MIL-101(Fe)对草甘膦的吸附机理及其复合物的光催化性能研究[D].郑州: 郑州大学, 2019. CUI K F. Study on adsorption mechanism of glyphosate on NH2-MIL-101(Fe) and photocatalytic performance of its complexes[D]. Zhengzhou: Zhengzhou University, 2019. |
| [16] |
江鲜英.改性生物炭对草甘膦和磺胺二甲基嘧啶的去除[D].广州: 华南理工大学, 2018. JIANG X Y. Removal of glyphosate and sulfamethazine by modified biochar[D]. Guangzhou: South China University of Technology, 2018. |
| [17] |
仝海娟, 左卫元, 史兵方, 等. 柚子皮生物炭的制备及对水体中锰离子的吸附[J]. 工业安全与环保, 2016, 42(11): 53-56. TONG H J, ZUO W Y, SHI B F, et al. Biochar prepared by the pomelopeel and its sorption ability for manganese(Ⅱ) in water[J]. Industrial Safety and Environmental Protection, 2016, 42(11): 53-56. |
| [18] |
肖乃傲.生物炭对水中邻苯二甲酸二甲酯的吸附研究[D].天津: 天津理工大学, 2019. XIAO N A. Adsorption of dimethyl phthalate in water by bio-char[D]. Tianjin: Tianjin University of Technology, 2019. |
| [19] |
SHEALS J, GRANSTRÖM M, SJÖBERG S, et al. Coadsorption of Cu(Ⅱ) and glyphosate at the water-goethite (α-FeOOH) interface:molecular structures from FTIR and EXAFS measurements[J]. Journal of Colloid and Interface Science, 2003, 262(1): 38-47. DOI:10.1016/S0021-9797(03)00207-8 |
| [20] |
陈鑫, 魏志远, 赵翰斌, 等. 紫根水葫芦基活性炭吸附氧氟沙星-铜特性及机理研究[J]. 农业资源与环境学报, 2020, 37(1): 59-65. CHEN X, WEI Z Y, ZHAO H B, et al. Adsorption characteristics and mechanisms of ofloxacin-Cu by activated carbon based on long-root Eichhor niacrassipes[J]. Journal of Agricultural Resources and Environment, 2020, 37(1): 59-65. |
| [21] |
ZHOU R J, ZHANG M, ZHOU J H, et al. Optimization of biochar preparation from the stem of Eichhor niacrassipes using response surface methodology on adsorption of Cd2+[J]. Scientific Reports, 2019, 9(1): 1034-1035. DOI:10.1038/s41598-018-37768-0 |
| [22] |
周丽丽, 管卫兵, 彭自然, 等. 运用响应面法优化芦苇基生物炭活化工艺[J]. 上海海洋大学学报, 2019, 28(6): 911-920. ZHOU L L, GUAN W B, PENG Z R, et al. Optimization of reed-based biochar activation process by response surface methodology[J]. Journal of Shanghai Ocean University, 2019, 28(6): 911-920. |
| [23] |
汤嘉雯, 陈金焕, 王凯男, 等. 加拿大一枝黄花生物炭对Cd2+的吸附特性及机理[J]. 农业环境科学学报, 2019, 38(6): 1339-1348. TANG J W, CHENJ H, WANGK N, et al. Characteristics and mechanism of cadmium adsorption by Solid agocanadensis derived biochar[J]. Journal of Agro-Environment Science, 2019, 38(6): 1339-1348. |
| [24] |
崔孝强.水体修复植物基生物炭的环境应用及其机理研究[D].杭州: 浙江大学, 2018. CUI X Q.The environmental applications and corresponding mechanisms of biochar derived from aquatic eco-remediation plants[D]. Hangzhou: ZhejiangUniversity, 2018. |
| [25] |
胡晓虹.磁性竹炭制备及其对重金属离子吸附性能影响研究[D].长沙: 中南林业科技大学, 2018. HU X H. Preparation of magnetic bamboo charcoal and its effect on the adsorption properties of heavy metal ions[D].Changsha: Central South University of Forestry and Technology, 2018. |
| [26] |
何迎东. 生物炭对污水典型污染物的去除机理与应用研究进展[J]. 农业与技术, 2020, 40(9): 109-114. HE Y D. Research progress on removal mechanism and application of typical pollutants in sewage by biochar[J]. Agriculture and Technology, 2020, 40(9): 109-114. |
 2020,
Vol. 29
2020,
Vol. 29


