2. 洞头区水产科技推广站, 浙江 洞头 325700
随着全球气候变暖,自然灾害频频发生,各国对CO2的控制和减排有着不可推卸的责任。联合国2009年《蓝碳》报告指出,地球上55%的生物碳或绿色碳的捕获是由海洋生物完成的[1]。大型海藻存在着极高的固碳潜力,同时吸收海水中氮、磷等元素转化为自身所需的营养成分[2]。我国海藻养殖产业位居全球之首,养殖种类非常丰富,据初步预计,到2050年,藻类固碳量可达23.5×105 t[3]。随着工农业发展及城市化进程加速,海域富营养化程度加剧,成为赤潮、绿潮等生态灾害频发的主要原因之一。如今,我国愈发关注海藻碳汇等生态效应并开展相关研究,大力发展海藻养殖业已经不仅仅局限于经济价值,更是对海洋碳汇和环境修复具有全球性的战略意义。
坛紫菜(Pyropia haitanensis),属红藻门(Rhodophyta)、紫球藻科(Porphyridiaceae),暖温带种类,是我国特有的可人工栽培品种,多分布于长江以南的福建、浙江和广东等地沿岸。坛紫菜长成后可连续采割,根据采收顺序俗称“头水”、“二水”、“三水”、“四水”[4]。作为大规模种植的经济海藻种类之一,坛紫菜营养价值高,素有“营养宝库”的美誉,同时在降低海域富营养化、改善海洋生态环境方面具有积极作用[5]。目前,关于坛紫菜的研究多集中于养殖技术、经济效益方面,其碳汇能力及氮磷元素转移的生态效益研究相对较少。
温州市洞头区自20世纪60年代开始人工试养坛紫菜,至今已有50多年养殖历史,截至2017年,洞头紫菜养殖面积2 000多公顷,素有“浙江省紫菜之乡”美誉。笔者选取了养殖于洞头区霓屿街道大背澳的2种不同坛紫菜品系为研究对象,对比不同收割期坛紫菜的生长参数、产量以及CNP固定效率,以期筛选出适宜在洞头海区养殖且具有渔业碳汇和海水净化能力的坛紫菜优势品种,为指导坛紫菜的人工繁育、优化养殖结构提供理论支撑。
1 材料与方法 1.1 养殖海区洞头区霓屿街道大背澳养殖海区位于大潮干潮线至小潮满潮线间的中低潮区,风浪较小,水质稳定,无工业污水,泥沙底质,温度适宜,符合坛紫菜的生长发育条件。“洞头本地菜”坛紫菜种苗为洞头本地传统养殖品系,“浙东1号”坛紫菜为洞头区从宁波大学藻种实验室引进的坛紫菜新品种,俗称“木耳菜”。一水至四水坛紫菜分别采收于2014年10月、11月、12月和2015年1月。各采收期的海水基本理化参数见表 1。

|
表 1 海水基本理化参数背景值 Tab.1 Background values of basic physicochemical characteristics of seawater |
养殖设施主要由毛竹和网帘两部分组成。插杆毛竹为固定桩,长11~16 m,是根据养殖区海水深度决定的,直径13~18 cm,插入泥底深2.8~3.5 m。每行插杆11根,每根毛竹系2张网帘,用横杆毛竹张开网帘,约3.7 m×4.7 m。吊绳长度可调节,使网帘能随着潮涨潮落在一定范围内上下浮动。为使潮流畅通,筏架之间的行距保持在4.8 m以上。
1.3 研究方法 1.3.1 坛紫菜叶状体长度和干质量不同采割期2种坛紫菜品系分别随机选取3网,每网随机测量8条叶状体的长度和经自然风干后的干质量,均取平均值。
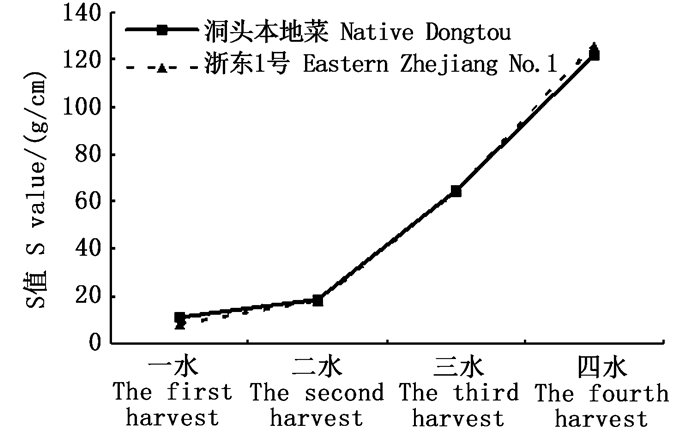
1.3.2 坛紫菜S值坛紫菜S值计算公式为
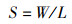 (1)
(1)
式中:S表示坛紫菜单位体长的湿质量,g/cm;W表示单条藻体湿质量,g;L表示藻体体长,cm。
1.3.3 坛紫菜的CNP含量用配有固体模块SSM-5000A的岛津TOC-LCPH总有机碳分析仪测定坛紫菜的C含量;用凯氏定氮法测定坛紫菜的N含量;用钒钼黄吸光光度法测定坛紫菜的P含量。
1.3.4 坛紫菜CNP固定效率坛紫菜CNP固定效率计算公式为
 (2)
(2)
式中:VC/N/P表示CNP固定效率;ΩC/N/P表示CNP含量;DP表示单位面积干质量产量。
1.4 统计分析采用Excel 2003进行数据计算及作图处理,用SPSS Statistics 17统计软件进行数据分析。用单因素方差分析法分析同一品系不同收割期差异性,用配对t检验分析不同品系间差异性。
2 结果与分析 2.1 不同采割期2种坛紫菜品系的长度变化由图 1可以看出,随着收割次数增加,2种坛紫菜品系的叶状体长度逐渐减小(P < 0.01),“洞头本地菜”和“浙东1号”一水的长度最高分别为38.08 cm和37.17 cm,四水长度最低分别为28.14 cm和19.67 cm。在整个生长过程中,“洞头本地菜”的长度均大于“浙东1号”(P>0.05),尤其四水阶段,前者的平均长度比后者高出43.1%。

|
图 1 2种坛紫菜品系一水至四水的平均长度 Fig. 1 Average length of two strains of Pyropia haitanensis at different harvest stages |
2种坛紫菜品系一至四水的单条叶状体干质量逐步升高(P < 0.01),尤其是在二水后,坛紫菜单条叶状体干质量增长速率较快。“洞头本地菜”和“浙东1号”的单条叶状体平均干质量峰值分别为0.63 g和0.44 g,最低值分别为0.07 g和0.05 g。在整个生长过程中,“洞头本地菜”单条叶状体干质量都高于“浙东1号”(P>0.05),尤其四水时,“洞头本地菜”单条叶状体干质量是“浙东1号”的1.43倍(图 2)。
|
图 2 2种坛紫菜品系一水至四水的单条平均干质量 Fig. 2 Average dry mass of two strains thallus at different harvest stages |
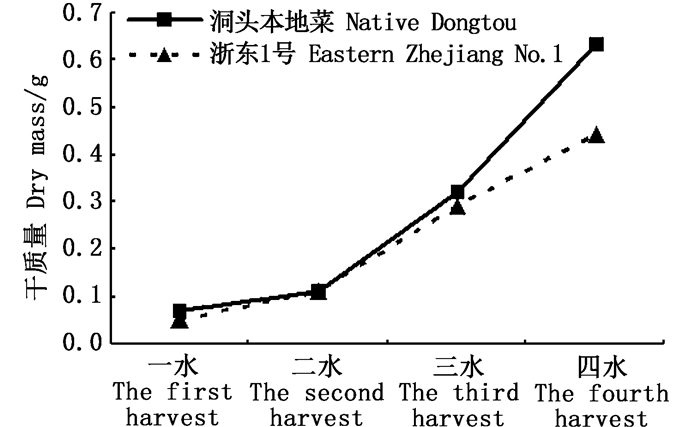
本实验所测定的产量值均以坛紫菜干质量计。由图 3可以看出,2种坛紫菜品系在采割期内,产量的变化趋势均是先升后降(P0.01),但是2种坛紫菜品系产量峰值出现的采割期不同,“洞头本地菜”和“浙东1号”的产量峰值分别出现在三水(765.00 kg/hm2)和二水(535.50 kg/hm2),最低值都出现在一水,分别为270.00 kg/hm2和371.25 kg/hm2。在整个收割过程中,除了一水“洞头本地菜”的产量低于“浙东1号”,二水至四水“洞头本地菜”的产量均高于“浙东1号”,“洞头本地菜”的总产量达2 412.00 kg/hm2,“浙东1号”的总产量为1 874.25 kg/hm2,不同品系间产量无显著差异(P>0.05)。
|
图 3 2种坛紫菜品系一水至四水的产量 Fig. 3 Yield of two strains of Pyropia haitanensis at different harvest stages |
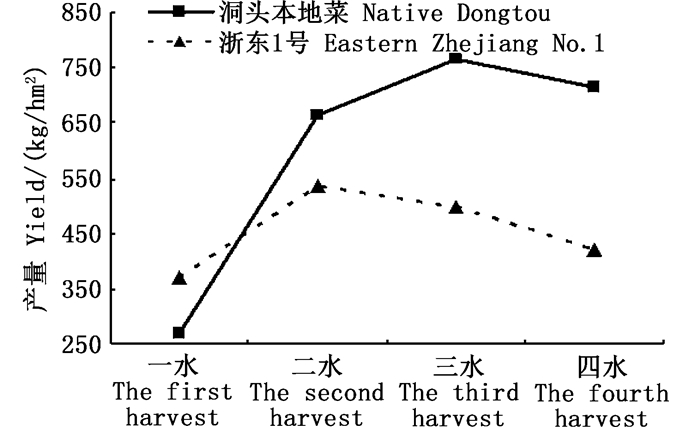
如图 4所示,2种坛紫菜品系S值的差异不显著(P>0.05),但采割期对S值的影响非常明显,一水至四水坛紫菜的S值呈不断增长趋势(P < 0.01),尤其在第二水后,S值的增长较快。“洞头本地菜”和“浙东1号”的S值峰值分别为122.6 g/cm和126.1 g/cm,最低值分别为11.0 g/cm和8.3 g/cm。
|
图 4 2种坛紫菜品系一水至四水的S值 Fig. 4 S value of two strains of Pyropia haitanensis at different harvest stages |
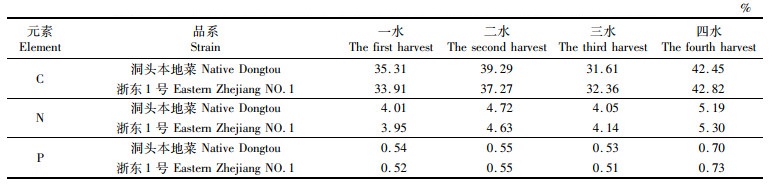
由表 2可以看出,在整个生长过程中,2种坛紫菜品系C、N含量的变化趋势一致,都是先升高后下降再升高,而P含量在一水至三水基本持平,四水明显升高。同一收割期,不同品系间同种元素含量的差异不显著(P>0.05),且“洞头本地菜”和“浙东1号”的CNP含量峰值均出现于四水,C含量最高值分别为42.45%和42.82%,N含量最高值分别为5.19%和5.30%,P含量最高值分别为0.70%和0.73%。
|
表 2 2种坛紫菜品系一至四水的CNP含量 Tab.2 CNP content of two strains of Pyropia haitanensis at different harvest stages |
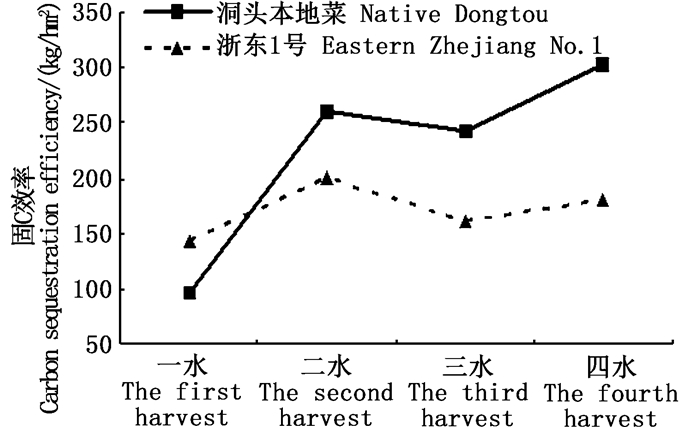
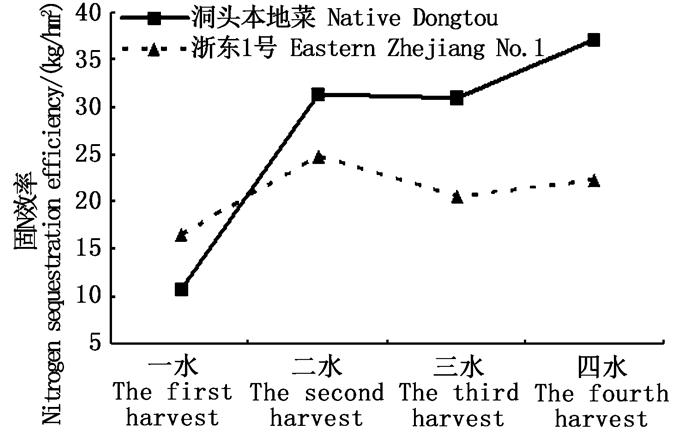
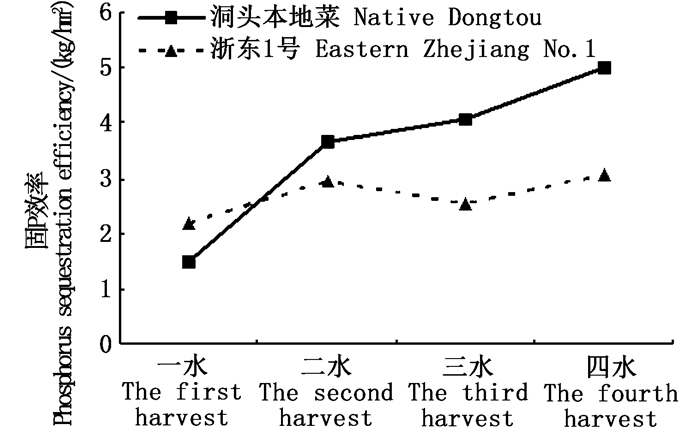
二水至四水“洞头本地菜”的CNP固定效率均高于“浙东1号”。“洞头本地菜”CNP最高固定效率均出现在四水,分别达303.09 kg/hm2、37.06 kg/hm2、5.00 kg/hm2,而“浙东1号”CN固定效率峰值出现在二水,分别达199.58 kg/hm2、24.79 kg/hm2,P固定效率峰值出现在四水达3.07 kg/hm2,见图 5~7。一水至四水“洞头本地菜”的总固C效率达900.74 kg/hm2,总固N效率达110.16 kg/hm2,总固P效率为14.16 kg/hm2,“浙东1号”的总固C效率为683.34 kg/hm2,总固N效率达84.3 kg/hm2,总固P效率为10.75 kg/hm2。不同收割期CNP固定效率差异极显著(P<0.01),2种品系间无显著差异(P>0.05)。
|
图 5 2种坛紫菜品系一水至四水的固C效率 Fig. 5 Carbon sequestration efficiency of two strains of Pyropia haitanensis at different harvest stages |
|
图 6 2种坛紫菜品系一水至四水的固N效率 Fig. 6 Nitrogen sequestration efficiency of two strains of Pyropia haitanensis at different harvest stages |
|
图 7 2种坛紫菜品系一水至四水的固P效率 Fig. 7 Phosphorus sequestration efficiency of two strains of Pyropia haitanensis at different harvest stages |
翁琳等[6]在不同温度下对冷藏坛紫菜进行恢复培养,发现坛紫菜的生长与其品系的生长适宜温度有关。从2014年10月到2015年1月分4次对坛紫菜进行采收,其间海水温度范围为13.10~22.85 ℃,逐月降低(表 1)。根据坛紫菜单条叶状体干质量的增长趋势,可以看出2种坛紫菜品系在13~15 ℃水温下的生长速率显著高于20 ℃及以上生存环境,这与丁柳丽等[7]研究不同温度对坛紫菜生长的影响结论基本吻合。产量作为影响碳汇效率的重要因素,变化趋势有所不同。三水产量最高,四水产量降低的原因可能与气温降低有关。“浙东1号”虽然是引进的新品种,但不论在叶状体长度、干质量还是产量方面,都不如“洞头本地菜”具有优势,可以说“洞头本地菜”坛紫菜是更适合在洞头养殖的高产品种。
我国的紫菜属于真紫菜亚属,即叶状体是由一层细胞组成的膜状体,在一定程度上,本实验的坛紫菜S值可以反映其单条叶片的宽度和厚度,陈昌生等[8]在坛紫菜选育实验中发现剪收次数能够促进紫菜增厚。随着栽培时间增长,2种坛紫菜品系的S值均不断升高,主要与坛紫菜叶状体长度变短及单体质量增加有关,S值升高也表明藻体变宽变厚,更有利于进行光合作用从而提高产量,这或许能够为坛紫菜叶状体干质量变化趋势与S值变化趋势颇为一致的结论提供解释。
3.2 2种坛紫菜品系的固C效率国内已有学者基于不同角度对我国海藻养殖固碳量进行了估算和预测。宋金明等[9-10]提出海藻养殖是海洋增加碳汇的重要措施,预测2020年我国大型人工海藻可实现的固碳量将达到93万t。权伟等[11]以1999—2012年《中国渔业统计年鉴》统计数据为基础,估算了中国及浙江近海藻类的固碳强度,得出全国海藻年均固碳量为41.85万t,浙江省海藻年均固碳量为1.03万t。
不同海区对于同种藻类碳含量并无显著性影响[12],海藻养殖形成的碳汇量主要取决于养殖品种和产量两个因素[13]。坛紫菜表面积比例大,所有细胞都可以进行营养盐的吸收并转化为新的藻体组织,所以呈现出快速生长的特性[14],能够多次收割,对其进行人工收获的过程就相当于将碳、氮、磷元素以水产品形式从海洋中移出,起到了渔业碳汇及水体修复的生态作用。
2种坛紫菜品系固碳效率最低值均在一水,主要是因为一水产量最低。二水坛紫菜产量和C含量较一水坛紫菜均有提升,故二水的固C效率有所提升。三水坛紫菜的C含量最低,直接导致了固C效率的下降。2种坛紫菜品系在四水时C含量均达到峰值,“洞头本地菜”的固C效率也随之出现峰值,而“浙东1号”四水受产量低的影响,固C效率略低于二水。就整个养殖期来看,“洞头本地菜”的总固C效率比“浙东1号”高出31.8%,可见“浙东1号”坛紫菜的固碳效率在洞头未表现出优势。
3.3 2种坛紫菜品系的N、P固定效率大型海藻作为海洋生态系统中重要的氮库与磷库[15],同样受到国内学者的关注。从20世纪80年代起,国外学者就开始利用大型海藻进行富营养水体的生态修复研究[16-17],并发现海藻可以有效地清除养殖水体中的营养盐,半浮动筏式条斑紫菜栽培可使沿岸海水的无机氮磷含量显著下降[18]。柴召阳等[18]根据大型海藻的年产量及递增速率预测到2020年,我国大型海藻养殖的年固氮量、年固磷量分别为16万t和0.8万t。
相对于C、N固定效率来说,在同等条件下坛紫菜的P固定效率最低。从藻类的经验分子式C106H263O110N16P来看,藻类对磷元素的需求量比C、N少。对比2种坛紫菜品系在整个栽培期的N、P固定效率,“洞头本地菜”的总固N效率是“浙东1号”的1.31倍,“洞头本地菜”的总固P效率是“浙东1号”的1.32倍,该区域“洞头本地菜”表现出较高的生态效益。
据公式(2)可知,CNP固定效率均与其产量有着直接的关系。蔡继晗等[19]研究发现,苍南县沿浦湾海域低潮区7个养殖群体中,“申福二号”产量最高,“沿浦种”次之,其次是“霞浦种”>“洞头本地菜”>“木耳菜”>“象山种”>“漳浦种”。这与本研究中“洞头本地菜”产量高于“浙东1号”相一致,但“申福二号”在温州苍南表现出了更高的产量,可见筛选适合本地的高产品系是提高坛紫菜CNP固定效率的重要途径。
| [1] |
刘慧, 唐启升. 国际海洋生物碳汇研究进展[J]. 中国水产科学, 2011, 18(3): 695-702. LIU H, TANG Q S. Review on worldwide study of ocean biological carbon sink[J]. Journal of Fishery Sciences of China, 2011, 18(3): 695-702. |
| [2] |
李纯厚, 齐占会, 黄洪辉, 等. 海洋碳汇研究进展及南海碳汇渔业发展方向探讨[J]. 南方水产, 2010, 6(6): 81-86. LI C H, QI Z H, HUANG H H, et al. Review on marine carbon sink and development of carbon sink fisheries in South China Sea[J]. South China Fisheries Science, 2010, 6(6): 81-86. DOI:10.3969/j.issn.1673-2227.2010.06.015 |
| [3] |
高学文. CDM机制下的碳汇渔业发展思考[J]. 中国城市经济, 2011(8): 41. GAO X W. Thoughts on the development of carbon sink fisheries under the CDM mechanism[J]. China Urban Economy, 2011(8): 41. |
| [4] |
应苗苗, 施文正, 刘恩玲. 不同收割期坛紫菜挥发性成分分析[J]. 食品科学, 2010, 31(22): 421-426. YING M M, SHI W Z, LIU E L. Analysis of volatile components in laver harvested in different time points[J]. Food Science, 2010, 31(22): 421-426. |
| [5] |
李钧, 谢双如. 坛紫菜藻场生态系统修复技术[J]. 齐鲁渔业, 2012, 29(10): 37-38. LI J, XIE S R. Ecosystem restoration technology of Porphyra haitanensis farm[J]. Shandong Fisheries, 2012, 29(10): 37-38. |
| [6] |
翁琳, 陈昌生, 纪德华, 等. 冷藏和恢复培养温度对坛紫菜存活生长的影响[J]. 集美大学学报(自然科学版), 2007, 12(2): 97-102. WENG L, CHEN C S, JI D H, et al. Effects of cold preservation and recuperative temperature on the survival and growth of Porphyra haitanensis[J]. Journal of Jimei University (Natural Science), 2007, 12(2): 97-102. DOI:10.3969/j.issn.1007-7405.2007.02.001 |
| [7] |
丁柳丽, 刘露, 邹定辉. 不同温度与CO2浓度对坛紫菜生长和光合作用温度反应特性的影响[J]. 生态科学, 2013, 32(2): 151-157. DING L L, LIU L, ZOU D H. Effects of different temperature and CO2 concentrations on the growth and photosynthetic response to temperature in Porphyra haitanensis[J]. Ecological Science, 2013, 32(2): 151-157. DOI:10.3969/j.issn.1008-8873.2013.02.003 |
| [8] |
陈昌生, 梁艳, 徐燕, 等. 坛紫菜薄叶新品系选育及经济性状的比较[J]. 渔业科学进展, 2009, 30(2): 100-105. CHEN C S, LIANG Y, XU Y, et al. Selective breeding and comparison of economic traits of the new thin-thallus strain Porphyra haitanensis[J]. Progress in Fishery Sciences, 2009, 30(2): 100-105. DOI:10.3969/j.issn.1000-7075.2009.02.017 |
| [9] |
宋金明, 李学刚, 袁华茂, 等. 中国近海生物固碳强度与潜力[J]. 生态学报, 2008, 28(2): 551-558. SONG J M, LI X G, YUAN H M, et al. Carbon fixed by phytoplankton and cultured algae in China coastal seas[J]. Acta Ecologica Sinica, 2008, 28(2): 551-558. DOI:10.3321/j.issn:1000-0933.2008.02.013 |
| [10] |
宋金明. 中国近海生态系统碳循环与生物固碳[J]. 中国水产科学, 2011, 18(3): 703-711. SONG J M. Carbon cycling processes and carbon fixed by organisms in China marginal seas[J]. Journal of Fishery Sciences of China, 2011, 18(3): 703-711. |
| [11] |
权伟, 应苗苗, 康华靖, 等. 中国近海海藻养殖及碳汇强度估算[J]. 水产学报, 2014, 38(4): 510-515. QUAN W, YING M M, KANG H J, et al. Marine algae culture and the estimation of carbon sink capacity in the coastal areas of China[J]. Journal of Fisheries of China, 2014, 38(4): 510-515. |
| [12] |
严立文, 黄海军, 陈纪涛, 等. 我国近海藻类养殖的碳汇强度估算[J]. 海洋科学进展, 2011, 29(4): 537-545. YAN L W, HUANG H J, CHEN J T, et al. Estimation of carbon sink capacity of algal mariculture in the coastal areas of China[J]. Advances in Marine Science, 2011, 29(4): 537-545. DOI:10.3969/j.issn.1671-6647.2011.04.014 |
| [13] |
岳冬冬. 海带养殖结构变动与海藻养殖碳汇量核算的情景分析[J]. 福建农业学报, 2012, 27(4): 432-436. YUE D D. Correlation between kelp aquaculture and carbon sinks[J]. Fujian Journal of Agricultural Sciences, 2012, 27(4): 432-436. DOI:10.3969/j.issn.1008-0384.2012.04.022 |
| [14] |
陆勤勤, 周伟, 邓银银. 条斑紫菜栽培的经济效益与生态效益概述[J]. 中国水产, 2016(1): 53-54. LU Q Q, ZHOU W, DENG Y Y. Summary of economic benefits and ecological benefits of Porphyra yezoensis cultivation[J]. China Fisheries, 2016(1): 53-54. DOI:10.3969/j.issn.1002-6681.2016.01.026 |
| [15] |
NALDI M, VIAROLI P. Nitrate uptake and storage in the seaweed Ulva rigida C.Agardh in relation to nitrate availability and thallus nitrate content in a eutrophic coastal lagoon (Sacca di Goro, Po River Delta, Italy)[J]. Journal of Experimental Marine Biology and Ecology, 2002, 269(1): 65-83. DOI:10.1016/S0022-0981(01)00387-2 |
| [16] |
NEORI A, KROM M D, ELLNER S P, et al. Seaweed biofilters as regulators of water quality in integrated fish-seaweed culture units[J]. Aquaculture, 1996, 141(3/4): 183-199. |
| [17] |
HAGLUND K, PEDERSÉN M. Outdoor pond cultivation of the subtropical marine red alga Gracilaria tenuistipitata in brackish water in Sweden.Growth, nutrient uptake, co-cultivation with rainbow trout and epiphyte control[J]. Journal of Applied Phycology, 1993, 5(3): 271-284. DOI:10.1007/BF02186230 |
| [18] |
柴召阳, 何培民. 我国海洋富营养化趋势与生态修复策略[J]. 科学, 2013, 65(4): 48-52. CAI Z Y, HE P M. Trends of marine eutrophication in China and ecological restoration strategy[J]. Science, 2013, 65(4): 48-52. |
| [19] |
蔡继晗, 陈高峰, 吕永林, 等. 申福二号等7个坛紫菜养殖群体的生长性能分析[J]. 水产养殖, 2011, 32(8): 1-3. CAI J H, CHEN G F, LV Y L, et al. Growth performance analysis of seven Porphyra haitanensis breeding populations such as Shenfu No.2[J]. Aquaculture, 2011, 32(8): 1-3. DOI:10.3969/j.issn.1004-2091.2011.08.001 |
2. Dongtou Fisheries Science and Technology Extension Service, Dongtou 325700, Zhejiang, China
 2019,
Vol. 28
2019,
Vol. 28


