2. 上海海洋大学 农业农村部淡水水产种质资源重点实验室, 上海 201306;
3. 上海海洋大学 水产科学国家级实验教学示范中心, 上海 201306
生物絮团养殖系统可以让养殖生物在低换水率或零换水的情况下实现高密度的养殖,较低的换水率有利于降低对水资源的需求、减少冬季养殖水体的热量损失、提高养殖生物安全[1]。不同于循环水养殖系统,生物絮团系统不需要外接生物过滤器,而是直接在水体中培养一个微生物生态系统[2]。絮团微生物可以降解养殖生物产生的有机颗粒、残饵和碎屑,将N、P等污染物质转化成絮团。研究表明,对虾可以摄食絮团,从而获得营养物质的二次利用,降低投饲成本[3]。
生物絮团系统中,氨氮有3种去除途径:藻类吸收, 硝化细菌氧化成硝氮, 异养细菌同化为生物蛋白[4]。藻类对营养的吸收有限,因此生物絮团系统对水质的调节主要是由细菌来完成的[5]。异养细菌通常利用有机碳源作为能源吸收氮素转化为菌体蛋白,添加碳源可以快速去除氨氮[6]。硝化细菌将氨氮氧化成硝酸盐氮。硝酸盐氮比氨氮和亚硝酸盐氮的毒性更小,在安全范围内可以接受水体中的硝酸盐氮积累,当然有研究[7]表明过高浓度的硝酸盐氮会降低对虾的生长速度和存活率。不过在以硝化系统为主的生物絮团系统中,养殖过程可以不额外添加碳源[8]。
除了水质,养殖密度也是引起养殖生物应激反应的重要因素,与养殖动物福利和养殖产量直接相关[9-10],也是决定生产经济回报的直接因素[11-12]。在较高的养殖密度下,物质投入量也随之增加,势必造成养殖水体中代谢废物和残余饵料等污染物含量增多,最终抑制对虾的生长[13]。当然,在较低的养殖密度下虽然可以使得对虾的生长速度加快,但是其空间利用率较低,养殖产量会不够理想。国内外对斑节对虾(Penaeus monodon)和凡纳滨对虾(Litopenaeus vannamei)养殖密度的研究发现,随着对虾养殖密度的增加,其生长速度会变得缓慢,增重率也随之降低[14-15]。
本实验在硝化型生物絮团系统内进行凡纳滨对虾养殖,并将凡纳滨对虾设置5个密度梯度,旨在研究养殖密度对硝化型生物絮团系统的水质调控和生长性能的影响。
1 材料与方法 1.1 实验时间和实验地点实验于2016年10月5日至11月20日在山东省莱州市单山水产有限公司的工厂化养殖车间进行,为期45 d。
1.2 实验设计和养殖管理实验用4.0 m×6.2 m养殖池,养殖水深0.8 m,有效水体19.84 m3,共10个。
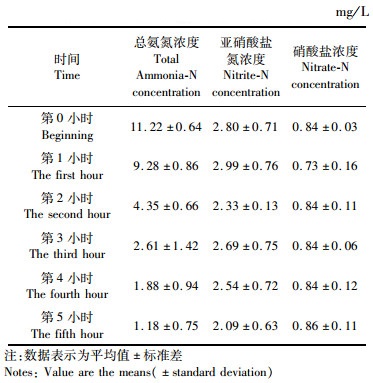
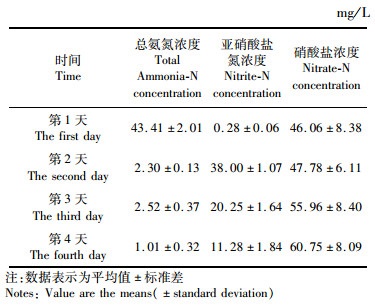
实验开始前,在另外车间池水中导入莱州湾的自然海水,盐度31,用漂白粉消毒。使用凡纳滨对虾配合饲料和葡萄糖,以及购买的复合芽孢杆菌(德国拜耳,诺必清生物净水剂)进行生物絮团的培育,第30天进行氨氮同化测试确定生物絮团初步形成(各取10 L絮团溶液于3个水桶中,均匀曝气,添加10 mg/L的NH4Cl和200 mg/L的葡萄糖,每小时测定1次三态氮浓度,见表 1),然后停止碳源添加,使生物絮团向硝化反应转变,第90天硝化系统形成,进行硝化反应测试确定该系统为硝化型生物絮团系统(各取10 L絮团溶液于3个水桶中,均匀曝气,添加40 mg/L的NH4Cl,每24小时测定1次三态氮浓度,见表 2)。向实验池导入驯化完成的硝化型生物絮团,调整生物絮团浓度(floc volume, Fv)为30 mL/L。
|
表 1 氨氮同化测试中的三态氮水平 Tab.1 The levels of the three forms of nitrogen in the ammonia nitrogen assimilation test |
|
表 2 硝化反应测试中的三态氮水平 Tab.2 The levels of the three forms of nitrogen in the nitration reaction test |
购买正大集团在海南的东方卜蜂苗场的不带特定病原的凡纳滨对虾虾苗,在单山水产有限公司标苗车间暂养, 实验开始前体长为(4.8±0.25)cm,体质量为(0.98±0.16)g。
原计划设计600、400、300、200、100尾/m3 5个密度组,并标记为B600组,B400组,B300组,B200组,B100组,每组两个平行养殖池。但由于生产上水体较大,无法按数量投放凡纳滨对虾仔虾,实际方法是通过抽样称重后计算出平均质量,按照公式(1)计算出需要投放的质量(WN),再进行投放。投放重量的计算公式如下:
 (1)
(1)
式中:WA为对虾均质量,g;DS为实验的设计密度;VE为有效水体的体积,m3。
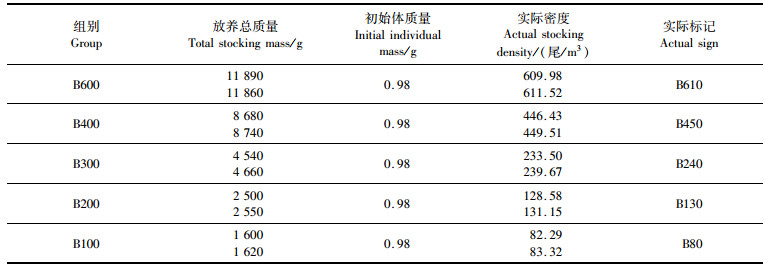
但由于操作过程中有误差,实际投放量与设计密度有差异,因此确定实际密度后以实际密度标记实验组,详情见表 3。
|
表 3 实际放养密度 Tab.3 The actual stocking density |
放苗后第2天开始投喂,养殖所用饲料购买自连云港正大饲料有限公司(CP≥42 %,凡纳滨对虾配合饲料)。每天分4次投喂,分别为7:00、11:00、15:00、19:00。首次投喂量为单个池内对虾体质量的5%,而后按照5%的速度增加投喂量。投喂1小时后通过抄底检查摄食情况,若出现剩余饲料则保持当天投喂量不增加,至无剩料后再增加投喂量。
实验期间每天进行排污。养殖池为锅底状,中心排污,排污口处裹有0.25 mm孔径的筛网,确保仔虾无法逃逸,每天8:00和16:00各排污1次,每5天补充1次排污损失的水。
1.3 样品的采集与测定 1.3.1 水样的采集与测定每天上午用WTW便携式多参数水质分析仪(Multi 3430, 德国)测定养殖池水的溶解氧(dissolved oxygen)、温度(temperature)、盐度(salinity)。
每天上午分别取各实验池水样50 mL,经0.45 μm滤膜过滤后测定总氨氮(total Ammonia-N, TAN),亚硝酸盐氮(nitrite-N, NO2--N)、硝酸盐氮(nitrate-N, NO3--N)。
TAN浓度的测定采用次溴酸钠氧化法;NO2--N浓度的测定采用萘乙二胺分光光度法;NO3--N浓度的测定采用锌镉还原法(见GB 17378.4—2007)。
测出TAN浓度后,通过养殖期间的pH水平,将其换算成非离子氨的浓度。
1.3.2 凡纳滨对虾生长性能的测定实验期间,每5天每池随机捞取凡纳滨对虾50尾测定1次凡纳滨对虾的体质量和体长,并记录。
实验结束后记录每个养殖池凡纳滨对虾的产量(Production, kg/m3), 并计算存活率(Survival Rate, RS)、体长增长量(Length increase amount, ΔL, cm)、体质量增加量(Mass increase amount, ΔW, g)。计算公式如下:
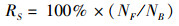 (2)
(2)
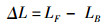 (3)
(3)
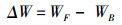 (4)
(4)
式中:NF为终末对虾数量;NB为初始对虾数量;LF为终末对虾体长,cm;LB为初始对虾体长,cm;WF为终末对虾体质量,g;WB为初始对虾体质量,g。
1.4 数据的分析与处理采用Excel进行数据分析,实验结果用平均值±标准差(Mean ±SD)表示。采用SPSS 19.0对数据进行单因素方差分析。
2 结果 2.1 硝化型生物絮团系统中不同养殖密度下的水质情况养殖池配有24 h工作的鼓风机,不间断地往水体中充氧,实验期间溶解氧保持在(7.58±0.31)mg/L的高水平。养殖池内铺设有地暖管道,实验期间通过锅炉加热在地暖管道内循环28 ℃的温水,保持水温在(25.7±0.84)℃。养殖期间水体pH保持在7.89±0.21,以上指标皆在凡纳滨对虾的适宜生长范围内。
非离子氨浓度和亚硝酸盐氮在养殖期间呈现上下波动,因此使用平均值±标准差来表示两者在养殖期间的整体水平。本实验开始前,通过90 d建立硝化型生物絮团系统,在此过程中硝酸盐氮含量积累到较高水平,因此使用硝酸盐氮的变化量来比较该数据。
不同密度组的非离子氨浓度无显著性差异(P>0.05),其中B80组波动更小。B610组的亚硝酸盐氮浓度与其他各组之间呈现显著性差异(P < 0.05),B450、B240、B130和B80之间并无显著性差异(P>0.05)。B610和B450组的硝酸盐氮浓度呈现正增长,且其增长量B610 >B450。B240、B130和B80组硝酸盐氮浓度呈现负增长,且增长量B80 >B240 >B130。见表 4。

|
表 4 养殖期间的三态氮水平 Tab.4 The levels of the three forms of nitrogen in the culture period |
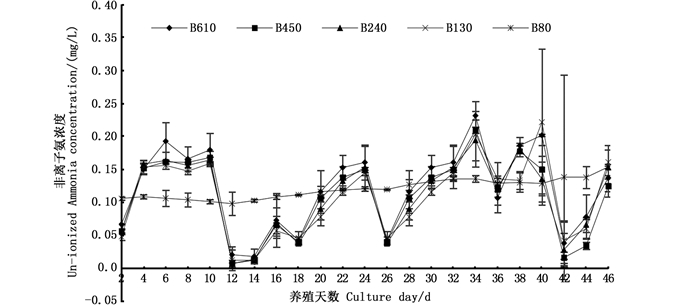
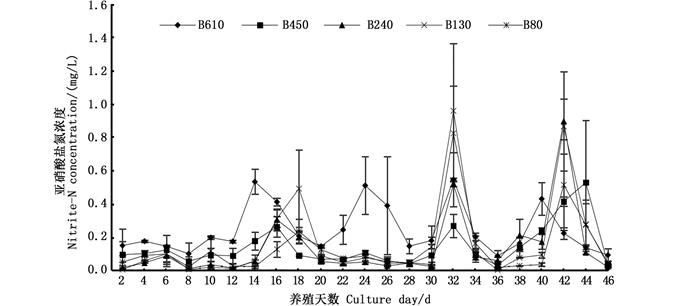
B80组的非离子氨浓度较为平稳,其他各组非离子氨浓度变化相似,一直处于上下波动中,但整个养殖周期中非离子氨浓度处于较低水平(图 1)。养殖期间,各密度组的亚硝酸盐氮水平一直处于上下波动中,但浓度水平较低(图 2)。养殖前24天,各组硝酸盐氮呈现上升趋势,24天后B610组上升趋势趋于平稳,其他各组都呈现出下降趋势(图 3)。
|
图 1 养殖期间非离子氨浓度的动态变化 Fig. 1 Dynamic changes of the un-ionized ammonia concentration throughout the culture period |
|
图 2 养殖期间亚硝酸盐氮浓度的动态变化 Fig. 2 Dynamic changes of the nitrite nitrogen concentration throughout the culture period |

|
图 3 养殖期间亚硝酸盐氮浓度的动态变化 Fig. 3 Dynamic changes of the nitrate nitrogen concentration throughout the culture period |
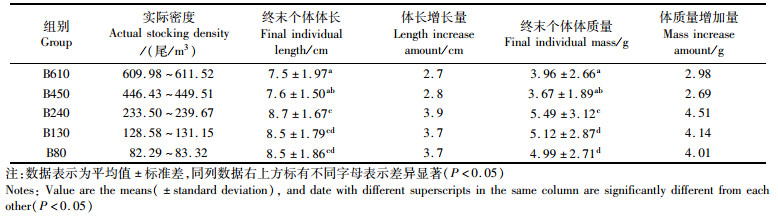
凡纳滨对虾的体长增长量B240>B130=B80>B450>B610。终末个体体长上,较高密度两组(B610和B450)之间差异不显著(P>0.05),与较低密度3组(B80、B130、B240)之间差异显著(P < 0.05),低密度3组(B80、B130、B240)之间差异不显著(P>0.05)。见表 5。
|
表 5 不同养殖密度下凡纳滨对虾的生长情况 Tab.5 The growth performance of Litopenaeus vannamei at different stocking densities |
体质量增加量B240 > B130 > B80>B610>B450。终末个体体质量上,较高密度两组(B610和B450)之间差异不显著(P>0.05),与较低密度3组(B80、B130、B240)之间差异显著(P < 0.05)。低密度3组中,B240与另外两组(B80、B130)之间差异显著(P < 0.05), B130和B80组之间差异不显著(P>0.05)。见表 5。
B240组的养殖池在养殖42 d时地暖管破损,维持水温的锅炉水流入养殖池中,水温和盐度的剧烈变化导致凡纳滨对虾大量死亡,因此B240组存活率偏低。
存活率上,B240 < B610 < B450 < B130 < B80。B240组与其他各组呈现显著性差异(P < 0.05),其余各组(B610、B450、B130和B80)之间无显著性差异(P>0.05)。产量上,B610 > B450 > B240 > B130 > B80。产量按照密度高低逐级递减,且各密度之间互相呈现显著性差异(P < 0.05)。见表 6。

|
表 6 不同养殖密度下凡纳滨对虾的存活率和产量 Tab.6 The survival rate and production of Litopenaeus vannamei at different stocking densities |
氨氮是残饵、粪便以及对虾残肢等含氮有机物分解的最终产物,在水体中以离子氨和非离子氨的形式存在,非离子氨不带电荷,具有较强的脂溶性,能够穿透细胞膜[16]。当水体中的氨氮达到一定浓度时,非离子氨容易透过细胞膜进入体内使得水生动物的生理调节失衡,从而引起体内组织缺氧,这就是氨中毒的症状[17]。整个养殖期间,非离子氨浓度上下波动较剧烈,日常投喂的氮素进入造成水体非离子氨浓度的上升,富集的氨氧化细菌不断将氨氮氧化为硝酸盐氮,将非离子氨浓度降低[18]。虽然非离子氨出现了剧烈波动,但从整个养殖周期来看,不同密度的养殖池非离子氨浓度都维持在0.2 mg/L以下,自养硝化细菌可以很好的抑制非离子氨的浓度,保持养殖环境的安全稳定。
亚硝酸盐氮是硝化过程的中间产物。氨氧化细菌的生长速率要快于亚硝酸盐氧化细菌,因此在养殖过程中经常出现亚硝酸盐氮的积累,亚硝酸盐氮会抑制虾类的生长和变态发育,尤其亚硝酸盐会与对虾血液中的血蓝蛋白结合,破坏血蓝蛋白的载氧能力,这是造成对虾致死的主要原因之一[19]。以换水为主的养殖模式中,亚硝酸盐氮都会在30 d左右出现,然后讯速上升并且居高不下[20-21]。而在异养型生物絮团模式中,则可以通过投入碳源刺激异养细菌同化作用,来控制亚硝酸盐氮的浓度,但养殖后期亚硝酸盐氮仍会缓慢积累[22],并且一旦停止输入碳源,亚硝酸盐氮会迅速上升,引起对虾的大量死亡。这与异养细菌对氨氮的利用率高于亚硝酸盐氮有关,并且氨氧化细菌一旦挂膜完成,其转化效率高于异养同化,这与谭洪新等[23]的研究相似。本实验中,由于亚硝酸盐氧化细菌挂膜完成,各密度养殖池中亚硝酸盐氮虽有出现,但浓度皆处于较低水平。其中B610密度组亚硝酸盐氮超出了安全浓度(0.24 mg/L),这与该组的投喂量较大,水中氮素水平较高有关。由于亚硝酸盐氮超出警戒范围,该组存活率较低,但差异性不显著。
完整的生物脱氮技术,是通过硝化作用将水体中的氨氮转化为硝酸盐氮后,再通过反硝化作用将硝酸盐氮转化为氮气脱出水体。但是由于反硝化作用一般要求低氧甚至厌氧环境,在水产养殖中很少涉及,主要是利用硝化作用将氨氮转化为硝酸盐氮,硝酸盐氮的毒性低于氨氮,且安全阈值较高(220 mg/L),因此可以接受一定程度硝酸盐氮的积累[7]。一般而言,硝化系统中硝酸盐氮应该是处于不断积累上升的,在本实验中,3个低密度组(B240、B130、B80)却出现了负增长,并且两个高密度组(B610、B450)的增长幅度也较小,这可能与每天的排污行为有关。实验过程中每天8:00和16:00各排污1次,可以去除水中的部分氮素,另外中心排污口下的管道会形成一个厌氧区域,会导致反硝化作用的出现,一部分硝酸盐氮被转化为氮气从水中逸出,因此低密度组硝酸盐氮出现了负增长,而高密度组由于投喂量较大,硝酸盐氮虽不断积累但涨幅较小。
综上所述,养殖密度在80~610尾/m3时,硝化型生物絮团系统对非离子氨和亚硝酸盐氮可以控制在警戒浓度(0.2 mg/L)上下,较为稳定,为凡纳滨对虾健康生长提供了良好的环境,保证养殖存活率,另外该系统下适当的排污可以避免高密度养殖下水体硝酸盐氮积累太快。
3.2 养殖密度对硝化型生物絮团系统中凡纳滨对虾生长的影响凡纳滨对虾的合理放养密度受到多种因素的影响,不同的养殖模式对水质的控制、病害的预防效果不同,这就造成了养殖密度的高低。在早期的凡纳滨对虾养殖中,粗放式养殖模式的养殖密度仅仅只有1~3尾/m3,之后使用半精养模式,养殖密度达到了8~10尾/m3[24]。凡纳滨对虾引进国内后,基于各地气候环境差异以及养殖模式的不同,养殖密度从50~300尾/m3不等[25]。
李倩等[21]使用传统的换水养殖模式探究凡纳滨对虾的适宜养殖密度,养殖67~118 d,养殖密度90~180尾/m3,存活率77.5%~89.6%,产量1.2~1.6 kg/m3,最佳养殖密度为150尾/m3。张许光等[22]报道了在异养型生物絮团系统养殖凡纳滨对虾,通过添加碳源来维持水质,养殖113 d,养殖密度200~600尾/m3,对虾的存活率为25.00%~75.30%,产量为1.53~4.01 kg/m3,最佳养殖密度为400尾/m3。刘鹰等[26]报道了利用循环水养殖系统,期间通过生物滤池维持水质,养殖86 d,养殖密度500~1500尾/m3,对虾存活率41.8%~86.3%,产量5.2~6.9 kg/m3,最佳养殖密度为1 000尾/m3。
本实验在硝化型生物絮团系统中养殖凡纳滨对虾,通过水体微生物的硝化反应来维持水质,养殖45 d,养殖密度80~610尾/m3,存活率61.94%~100.0%,产量0.48~1.93 kg/m3。其中B240组养殖后期地暖管破损,锅炉水流入养殖池中,水温和盐度的剧烈变化导致了凡纳滨对虾的大量死亡,因此实际存活率和产量偏低,由于该数据并非由养殖密度所致,去除该组数据比较,可以观察到存活率随养殖密度升高而降低,该结论与大量的研究[26-28]相似。另外去除B240组数据后,各组的存活率差异不显著,这表明在80~610尾/m3的密度范围内,产量随密度升高而增加。对比张许光等[22]对异养型生物絮团系统的研究,本实验的产量较低,但在本实验中表现出了更高的存活率,这与本系统以自养硝化细菌为主有关,相比异养细菌,自养硝化细菌处理能力更稳定。生物絮团系统对于水质的良好控制提高了养殖密度的上限,硝化型生物絮团系统更减少了碳源添加,使得养殖成本降低、养殖操作简化,但产量、存活率仍低于循环水养殖系统,这可能与循环水养殖系统拥有更好的氮素控制有关。不过相比循环水养殖系统高昂的投资成本,硝化型生物絮团系统也不失为一种更实惠的选择。
B240密度组的体长增长量和体重增加量是所有密度组中最高的,并且其终末个体的体长体重与B130、B80差异不显著,与B610、B450差异显著,并且B610组和B450组的体质量体长差异不显著。该实验中,凡纳滨对虾在80~250尾/m3密度范围内,体长体质量增长量随密度上升而增大,而450~610尾/m3密度范围内体长体质量增长显著较低。大部分研究[27-28]结果都表明凡纳滨对虾的生长与养殖密度呈负相关,即养殖密度越高,对虾的体长体质量增长越慢。不过本实验中,80~240尾/m3密度范围内凡纳滨对虾生长却和密度呈现正相关,这可能和生物絮团的营养补充作用有关。SCHVEITZER等[29]报道了对虾可以摄食生物絮团作为营养补充。本实验中初始絮团浓度(floc volume,Fv)都调整为30 mL/L,随着养殖的进行,由于投喂量的差异导致高密度组拥有更高的絮团量,凡纳滨对虾摄食生物絮团后获得了更多的营养,提高了生长速度。这在高密度组中也可以看出,B400组和B600组虽然由于密度胁迫效应导致了对虾生长出现抑制,但两者之间的差异并不显著,这表明生物絮团的营养补充作用仍然有效果。
综上所述,本实验表明,在硝化型生物絮团系统下放养80~610尾/m3的密度,存活率随密度升高而下降,但产量随密度升高而增加。
| [1] |
EMERENCIANO M, GAXIOLA G, CUZO G. Biofloc Technology (BFT): a review for aquaculture application and animal food industry[M]//MATOVIC M D. Biomass Now-Cultivation and Utilization. Rijeka: InTech, 2013.
|
| [2] |
高启.两种养殖模式下吉富罗非鱼的生长效果研究[D].上海: 上海海洋大学, 2013. GAO Q. Study on the breeding effect of tilapia in two Systems[D]. Shanghai: Shanghai Ocean University, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10264-1014013478.htm |
| [3] |
BURFORD M A, THOMPSON P J, MCINTOSH R P, et al. The contribution of flocculated material to shrimp (Litopenaeus vannamei) nutrition in a high-intensity, zero-exchange system[J]. Aquaculture, 2004, 232(1/4): 525-537. |
| [4] |
EBELING J M, TIMMONS M B, BISOGNI J J. Engineering analysis of the stoichiometry of photoautotrophic, autotrophic, and heterotrophic removal of ammonia-nitrogen in aquaculture systems[J]. Aquaculture, 2006, 257(1/4): 346-358. |
| [5] |
BRUNE D E, SCHWARTZ G, EVERSOLE A G, et al. Intensification of pond aquaculture and high rate photosynthetic systems[J]. Aquacultural Engineering, 2003, 28(1/2): 65-86. |
| [6] |
DE SCHRYVER P, CRAB R, DEFOIRDT T, et al. The basics of bio-flocs technology:the added value for aquaculture[J]. Aquaculture, 2008, 277(3/4): 125-137. |
| [7] |
KUHN D D, SMITH S A, BOARDMAN G D, et al. Chronic toxicity of nitrate to Pacific white shrimp, Litopenaeus vannamei:impacts on survival, growth, antennae length, and pathology[J]. Aquaculture, 2010, 309(1/4): 109-114. |
| [8] |
RAY A J, LOTZ J M. Comparing a chemoautotrophic-based biofloc system and three heterotrophic-based systems receiving different carbohydrate sources[J]. Aquacultural Engineering, 2014, 63: 54-61. DOI:10.1016/j.aquaeng.2014.10.001 |
| [9] |
BRAUN N, DE LIMA R L, BALDISSEROTTO B, et al. Growth, biochemical and physiological responses of Salminus brasiliensis with different stocking densities and handling[J]. Aquaculture, 2010, 301(1/4): 22-30. |
| [10] |
ELLIS T, NORTH B, SCOTT A P, et al. The relationships between stocking density and welfare in farmed rainbow trout[J]. Journal of Fish Biology, 2002, 61(3): 493-531. DOI:10.1111/j.1095-8649.2002.tb00893.x |
| [11] |
HUCHETTE S M H, KOH C S, DAY R W. Growth of juvenile blacklip abalone (Haliotis rubra) in aquaculture tanks:effects of density and ammonia[J]. Aquaculture, 2003, 219(1/4): 457-470. |
| [12] |
SAHIN K, YAZLAK H, ORHAN C, et al. The effect of lycopene on antioxidant status in rainbow trout (Oncorhynchus mykiss) reared under high stocking density[J]. Aquaculture, 2014, 418-419: 132-138. DOI:10.1016/j.aquaculture.2013.10.009 |
| [13] |
李玉全, 李健, 王清印, 等. 养殖密度对工厂化对虾养殖池氮磷收支的影响[J]. 中国水产科学, 2007, 14(6): 926-931. LI Y Q, LI J, WANG Q Y, et al. Effect of stocking density on input and output of nitrogen and phosphorus in super-intensive shrimp farming pond[J]. Journal of Fishery Sciences of China, 2007, 14(6): 926-931. DOI:10.3321/j.issn:1005-8737.2007.06.007 |
| [14] |
ALLAN G L, MAGUIRE G B. Effects of stocking density on production of Penaeus monodon Fabricius in model farming ponds[J]. Aquaculture, 1992, 107(1): 49-66. |
| [15] |
SOOKYING D, SILVA F S D, DAVIS D A, et al. Effects of stocking density on the performance of Pacific white shrimp Litopenaeus vannamei cultured under pond and outdoor tank conditions using a high soybean meal diet[J]. Aquaculture, 2011, 319(1/2): 232-239. |
| [16] |
李建, 姜令绪, 王文琪, 等. 氨氮和硫化氢对日本对虾幼体的毒性影响[J]. 上海水产大学学报, 2007, 16(1): 22-27. LI J, JIANG L X, WANG W Q, et al. The toxic effect of ammonia nitrogen and sulfurated hydrogen on the larvae of Penaeus japonicus[J]. Journal of Shanghai Fisheries University, 2007, 16(1): 22-27. |
| [17] |
刘健, 侯冬伟, 曾燊正, 等. 凡纳滨对虾封闭式养殖池塘水体氨氮、亚硝氮、硝氮变化规律及消减措施[J]. 中山大学学报(自然科学版), 2017, 56(6): 116-122. LIU J, HOU D W, ZENG S Z, et al. The change regularity and control measure of ammonia, nitrite and nitrate nitrogen in closed culture ponds of Litopenaeus vannamei[J]. Acta Scientiarum Naturalium Universitatis Sunyatseni, 2017, 56(6): 116-122. |
| [18] |
刘军, 戴习林, 臧维玲. 凡纳滨对虾温棚高位池养殖密度及简易水质调控措施效果研究[J]. 上海海洋大学学报, 2016, 25(2): 189-197. LIU J, DAI X L, ZANG W L. Research of breeding density and water quality control measures in Litopenaeus vannamei greenhouse high-intensive ponds[J]. Journal of Shanghai Ocean University, 2016, 25(2): 189-197. |
| [19] |
CHAND R K, SAHOO P K. Effect of nitrite on the immune response of freshwater prawn Macrobrachium malcolmsonii and its susceptibility to Aeromonas hydrophila[J]. Aquaculture, 2006, 258(1/4): 150-156. |
| [20] |
孔巧香, 李仁伟, 张宾, 等. 南美白对虾养殖水质理化因子的初步研究[J]. 环境化学, 2012, 31(11): 1823-1824. KONG Q X, LI R W, ZHANG B, et al. Preliminary study on physical and chemical factors of water quality in Penaeus vannamei culture[J]. Environmental Chemistry, 2012, 31(11): 1823-1824. |
| [21] |
李倩, 周志明, 杭小英, 等. 南美白对虾不同养殖密度水质变化规律与养殖效益的分析[J]. 中国农学通报, 2014, 30(2): 100-104. LI Q, ZHOU Z M, HANG X Y, et al. Analysis of water quality changes under different breeding density and breeding benefit of Penaeus vannamei[J]. Chinese Agricultural Science Bulletin, 2014, 30(2): 100-104. |
| [22] |
张许光, 赵培, 王国成, 等. 不同放苗密度凡纳滨对虾生物絮团养殖的环境和产出效应[J]. 渔业科学进展, 2013, 34(3): 111-119. ZHANG X G, ZHAO P, WANG G C, et al. The environmental and production effect of bio-floc aquaculture of Litopenaeus vannamei at different stocking densities[J]. Progress in Fishery Sciences, 2013, 34(3): 111-119. DOI:10.3969/j.issn.1000-7075.2013.03.015 |
| [23] |
谭洪新, 庞云, 王潮辉, 等. 驯化硝化型生物絮体养殖南美白对虾的初步研究[J]. 上海海洋大学学报, 2017, 26(4): 490-500. TAN H X, PANG Y, WANG C H, et al. Preliminary study on domesticating nitrifying bio-flocs to rear Litopenaeus vannamei[J]. Journal of Shanghai Fisheries University, 2017, 26(4): 490-500. |
| [24] |
张吕平, 胡超群, 沈琪, 等. 不同养殖密度对我国热带地区集约化养殖凡纳滨对虾水质和成活率的影响[J]. 热带海洋学报, 2011, 30(4): 85-91. ZHANG L P, HU C Q, SHEN Q, et al. Water quality and survival rate for intensive culture of white leg shrimp, Litopenaeus vannamei, under different cultural density in tropic area of China[J]. Journal of Tropical Oceanography, 2011, 30(4): 85-91. DOI:10.3969/j.issn.1009-5470.2011.04.013 |
| [25] |
赖秋明. 我国对虾养殖进程及养殖模式演变[J]. 海洋与渔业:水产前沿, 2011, 30(6): 37-40. LAI Q M. The process of shrimp culture and the evolution of culture mode in China[J]. Ocean & Fishery, 2011, 30(4): 85-91. |
| [26] |
刘鹰, 杨红生, 刘石林, 等. 封闭循环系统对虾合理养殖密度的试验研究[J]. 农业工程学报, 2005, 21(6): 122-125. LIU Y, YANG H S, LIU S L, et al. Experimental study on the approprite breeding density for the production of prawn in closed-recirculating system[J]. Transactions of the Chinese Society of Agricultural Engineering, 2005, 21(6): 122-125. DOI:10.3321/j.issn:1002-6819.2005.06.028 |
| [27] |
李玉全, 王仁杰, 姜令绪. 密度胁迫对日本囊对虾生长和水环境的影响[J]. 海洋科学, 2013, 37(10): 53-57. LI Y Q, WANG R J, JIANG L X. Effects of density-stress on water quality and growth of Marsupenaeus japonicus[J]. Marine Sciences, 2013, 37(10): 53-57. |
| [28] |
侯文杰, 臧维玲, 刘永士, 等. 室内凡纳滨对虾养殖密度对水质与生长的影响[J]. 安徽农业大学学报, 2010, 37(2): 284-289. HOU W J, ZANG W L, LIU Y S, et al. Effects of stocking densities on growth and water quality in Litopenaeus vannamei indoor culture[J]. Journal of Anhui Agricultural University, 2010, 37(2): 284-289. |
| [29] |
SCHVEITZER R, ARANTES R, COSTóDIO P F S, et al. Effect of different biofloc levels on microbial activity, water quality and performance of Litopenaeus vannamei in a tank system operated with no water exchange[J]. Aquacultural Engineering, 2013, 56: 59-70. DOI:10.1016/j.aquaeng.2013.04.006 |
2. Key Laboratory of Freshwater Aquatic Genetic Resources, Ministry of Agriculture and Rural Affairs, Shanghai Ocean University, Shanghai 201306, China;
3. National Demonstration Center for Experimental Fisheries Science Education, Ministry of Education, Shanghai Ocean University, Shanghai 201306, China
 2020,
Vol. 29
2020,
Vol. 29


