双斑东方鲀(Takifugu bimaculatus)属鲀形目(Tetraodontiformes),东方鲀科(Tetraodontidae),东方鲀属(Takifugu),为近海暖温性底层鱼类,仅分布于我国南海、东海和黄海南部[1]。双斑东方鲀肉鲜嫩可口,营养价值高。野生种群的肝脏、生殖腺和血液剧毒,具有极高的农药用和医用价值[2]。目前双斑东方鲀的全人工繁育技术已经成熟,苗种已可批量生产[3-4]。
鱼类三倍体育种属于“染色体组工程”,它的不育性具有可在任何水域养殖的潜力,不会干扰自然界的种质资源,加上生长速度快、寿命长、肉质好、成活率高等优点,具有广阔的应用前景[5]。
有关双斑东方鲀的倍性研究已有温度休克这一种方法[6],但尚未能用于规模化生产。静水压法在大黄鱼、半滑舌鳎等鱼类的三倍体研究中已有所应用[7-11],但在双斑东方鲀尚未见有报道。本文采用静水压法诱导双斑东方鲀三倍体,为双斑东方鲀三倍体育苗生产提供另一可行途径,为将来更全面地开展双斑东方鲀乃至其他东方鲀类鱼类的规模化三倍体育苗提供重要的实践和理论资料。
1 材料与方法 1.1 材料实验用双斑东方鲀亲鱼为购自浙江省台州市三门县海域的野生2龄鱼,体质量约为350~400 g。用宁波第二激素厂生产的LRH-A2和HCG混合使用进行胸鳍基部注射催产,干法授精。从受精、孵化到苗种培育整个过程的水温控制在18~20 ℃。
1.2 方法 1.2.1 亲鱼培育、催产、受精亲鱼培育于深水池塘网箱中,饵料以消毒后新鲜贝类为主,搭配配合饲料,饲料中添加鱼用维生素E,促进性腺成熟。
对已达性成熟的亲鱼采用10 μg LRH-A2+200单位HCG/kg一次性胸鳍基部注射,干法授精,受精后用滑石粉作脱粘处理。
1.2.2 静水压处理在18~20 ℃的温度下,用孔径250 μm(60目)筛绢将受精卵(湿质量295~305 g)滤出,浓缩收集在密封容器中,放置于静水压仪(项目组自行研制)的压力缸中,缸中放满液压油。在相同的温度条件下,采用静水压处理的压力强度分别为5、10、15、20、30 MPa;根据作者2005年研究成果[6],在授精后5 min进行三倍体诱导处理,处理的持续时间为3、5、7、10、15 min,另设对照组(人工受精后直接进行孵化,不经静水压处理)。
1.2.3 受精卵孵化将诱导后的受精卵分组置于孔径250 μm(60目)筛绢网制成的体积0.25 m3的锥形网箱中孵化(孵化密度≤1 kg/m3)。网箱固定于水泥池中,80 %箱体浸于水中,箱底不与池底接触,网箱中放置气石强烈充气使卵不沉底,并保持微流水。各处理组和对照组在相同条件下进行正常孵化、培育,分别计算其孵化率,养至全长2 cm左右每组抽样30尾测苗种三倍体诱导率。
1.2.4 倍性鉴定与数据分析以小公鸡血红细胞为参照,流式细胞法[12]检测实验动物不同实验组血红细胞中的DNA的相对含量,计算出实验动物不同实验组的染色体倍型。在相同的流式细胞术条件下,测得鸡血红细胞的相对DNA含量为105,二倍体对照DNA相对含量为33,三倍体DNA相对含量为50(如图 1)。三倍体检出个体数与总检测个体比值数即为三倍体诱导率。

|
图 1 流式细胞仪检测DNA含量
Fig. 1 Flow cytometric analysis for DNA content
(a)鸡血红细胞DNA相对含量;(b)东方鲀二倍体DNA相对含量;(c)东方鲀三倍体DNA相对含量 (a) cock erythrocyte; (b) T. bimaculatus diploid erythrocyte; (c) T. bimaculatus triploid erythrocyte |
利用Excel 2007和SPSS 16.0软件对所得数据进行统计分析。其中,不同处理组间孵化率的差异用方差分析法检验,组间诱导率的差异用卡方检验法。
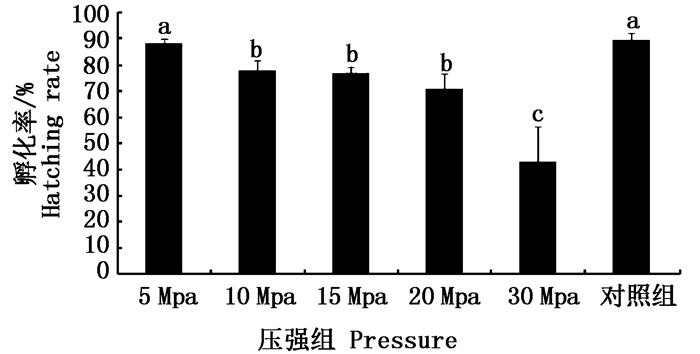
2 结果 2.1 不同压强条件对三倍体诱导效果的影响本实验在不同压强处理下的双斑东方鲀和对照组的孵化率存在极显著差异(F=22.28,P < 0.01,图 2),除5 Mpa处理组外,其他各处理组均显著低于对照组,且随压强增大有递减趋势,30 Mpa处理组的孵化率仅为对照组的一半。但在10、15和20 Mpa处理条件下的存活率无显著差异。
|
图 2 不同压强处理条件双斑东方鲀的孵化率
Fig. 2 T. bimaculatus hatching rate under different pressure
|
5个处理组经后期培育后进行三倍体倍性检测,结果表明不同处理组的诱导率间存在显著差异(X2=66.1,P < 0.01, 图 3),其中5 Mpa处理组的三倍体诱导率偏低(仅40%),其余各组均高于96%。

|
图 3 不同压强处理条件双斑东方鲀的三倍体诱导率
Fig. 3 T. bimaculatus triploid induction rate under different pressure
|
本实验选取10 Mpa作为压强条件,观察发现不同处理时间条件及其与对照组的孵化率均存在极显著差异(F=13.05,P < 0.01,图 4),且各处理组的孵化率均显著低于对照组,其中15 min处理组的孵化率仅为对照组的71%。

|
图 4 不同处理时间条件下双斑东方鲀三倍体的孵化率
Fig. 4 T. bimaculatus hatching rate under different pressure duration
|
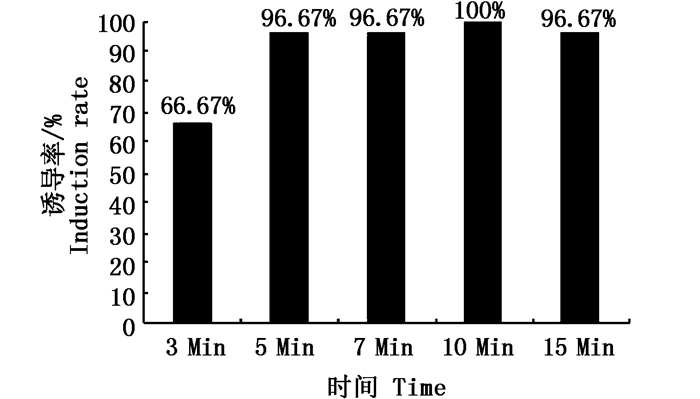
通过对每个处理组均随机抽样30尾进行三倍体检测,发现各处理组间的三倍体诱导率有显著差异(X2=29.1,P < 0.01,图 5)。其中3 min处理组的三倍体诱导率最低(仅66.67 %),而其余各组均高于96 %。
|
图 5 不同处理时间条件下双斑东方鲀的三倍体诱导率
Fig. 5 T. bimaculatus triploid induction rate under different pressure duration
|
三倍体鱼类具有性腺不能发育成熟、控制过度繁殖、促进生长以及提高鱼肉品质等优点,受到广大科研人员和养殖户的欢迎,人工诱导三倍体具有广阔的生态、经济应用前景。用人工的方法获得三倍体可通过两条途径,一条是直接途径,即用物理或化学的方法对受精卵进行处理,阻碍第二极体外排;另一条是间接途径,即首先诱导获得四倍体,待四倍体个体性成熟后再与二倍体个体自然交配,获得三倍体[13]。本文采用直接途径中物理方法进行三倍体诱导。
作者于2005年通过温度休克的方法获取了双斑东方鲀的三倍体苗种,虽然获得了较高的诱导率,但是可能由于温度休克时受精卵受损导致孵化率偏低,处理组最高孵化率才61%[6]。据国内其他鱼类三倍体的研究显示,静水压法与温度休克法相比可获得较高的诱导率和孵化率[7-8、14]。本实验中静水压的诱导效果也同样优于温度休克法,压强20 Mpa以内,处理时间10 min以内孵化率均大于70 %,并且在处理时间5~10 min,压强10~20 Mpa这些条件下,诱导率均达96 %以上。
3.2 静水压法诱导三倍体的最佳条件静水压法是一种有效的三倍体物理诱导方法,其诱导效果受处理起始时间、处理压强、处理持续时间三个条件制约。本实验处理起始时间采用先前的研究成果,作者在2005年时掌握了双斑东方鲀苗种的三倍体温度休克方法,摸清了其胚胎发育进度,认为在授精后5 min进行三倍体诱导能达到最佳效果[6]。因此,在孵化温度一致的前提下,采用5 min作为处理起始时间。
在寻找最佳处理压强条件时,预实验使用30 Mpa处理5 min,发现有受精卵受损的情况,于是最高压强选取了30 Mpa。实验结果显示,在处理持续时间为5 min时,压强为5 Mpa时诱导率较低,仅为40%,但孵化率接近对照组;处理压强为10~30 Mpa时,所得东方鲀苗种的三倍体诱导率均达96 %以上,其中15 Mpa时达到100 %;孵化率随着压强的增大呈递减趋势,当压强为30 Mpa时,孵化率仅为对照组的43 %。结果表明受精卵在30 Mpa受压过程中受损较为严重,5 Mpa时压强太小没有达到相应的诱导效果。因此,作者认为压强处理宜为10~15 Mpa,在该范围内孵化率达77 %以上,诱导率达96 %以上。这一处理压强与其他鱼类的三倍体最适处理压强稍有不同[7-11],与它们相比普遍较低,这可能是由于不同鱼类受精卵对压力刺激敏感性不尽相同,从而造成了耐受压力的差异。
在寻找最佳处理持续时间时,采用前期实验成果——压强10 Mpa,起始处理时间5 min,分别处理了3、5、7、10、15 min 5组。实验结果显示,3~7 min处理持续时间中,孵化率均能达到77 %以上,5~15 min组诱导率可达96%以上。由此可见,较短的处理时间虽然孵化率较高但达不到较理想的诱导率,较长的处理时间却相反,也就是说短时间内受精卵受损较轻,但是达不到诱导刺激效果,长时间虽然能达到较好的诱导率但是受精卵受压受损会导致孵化率降低,因此,5~7 min的处理持续时间对于双斑东方鲀来说是最佳的条件,既保障了诱导率又能有较高的孵化率。这一结果与鲆鲽类[9]的结果是一致的,而比半滑舌鳎[8]、水晶彩鲫[10]、大黄鱼[11]等稍长了一些。
3.3 静水压法诱导三倍体的优势静水压法属于物理诱导方法,诱导三倍体过程中没有用到秋水仙素、细胞松弛素等化学药品,有效避免了药物残留对环境的影响,确保水产品质量安全;采用直接方法诱导出三倍体,该三倍体的不育性可以防止养殖鱼类对天然鱼群基因库的遗传干扰,对保护天然种质资源也具有极其重要的意义;静水压法虽然比温度休克法需要更专门的设备,但其处理的最佳条件易于掌握,程序较为标准化,是一个值得推广的有效方法。
4 结论本实验研究采用静水压法诱导双斑东方鲀三倍体,筛选出了诱导双斑东方鲀的最佳条件:处理起始时间为授精后5 min,处理压强为10~15 Mpa,处理持续时间为5~7 min,在此条件下三倍体诱导率可达96 %以上,受精卵孵化率也能达77%以上。本文首次建立了双斑东方鲀的三倍体苗种的静水压诱导法,填补了我国通过静水压法诱导东方鲀三倍体的空白,不仅丰富了双斑东方鲀苗种的三倍体诱导方法,在保证高诱导率的条件下,使其孵化率得到显著提高,并可为其他东方鲀多倍体育种研究提供参考。
| [1] |
《福建鱼类志》编写组. 福建鱼类志[M]. 福州: 福建科学技术出版社, 1984: 606-607.
"Fishes of Fujian Province" Editorial Subcommittee. The Fishes of Fujian Province[M]. Fuzhou: Fujian Science and Technology Press, 1984: 606-607. |
| [2] |
钟建兴, 许鼎盛, 陈有铭, 等. 双斑东方鲀人工繁殖及育苗技术[J].
台湾海峡, 2002, 21(3): 305–309.
ZHONG J X, XU D S, CHEN Y M, et al. Study on artificial propagation and breeding technique of Fugu bimaculatus[J]. Journal of Oceanography in Taiwan Strait, 2002, 21(3): 305–309. |
| [3] |
蔡志全, 刘韬, 林永泰, 等. 双斑东方鲀人工繁殖及苗种培育技术的研究[J].
水利渔业, 2004, 24(2): 28–30.
CAI Z Q, LIU T, LIN Y T, et al. Study on the artificial propagation and larval rearing of Fugu bimaculatus[J]. Reservoir Fisheries, 2004, 24(2): 28–30. |
| [4] |
钟建兴. 双斑东方鲀生物学特性及繁养殖技术[J].
海洋科学, 2003, 27(9): 8–12.
ZHONG J X. The biological characteristic and propagation-culturing technique of Fugu bimaculatus[J]. Marine Sciences, 2003, 27(9): 8–12. |
| [5] |
孙远东, 谭立军, 唐新科, 等. 鱼类人工多倍体育种的研究进展[J].
现代生物医学进展, 2008, 8(9): 1778–1779.
SUN Y D, TAN L J, TANG X K, et al. Research progress on fish artificially induced polyploidy[J]. Progress in Modern Biomedicine, 2008, 8(9): 1778–1779. |
| [6] |
尤颖哲. 双斑东方鲀三倍体苗种培育研究[J].
中国水产, 2005: 65–67.
DOI:10.3969/j.issn.1002-6681.2005.12.043 YOU Y Z. Study on triploid fry breeding of Takifugu bimaculatus[J]. China Fisheries, 2005: 65–67. DOI:10.3969/j.issn.1002-6681.2005.12.043 |
| [7] |
许建和, 尤峰, 吴雄飞, 等. 冷休克法和静水压法人工诱导大黄鱼三倍体[J].
中国水产科学, 2006, 13(2): 206–210.
XU J H, YOU F, WU X F, et al. Artificial induction of triploidy Pseudosciaena crocea by cold and hydrostatic pressure shock[J]. Journal of Fishery Sciences of China, 2006, 13(2): 206–210. |
| [8] |
陈松林, 李文龙, 季相山, 等. 半滑舌鳎三倍体鱼苗的人工诱导与鉴定[J].
水产学报, 2011, 35(6): 925–931.
CHEN S L, LI W L, JI X S, et al. Induction and identification of artificial triploid fry in Cynoglossus semilaevis[J]. Journal of Fisheries of China, 2011, 35(6): 925–931. |
| [9] |
刘金相, 王旭波, 刘聪辉, 等. 静水压法人工诱导牙鲆(♀)×圆斑星鲽(♂)杂交三倍体的探索[J].
中国海洋大学学报, 2014, 44(2): 41–47.
LIU J X, WANG X B, LIU C H, et al. Induction of triploid hybrid of Japanese flounder (Paralichthys olivaceus, ♀)×spotted halibut (Verasper variegatus, ♂) by hydrostatic pressure shocks[J]. Periodical of Ocean University of China, 2014, 44(2): 41–47. |
| [10] |
桂建芳, 梁绍昌, 孙建民, 等. 鱼类染色体组操作的研究:Ⅰ.静水压休克诱导三倍体水晶彩鲫[J].
水生生物学报, 1990, 14(4): 336–344.
GUI J F, LIANG S C, SUN J M, et al. Studies on genome manipulation in fish:Ⅰ. Induction of triploid transparent colored crucian carp (Carassius auratus transparent colored variety) by hydrostatic pressure[J]. Acta Hydrobiologica Sinica, 1990, 14(4): 336–344. |
| [11] |
林琪, 吴建绍, 曾志南. 静水压休克诱导大黄鱼三倍体[J].
海洋科学, 2001, 25(9): 6–9.
LIN Q, WU J S, ZENG Z N. Induction of triploid in Pseudosciaena crocea by hydrostatic pressure[J]. Marine Sciences, 2001, 25(9): 6–9. |
| [12] |
高静, 黄晓红, 曾华嵩, 等. 中国6种经济鱼类的基因组大小测定[J].
中国水产科学, 2010, 17(4): 689–694.
GAO J, HUANG X H, ZENG H S, et al. Genome size for six commercially important fishes in China[J]. Journal of Fishery Sciences of China, 2010, 17(4): 689–694. |
| [13] |
薛良义. 鱼类的三倍体育种[J].
生物学通报, 1996, 31(11): 8–10.
XUE L Y. Triploid breeding of fish[J]. Bulletin of Biology, 1996, 31(11): 8–10. |
| [14] | PERUZZI S, CHATAIN B. Pressure and cold shock induction of meiotic gynogenesis and triploidy in the European sea bass, Dicentrarchus labrax L.:relative efficiency of methods and parental variability[J]. Aquaculture, 2000, 189(1/2): 23–37. |
 2017,
Vol. 26
2017,
Vol. 26

