污水污泥是污水处理后的产物,随着污水处理厂的不断建成和污水处理能力的不断提高,污水污泥的产生量也越来越多。同时,对含有大量水分和污染物的污水污泥的处理难度也越来越大,对于一些靠海的国家和地区,污泥投海曾经是一种既节约费用又可以较好地处理污泥的方法,但这种方法最后被禁止使用,其关键原因是污泥中的污染物会危害海洋生态系统[1],特别是重金属的危害更为严重[2]。虽然很多国家已经明确禁止污水污泥投海,但是已经投入海洋中的污水污泥仍然对海洋环境产生了不良的影响。因此,研究海水环境下影响污泥中重金属浸出的主要因素不仅对污泥的合理处置有指导意义,同时对海洋环境保护和海洋环境质量评价和评估也具有实际参考价值[3]。pH、温度、盐度、氧化还原电位和微生物活动等是影响重金属从污泥中浸出的主要因素[4, 5, 6],其中李娟英等[7]已经就pH对污泥中包括重金属在内的污染物浸出的影响有过相关的报道,提出偏酸和偏碱性的海洋水体环境会刺激Zn、Cd、Pb和As等从污水污泥中浸出。然而诸如温度、盐度等海水条件对重金属浸出的影响以及变化规律的研究并不完善,而这直接涉及到污水污泥处置季节和处置地点的选择。本文通过研究温度、盐度以及微生物活动等因素对污水污泥中重金属浸出的影响规律,对该领域的基础研究进行补充,完善海洋中污水污泥污染物浸出的相关数据,并为污泥合理处置和海洋生态环境保护提供数据依据。
1 材料与方法 1.1 实验材料实验污泥取自于上海浦东新区、嘉定区、宝山区、南汇区、金山区5个区的7个污水处理厂(分别用S1、S2、S3、S4、S5、S6、S7表示)。污泥的保存及使用参照ISO5667-15:2009[8]进行。实验中所用清洁海水(盐度16±0.3、pH为7.5±0.4)取自上海洋山港,不同盐度的人工海水为盐卤与蒸馏水按不同比例配制而得,均通过0.45 μm的纤维滤膜后使用。
1.2 实验方法在水温和盐度这两个因素对污水污泥中重金属浸出的影响实验中,沉积物浸出液获取方法采用改进的HJ557—2010水平振荡法,具体实验操作条件如表1和表2所示。

|
表1 不同温度下污水污泥中重金属浸出的实验条件 Tab. 1 The experimental conditions about the influence of temperature on the leaching of heavy metals in sewage sludge |
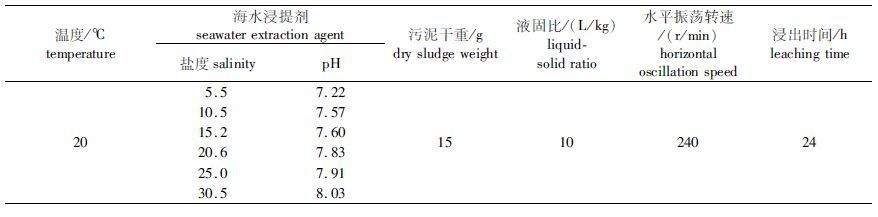
|
表2 不同盐度下污水污泥中重金属浸出的实验条件 Tab. 2 The experimental conditions about the influence of salinity on the leaching of heavy metals in sewage sludge |
测定微生物活动对污水污泥中污染物浸出的影响时,每个地点取适量污泥,分为两份,将其中一份通过高温高压进行灭菌,参考LORS等[6]给出的实验方法,其中对污水污泥进行水平振荡的时间和液固比分别为16天和10 L/kg。污泥浸出液中重金属指标的测定,参照GB17378.4—2007相应标准进行。
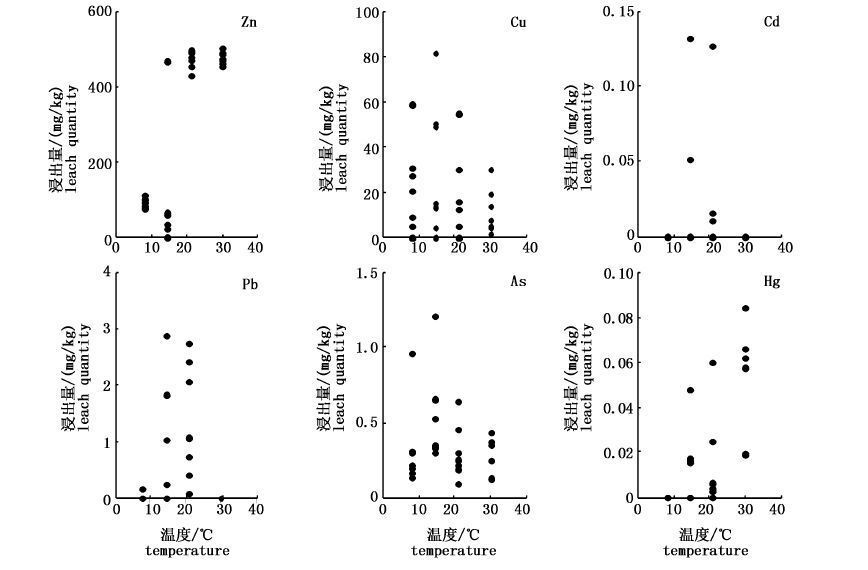
2 结果与讨论 2.1 水温对污水污泥中重金属浸出的影响由于各个污水处理厂污水处理规模、处理工艺及污水中工业废水比例不尽相同,因此不同污泥样品在相同温度下重金属浸出量也会有所差异,但此处着重研究重金属浸出的变化趋势,差异对趋势变化影响很小。不同的海水水温条件对7处污水处理厂的污水污泥中重金属浸出的影响结果如图1所示。由图1可知,Zn的浸出量最高,Cu次之,而后是Pb和As,Cd和Hg的浸出量最低,这与Zn和Cu在污水污泥中的总量较高且具有良好的迁移性有关[9] 。另外,大体上Zn和Hg的浸出量随水温的升高而增高,其中Hg的浸出量变化较小;其余4种重金属的浸出量随水温升高变化不大,在中偏低温或中温(14.5 ℃或21 ℃)浸出量略高。
|
图1 污泥中重金属的浸出量与温度的关系 Fig.1 The relationship between temperature and leaching ability of heavy metals in sewage sludge samples |
廖文卓[4]指出温度影响着重金属浸出的速度,一般情况下,随着温度的升高重金属的释放率增大,这与本实验中浸出量最大的Zn所表现的结果相一致。SCHUHMACHER等[10]指出某种温度依赖型细菌随着温度升高将Hg化合物转化生成二甲基Hg的速率增大,因此这可能是Hg的浸出量随温度升高而增高的另一个原因。张再利[11]指出存在于污泥中的氧化亚铁硫杆菌和氧化硫硫杆菌的最适生长温度分别为25~30 ℃和25~35 ℃,因此,Zn在21 ℃和30 ℃浸出量最高不仅仅与其水溶态和可交换离子态随温度的升高而释放得多有关,还与这个温度适合于硫杆菌生长而使得更多的硫化物结合态Zn转变为可溶性Zn有关。
其余4种浸出量随温度变化不大的重金属,其中对于易被污泥吸附的Cd和Pb而言[3, 12],中温和中偏高温(21 ℃和30 ℃)时污泥中其水溶态和可交换离子态释放得较快,以至于可能在24 h内就已经到达释放最大值并被污泥重新吸附,故而21 ℃时二者的浸出量和14.5 ℃时差不多且30 ℃时二者的浸出量略低;而Cu和As在14.5 ℃时的浸出量略高可能是因为其有机结合态转换为水溶态或可交换离子态[13]。
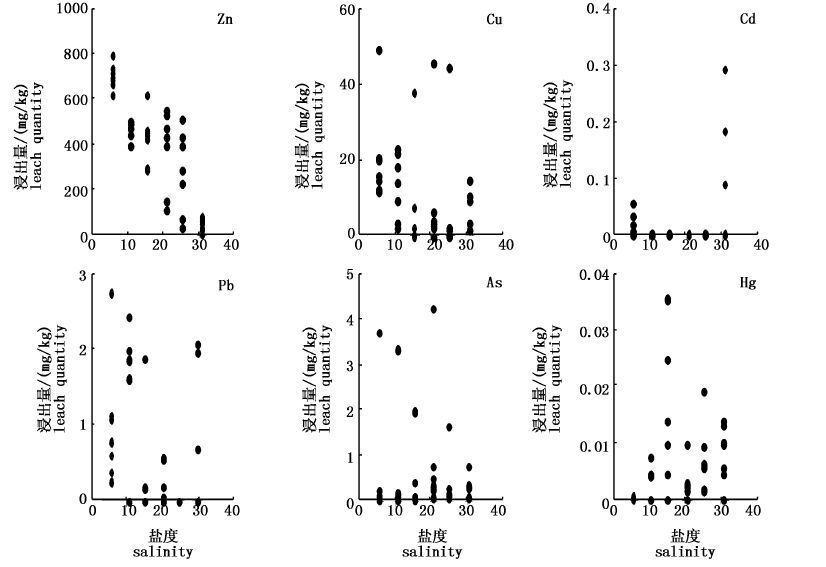
2.2 盐度对污水污泥中重金属浸出的影响不同的海水盐度条件对7处污水处理厂的污水污泥中重金属浸出的影响结果如图2所示。由图2可以看出,6种重金属中Zn的浸出量最高,但是总体上来说,污水污泥中重金属的浸出量随着盐度的升高而降低,而由于污泥中Cd和Hg的浸出量较低,盐度对它们的浸出影响没有表现出明显的规律特征。但是它们相对于Cu和Zn等生命必需微量元素来说,往往对生物和人体具有很大的毒害作用[14],因此也应引起密切关注。
|
图2 污泥中重金属的浸出量与盐度的关系 Fig.2 The relationship between salinity and leaching ability of heavy metals in sewage sludge samples |
Zn的浸出量随盐度的升高而降低,可能是因为低盐度时水中电解质浓度不高,海水中本身存在以及污泥浸出的胶体粒子不容易发生絮凝,浸出的重金属就不容易被富集而沉淀[15]。Cu和Pb的浸出量大致与Zn相似,而在盐度30.5时二者浸出量又略有增高可能与一定量的氯离子对重金属形成氯络合物的能力强于污泥和胶体粒子对重金属的吸附能力[16]有关。As浸出量中等且浸出量随盐度的升高而降低的趋势并不是特别明显。结果显示,不同重金属对盐度的变化有不同的浸出反应。其中的原因也存在不同的解释,有人认为海水中盐度的改变可以改变污泥的絮凝性,从而对污泥中重金属的约束能力发生变化。还有一些学者认为盐度的变化可以影响微生物代谢酶的活性,从而影响了微生物对重金属的作用[17]。
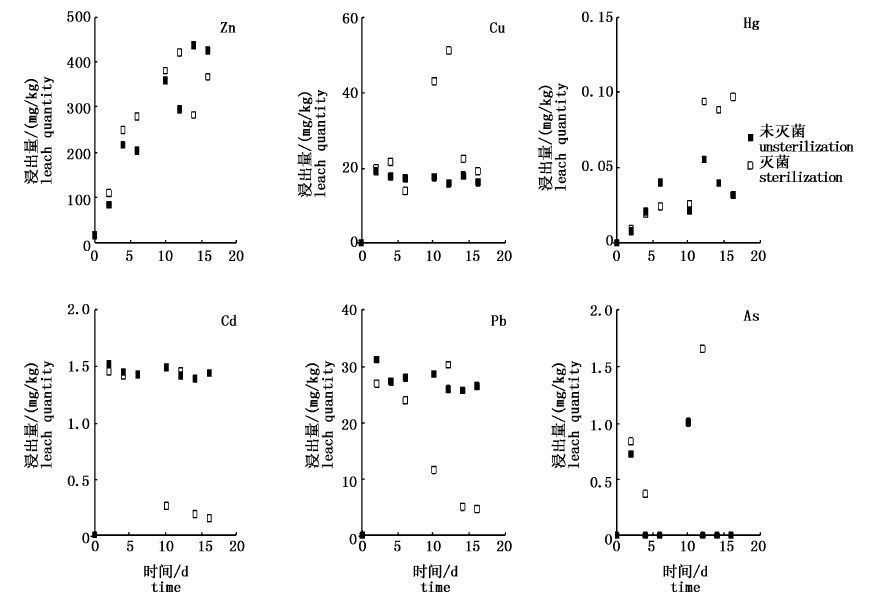
2.3 微生物活动对污水污泥中重金属浸出的影响通过测定灭菌和未灭菌的污水污泥浸出液中重金属的浸出情况,发现其中Zn、Cu、Hg 3种重金属的浸出趋势大致相同(图3),随时间增加浸出量基本上呈先增高后平衡的趋势,且重金属浸出量总体上表现为灭菌高于未灭菌,与LORS等[6]的研究结果一致。而Cd和Pb浸出量随时间增加的变化规律相似(图3),都表现为浸出趋势不统一,二者的浸出量总体上表现为未灭菌高于灭菌,其中Cd的比较结果与LORS等[6]的研究结果一致。对于浸出量较低的As,大部分污泥样品随时间增加一直没有浸出,只有未灭菌的S1和灭菌的S1、S5、S6有浸出,且灭菌的浸出量高于未灭菌,但并未表现出比较明显的规律性。
|
图3 微生物活动对重金属浸出的影响 Fig.3 The relationship between microbial activities and leaching ability of heavy metals in sewage sludge samples |
对于Zn、Cu、Hg这3种重金属,未灭菌时,微生物可吸附或主动吸收重金属,将重金属富集在细胞表面或内部[18];Cu主要存在于硫化物及有机结合态中,Zn也有相当比例存在于此形态中,灭菌不仅使死亡的微生物细胞不能富集重金属,还会将本来有机物结合态的重金属随着DOC的释放而释放出来[3]。对于主要存在于残渣态中的Hg,灭菌可能对其残渣态造成了一定影响,故而能够释放出一部分Hg。而对于Cd和Pb,有研究发现[19],灭菌后沉积物中水溶态、可交换离子态、碳酸盐结合态Cd含量较未灭菌时低,未灭菌时Pb、Cd的浸出量高于灭菌时可能与此有关。污水污泥中可能存在有机物氧化、生物硝化、生物反硝化、生物除磷等生化过程,在这些过程中微生物起到了重要的作用[20]。微生物生长机理复杂,并且重金属具有不同的形态及吸附状态,因此微生物在污泥中重金属的浸出中具有重要的影响。
3 结论(1)不同季节海水温度不同,对污水污泥中不同重金属的浸出影响不同。污水污泥样品中Zn和Hg在温度较高时释放较多,而Cu、Cd、Pb和As在低温时释放较多。
(2)不同海域海水盐度不同对污水污泥中重金属浸出的影响也不同。Zn、Cd、Cu和Pb的浸出量随盐度增加而下降,因此在近岸低盐度海域海水中浸出量可观;而As和Hg浸出量随盐度变化不大。
(3)细菌活性对Zn、Cu、Hg和As在海水中浸出量的影响较大,灭菌后污水污泥中重金属的浸出量明显增大。
| [1] | 蒋成爱, 黄国锋, 吴启堂. 城市污水污泥处理利用研究进展[J]. 农业环境与发展, 1999, 16(1): 13-18. JIANG C A, HUANG G F, WU Q T. Advance of municipal sewage sludge treatment and utilization[J]. Agro-Environment and Development, 1999, 16(1): 13-18. |
| [2] | 田慧娟, 刘吉堂, 吕海滨, 等. 海洋疏浚物对连云港局部海域生态环境的影响评价[J]. 上海海洋大学学报, 2015, 24(3): 414-421. TIAN H J, LIU J T, LV H B, et al. Evaluation of the impact of ocean dredged materials upon the ecology and environment in certain Lianyungang sea areas[J]. Journal of Shanghai Ocean University, 2015, 24(3): 414-421. |
| [3] | 王菊英. 海洋沉积物的环境质量评价研究[D]. 青岛: 中国海洋大学, 2004. WANG J Y. Study on environmental quality assessment of marine sediment[D]. Qingdao: Ocean University of China, 2004. |
| [4] | 廖文卓. 疏浚物中镉释放的影响条件[J]. 台湾海峡, 2000, 19(2): 170-176. LIAO W Z. Influence conditions of Cd release in dredged sediments[J]. Journal of Oceanography in Taiwan, 2000, 19(2): 170-176. |
| [5] | CANTWELL M G, BURGESS R M, KING J W. Resuspension of contaminated field and formulated reference sediments Part I: Evaluation of metal release under controlled laboratory conditions[J]. Chemosphere, 2008, 73(11): 1824-1831. |
| [6] | LORS C, TIFFREAU C, LABOUDIGUE A. Effects of bacterial activities on the release of heavy metals from contaminated dredged sediments[J]. Chemosphere, 2004, 56(6): 619-630. |
| [7] | 李娟英, 陈洁芸, 曹宏宇, 等. pH 对污水污泥中污染物浸出的影响[J]. 环境工程学报, 2013, 7(12): 4983-4989 LI J Y, CHEN J Y, CAO H Y, et al. Influence of pH on leaching of pollutants from sewage sludge[J]. Chinese Journal of Environmental Engineering, 2013, 7(12): 4983-4989 |
| [8] | BRITISH STANDARDS INSTITUTION. ISO 5667-15: 2009, Guidance on the preservation and handling of sludge and sediment samples[S]. Britain: British Standards Institution, 2009. |
| [9] | 王利军, 卢新卫, 雷凯. 宝鸡城市街尘、土壤及河流沉积物重金属形态迁移特征[J]. 城市环境与城市生态, 2011, 24(1): 22-26. WANG L J, LU X W, LEI K. Speciation and transfer of heavy metals in street dust, soil and river sediment of Baoji city[J]. Urban Envirnoment & Urban Ecology, 2011, 24(1): 22-26. |
| [10] | SCHUHMACHER M, DOMINGO J L, LLOBET J M, et al. Evaluation of the effect of temperature, pH, and bioproduction on Hg concentration in sediments, water, molluscs and algae of the delta of the Ebro river[J]. Science of the Total Environment, 1993, 134(s): 117-125. |
| [11] | 张再利. 氧化亚铁硫杆菌与氧化硫硫杆菌的特性及应用研究[D]. 广州: 中山大学, 2007. ZHANG Z L. Study on the characteristics and applications of Thiobacillus ferrooxidans and Thiobacillus thiooxidans[D]. Guangzhou: Zhongshan University, 2007. |
| [12] | 田冬梅, 李延升, 宋学君, 等. 城市污泥中痕量Cd活性形态的分析[J]. 环境科学与技术, 2005, 28(6): 14-15, 18. TIAN D M, LI Y S, SONG X J, et al. Trace Cadmium mobility analysis as a consequence of sewage sludge disposal[J]. Environmental Science & Technology, 2005, 28(6): 14-15, 18. |
| [13] | TSAI L J, YU K C, CHEN S F, et al. Effect of temperature on removal of heavy metals from contaminated river sediments via bioleaching[J]. Water Research, 2003, 37(10): 2449-2457. |
| [14] | 滑丽萍, 华珞, 高娟, 等. 中国湖泊底泥的重金属污染评价研究[J]. 土壤, 2006, 38(4): 366-373. HUA L P, HUA L, GAO J, et al. Heavy metal pollution of sediments of lakes in China[J]. Soils, 2006, 38(4): 366-373. |
| [15] | 许昆灿, 黄水龙, 吴丽卿. 长江口沉积物中重金属的含量分布及其与环境因素的关系[J]. 海洋学报, 1982, 4(4): 440-449. XU K C, HUANG S L, WU L Q. Studies of heavy metals in the estuarine sediments of the Changjiang River[J]. Acta Oceanologica Sinica, 1982, 4(4): 440-449. |
| [16] | HATJE V, PAYNE T E, HILL D M, et al. Kinetics of trace element uptake and release by particles in estuarine waters: Effects of pH, salinity, and particle loading[J]. Environment International, 2003, 29(5): 619-629. |
| [17] | 陈纯. 污泥对重金属离子的吸附的研究及其对高盐废水的处理[D]. 郑州: 郑州大学, 2005. CHEN C. Study of sewage sludge for biosorption of heavy metals and treatment of high salt wastewater[D]. Zhengzhou: Zhengzhou University, 2005. |
| [18] | 郭学军, 黄巧云, 赵振华, 等. 微生物对土壤环境中重金属活性的影响[J]. 应用与环境生物学报, 2002, 8(1): 105-110. GUO X J, HUANG Q Y, ZHAO Z H, et al. Effects of microorganisms on the mobility of heavy metals in soil environment[J]. Chinese Journal of Applied and Environmental Biology, 2002, 8(1): 105-110. |
| [19] | 朱维晃, 黄廷林, 柴蓓蓓, 等. 水源水库沉积物中重金属形态分布特征及其影响因素[J]. 环境化学, 2010, 29(4): 629-635. ZHU W H, HUANG T L, CHAI B B, et al. Influence of the environmental conditions on the speciation of heavy metals in the reservoir sediment[J]. Environmental Chemistry, 2010, 29(4): 629-635. |
| [20] | 孙培德, 宋英琦. 基于微生物相互作用机理的完全耦合活性污泥模型研究[J]. 环境科学学报, 2006, 26(9): 1559-1567. SUN P D, SONG Y Q. Study on full coupled activated sludge model (FCASM) based on coupling interaction mechanism of microorganisms[J]. Acta Scientiae Circumstantiae, 2006, 26(9): 1559-1567. |
 2016, Vol. 25
2016, Vol. 25


