扩展功能
文章信息
- 欧阳轶强, 胡冰, 张莹, 罗少仕, 梁锦宁, 李家富, 郭松超
- OUYANG Yiqiang, HU Bing, ZHANG Ying, LUO Shaoshi, LIANG Jinning, LI Jiafu, GUO Songchao
- 阿尔茨海默病树鼩模型建立的探索
- Establishment of the Alzheimer's Disease Model in Tupaia belangeri
- 四川动物, 2016, 35(2): 270-274
- Sichuan Journal of Zoology, 2016, 35(2): 270-274
- 10.11984/j.issn.1000-7083.20150284
-
文章历史
- 收稿日期: 2015-09-17
- 接受日期: 2015-12-15
2. 广西医科大学生物靶向诊治研究中心, 南宁 530021
2. Biological Targeting Therapy & Diagnosis Center of Guangxi Medical University, Nanning 530021, China
阿尔茨海默病(Alzheimer’s disease,AD)是一种威胁人类健康的神经系统疾病。目前对于AD的治疗还没有十分明确的方法(Mohammad et al.,2012)。建立良好的AD动物模型,有助于增加对AD病因病机的认识,并可以指导AD的预防和治疗。目前的AD模型按动物种类划分主要有灵长类动物模型和啮齿类动物模型两大类。灵长类动物模型价格十分昂贵,啮齿类动物模型则与人类神经系统差别较大。建立一种费用相对低廉,但是比啮齿类动物更接近人类的动物模型对于AD等神经系统疾病研究很有意义。树鼩Tupaia belangeri的遗传学研究表明其在生物学上比啮齿类动物更接近灵长类动物(Li et al.,2012;许凌等,2013),有着明显大于大鼠的大脑和更高级的神经系统,应用树鼩进行神经系统疾病研究有着良好的前景。与灵长类动物相比,树鼩又具有体型小、繁殖能力强的特点,值得我们进行相关的探索。同时,树鼩有着远低于灵长类动物的价格,在实验操作上也更为简便。开发树鼩模型,有助于减少灵长类动物的实验用量。目前尚无利用树鼩成功制作AD模型的报道。国内也有学者利用树鼩进行AD的相关研究(何保丽等,2013),但该研究仅对脑内注射β-淀粉蛋白(Aβ1~40)的树鼩进行了基因表达方面的探讨,未对树鼩进行行为学、病理学检测以判定模型是否成立。树鼩的体型与大鼠相似,头部外形也比较接近,可以利用大鼠脑立体定位仪进行脑内注射。大鼠的AD模型造模方法相对成熟,故我们参照目前常用的大鼠AD模型的造模方法和检测指标,尝试用树鼩制作AD模型,探索其可行性,为探索树鼩神经系统疾病模型的开发和利用奠定基础。
1 材料 1.1 实验动物雄性树鼩30只,3月龄,体质量120 g±10 g,昆明医学院实验动物中心提供。实验动物生产许可证号:SCXK(滇)2013-0002。
1.2 主要试剂和仪器β淀粉蛋白(Aβ1~42),鹅膏蕈氨酸(ibotenic acid,IBO),D半乳糖(D-gal)美国Sigma公司生产。Aβ1~42浓度为2 g·L-1,用灭菌生理盐水配制,在37 ℃下孵育72 h,使其成为凝聚态的Aβ1~42。
脑立体定向仪:RWD68002,深圳市瑞沃德生命科技有限公司;Morris水迷宫:广西医科大学研制;微量注射器:上海安亭微量进样器厂;电子天平:ML204,瑞士梅特勒-托利多公司。
2 方法 2.1 动物分组将30只树鼩按体质量随机分为3组:模型组,对照组和空白组,每组10只。模型组:参考关于大鼠复合AD造模方法的文献进行改良方法造模(刘学凤等,2012);对照组:操作与模型组相同,所有药物改为生理盐水,注射剂量和部位与模型组相同;空白组:不做任何处理。
2.2 动物模型的建立动物实验在广西医科大学实验动物中心进行。实验动物使用许可证号:SYXK(桂)2009-0004。
模型组树鼩连续30 d腹腔注射D-gal 50 mg·(kg·d)-1,使其早衰。第31天用1%戊巴比妥钠,2 mL每千克体质量腹腔注射麻醉。麻醉成功后,将树鼩固定于大鼠脑立体定向仪上。沿头顶部正中切开皮肤暴露矢状缝,以矢状缝同对耳线的交点作为起始原点,向前3.3 mm,左右两侧5 mm处钻开颅骨,将微量注射器针头通过立体定位仪经开孔垂直刺入脑10 mm,缓慢匀速进针时,用时5 min使针尖达到树鼩海马区(海马区定位参照树鼩脑立体定位图谱)(杨文光,1990),缓慢推入Aβ1~42和IBO混合液5 μL(Aβ1~42 10 μg和IBO 10 μg溶于生理盐水),15 min内注射完毕,留针10 min后缓慢提出针头,缝合,75%乙醇消毒。
脑内注射后观察树鼩外观、饮食、饮水、自主活动情况,4周后进行行为学指标观察。
2.3 行为学指标检测采用经典的Morris水迷宫观察树鼩的学习记忆能力。
Morris水迷宫系统主要由盛水的圆形水槽迷宫、隐藏在水面下的平台、视频分析系统(包括摄像机、数字图像采集卡、计算机系统和分析软件)组成。水槽直径150 cm,深60 cm,摄像镜头安放于水槽中心上方3 m高度。按东南西北4个方向将水槽平均划分为4个象限:东北、西北、东南、西南,将各象限水槽壁中点标为入水点,入水点处贴上醒目标记以区分不同象限。站台半径5 cm,高30 cm,纯黑色塑料材质,固定放置于任一象限的中央,水槽中水面高出站台平面0.5 cm,将水用奶粉调成白色,以肉眼看不见平台为准,保持水温(21±0.5)℃。房间内光照恒定,保持完全安静,无光线直射在水池内。
先对树鼩进行水迷宫适应性训练,再进行正式指标检测。
2.3.1 水迷宫适应性训练将树鼩头朝池壁放入水中,引导树鼩找到水下平台。放入位置随机取东北、西北、东南、西南4个起始位置之一。记录树鼩找到水下平台的时间(s)。在前几次训练中,如果这个时间超过75 s,则引导树鼩到平台。让树鼩在平台上停留10 s。连续训练7 d,每天2次,筛选游泳能力好,能自主找到平台的树鼩进行正式实验。
2.3.2 正式指标检测定位巡航实验(navigation test)在08∶ 30—10∶ 00进行,每次75 s,连续测试4 d。将树鼩随机地头朝池壁按东北、西北、东南、西南4个象限轻轻放入池中,记录树鼩寻找并爬上平台所需的时间即逃避潜伏期和游泳速度。树鼩找到平台后使其在平台上停留10 s,让其适应平台站立和周围环境,如果树鼩在75 s内未找到平台,计算机停止跟踪,记录逃避潜伏期时间为75 s,并由实验者将树鼩引导至平台,让其停留15 s。每次训练结束,迅速用吸水毛巾将树鼩毛发擦干,并用电吹风吹干,以防树鼩低体温。
空间探索实验(probe test):定位巡航实验结束后次日撤走平台,任选一个入水点将树鼩面向池壁放入水中,游泳时间均为90 s,记下其穿越原平台所在区域的次数,以此作为空间记忆力的成绩。
2.4 病理学检测行为学指标检测结束后,采用1%戊巴比妥钠溶液按每100 g体质量0.15 mL对树鼩腹腔注射麻醉。待树鼩麻醉后固定,从胸骨剑突处开胸,经左心室插管至主动脉,快速灌注生理盐水100 mL冲洗血液,之后用4%多聚甲醛500 mL灌注,取脑组织后立刻固定于4%中性福尔马林溶液中,常规石蜡切片,苏木精-伊红(HE)染色,观察脑组织形态改变,神经纤维缠结(neurofibrillary tangles,NFT)形成情况用Bieloschsky镀银法检测。
2.5 统计分析所有计量资料数据采用x±s表示,所有数据均用SPSS 19.0进行处理,进行单因素方差分析(ANOVA),根据方差齐性与否,分别选用不同的检验方法,即方差齐的资料的两两比较用LSD法检验,方差不齐的资料的两两比较用Games-Howell法检验,以双侧α=0.05为显著性水平。
3 结果 3.1 行为学观察 3.1.1 定位巡航实验结果空白组与对照组的学习进度类似,随着时间延长,潜伏期下降,两组之间没有明显的差别。模型组从第3天开始,潜伏期明显长于空白组,差异有统计学意义(P < 0.05),从第4天起与对照组也出现明显差异(表 1,图 1)。
| (x±s,n=10) | |||
| 时间 | 模型组 | 对照组 | 空白组 |
| 第1天 | 67.10±22.51 | 64.21±21.35 | 63.25±18.75 |
| 第2天 | 67.78±21.63 | 62.78±21.16 | 60.58±18.95 |
| 第3天 | 65.95±23.52a | 58.73±23.42 | 53.55±19.64 |
| 第4天 | 61.35±25.16ab | 47.78±20.13 | 45.53±18.75 |
| 第5天 | 58.49±26.17ab | 39.77±19.88 | 41.32±23.45 |
| 第6天 | 54.78±27.35ab | 40.87±25.17 | 35.78±24.11 |
| 第7天 | 55.12±27.65ab | 37.91±24.38 | 36.42±24.33 |
| 注:a. 与空白组比较, P < 0.05; b. 与对照组比较, P < 0.05; 下表同。 Notes: a. compared with the normal group, P < 0.05; b. compared with the control group, P < 0.05; the same below. |
|||
结果显示在搜索策略上,空白组和对照组树鼩有一定的趋向性,更倾向于在原 有平台的象限进行搜索,两组之间差异无统计学意 义;模型组则出现随机搜索的趋势,模型组与空白组差异有统计学意义(P < 0.05)。在游泳速率上3组差异无统计学意义(表 2)。
| (x±s,n=10) | ||
| 组别 | 穿越目标象限次数 | 游泳速度/(cm·s-1) |
| 模型组 | 1.33±1.32ab | 15.21±6.75 |
| 对照组 | 3.15±1.98 | 14.87±7.56 |
| 空白组 | 4.11±1.95 | 15.37±6.74 |
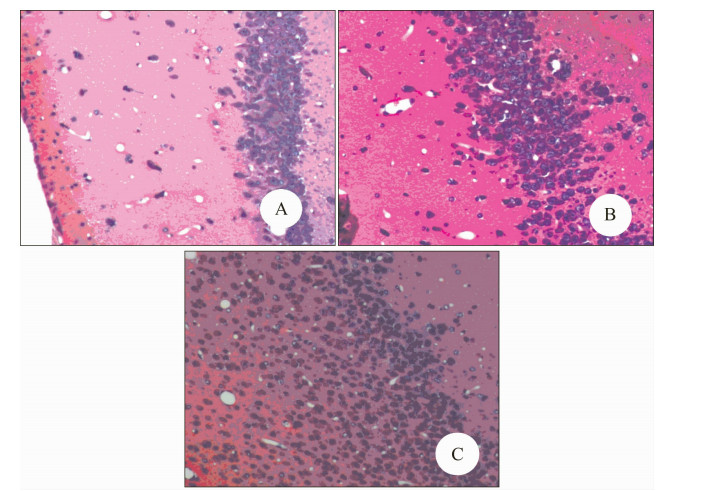
模型组树鼩海马皮质HE染色切片可观察到胶质细胞增生,而空白组和对照组未见明显病理改变(图 1)。
|
|
图 1 树鼩海马HE病理组织图片
Fig. 1 Histopathological changes in hippocampus of Tupaia belangeri, using HE staining
A. 空白组, B. 对照组, C. 模型组。 A. Blank group, B. Control group, C. Model group. |
Bieloschsky 镀银法切片可以看到模型组树鼩海马形成NFT,而空白组、对照组均未看到明显病理改变(图 2)。

|
|
图 2 树鼩海马Bieloschsky镀银法病理组织切片
Fig. 2 Histopathological changes in hippocampus of Tupaia belangeri, using Bieloschsky silver staining
A. 空白组, B. 对照组, C. 模型组。 A. Blank group, B. Control group, C. Model group. |
AD模型目前主要有老化型动物模型(Kimura et al.,2004)、转基因动物模型(Miranda et al.,2010)和损伤型动物模型(Schliebs & Arendt,2011)等,损伤型动物模型被多数研究者采用。本实验采用的造模方法是Aβ、IBO、D-gal联合使用的方法,此造模方法在大鼠身上已经取得了成果,在猕猴身上也有联合使用多种药物制作AD模型的报道(李文德等,2010)。单一的物理或者化学因素造成动物脑组织损伤的造模方法,都只能模拟AD表现的一个方面,联合使用多种药物更能表现AD复杂的病理过程。
在对树鼩的水迷宫实验结果进行分析后发现,AD模型组的学习记忆能力明显下降,但没有发现树鼩在水中的协调运动能力受到明显影响。脑内注射制作神经系统疾病模型的缺陷之一就是会对脑组织产生物理破坏,形成类似外伤的损害,从而产生一定的干扰,利用微泵注射技术能减小物理损伤,但也不是完美的解决方案。为了排除注射器贯穿脑组织对树鼩智力的损伤,我们设计了脑内注射生理盐水的对照组,结果表明生理盐水脑内注射未对树鼩的水迷宫实验表现产生明显影响。证明AD模型组的学习记忆能力下降确实是药物毒性作用引起的,而不是物理损伤的结果。
AD动物模型成立的判定指标一般是将行为学观察同病理检测相结合。目前还没有树鼩AD模型的判定标准。我们参考大鼠AD模型和猕猴AD模型的判定标准进行评价。大鼠AD模型的行为学观察指标是经典的Morris水迷宫实验,经过训练,树鼩也能适应Morris水迷宫实验。所以我们采用Morris水迷宫来作为树鼩学习记忆能力测试的方法。AD的病理特征为额颞叶和海马等部位出现选择性胆碱能神经元和突触缺失、老年斑(senile plaques)和NFT(St George-Hyslop & Fraser,2012),在大鼠AD模型(武聪等,2012),猕猴AD模型(李文德等,2010)中,海马病理都出现了胶质细胞增多和NFT,是AD模型公认的病理指标。病理学检测发现模型组树鼩出现了胶质细胞增多和NFT,是典型的AD表现。综合Morris水迷宫实验结果,认为模型组树鼩符合AD的主要表现,模型是成立的。
综合行为学观察和病理学检测结果,表明腹腔注射D-gal,双侧海马注射Aβ1~42和IBO混合液的方法可以造成树鼩学习记忆能力下降,并出现神经胶质细胞增生和NFT,是一种可行的树鼩AD模型造模方法。
本研究目前只进行了表观现象的观察,对于模型机理机制的研究还有待下一步用分子生物学的方法进行研究和探索。
| 何保丽, 角建林, 李波, 等. 2013. 天麻素对老年痴呆树鼩海马BDNF 表达的影响[J]. 昆明医科大学学报, (9): 29-30. |
| 刘学凤, 李义松, 冯丽谦, 等. 2012. 阿尔茨海默病大鼠模型复制的实验研究[J]. 中医学报, 27(175): 1606-1608. |
| 武聪, 庄莹, 李艳茹, 等. 2012. 人参皂苷Rg2对阿尔茨海默病模型大鼠海马神经元结构及突触素表达的影响[J]. 中国老年学杂志, 3(32): 989-992. |
| 许凌, 范宇, 蒋学龙, 等. 2013. 树鼩进化分类地位的分子证据[J]. 动物学研究, 34(2): 70-76. |
| 李文德, 吴玉娥, 闵凡贵, 等. 2010. 颅内注射淀粉样β蛋白片段1-42和thiorphan对恒河猴脑内淀粉样β蛋白表达的影响[J]. 中国药理学与毒理学杂志, 2(24): 89-95. |
| 杨文光. 1990. 中缅树鼩和广西猕猴脑立体定位图谱[M]. 南宁: 广西科学技术出版社. |
| Kimura N, Tanemura K, Nakamura SI, et al. 2004. Age-related changes of Alzheimer's disease-associated proteins in cynomolgus monkey brains[J]. Neurobiology of Aging, 25(Supplement 2): S145-S146. |
| Li RX, Xu W, Wang Z, et al. 2012. Proteomic characteristics of the liver and skeletal muscle in the Chinese tree shrew (Tupaia belangeri chinensis)[J]. Protein Cell, 3(9): 691-700. |
| Miranda L, Bader Lange, Daret St Clair, et al. 2010. Age-related loss of phospholipid asymmetry in APP (NLh)/APP(NLh)×PS-1 (P264L)/PS-1 (P264L) human double mutant knock in mice: relevance to Alzheimer disease[J]. Neurobiology of Disease, 38(1): 104-115. |
| Mohammad AI, Charles DeCarli. 2012. Next frontiers in the genetic epidemiology of Alzheimer's disease[J]. European Journal of Epidemiology, 27: 831-836. |
| Schliebs R, Arendt T. 2011. The cholinergic system in aging and neuronal degeneration[J]. Behavioural Brain Research, 221(2): 555-563. |
| St George-Hyslop P, Fraser PE. 2012. Assembly of the presenilin γ-/ε-secretase complex[J]. Journal of Neurochemistry, 120(supplement s1): 84-88. |
 2016, Vol. 35
2016, Vol. 35




