扩展功能
文章信息
- 倪宝森, 刘旭红, 张晓翠, 鲍永红, 敬凯
- NI Baosen, LIU Xuhong, ZHANG Xiaocui, BAO Yonghong, JING Kai*
- 云南新平哀牢山红瘰疣螈的陆地求偶交配行为模式
- Courtship Behavior Mode of Red Knobby Newt, Tylototriton shanjing,in Land Environment of Ailao Mountain, Xinping, Yunnan
- 四川动物, 2015, 34(6): 838-845
- Sichuan Journal of Zoology, 2015, 34(6): 838-845
- 10.11984/j.issn.1000-7083.20150163
-
文章历史
- 收稿日期: 2015-05-06
- 接受日期: 2015-06-08
与无尾两栖类不同,大多数有尾两栖类都是体内受精的,但雄性缺乏交配器官,精子的转移主要依靠精包(Halliday,1990)。精子贮存在雌性体内(Sever,1997;Sever & Siegel,2006),当雌性排卵时,精子穿过卵胶膜与卵结合受精(Hiyoshi et al.,2007)。在精子转移过程中,有尾两栖类表现出复杂的求偶交配行为(Propper,1991;Gong & Mu,2008;Bruni & Romano,2011)。不同的有尾动物类群和种类在求偶交配行为复杂程度、模式上存在着很大差异(Salthe,1967;Arnold,1976)。个体求偶交配成功与否与其适合度密切相关,在求偶交配行为中的表现又影响个体的繁殖成功,进而又影响到种群的补充。
国际上对有尾两栖类的求偶交配行为的研究大多集中在无肺螈科Plethodontidae、钝口螈科Ambystomatidae、蝾螈科Salam and ridae欧螈属Triturus和山螈属Euproctus等(Halliday,1977;Verrell & Mabry,2000;Denoel et al.,2005),国内则对蝾螈科Salam and ridae动物的繁殖行为研究较多(田应洲等,1998;Gong & Mu,2008;李骏等,2012;杨国辉等,2012)。虽然大多数研究工作都涉及到求偶交配行为,但缺乏对求偶交配行为模式的系统研究,较为深入而系统的研究是对镇海棘螈Echinotriton chinhaiensis开展的工作(Sparreboom et al.,2001)。红瘰疣螈Tylototriton shanjing是分布于云南山地环境中的典型有尾两栖类,其求偶交配行为主要在陆地上进行(李骏等,2012)。虽然已有的研究对红瘰疣螈的求偶交配行为也有所涉及(李骏等,2012;杨国辉等,2012),但对其在陆地上的求偶交配行为模式还没有系统的研究。
2013—2014年,在繁殖季节对云南省新平县哀牢山的红瘰疣螈陆上求偶交配行为进行了野外观察,并结合室内的求偶交配行为实验,系统地观察和记录了红瘰疣螈的求偶交配过程,以了解其在陆地环境中的求偶交配行为模式,为该物种的科学保护提供依据。
1 研究方法 1.1 繁殖地求偶交配场红瘰疣螈的陆地求偶交配行为的研究在海拔1850~2000 m的云南省新平县哀牢山(24°00′52″N,101°32′35″E)野外繁殖地(李骏等,2012)和云南师范大学的实验室进行。受印度洋季风的影响,哀牢山干湿季分明,4月下旬至10月中上旬为雨季,降雨充沛(年均降雨量2000 mm),每年雨季来临前,山涧溪流被引入旱地形成水田用于水稻种植,稻田随后成为红瘰疣螈繁殖地。
在非繁殖季节,红瘰疣螈主要栖息于旱地的岩石缝隙和潮湿的土洞中。5月上旬随着雨季的到来和气温的逐步升高,大量红瘰疣螈个体从越冬栖息地出来,于降雨后开始繁殖迁徙、求偶交配和产卵等各种繁殖活动。红瘰疣螈在临近稻田的旱地进行求偶交配,完成求偶交配后,雌性个体迁徙到水田产卵。多年的观察发现,在本研究地,虽然红瘰疣螈也会在稻田的水中求偶交配,但大多数雌雄个体都选择在离稻田不远的一条布满杂草的陆地排水沟中进行求偶交配活动。沟内生长的众多杂草为红瘰疣螈的求偶交配提供了较好的隐蔽场所。标记重捕显示,繁殖期间雄性个体可在此停留超过1周的时间(李骏等,2012)。
1.2 求偶交配行为观察和记录 1.2.1 野外观察和视频采集红瘰疣螈求偶交配行为的野外观察于2013年4—5月和2014年5—6月在野外繁殖地进行。受降雨的影响(刘旭红等,2013),红瘰疣螈求偶交配行为一般发生在降雨之后,因此求偶交配行为的观察和记录也选在连续天晴后的降雨天。在繁殖地随机选择求偶交配个体进行全程连续跟踪观察,使用索尼PJ600-E摄像机对其求偶交配整个过程进行拍摄记录。
1.2.2 室内视频采集2013年5月13日—6月8日,将在野外繁殖地捕获的红瘰疣螈个体带回室内进行实验。由于在野外自然条件下,红瘰疣螈是在降雨后开始求偶交配行为,室内通过模拟降雨来刺激求偶交配行为的出现。实验在160 cm×30 cm×40 cm的玻璃缸中进行,玻璃缸底部铺以碎地板砖,缸一端的放置瓦片作为红瘰疣螈隐蔽场所,另一端的底部连接排水管。玻璃缸的侧上方放置水箱,用直径2.5 cm的塑料水管接入玻璃缸并环绕固定在玻璃缸内壁上,末端保持封闭。水管上留有大小不一的孔洞,水流可借助于水压形成水柱喷入玻璃缸,模拟自然环境下的降雨(Ziegler et al.,2008)。在玻璃缸的一端正上方设置摄像头,并且保证红瘰疣螈的整个活动区域都在拍摄范围内。先将雌雄个体分开饲养,保持饲养环境干燥,然后同时放入玻璃缸,每次放入4只雄螈和2只雌螈。将自来水放置2 d后倒入水箱开始实验。人工模拟降雨后,部分个体便立即开始求偶交配行为。将监视摄像头与电脑连接,使用Debut视频捕获软件进行不间断的视频录像,一般持续24 h。
1.3 求偶交配行为分析有尾类的求偶交配行为模式各不相同,但都是由一系列行为活动所组成:包括雄性对雌性的识别、劝导、求偶交配,以及雌性对雄性的接受和拒绝等行为。本文对在野外观察和室内实验所获得的视频进行视频回放,参照斑点钝口螈Ambystoma maculatum、虎纹钝口螈A. tigrinum、红颊无肺螈Plethodon jordani(Arnold,1976)、欧螈T. pygmaeus(Hidalgo-Vila et al.,2002)和棘螈Echinotriton(Sparreboom et al.,2001)等多种有尾两栖类的求偶交配行为研究,观察记录求偶交配行为的行为过程,对红瘰疣螈的求偶交配行为进行识别,确定求偶交配过程的行为时序以及求偶交配过程中雄性和雌性的典型求偶交配行为类型。
2 结果 2.1 红瘰疣螈求偶交配行为时序野外的观察共记录到视频137段,其中2013年62段,2014年75段。视频时长从2 min到1.3 h不等。室内共采集到视频15段,其中包含完整求偶交配行为过程的视频2段。
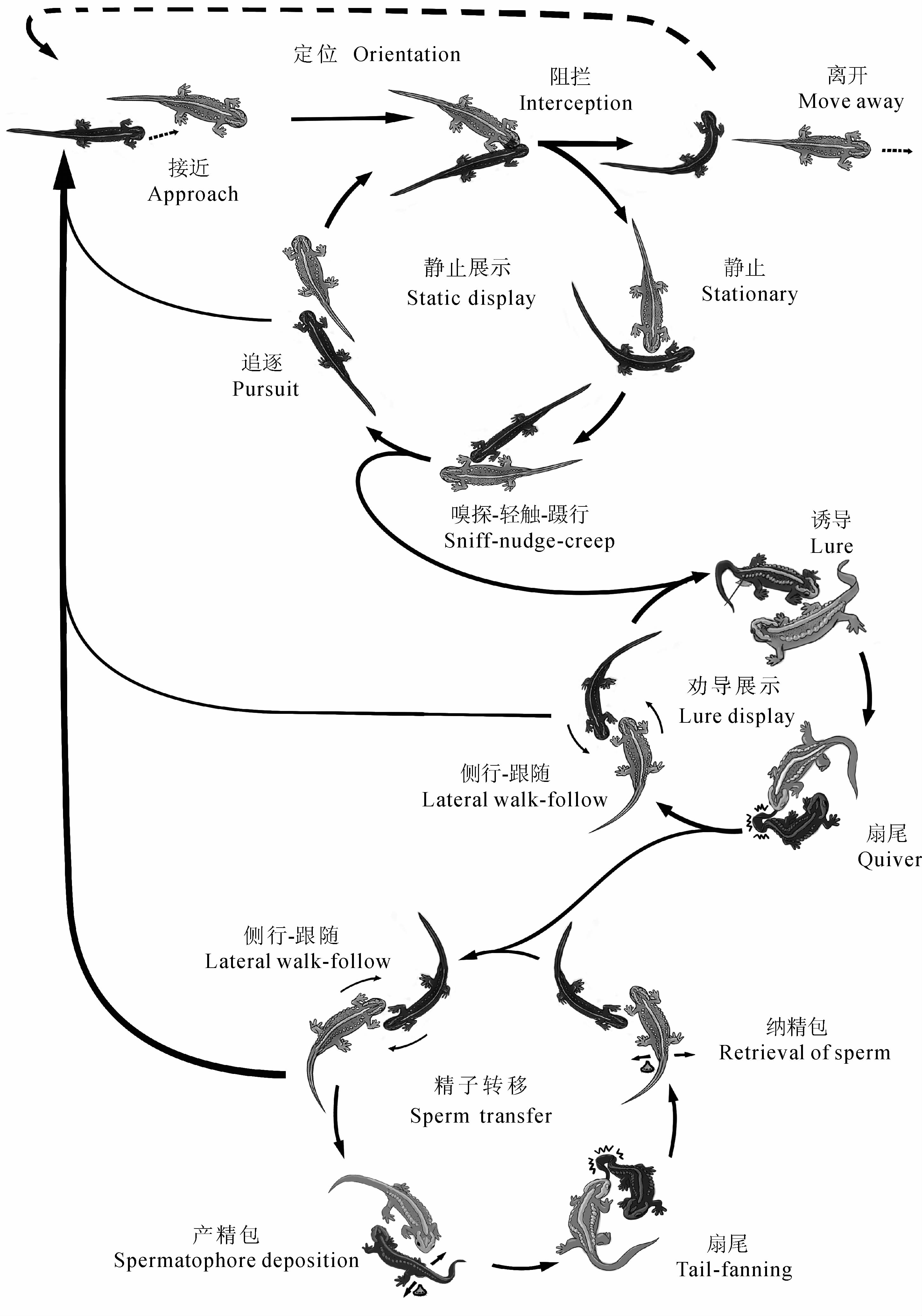
视频分析显示,红瘰疣螈的求偶交配行为是按照一定顺序进行的,按时间顺序可分为定位、静止展示、劝导展示和精子转移4个阶段(图 1)。
|
| 图 1 红瘰疣螈求偶交配行为序列(雄性深色,雌性浅色) Fig. 1 The courtship behavior sequence of Tylototriton shanjing(male in dark color,female in light color) |
雄螈寻找、发现和接近求偶对象并将其阻停,为雌雄个体求偶交配行为的定位阶段。包括雄螈接近雌螈,雄螈对雌螈进行阻拦,接受性雌螈停下或非接受性雌螈离开等行为过程。
在野外降雨后和室内模拟降雨条件下,红瘰疣螈开始在求偶场所活动,雄螈在求偶交配地寻找雌螈。当任何个体(无论雌雄)出现在雄螈附近时,雄螈都表现出一定的警戒行为,静止注视其身边移动的个体,几秒后雄螈迅速爬向移动的个体。靠近移动个体时,雄螈迅速用前肢和身体按压或阻拦移动个体,阻慢并试图使其停止。移动个体一般会摆脱阻拦继续前行,雄螈则持续不断地重复出现追逐-阻拦动作。每次阻拦的持续时间为15~20 s。
整个接近-阻拦的过程中,雌螈会受到雄螈追逐-阻拦行为的影响,移动速度逐渐减慢,最终停下来并进入下一阶段的求偶交配;当被追逐个体是雄螈时,雄螈会极力摆脱阻拦并离开;大部分雌螈也会径直离开。
2.1.2 静止展示(Static display)雌雄个体相互识别的阶段。包括雌性静止,雄性轻触、嗅探和蹑行等行为过程。
雄螈持续不断地追逐和阻拦移动个体,直至移动个体停下来呈静止状态。移动个体停下后,雄螈在移动个体前方或侧面极为缓慢地移动身体,呈蹑行状态,持续时间可长达90 s。雄螈不停地摇摆头部,用吻端轻轻接触被阻个体,对阻停个体进行嗅探,从头侧到颈部,再沿体侧一直延续至泄殖腔,主要部位是身体两侧的瘰粒。接触过程中被追逐个体一直保持静止状态,表现为短时间的注视雄螈或注视正前方,持续时间10~75 s。被阻个体若为雄螈,个体在静止一段时间后会直接离开。若为雌螈,非接受个体也会迅速离开,接受性个体会停止注视,缓慢移动,进入下一阶段的求偶交配行为。大多数情况下,雌雄个体都会不断重复追逐、阻拦和静止的过程。
2.1.3 劝导展示(Lure display) 雄性诱导雌性进入精子转移阶段。包括雄性轻推、扇尾、诱导和雌性跟随等行为过程。静止展示后,雄螈调整身体位置,使身体向雌螈一侧弯曲,用头部轻推雌螈,雌螈呈注视状态并向前轻微移动,雌雄个体身体呈现头对头的姿态。在雄螈推动下,雌雄个体向一侧转圈,雄螈向前侧行,雌螈侧行跟随。雌螈若未作出反应,雄性会扇尾1~3次,甚至用吻推动雌螈进入转圈。有些雄螈会在泄殖腔部位分泌一团无色透明粘状物,粘状物上无白色的精包。粘状物附着在地面,随雄螈的移动形成一条白线。但并不是所有的求偶交配过程都会出现这样的分泌行为。扇尾和粘状物分泌的作用可能是吸引雌螈注意并诱导雌螈进入后续的求偶交配行为。
受雌螈自身因素或外界干扰的影响,求偶交配在这个阶段依然会中断,并重复接近-阻拦和静态展示等过程。这样的反复接近、阻拦、静止、劝导过程可持续20 min~51 min 38 s不等。
2.1.4 精子转移(Spermatophore transfer) 求偶交配的精子转移阶段。包括雄性侧行、产精包、扇尾,雌性侧行跟随、纳精包等行为过程。在雄螈的引导下,雌雄保持头对头的姿态,进入雄螈向侧前方移动、雌螈侧行跟随的侧向转圈状态。雄螈身体弯曲呈弓形侧行,尾侧弯并于地面拖行。当雄螈的泄殖腔与地面突出物接触时停下,臀部抬升,将泄殖腔口紧贴地面突出物,臀部左右摆动5~10次,摆臀后静止不动8~10 s,头部左右摇摆3~4次,身体向侧前方移动,留下圆锥状精包。产精包前,雄螈出现扇尾行为,即尾基部弯曲,将尾向前折向身体,与躯体平行,尾尖左右颤动6~8次。但不是每次产精包前都会出现扇尾行为,地面有水时扇尾的频率高,观察到产12枚精包,出现6次扇尾,而无水时频率低,23枚精包仅有8次扇尾;在雄螈产精包的短暂静止期间,雌螈用吻接触雄螈前后肢之间的躯干侧,摆头3~5次。雄螈侧行时,雌螈跟随侧行转圈。到达精包位置后,雌螈将身体调整到与精包在腹中线上接触。精包接触泄殖腔孔时,雌螈用后肢抬起臀部,然后下降使泄殖腔对准精包,臀部轻微左右来回移动,将精包先端精子纳入泄殖腔口,留下精包基部的胶质。雌雄个体不断重复上述转圈的精子转移行为过程,直到求偶交配过程结束。持续时间可长达75 min。
在求偶交配的精子转移阶段,不同个体在持续时间、转圈数和雄螈所产的精包数上各不相同。精包在不同阶段也有差异,精子转移初期,雄螈仅分泌一些粘性分泌物,精包顶端无精子;有些雄螈在雌螈未跟随时,所产的精包上也无精子;有时雄螈有产精包的动作,但无精包。长时间交配的个体在精子转移阶段的末期,雄螈所产的精包上只有胶膜而无精子。雄螈的精包往往产在前一个精包的位置上,这些位置一般是地面的突出物,部分精包完全覆盖上一个精包,有些则无法准确覆盖。2只雄螈与1只雌螈求偶交配时,雄螈之间也彼此将精包产在对方的精包上,将对方精包覆盖。有时也出现2只甚至多只雄螈相互转圈,分别产精包,但无雌螈的情况。
精子转移阶段,求偶交配同样会受到干扰而被阻断,被阻断后会重新进入追逐-阻拦的行为过程,或者雌螈直接离开求偶场所。
2.2 红瘰疣螈求偶交配的行为类型 2.2.1 雄性的交配行为红瘰疣螈雄性在整个繁殖季节都比较活跃,在求偶交配行为过程中始终处于主动,行为较为复杂,行为类型丰富。野外观察和室内实验的视频分析显示,雄性的行为主要包括以下类型:
警戒(Alert):繁殖期,雄螈在靠近繁殖水体附近的陆地求偶交配场所内无方向性地爬行,每隔一段时间将前肢攀附在地面枯枝或石块等位置较高的支撑物上,前肢将头部抬高,整个身体静止5~35 s,注视和观察其他从身边经过的个体,表现出警戒行为(图 2:A)。警戒行为通常出现在求偶交配的最初阶段和求偶交配行为受到干扰时。

|
| 图 2 红瘰疣螈求偶交配行为类型 Fig. 2 Behavior types of mating Tylototriton shanjingBehavior types of mating Tylototriton shanjingA. 警戒,B. 追逐,C1~3. 阻拦,D. 蹑行,E. 嗅探,F. 轻推,G. 诱导,H. 扇尾,I. 侧行,J. 产精包,K. 离开,L. 静止,M. 纳精包。A. Alert,B. Pursuit,C1-3. Interception,D. Creep,E. Sniff,F. Nudge,G. Lure,H. Tail-fanning,I. Lateral walk,J. Spermatophore deposition,K. Move away,L. Stationary,M. Retrieval of sperm. |
追逐(Pursuit):在发现有其他个体经过时,无论经过的个体是雌螈还是雄螈,雄螈立即向经过的个体追去,速度明显快于被追个体(图 2:B)。追逐多发生在求偶交配行为的第一阶段,也发生在求偶交配行为过程中断后雌螈离开时。追逐行为经常反复出现,直至被追逐个体停下或最终离去。
阻拦(Interception):当雄螈靠近被追逐个体时,用前肢和身体按压被追逐个体。按压的方式有3种:雄螈从被追逐个体后方背部按压被追逐个体(图 2:C1);从被追逐个体的背部或一侧迅速爬到被追逐个体的肩部和头部,用前肢按压被追逐个体头部(图 2:C2);追逐个体将自己的身体置于雌螈的正前方(图 2:C3),阻止被追逐个体向前移动直至被追逐个体停下。阻拦发生在个体初次相遇和任何求偶交配行为中断后的重新追逐时。
蹑行(Creep):雄螈移动其前后肢,动作极为缓慢,身体保持弓状,身体位置垂直于雌螈,侧向转圈爬行(图 2:D)。蹑行主要出现在阻拦成功时。
嗅探(Sniff):雄螈位于雌螈身体一侧,用吻从雌螈颈部开始沿后肢方向轻轻试探并接触雌螈身体侧面,直至雌螈泄殖腔位置结束(图 2:E),以确定求偶对象的性别。雄螈对阻拦成功的个体表现出嗅探行为,嗅探行为也会出现在精包转移阶段。
轻触(Nudge):雄螈头部与雌螈的头部侧弯相对呈头对头姿态,彼此接触,雄螈不断摆动头部,用吻将雌螈向前轻轻推动,使其身体向一侧缓慢移动,推动雌螈跟随雄螈进入转圈(图 2:F)。轻触行为通常出现在求偶交配的静止展示和精子转移阶段。在静止展示阶段,轻触行为持续时间较长。在精子转移阶段,雄螈使用轻触带动雌螈跟随并接纳精包。
诱导(Lure):雄螈在产第1枚精包之前分泌一团无色透明的粘液物质(图 2:G),粘液分泌后雄螈向前缓慢移动,在地面形成1条粘液线,诱导雌螈跟随。
扇尾(Tail-fanning):雄螈与雌螈侧向相对,臀部和尾弯曲成S形,将尾后部向身体侧面雌螈方向折叠,尾尖左右快速摆动6~8次(图 2:H)。扇尾行为主要出现在劝导展示和精包转移阶段。在劝导展示阶段,雄螈在静止的雌螈面前扇尾,吸引雌螈跟随。在精子转移阶段,扇尾出现在雌雄个体转圈过程中的雄螈产精包前,提示雌螈接纳精包。但并不是雄螈每次产精包前都会出现扇尾动作,雄螈每产1~4个精包才出现1次扇尾。扇尾行为可能在维持求偶交配行为正常进行中起到关键作用。
侧行(Lateral walk):雄螈在与雌螈转圈过程中,雄螈身体弯曲成弓状,身体向前侧方移动,一侧的前后肢移动幅度大,另一侧移动幅度小(图 2:I),移动速度比蹑行快。侧行出现在劝导展示和精子转移阶段。
产精包(Spermatophore deposition):雄螈侧行、雌螈跟随的转圈过程中,雄螈拖拽泄殖腔孔与地面接触。当雄螈的泄殖腔孔与地面凸起物相遇时,臀部和尾弯曲成S形,后肢支撑地面,臀部抬起,将泄殖腔口对准地面突出物,臀部再下压,紧贴突出物左右摇摆5~10次,然后保持静止不动8~10 s,接着雄螈离开,留下圆锥状的精包(图 2:J)。精包基部为无色透明胶质物,顶端为白色精子,无色胶膜和白色精子之间界限清楚。精包附着于地面,一般分布在求偶交配地的2~4个点,大多是在地面突出物上。产精包仅出现在求偶交配行为过程中的精子转移阶段。
2.2.2 雌性的交配行为在求偶交配过程中,雌性红瘰疣螈个体的表现往往是被动的,在整个求偶交配过程中的行为表现相对比较单一。
离开(Move away):雌螈在雄螈多次追逐阻拦下,一直向前爬行,径直离开(图 2:K),在雌螈离开雄螈2~3个身长后,雄螈不再追逐。离开为雌螈在求偶交配过程中拒绝雄螈的行为,可能发生在求偶交配的任何阶段。
静止(Stationary):受到雄螈阻拦,雌螈停下维持静止不动的状态(图 2:L)。静止行为发生在静止展示阶段。
跟随(Follow):雌螈随雄螈进入转圈运动,雄螈侧行时,雌螈在内侧后方跟随(图 2:I),其运动方式和雄螈的侧行行为保持一致。跟随发生在劝导展示阶段和精子转移阶段。
纳精包(Retrieval of sperm):雌螈跟随雄螈侧行转圈移动,保持与精包在腹中线上接触,当精包与泄殖腔孔接触时,雌螈身体弯曲成S形,用后肢抬起臀部,然后后肢下降使泄殖腔对准精包,臀部左右来回移动将精包先端纳入泄殖腔(图 2:M)。雌螈只纳入精包顶端的精子,留下无色透明的胶膜。当精子纳入后,雌螈会出现短暂的静止状态,静止时间为8~10 s。纳精包仅发生在精子转移阶段,是求偶交配成功的表现。
3 讨论有尾类的求偶交配行为包括识别、跟随、注视、产精包、纳精包等5个不同阶段(Salthe,1967),具有定位、劝导、生殖同步化和异种生殖隔离等多种功能。求偶过程中通过雌雄个体的相互识别、雄性对雌性的控制以及雄性的求偶展示等行为来实现交配,完成精子的转移。然而水中求偶的有尾类和陆地上求偶的有尾类在这些行为上却存在着一定差异。
在雌雄个体的识别方面,蝾螈科的动物大多是夜行性的,嗅觉在不同物种、个体和性别之间的识别上起着重要作用(Wells,2010)。许多有尾两栖类的两性个体在求偶交配场所的出现可能是依靠嗅觉来实现的,如雌性掌欧螈Triturus helveticus就是受到同种个体(无论雌雄)气味的吸引(Secondi et al.,2005)而聚集在繁殖地的。这种相互吸引可促进雌雄个体向繁殖地的聚集,增加每个个体找到配偶的机会。然而在繁殖场所,雌雄个体在求偶交配场上的首次相遇却是偶然的,对欧螈的研究显示,雌雄都没有表现出远距离的相互吸引行为(Halliday,1977)。红瘰疣螈具有很强的陆生性,非繁殖期完全陆生,即使繁殖期也只是雌性迁入繁殖水体,并且产卵在陆地上(李骏等,2012),这与文县疣螈T. wenxianensis非常相似(Gong & Mu,2008)。红瘰疣螈在陆地的求偶交配过程中对异性的识别可能是通过视觉来实现的,且并不是很准确,表现在雄螈对身边经过的任何个体(无论雌雄)的追逐,一旦被追逐个体离开视线范围则不再继续追逐。并且被追逐个体即使是雄性,雄螈也表现出进一步的求偶交配行为,甚至出现2只或多只雄螈同时产精包而没有雌螈的情况。雌雄之间的识别似乎是依赖于雄螈和非接受性雌螈在被追逐时逃离,接受性雌螈留下来实现的。这种依靠视觉的识别可能是对逐渐增强的陆地生活的重要适应。
很多雄性有尾类以抱握行为来独占雌性,减少与其他雄性的竞争(Houck & Arnold,2003)。蝾螈科动物Salam and ridae不同属的抱握方式常常具有多样性。肋突螈属Pleurodeles、真螈属Salam and ra、伸舌螈属Chioglossa和小默螈属Mertensiella等的种类为腹部抱握(Houck & Arnold,2003)。东美螈属Notophthalmus则是背部抱握,用后肢抓握住雌螈胸部(Verrell,1982)。渍螈属Taricha的雄螈用前肢和后肢抓住雌螈的侧部(Hiyoshi et al.,2007)。日本红腹蝾螈Cynops pyrrhogaster求偶过程中,雄螈只以后肢轻轻地控制雌螈(Halliday,1977)。欧螈属和棘螈的雌螈则未受到雄螈的控制(Halliday,1990;Sparreboom et al.,2001)。疣螈属为腹部抱握方式,但常具有可塑性(Sparreboom et al.,2001),某些种在交配过程中会出现抱对行为,而另外一些种则不会,如分布于喜马拉雅山大吉岭地区的棕黑疣螈T. verrucosus,在室内水中繁殖实验中,雄螈用前肢从腹部抓住雌螈前肢(Kuzmin et al.,1994;Roy & Mushahidunnabi,2001),贵州疣螈T. kweichowensis也是从腹部抱握(田应洲等,1998)。大凉疣螈的生殖过程中也出现了抱握行为(Sparreboom et al.,2001),文县疣螈雄螈则是用嘴咬住雌螈尾部或后肢(Gong & Mu,2008)。在水中求偶的红瘰疣螈则用前肢抱握雌螈后肢股部(杨国辉等,2012)。然而我们的研究发现,在陆地上的求偶过程中未见红瘰疣螈有抱握行为,但出现了从背部和身体前方对雌性的阻拦行为。红瘰疣螈的水中求偶腹部抱握行为在陆地求偶中的退化以及阻拦行为的出现可能与红瘰疣螈由水生向陆地生活的转化有关。
蝾螈科动物的求偶交配过程中出现了很多展示行为,大多表现为尾部的运动。欧螈在水中求偶,尾部的运动比较丰富(Halliday,1977),包括持尾(Wave)、鞭尾(Whip)、扇尾(Fan)和颤尾(Quiver)。而红瘰疣螈的尾部运动则比较单一,仅在劝导阶段和精子转移阶段有扇尾行为。在完全陆地求偶时,扇尾的频率低,而在地面有水时频率较高。一般认为,雄性尾部运动的作用是在雌性头部周围形成局部水流(Halliday,1977),将雄性分泌的化学物质传递给雌性,在嗅觉、视觉和触觉上刺激雌性,激发和维持雌性的性活动。扇尾行为是雄性在求偶交配过程中的一种行为类型,对于有尾类在水中传递化学信息具有重要作用,而在陆地环境中,这种化学传递作用已经弱化。求偶交配行为从水生到陆生的进化过程中,扇尾行为得以保存,但其功能已发生变化,由传递嗅觉信息转变为了视觉展示,这可能是对陆地生活的适应。
综上所述,红瘰疣螈陆地求偶交配行为模式的研究暗示有尾两栖类在从水生向陆生生活方式的转变过程中,随着求偶交配行为逐渐从水中转移到陆地上,其求偶交配的行为模式也发生了显著的改变,如两性的相互识别、雄性控制雌性的抱握行为以及求偶展示的扇尾行为等。
| 李骏, 刘安柱, 李湘, 等. 2012. 红瘰疣螈的繁殖生态[J]. 动物学杂志, 47(2): 8-15. |
| 刘旭红, 张晓翠, 李骏, 等. 2013. 降雨决定繁殖期红瘰疣螈的活动性[J]. 四川动物, 32(6): 867-872. |
| 田应洲, 孙爱群, 李松. 1998. 贵州疣螈繁殖生态的研究[J]. 四川动物, 17(2): 60-64. |
| 杨国辉, 杨自忠, 徐吉山. 2012. 红瘰疣螈繁殖习性初步研究[J]. 大理学院学报: 综合版, 11(4): 50-52. |
| Arnold SJ. 1976. Sexual behavior, sexual interference and sexual defense in the salamanders Ambystoma maculatum, Ambystoma tigrinum and Plethodon jordani[J]. Zeitschrift für Tierpsychologie, 42(3): 247-300. |
| Bruni G, Romano A. 2011. Courtship behaviour, mating season and male sexual interference in Salamandrina perspicillata (Savi, 1821)[J]. Amphibia-Reptilia, 32(1): 63-76. |
| Denoel M, Hector MP, Poncin P. 2005. Courtship behavior in the Alpine newt Triturus alpestris at two different densities of males[J]. Herpetologica, 61(4): 373-379. |
| Gong DJ, Mu M. 2008. Behavioral observations and descriptions of the endangered knobby newt Tylototriton wenxianensis and their application in conservation[J]. Asian Herpetological Research, 11: 31-38. |
| Halliday T. 1977. The courtship of European newts: an evolutionary perspective[M].// Taylor DH, Guttman SI. The reproductive biology of amphibians. New York: Springer: 185-232. |
| Halliday TR. 1990. The evolution of courtship behavior in newts and salamanders[M].// Slater PJB, Rosenblatt JS, Beer C. Advances in the study of behavior 19. San Diego: Academic Press: 137-169. |
| Hidalgo-Vila J, Perez-Santigosa N, Diaz-Paniagua C. 2002. The sexual behaviour of the Pygmy newt, Triturus pygmaeus[J]. Amphibia-Reptilia, 23(4): 393-405. |
| Hiyoshi W, Sasaki T, Takayama-Watanabe E, et al. 2007. Egg jelly of the newt, Cynops pyrrhogaster contains a factor essential for sperm binding to the vitelline envelope[J]. Journal of Experimental Zoology Part A-Ecological Genetics and Physiology, 307A(6): 301-311. |
| Houck LD, Arnold SJ. 2003. Courtship and mating behavior[M].// Sever DM. Reproductive biology and phylogeny of Urodela. Enfield: Science Publishers, Inc.: 383-424. |
| Kuzmin SL, Dasgupta R, Smirina EM. 1994. Ecology of the Himalayan newt (Tylototriton verrucosus) in Darjeeling Himalayas, India[J]. Russian Journal of Herpetology, 1(1): 69-76. |
| Propper CR. 1991. Courtship in the rough-skinned newt Taricha granulosa[J]. Animal Behaviour, 41: 547-554. |
| Roy D, Mushahidunnabi M. 2001. Courtship, mating and egg-laying in Tylototriton verrucosus from the Darjeeling district of the eastern Himalaya[J]. Current Science, 81(6): 693-695. |
| Salthe SN. 1967. Courtship patterns and the phylogeny of the Urodeles[J]. Copeia, 1967(1): 100-117. |
| Secondi J, Haerty W, Lode T. 2005. Female attraction to conspecific chemical cues in the Palmate newt Triturus helveticus[J]. Ethology, 111(8): 726-735. |
| Sever DM, Siegel DS. 2006. Sperm aggregations in the spermatheca of the red back salamander (Plethodon cinereus)[J]. Acta Zoologica, 87(4): 331-340. |
| Sever DM. 1997. Sperm storage in the spermatheca of the red-back salamander, Plethodon cinereus (Amphibia: Plethodontidae)[J]. Journal of Morphology, 234(2): 131-146. |
| Sparreboom M, Xie F, Fei L. 2001. Reproductive behaviour of the Chinhai salamander (Echinotriton chinhaiensis) (Caudata: Salamandridae)[J]. Amphibia-Reptilia, 22(3): 309-320. |
| Verrell P, Mabry M. 2000. The courtship of Plethodontid salamanders-form, function, and phylogeny[M].// Bruce RC, Jaeger RG, Houck LD. The biology of plethodontid salamanders. New York: Springer: 371-380. |
| Verrell P. 1982. The sexual behaviour of the red-spotted newt, Notophthalmus viridescens (Amphibia: Urodela: Salamandridae)[J]. Animal Behaviour, 30(4): 1224-1236. |
| Wells KD. 2010. The ecology and behavior of amphibians[M]. Chicago: University of Chicago Press: 403-450. |
| Ziegler T, Hartmann T, Van der Straeten K, et al. 2008. Captive breeding and larval morphology of Tylototriton shanjing Nussbaum, Brodie & Yang, 1995, with an updated key of the genus Tylototriton (Amphibia: Salamandridae)[J]. Der Zoologische Garten, 77: 246-260. |
 2015, Vol.
2015, Vol. 




