扩展功能
文章信息
- 张超华, 袁思棋, 夏云, 曾晓茂
- ZHANG Chaohua, YUAN Siqi, XIA Yun, ZENG Xiaomao
- 康定湍蛙物种界定
- Species Delimitation of Amolops kangtingensis
- 四川动物, 2015, 34(6): 801-809
- Sichuan Journal of Zoology, 2015, 34(6): 801-809
- 10.11984/j.issn.1000-7083.20150122
-
文章历史
- 收稿日期: 2015-04-02
- 接受日期: 2015-05-08
2. 中国科学院大学, 北京100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
康定湍蛙Amolops kangtingensis是Liu(1950)依据1942年7月采自康定城内雅拉沟岸(Yalakou)、泸定城附近大渡河边(Tatu River)、炉霍朱倭(Chuwo)和康定新都桥(Hsintuchiao)等地,海拔在1370~3414 m范围内的多地混合标本订立的。其后,刘承钊和胡淑琴(1961)重新查看了标本,指出“康定湍蛙与四川湍蛙A. mantzorum(模式产地四川宝兴)个体变异较大,液浸标本难以辨认”,暂将其作为四川湍蛙的同物异名。
吴贯夫等(1987)对采自康定新都桥附近3700 m山溪的标本进行了染色体核型研究,结果表明康定湍蛙不具有与性别相关的异形染色体,而四川湍蛙具有XX/XY雌雄异形的核型(吴贯夫,赵尔宓,1984),以细胞遗传学证据恢复康定湍蛙为有效物种。其后数年间,一些学者认可康定湍蛙的有效性(Dubois,1992;Zhao & Adler,1993);而另一些学者则不赞同,仍然将其作为四川湍蛙的同物异名处理(费梁等,2005,2009)。
蔡红霞和赵尔宓(2008)以线粒体COⅠ和Cyt b基因片段为标记,发现康定湍蛙与四川湍蛙种间遗传距离与其各自种下居群间遗传距离相当,提出四川湍蛙和康定湍蛙在不同种群间具有很高的遗传分化。可量性状主成分分析表明,采自四川康定新都桥的康定湍蛙标本可与其他物种分离,而采自四川泸定的康定湍蛙标本则完全进入四川湍蛙内部。然而,研究所依赖的样本量及样点量明显不足。这一研究并未对康定湍蛙的有效性给出明确的结论,而是提出了康定湍蛙种下存在更多分化的可能。
Lu等(2014)对四川湍蛙种组分子系统发育分析发现,基于高海拔地区标本聚集为一单系而支持康定湍蛙A. kangtingensis为有效物种,较低海拔中部地区标本聚集为一单系,因包含地模标本而被指认为四川湍蛙A. mantzorum。这一研究提出了新的分类建议,然而仅是依赖于单一分子证据,缺乏形态、细胞等多层次、多侧面证据的支持和相互印证,此外样本及样点数的局限也使其说服力降低。
迄今,以不具备性染色体为主要论据而成立的康定湍蛙A. kangtingensis,仍存诸多矛盾和疑惑。其一,吴贯夫等(1987)的研究仅依据模式产地之一康定新都桥地区的标本而进行,而康定湍蛙模式产地为多个采集地点(Liu,1950),涉及折多山以西的雅砻江流域高原地区(海拔3000 m以上)、大渡河流域中高山区(海拔1800 m上下幅度大约600 m),其分布跨度范围大而广,那么其他几个模式产地及其相关范围的标本核型又如何呢?无性染色体这一重要的依据是否在其他种群成立?另一方面,四川湍蛙的核型研究现仅局限在物种水平,仅有宝兴盐井坪核型报道(吴贯夫,赵尔宓,1984),其他种下居群是否同样具有异形性染色体核型?其二,费梁等(2009)指出,四川湍蛙(含康定湍蛙)不同居群间及居群内不同个体的体形等差异变化较大,那么这些变化在一定的统计数量下是否存在规律可循?
故此,本研究拟以康定湍蛙的多个模式产地及其相关范围的标本为主要研究材料,从染色体核型、形态可量性状、分子系统发育等多个侧面展开研究,旨在对康定湍蛙的有效性及物种进行界定。
1 材料和方法 1.1 材料蔡红霞和赵尔宓(2008)、蔡红霞(2008)联合形态及分子数据的研究指出,四川湍蛙复合群所涉景东湍蛙A. tuberodepressus和金江湍蛙A. jinjiangensis为有效物种,凉山湍蛙为棕点湍蛙A. loloensis的同物异名,仅康定湍蛙尚存争议。故本研究标本范围将重点涵盖康定湍蛙和四川湍蛙模式产地及其各毗邻分布区。
康定湍蛙标本采自其多个模式产地及其分布区,包括折多山以西的高原地区、大渡河流域沿岸山溪。四川湍蛙标本采自其模式产地及多个分布区,包括大相岭及邛崃山系。核型研究标本共计16个居群173号个体(附录1),形态标本共计13个居群243号个体(附录2),分子标本采集康定湍蛙模式产地雅拉沟居群并联合GenBank下载数据(Lu et al.,2014),共计13个居群117号个体(附录3)。
1.2 方法 1.2.1 核型染色体标本制作方法参照吴贯夫和赵尔宓(1984),并稍加改进,即进行了2次注射,第一次皮下注射,间隔8~12 h后再次腹腔注射,第二次注射2 h后取材。选取康定湍蛙和四川湍蛙雌雄各10个较好的中期分裂相,用Leica DM2500显微镜对分裂相放大照相,并对染色体进行测量统计。染色体分类按Levan等(1964)的标准划分。
1.2.2 数量性状分析性状的测量依据刘承钊和胡淑琴(1961)的标准,并参照蔡红霞等(2008)选取并测量了其中25项常规性状:(1)头体长(SVL),(2)头长(HL),(3)头宽(HW),(4)鼻间距(IND),(5)眼间距(IOD),(6)上眼睑宽(UEW),(7)眼径(EL),(8)吻长(SL),(9)鼻吻距(NSD),(10)鼻眼距(NED),(11)上臂长(UAL),(12)前臂及手长(LAL),(13)手长(HAL),(14)臂长(AL),(15)前肢长(FLL),(16)第3指长(FL3),(17)第4指长(FL4),(18)股长(FEL),(19)胫长(TL),(20)跗足长(FRL),(21)足长(FOL),(22)后肢长(HLL),(23)跗部长(TAL),(24)第4趾长(TL4),(25)第3趾长(TL3)。所有标本均为性成熟个体,测量采用电子数显游标卡尺,精度0.01 mm。
本研究的湍蛙类群雌雄个体间的大小差异明显,故本文将雌、雄标本分别进行分析。全部形态学数据用Excel软件进行统计,为了消除异速生长差异,先将所得的25个常规性状数据进行常用对数lg的转换,然后使用SPSS 22.0软件进行主成分分析。
1.2.3 分子分析获取所有受检标本Cyt b基因片段。引物为Cyt b F:CATACATTACGCAGCCGATAC;Cyt b R: GGGGACGAGAAGGGCAAAGAT。引物设计及DNA片段扩增体系及程序参照Shan等(2014)。运用Bioedit(version 7.0.9.0,Hall,1999)进行序列分析,校正后的序列用MEGA(version 5,Tamura et al. ,2011)来进行DNA序列比对,并用DnaSP 5.0(Librado & Rozas,2009)进行单倍型统计,然后运用MRBAYES(version 3.2;Huelsenbeck & Ronquist,2001;Ronquist et al. ,2012)软件构建单倍型贝叶斯树(BI)。
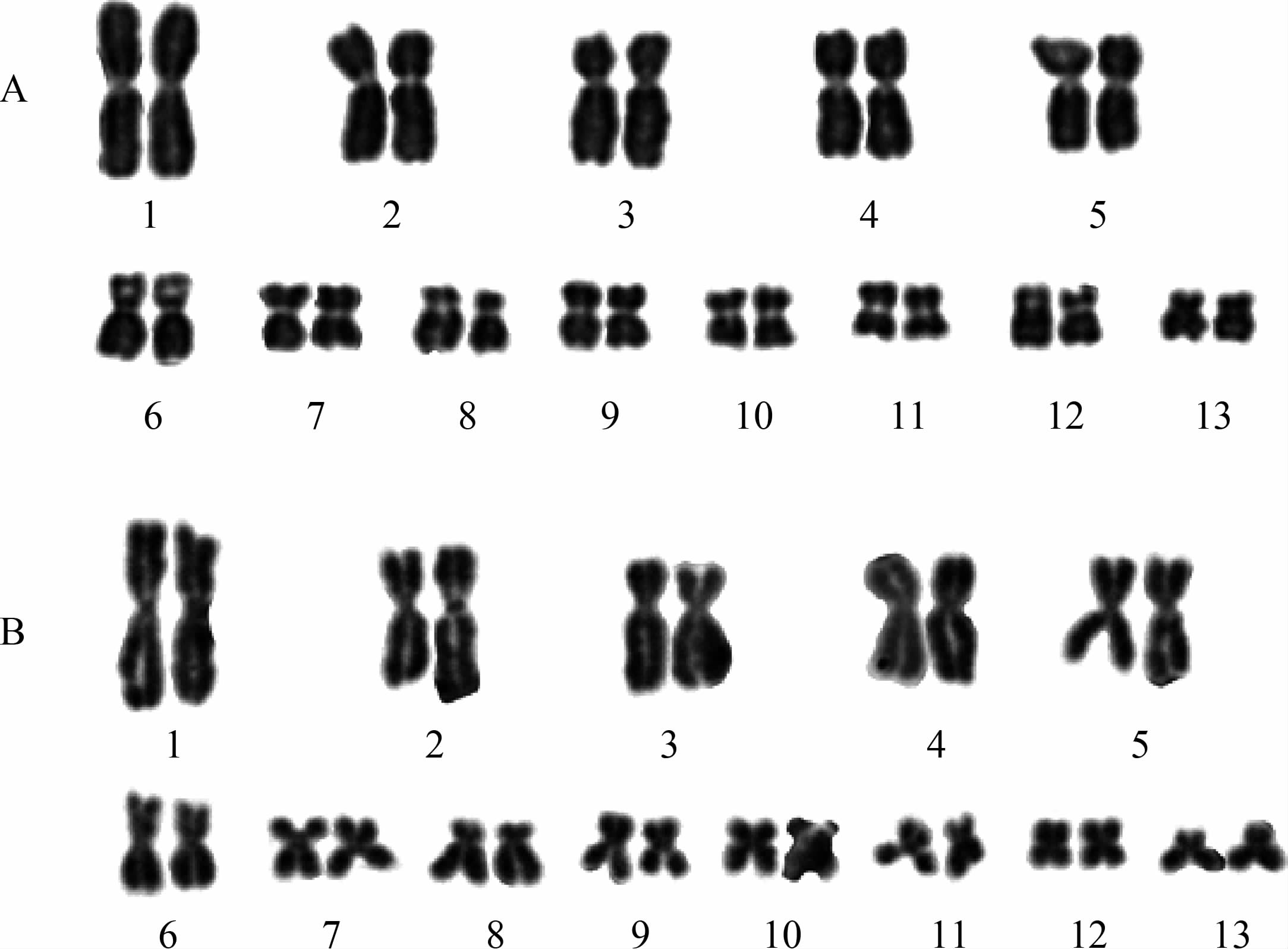
2 结果 2.1 染色体核型 2.1.1 康定湍蛙 检测出康定湍蛙种下存在2种明显不同的染色体核型,一种存在于折多山以西的雅砻江流域高原地区各种群,另一种存在于大渡河流域各种群。雅砻江流域核型:各居群标本染色体核型均为2n=26,由5对大染色体和8对小染色体组成,没有发现与性别相关的异形染色体(图 1,表 1)。
|
|
图 1 康定湍蛙核型
Fig. 1 Karyotype of Amolops kangtingensis
A. 康定朋布西雌性, B. 康定甲根坝雄性。 A. A female from Pengbuxi of Kangding, B. A male from Jiagenba of Kangding. |
| No. | 四川湍蛙Amolops mantzorum | 康定湍蛙Amolops kangtingensis | ||||
| 相对长度RL | 臂比AR | 着丝点类型Type | 相对长度RL | 臂比AR | 着丝点类型Type | |
| 1 | 13.86±0.99 | 1.16±0.11 | M | 14.16±0.74 | 1.12±0.12 | M |
| 2 | 11.85±0.85 | 1.44±0.12 | M | 11.92±0.64 | 1.48±0.15 | M |
| 3 | 10.57±0.76 | 1.91±0.13 | SM | 10.89±0.69 | 1.91±0.22 | SM |
| 4 | 10.09±0.77 | 1.38±0.12 | M | 10.53±0.57 | 1.38±0.13 | M |
| 5x | 9.30±0.59 | 1.25±0.13 | M | 9.61±0.42 | 1.26±0.15 | M |
| 5y | 9.05±0.47 | 3.29±0.62 | ST | — | — | — |
| 6 | 6.64±0.59 | 1.12±0.12 | M | 7.46±0.53 | 1.20±0.13 | M |
| 7 | 5.69±0.59 | 1.12±0.07 | M | 6.08±0.32 | 1.14±0.09 | M |
| 8 | 5.37±0.39 | 2.02±0.58 | SM | 5.66±0.36 | 2.11±0.37 | SM |
| 9 | 5.06±0.30 | 1.15±0.09 | M | 5.38±0.34 | 1.26±0.14 | M |
| 10 | 4.71±0.25 | 1.15±0.11 | M | 4.97±0.24 | 1.22±0.18 | M |
| 11 | 4.51±0.29 | 1.11±0.11 | M | 4.72±0.27 | 1.17±0.14 | M |
| 12 | 4.25±0.31 | 1.22±0.22 | M | 4.48±0.22 | 1.28±0.17 | M |
| 13 | 3.55±0.82 | 1.16±0.17 | M | 4.14±0.31 | 1.48±0.34 | M |
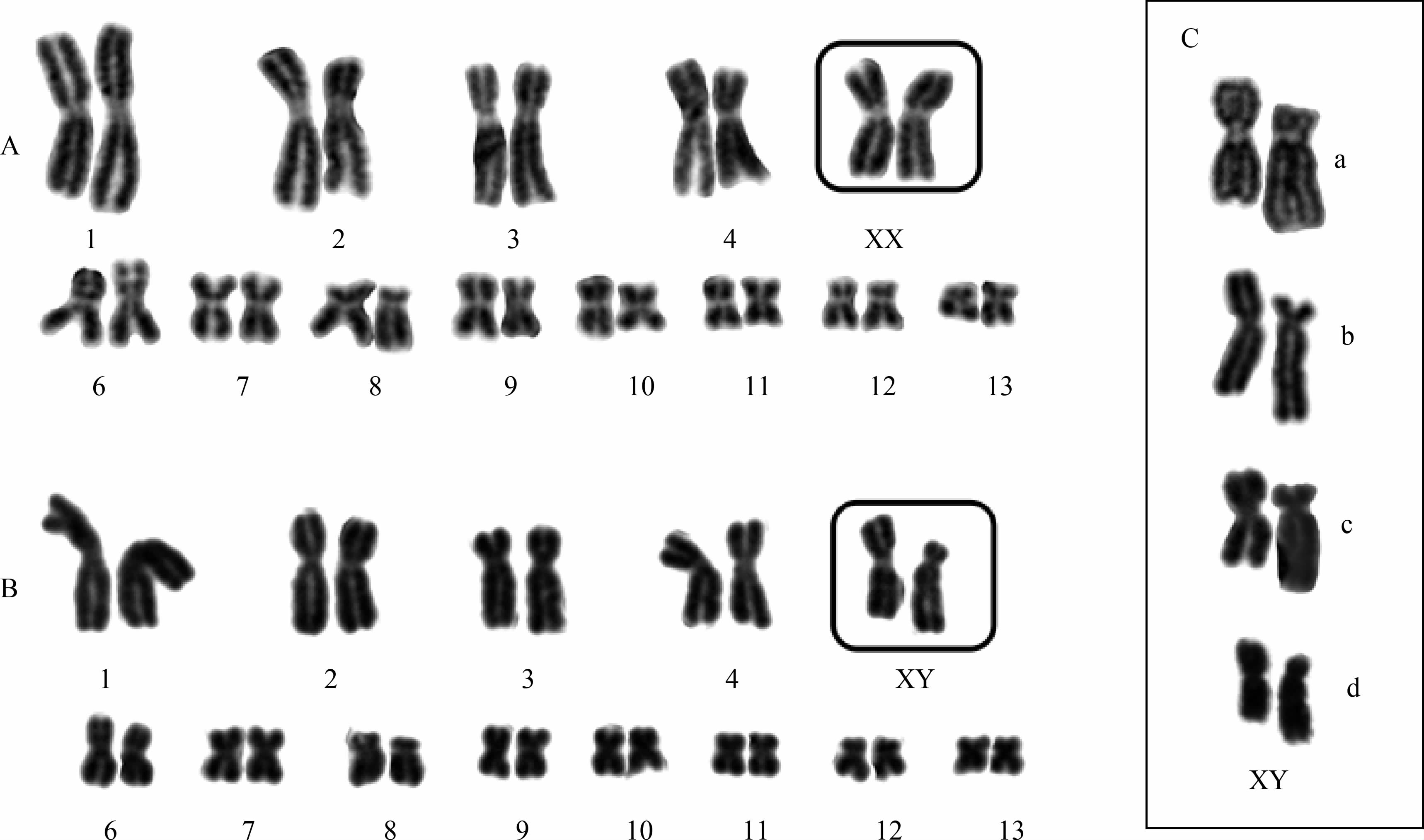
大渡河流域核型:所有受检居群标本染色体核型均为2n=26,由5对大染色体和8对小染色体组成。检测到与雄性性别相关的异形染色体对。雌性个体No.5染色体对同形,为中着丝粒染色体;雄性个体No.5染色体对异形,X为中着丝粒染色体,Y为亚端着丝粒染色体(图 2,表 1)。
|
|
图 2 四川湍蛙核型
Fig. 2 Karyotype of Amolops mantzorum A. 天全两路乡雌性, B. 泸定田坝乡雄性, C. 不同居群雄性No.5染色体对: 大邑西岭雪山(C-a)、泸定德威(C-b)、天全两路乡(C-c)、康定柳杨村(C-d)。 A. A female from Lianglu of Tianquan, B. A male from Tianba of Luding, C. Chromosomes No. 5 of four males from Xilingxueshan of Dayi(C-a), Dewei of Luding (C-b), Lianglu of Tianquan (C-c) and Liuyang of Kangding (C-d). |
所有受检居群标本染色体核型均为2n=26,由5对大染色体和8对小染色体组成。检测到与雄性性别相关的异形染色体对。雌性个体No.5染色体对同形,为中着丝粒染色体;雄性个体No.5染色体对异形,X为中着丝粒染色体,Y为亚端着丝粒染色体(图 2,表 1)。
2.2 数量性状分析 2.2.1 与主成分相关的特征雄性 前2个主成分的特征值分别为21.076、1.394,解释了总变异的89.88%(>85%)。一般而言,累计贡献率达到85%以上,即信息损失量在15%以下就能够反映综合指标所隐含信息的基本情况。因此,本文对PC1、PC2进行主成分分析。第一主成分解释了总变量的84.31%,除了鼻吻距和吻长2个性状以外,其余各个性状对第一主成分起了关键作用;第二主成分分析解释了总变异的5.58%,其中鼻吻距和吻长对其有关键作用(表 2:左)。雌性 前2个主成分的特征值分别为21.331、1.440,解释了总变异的91.08%(>85%),可以替代全部的基本信息,所以本文对 PC1、PC2 进行主成分分析。第一主成分解释了总变量的85.33%,除了鼻吻距和吻长2个性状以外,其余各个性状对第一主成分起了关键作用;第二主成分分析解释了总变异的5.76%,其中鼻吻距和吻长对其有关键作用(表 2:右)。
| 雄性Male | 雌性Female | ||||
| 变量 Variable | 成分Component | 变量 Variable | 成分Component | ||
| PC1 | PC2 | PC1 | PC2 | ||
| HAL | 0.953 | 0.250 | HAL | 0.956 | 0.235 |
| FLL | 0.952 | 0.264 | FLL | 0.953 | 0.270 |
| LAL | 0.943 | 0.250 | LAL | 0.941 | 0.307 |
| HLL | 0.935 | 0.323 | UAL | 0.927 | 0.195 |
| FRL | 0.934 | 0.313 | HLL | 0.927 | 0.336 |
| TL | 0.926 | 0.308 | TL | 0.924 | 0.307 |
| SVL | 0.924 | 0.271 | FRL | 0.921 | 0.332 |
| FEL | 0.909 | 0.337 | FL3 | 0.912 | 0.271 |
| UAL | 0.909 | 0.269 | FEL | 0.909 | 0.358 |
| FOL | 0.897 | 0.345 | SVL | 0.908 | 0.365 |
| FL4 | 0.891 | 0.383 | FL4 | 0.897 | 0.208 |
| FL3 | 0.883 | 0.386 | UEW | 0.894 | 0.239 |
| IOD | 0.857 | 0.431 | FOL | 0.888 | 0.367 |
| AL | 0.853 | 0.218 | EL | 0.877 | 0.299 |
| TAL | 0.849 | 0.204 | HW | 0.865 | 0.435 |
| TL4 | 0.849 | 0.204 | IND | 0.861 | 0.403 |
| TL3 | 0.846 | 0.386 | TL3 | 0.852 | 0.394 |
| EL | 0.845 | 0.347 | HL | 0.845 | 0.468 |
| HW | 0.844 | 0.355 | TAL | 0.833 | 0.239 |
| UEW | 0.811 | 0.401 | TL4 | 0.833 | 0.239 |
| HL | 0.797 | 0.512 | IOD | 0.827 | 0.507 |
| IND | 0.778 | 0.495 | AL | 0.814 | 0.413 |
| NED | 0.751 | 0.545 | NED | 0.721 | 0.599 |
| NSD | 0.109 | 0.967 | NSD | 0.091 | 0.980 |
| SL | 0.436 | 0.890 | SL | 0.453 | 0.883 |
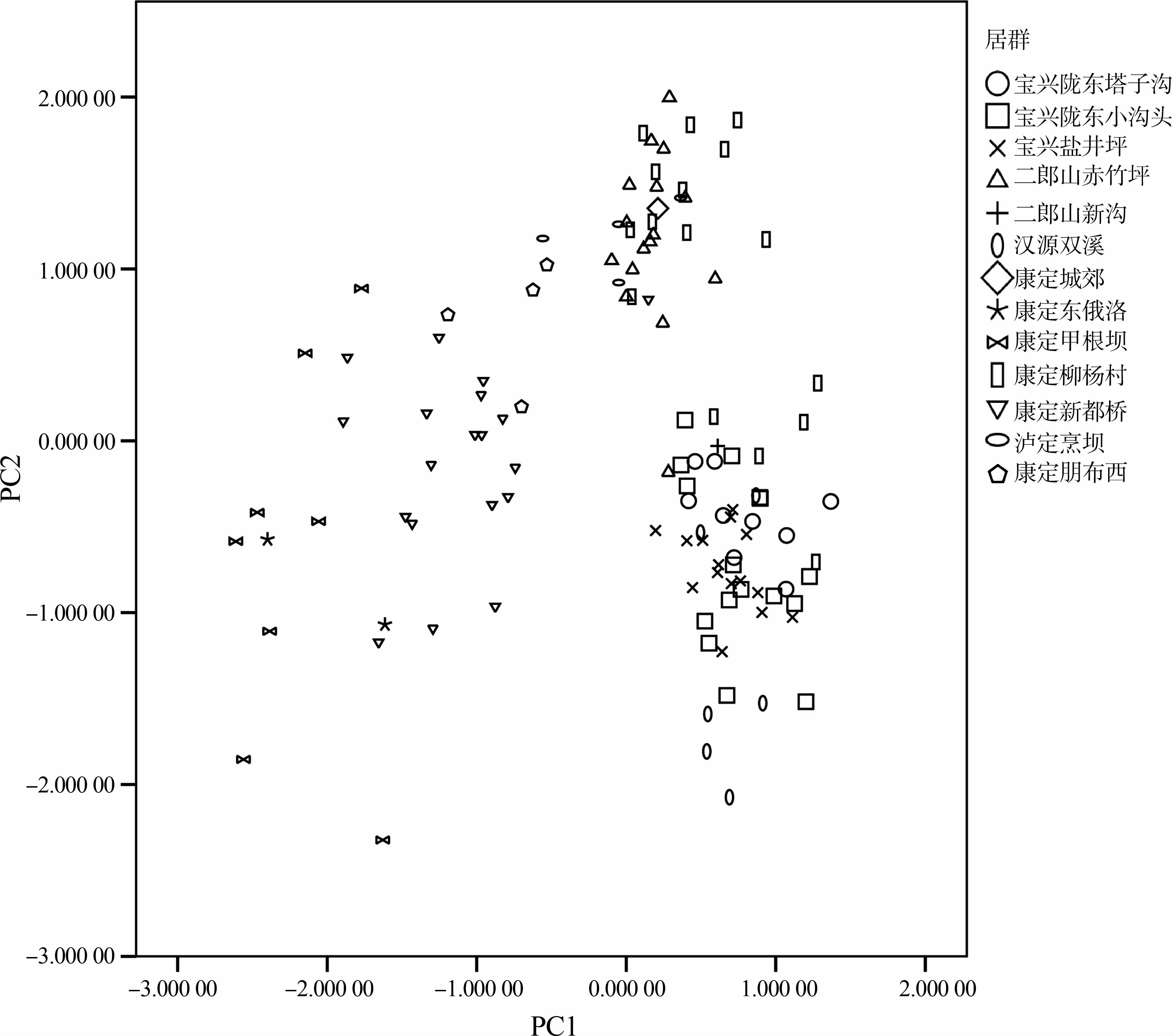
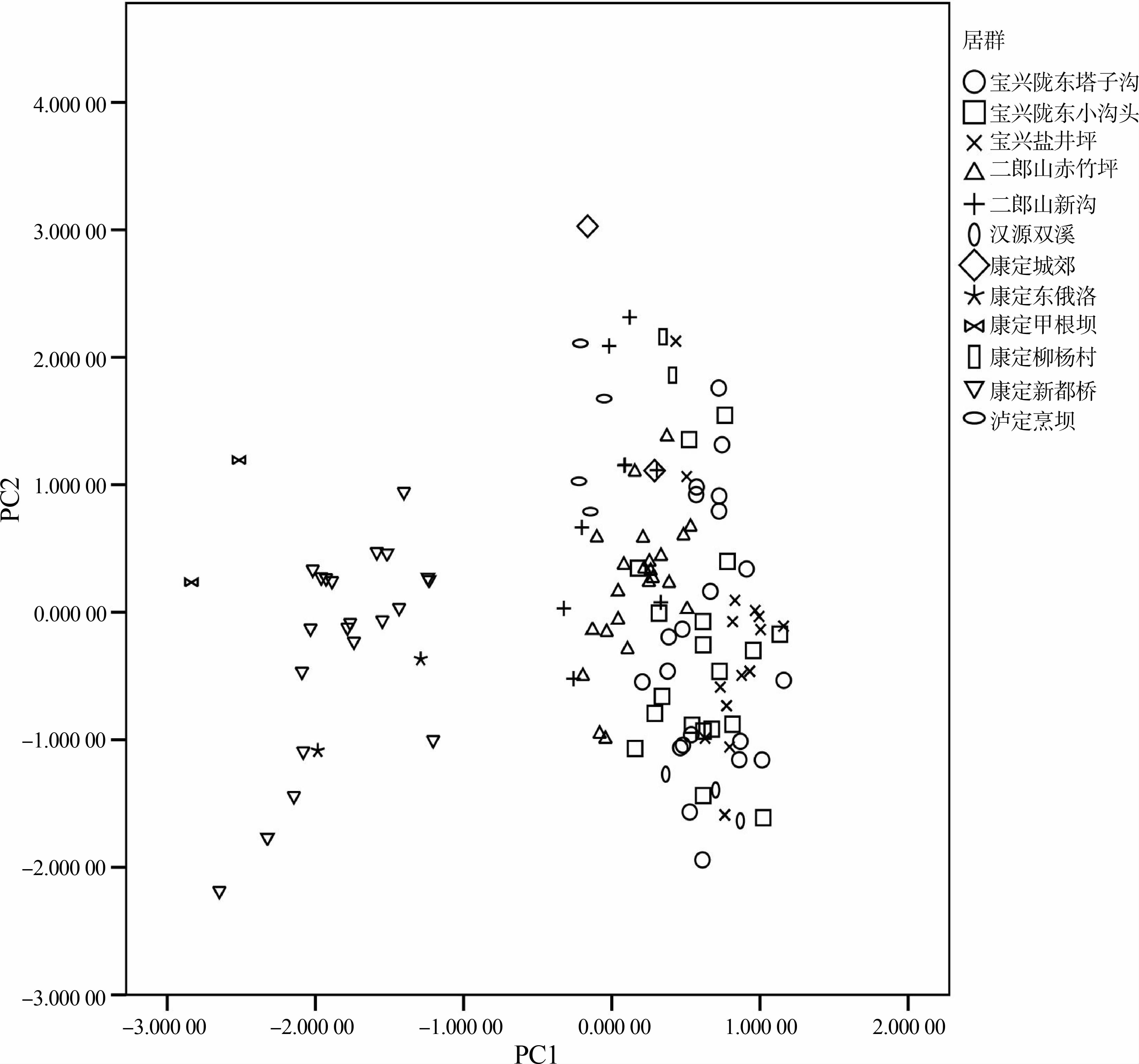
由上可知,雌性和雄性的前2个主成分解释的总变异都大于85%,表明对测量的雌、雄湍蛙的PC1、PC2 进行主成分分析能够反映综合指标隐含信息的基本情况。因此,本文用PC1为横坐标,PC2为纵坐标作散点图,以区别四川湍蛙和康定湍蛙各居群中在二维空间的分布情况(图 3、图 4)。
|
| 图 3 雄性湍蛙的第一、二主成分散点图 Fig. 3 Plots of principal component factors 1 and 2 of male Amolops sp. |
|
| 图 4 雌性湍蛙的第一、二主成分散点图 Fig. 4 Plots of principal components factors 1 and 2 of female Amolops sp. |
如图 3、图 4所示,雌、雄两性散点图基本一致(除去雌性中没有康定朋布西居群)。雌、雄个体均在水平轴方向形成左右2个分布区域,右边区域的居群包括:康定湍蛙的大渡河流域居群,即泸定烹坝、康定城郊和康定柳杨村;四川湍蛙的二郎山新 沟、二郎山赤竹坪、宝兴陇东塔子沟、宝兴陇东小沟头、宝兴盐井坪和汉源双溪居群。散点图的左边分布的居群有:康定湍蛙西部高原居群,即康定甲根坝、康定新都桥、康定东俄洛和康定朋布西居群。2个区域都存在较为明显的分布中心,较之雄性个体在散点图中的分布,雌性在水平轴方向形成左右2个完全分离的分布区域。仅一号雄性康定新都桥标本进入大渡河流域居群分布区。散点图上,康定湍蛙种下居群拆分成为2种分布状态:西部高原居群独立成为一个分布区,而大渡河流域居群则进入四川湍蛙模式产地所在的分布区域。
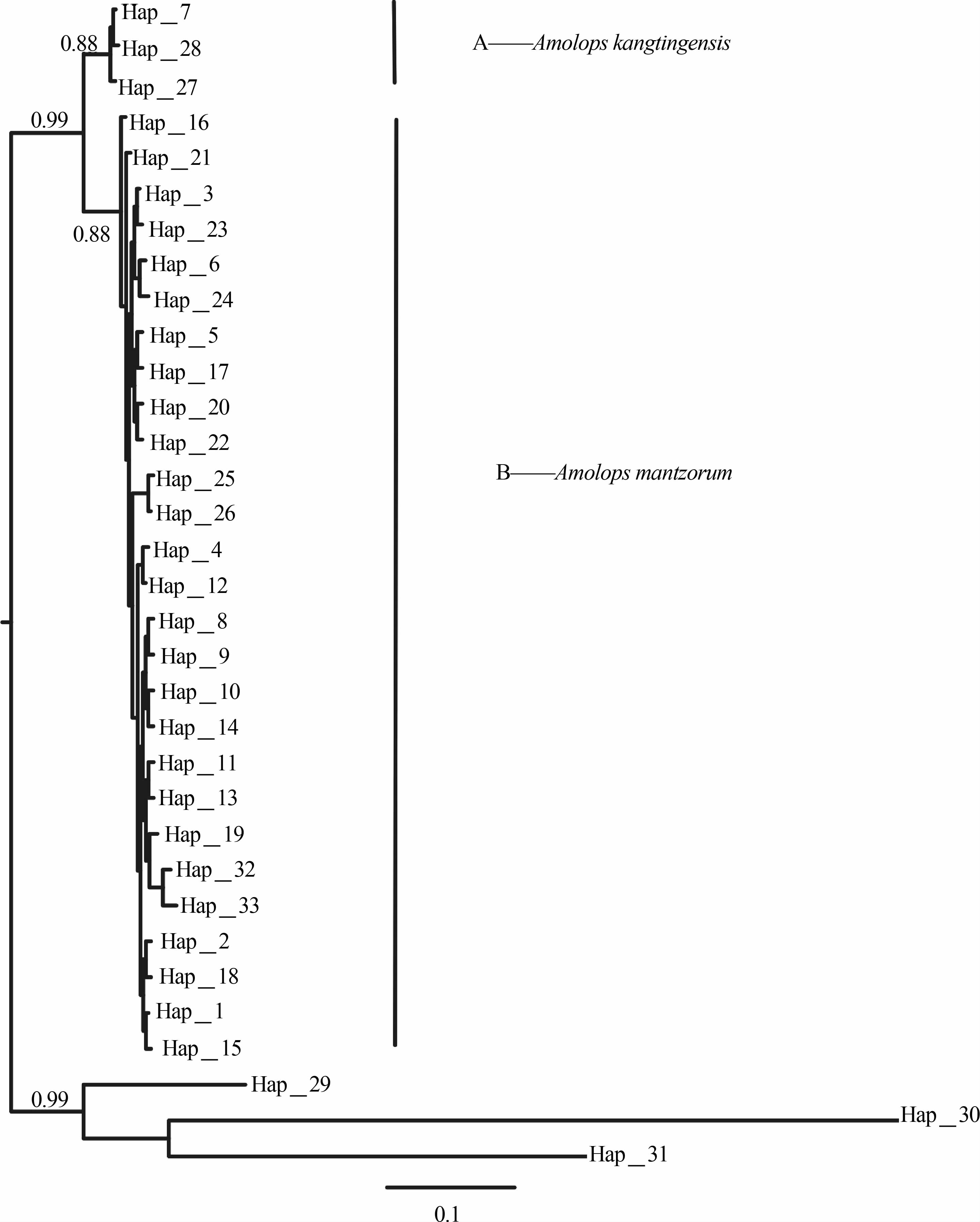
2.3 基于Cyt b基因片段构建的系统发生关系本研究运用MrBayes软件基于线粒体Cyt b基因片段所定义的33个单倍型构建了BI树(图 5),除去外群BI树主要分成A、B两大分支,其后验概率达到99%,显著支持了这2个分支的独立性。117条Cyt b基因片段共定义了33个单倍型,其中单倍型Hap7、Hap27、Hap28形成一个独立的分支A,其支持率为88%,包括康定甲根坝、炉霍、 雅江3个地方的标本,被Lu等(2014)指认为康定湍蛙。本文加入的3号康定雅拉沟标本YSQ472(Hap32)、xm5543(Hap32)、xm5804(Hap1)与Lu等(2014)的四川湍蛙宝兴陇东和盐井坪等居群的单倍型形成了独立的分支B,支持率为88%。单倍型情况详见附录3。
|
| 图 5 基于Cyt b基因33个单倍型的Bayesian树, 分支上方为分歧后验概率 Fig. 5 Cladgrame based on distances obtained from MrBayes, based on 33 haplotypes of Cyt b genes |
物种界定是生物学中最基本的问题之一。对于物种复合群(species complex)而言,一方面由于形态相似难以有明显间断的鉴别特征可使用,而另一方面不完全谱系筛选(incomplete linkage sorting)与种间渐渗(introgression)常常阻碍准确鉴定物种,来自遗传信息的证据也存在干扰。复合群的分类研究发展至今,居群水平的多论据支持较之过去更加必要(Barley et al.,2013)。
康定湍蛙依据多地混合标本订立,其模式产地包括康定雅拉沟、泸定城附近大渡河边、炉霍朱倭和康定新都桥等4个采集点。其分布范围可大致划分为大渡河和雅砻江两大流域,海拔跨度范围大致可划分为折多山以西的雅砻江流域高原地区(海拔3000 m以上)和大渡河流域中高山区(海拔1800 m,上下幅度大约600 m)。4个模式产地中,康定雅拉沟和泸定大渡河边隶属大渡河流域,炉霍朱倭和康定新都桥则隶属雅砻江流域高原地区。
康定湍蛙从四川湍蛙中分出独立成种,最主要的依据来自细胞遗传学研究。四川湍蛙模式产地宝兴(盐井坪)标本雄性No.5染色体对高度异形,雌性No.5染色体对同形,表现为XY雄性异配核型,其X染色体为M型,Y染色体为ST型(吴贯夫,赵尔宓,1984;吴政安等,1987)。吴贯夫等(1987)发现康定湍蛙模式产地(新都桥)标本中并不存在与性别相关的异形染色体对,其雌雄两性No.5染色体对均为M型,据此认为康定湍蛙应为有效物种。本文研究结果表明(图 2,表 1),含四川湍蛙模式产地在内的分布区(大相岭和邛崃山系)所有受检6个居群(附录1)标本染色体核型均与模式产地宝兴盐井坪核型一致,其雄性No.5染色体对高度异形,为XY雄性异配核型。然而,康定湍蛙种下存在2种明显不同的染色体核型。折多山以西的雅砻江流域高原地区各居群(附录1)与模式产地新都桥标本核型一致(图 1,表 1),而大渡河流域各居群(附录1)与四川湍蛙模式产地宝兴盐井坪核型一致,也与本文所有四川湍蛙受检居群核型一致(图 2,表 1)。细胞遗传学证据支持以新都桥为模式产地的康定湍蛙成立,雅砻江流域高原地区各居群隶属于该物种,而康定湍蛙大渡河流域各居群应划归四川湍蛙物种之中。
可量性状主成分分析结果表明(图 3,图 4),包括四川湍蛙模式产地居群在内的多个分布区(大相岭和邛崃山系),所有受检6个居群156号个体(附录2)在散点图中集中分布于水平轴的右边,可与水平轴左边的康定湍蛙雅砻江流域各居群个体完全分开(含模式产地康定新都桥,附录2),而康定湍蛙大渡河流域各居群个体(附录2)全部进入四川湍蛙内部,二者各居群间个体相互交错、重叠。这一结果与蔡红霞(2008)的相关可量性状分析相吻合,该研究利用9个种群246号馆藏标本,对四川湍蛙复合群所涉及的康定湍蛙、景东湍蛙、凉山湍蛙和金江湍蛙进行了可量性状主成分分析,发现采自康定新都桥的康定湍蛙标本可与其他物种各自分离,而采自泸定的康定湍蛙标本(4♀)则完全进入四川湍蛙内部。由此,形态可量性状证据同样支持以新都桥为模式产地的康定湍蛙成立,而康定湍蛙大渡河流域各居群应划归四川湍蛙物种之中。
在Lu等(2014)的基础上,新增加康定湍蛙模式产地康定雅拉沟标本,重建的线粒体Cyt b系统发育树与原有的结果一致(图 5)。即康定湍蛙折多山以西的雅砻江流域高原地区各居群(包括康定新都桥、炉霍等模式产地在内,附录3)构成一独立的支系,支持以新都桥为模式产地的康定湍蛙成立;康定湍蛙大渡河流域各居群进入四川湍蛙大相岭及邛崃山支系(包括康定湍蛙模式产地雅拉沟在内,附录3),应划归四川湍蛙物种之中。
3.2 分布区域界定形态、细胞、分子三方证据一致支持,以新都桥为模式产地的康 定湍蛙成立,而原康定湍蛙大渡河流域(包括康定湍蛙原模式产地康定雅拉沟和泸定城附近大渡河边在内)各居群应划归四川湍蛙物种之中。
综合现有的研究数据,将康定湍蛙分布区域大致界定于折多山以西的雅砻江流域高原地区,海拔3000 m及以上高山区,包括折多山以西的康定地区、泸霍、雅江等地。
附录1 核型分析标本(“*”示雅砻江流域,“#”示大渡河流域,“##” 示大相岭,“###”示邛崃山系) Appendix 1 Specimens in karyotype analysis(“*”shows Yalong River district,“#” shows Tatu River district,“##”shows Daxiangling Mt. ranges,and “###” shows Qionglai Mt. ranges) *康定甲根坝(Jiagenba of Kangding): ♀4,♂ 3 *康定朋布西(Pengbuxi of Kangding): ♀3 #康定柳杨村(Liuyang of Kangding): ♀1,♂ 1 #泸定烹坝乡(Pengba of Luding): ♀6,♂ 2 #泸定田坝乡(Tianba of Luding): ♀13,♂ 18 #泸定德威乡(Dewei of Luding): ♀6,♂ 13 #泸定杵泥乡(Chuni of Luding): ♀1 ###宝兴盐井坪(Yanjingping of Baoxing): ♀4,♂ 8 ###宝兴陇东崇义村(Chongyi of Baoxing): ♀3,♂ 3 ###宝兴陇东新江村(Xinjiang of Baoxing): ♀7,♂ 13 ###大邑西岭雪山(Xilingxueshan of Dayi): ♀18,♂ 6 ##荥经县泗坪乡(Siping of Yingjing): ♀9,♂ 4 ###天全两路乡(Lianglu of Tianquan): ♀3,♂ 11 #九龙湾坝乡(Wanba of Jiulong): ♀3,♂ 2 #九龙洪坝乡(Hongba of Jiulong): ♀3,♂ 2 #石棉蟹螺乡(Xieluo of Shimian): ♀2,♂ 1 附录2 形态测量标本(“*”示雅砻江流域,“#”示大渡河流域,“##” 示大相岭,“###”示邛崃山系) Appendix 2 Specimens examined in the morphological study(“*”shows Yalong River district,“#” shows Tatu River district,“##”shows Daxiangling Mt. ranges,and “###” shows Qionglai Mt. ranges) *康定甲根坝(Jiagenba of Kangding,KDJGB): ♀2,♂ 8 *康定朋布西(Pengbuxi of Kangding,KDPBX): ♂ 4 *康定新都桥(Xinduqiao of Kangding,KDXDQ): ♀21,♂ 19 *康定东俄洛(Dongerluo of Kangding,KDDEL): ♀2,♂ 2 #康定城郊(Chengjiao of Kangding,KDCJ): ♀2,♂ 1 #康定柳杨村(Liuyang of Kangding,KDLYC): ♀2,♂ 16 #泸定烹坝乡(Pengba of Luding,LDPB): ♀4,♂ 4 ###二郎山新沟(Xingou of Erlangshan,ELSXG): ♀9,♂ 1 ###二郎山赤竹坪(Chizhuping of Erlangshan,ELSCZP): ♀23,♂ 16 ###宝兴陇东塔子沟(Tazigou of Baoxing,BXLDTZG): ♀21,♂ 9 ###宝兴陇东小沟头(Xiaogoutou of Baoxing,BXLDXGT): ♀19,♂ 16 ###宝兴盐井坪(Yanjingping of Baoxing,BXYJP): ♀18,♂ 15 ##汉源双溪(Shuangxi of Hanyuan,HYSX): ♀3,♂ 6 附录3 分子分析标本(“*”示雅砻江流域,“#”示大渡河流域,“##” 示大相岭,“###”示邛崃山系)及单倍型 Appendix 3 Specimens/halotype examined in the molecular study(“*”shows Yalong River district,“#” shows Tatu River district,“##”shows Daxiangling Mt. ranges,and “###” shows Qionglai Mt. ranges) 外群(Outgroup) 绿点湍蛙A. viridimaculatus,腾冲(Tengchong): n=1,KJ008459/Hap29 华南湍蛙A. ricketti,张家界(Zhangjiajie): n=1,KJ008461/Hap30 崇安湍蛙A. chunganensis,大邑县茶地坪(Chadiping of Dayi): n=1,KJ008460/Hap31 康定湍蛙A. kangtingensis *康定甲根坝(Jiagenba of Kangding): n=2,KJ008415,KJ008423/Hap7 *雅江(Yajiang): n=12,KJ008410~KJ008422,KJ008380/Hap7,Hap27,Hap28 *炉霍(Luhuo): n=12,KJ008381~KJ008392/Hap7 四川湍蛙 A. mantzorum #康定雅拉沟(Yalakou of Kangding): n=3,YSQ472,xm5804,xm5543/Hap1,Hap32,Hap33 #康定(Kangding): n=17,KJ008393~KJ008409/Hap1,Hap8,Hap10 #泸定烹坝乡(Pengba of Luding): n=4,KJ008328~329,KJ008424~425/Hap1,Hap2,Hap13 ##荥经泥巴山(Nibashan of Yingjing): n=10,KJ008292~293,321,KJ008325~327,KJ008333~335/Hap1,Hap3,Hap14,Hap19,Hap24 ##汉源(Hanyuan): n=7,KJ008295~296,321,KJ008325~327/Hap1,Hap3,Hap8,Hap12,Hap22 ### 宝兴盐井坪(Yanjingping of Baoxing): n=9,KJ008307~314,KJ008317~318/Hap1,Hap3,Hap12,Hap16,Hap20,Hap21 ###宝兴陇东(Longdong of Baoxing): n=14,KJ008288~291,KJ008297~306/Hap1,Hap3,Hap11,Hap17,Hap18,Hap21,Hap26 ###大邑西岭(Xiling of Dayi): n=13,KJ008341~351,KJ008370~371/Hap1,Hap3,Hap5,Hap23,Hap25 ###天全(Tianquan): n=8,KJ008319~324,KJ008330~332/Hap1,Hap4,Hap6,Hap9,Hap15 ###崇州(Chongzhou): n=3,KJ008339~340,KJ008311/Hap3,Hap5| 蔡红霞, 赵尔宓. 2008. 中国横断山区湍蛙属4个物种有效性的探讨[J]. 四川动物, 27(4): 483-488. |
| 蔡红霞. 2008. 湍蛙亚科Amolopsinae (sensu Yang, 1991)的系统发育学研究[D]. 成都: 四川大学. |
| 费梁, 胡淑琴, 叶娼媛, 等. 2009. 中国动物志: 两栖纲(下卷)(无尾目 蛙科)[M]. 北京: 科学出版社: 1538-1545. |
| 费梁, 叶昌媛, 黄永昭. 2005. 中国两栖动物检索及图解[M]. 四川: 四川科学技术出版社: 150-158. |
| 刘承钊, 胡淑琴. 1961. 中国无尾两栖类[M]. 北京: 科学出版社: 226-243. |
| 吴贯夫, 谭安鸣, 赵尔宓. 1987. 康定湍蛙为一有效种的细胞学证据[J]. 两栖爬行动物学报, 6(4): 9-41. |
| 吴贯夫, 赵尔宓. 1984. 无尾类两种罕见的核型——四川湍蛙及凉山湍蛙的核型[J]. 两栖爬行动物学报, 3(4): 5-10. |
| 吴政安, 谭安鸣, 赵尔宓. 1987. 横断山区四种湍蛙的细胞遗传学研究[J]. 遗传学报, 14(1): 63-68. |
| Barley AJ, White J, Diesmos AC, et al. 2013. The challenge of species delimitation at the extremes: diversification without morphlogical logical change in Philippine Sun Skink[J]. Evolution, 67(12): 3556-3572. |
| Dubois A. 1992. Notes sur la classification des Ranidae (Amphibiens; Anoures)[J]. Bull mens Soc Linn Lyon, 61: 305-352. |
| Frost DR. 2014. Amphibian species of the world: an online reference. version 5.6[EB/OL].(2013-01-09). http://research.amnh.org/herpetology/amphibia/index.html. |
| Hall TA. 1999. Bioedit: a user-friengly biological sequence alignment editor an analysis program for Windows 95/98NT[J]. Nycleicacids Symposium Series, 41: 95-98. |
| Huelsenbeck JP, Ronquist F. 2001. MrBayes: Bayesian inference of phylogeny[J]. Bioinformatics, 17: 754-755. |
| Levan A, Fredga K, Sandberg A. 1964. Nomenclature for centromeric position on chromosomes[J]. Hereditas, 5(2): 201-220. |
| Librado P, Rozas J. 2009. DnaSP v5: a software for comprehensive analysis of DNA polymorphism data[J]. Bioinformatics, 25(11): 1451-1452. |
| Liu CC. 1950. Amphibian of western China[M]. Fieldiana Zool Mem Chicago, 2: 349-352. |
| Lu B, Bi K, Fu JZ. 2014. A phylogeographic evaluation of the Amolops mantzorum species group: cryptic species and plateau up-lift[J]. Mol Phylogenet Evolution, 73: 40-52. |
| Ronquist F, Teslenko M, van der Mark P, et al. 2012. MrBayes 3.2: efficient Bayesian phylogenetic inference and model choice across a large model space[J]. Syst Biol, 61: 539-542. |
| Shan X, Xia Y, Kakehashi R, et al. 2014. Complete mitochondrial genome of Amolops mantzorum(Anura:Ranidae)[J]. Mitochondrial DNA, Early Online: 1-3. |
| Tamura K, Peterson D, Peterson N, et al. 2011. MEGA5: molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods[J]. Mol Biol Evol, 28: 2731-2739. |
| Zhao EM, Adler K. 1993. Herpetology of China[M]. Oxford, Ohio, USA: The Study of Amphibians and Reptiles in cooperation with Chinese Society for the Study of Amphibians and Reptiles: 134. |
 2015, Vol.
2015, Vol. 




