扩展功能
文章信息
- 孙云霄, 张艳春, 靳丽莎, 陈子亮, 张秀娟, 沈琪琦, 饶军华, 张礼标
- SUN Yunxiao, ZHANG Yanchun, JIN Lisha, CHEN Ziliang, ZHANG Xiujuan, SHEN Qiqi, RAO Junhua, ZHANG Libiao
- 雄性食蟹猴高敏C反应蛋白基础值及高脂膳食诱导后与血脂变化的关系研究
- Study on the High Sensitive C-reactive Protein Basic Values of Male Cynomolgus Monkeys and the Relationship with High-fat Diet Induced Blood Lipid Change
- 四川动物, 2015, 34(5): 734-738
- Sichuan Journal of Zoology, 2015, 34(5): 734-738
- 10.11984/j.issn.1000-7083.20140549
-
文章历史
- 收稿日期:2014-12-6
- 接受日期:2015-06-08
2. 广东蓝岛生物技术有限公司, 广州 510555
2. Guangdong Landau Biotechnology Co., Ltd, Guangzhou 510555, China
心血管疾病是当今许多国家高死亡率的主要原因(Kahn et al.,2008),这与当前人们膳食水平明显提高密切相关,血脂水平的升高是动脉粥样硬化(atherosclerosis,AS)重要危险因素。AS是心血管病的病理基础,是一种炎症性自身免疫性疾病,炎症反应参与了其整个发生发展过程。研究表明AS、高脂血症和胰岛素抵抗都与慢性和亚临床炎症相关,表现为血液循环中致炎蛋白水平的升高(Mendall et al.,1996;Yudkin et al.,1999)。在众多炎症标志物中,高敏C反应蛋白(high sensitive C-reactive protein,hs-CRP)研究的相对较多,有研究表明它可能在AS斑块形成的过程中起着直接的促进作用(Pasceri et al.,2000)。对hs-CRP的研究及其在AS包括其他心血管病研究中越来越受到科研人员的重视(Fernández,2007;Cozlea et al.,2013;Juan et al.,2014)。用于心血管病研究的实验动物有很多,但猕猴属Macaca动物(包括食蟹猴M. fascicularis和恒河猴M. mulatta)与人类的遗传同源性达到92.5%~95.0%(Yang et al.,2010),且在心血管功能、脂质代谢、AS病变的性质和部位、临床症状以及各种药品的疗效关系等,都与人体的非常相似。尽管早在20世纪80、90年代就有很多研究人员利用恒河猴作为模式动物研究心血管病,但恒河猴价格更为昂贵,体型较大,性格较为暴烈,在实验过程中不易操作,且在实验过程中用药量也相对较大,当前许多研究工作越来越倾向于采用体型较小、性格相对温和的食蟹猴作为疾病动物模型。目前针对食蟹猴hs-CRP基础值的调查研究还鲜有报道,对心血管病的相关研究缺乏相应的基础数据进行参考比对,因此,对hs-CRP本底数据的调查就显得尤为重要。
临床上男性心血管病的发病率与致死率明显高于女性,实验动物的选择上也多应用雄性动物来进行相关研究。因此,本研究的调查对象为雄性食蟹猴,检测不同年龄段雄性食蟹猴的hs-CRP基础值,并进行差异比较分析,以期初步获得雄性食蟹猴hs-CRP的基础数据,为高脂血症及心血管病的相关研究提供重要的参考依据。另外,选择一定数量的成年食蟹猴通过高脂诱导,观察血脂升高后hs-CRP值的变化,考察血脂主要指标与hs-CRP关系,为高脂血症及心血管病的研究提供更为详细的参考数据。
1 材料1.1 动物选择雄性食蟹猴共150只,来源于广东蓝岛生物技术有限公司,使用许可证编号为SYXK(粤)2013-0088,生产许可证编号为SCXK(粤)20014-0010。年龄3~25岁,采用单笼(规格:70 cm×70 cm×80 cm)饲养,每笼 1只,饲养室内温度18~26 ℃,相对湿度60%~80%。将150只食蟹猴分批次置于单笼喂养1~2周后,检测后排除指标异常猴,筛选出健康猴,并按3个年龄段进行分组(季芳等,2006;郝香芬等,2011):3~6岁组、7~10岁组和大于11岁组,体质量3.3~14.0 kg,各组食蟹猴数量分别为34只、56只、22只。饲料为实验猴专用饲料,且辅以时令水果等青饲料,人工每日定时喂养,对不同年龄段hs-CRP的基础值进行检测分析;另外选择15只8~9岁雄性食蟹猴,其中10只高脂饲料进行喂养,5只正常饲料,均每日配以适量青饲料,所有食蟹猴均自由取水饮用。
1.2 实验材料高脂饲料由广州市饲料研究所根据配方进行生产,置于低温冷库保存,保质期2周。胆固醇来自广州市齐云生物技术有限公司,纯度≥95%。麻醉药盐酸氯胺酮由沈阳兽药厂生产。
2 方法2.1 正常食蟹猴血样的采集采血前需隔夜禁食,用盐酸氯胺酮(0.05 mg·kg-1)轻度麻醉食蟹猴,待麻醉10~20 min后,测定体质量和坐高,采后肢静脉全血,室温静置30 min,低温4 ℃,4000 r·min-1离心(Ependorf 5810r),取上层血清,低温状态下送检。检测的主要血生化指标包括总胆固醇(total cholesterol,TC),低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)及hs-CRP(免疫比浊法测定),全部由广州金域医学检验中心检测获得,所用仪器为罗氏P800,且均为罗氏配套试剂与试剂盒。采血时间为1.5个月左右一次,高脂膳食诱导前采集3次,随即开始高脂膳食饲喂食蟹猴,高脂诱导后第1次检测在2个月后,再连续收集8次血清并送检。
2.2 高脂膳食诱导采用高脂膳食饲料,饲料配方为1.5%胆固醇,15.0%油脂,83.5%猴生长期基础饲料补足,单笼喂养筛选出的15只健康雄性食蟹猴,10只高脂膳食喂养,另外5只普通饲料喂养作为对照组。实验过程中观察记录食蟹猴外观、行为及日常饮食情况。
2.3 数据处理方法文中所有数据采用SPSS软件进行统计学分析,统计分析采用Student’s t test,实验中测得所有数据以x±s的形式表示,P<0.01表示差异有高度统计学意义,P<0.05表示差异有统计学意义。
3 结果3.1 不同年龄段雄性食蟹猴hs-CRP基础值分别对不同年龄段的雄性食蟹猴进行血生化检测,排除血脂和血糖异常猴,对正常食蟹猴的hs-CRP值进行统计分析(表 1)。
| 年龄组/岁 Age group/yr |
数量 Number |
高敏C反应蛋白 hs-CRP/mg·L -1 |
| 3~6 | 34 | 2.78±1.48 * |
| 7~10 | 56 | 2.31±1.52 * |
| ≥11 | 22 | 6.09±2.06 |
| 注:*与大于11岁组相比,P<0.05。 Note:* compared with the group of ≥11 year-old monkeys, P<0.05. |
||
从上述结果看,低龄食蟹猴、中年食蟹猴与老年食蟹猴的hs-CRP差异均有统计学意义,而低龄组与中年组食蟹猴之间没有表现出明显差异。
3.2 不同年龄段雄性食蟹猴与雄性食蟹猴群体hs-CRP基础值的比较对112只雄性食蟹猴进行hs-CRP的总体分析统计,hs-CRP群体均值为3.19 mg·L-1±2.16 mg·L-1(表 2)。
| 年龄组/岁 Age group/yr |
数量 Number |
高敏C反应蛋白 hs-CRP/mg·L -1 |
| 3~6 | 34 | 2.78±1.48 |
| 7~10 | 56 | 2.31±1.52 * |
| ≥11 | 22 | 6.09±2.06 * |
| 群体 | 112 | 3.19±2.16 |
| 注:*与雄性群体hs-CRP值相比, P<0.05。 Note: * compared with the hs-CRP value of the whole, P<0.05. |
||
老年食蟹猴的平均值明显高于群体平均值。而中年食蟹猴的平均值明显低于雄性群体均值。考虑到老年食蟹猴hs-CRP结果与低年龄段食蟹猴的明显差异,因此,此结果与群体检测时选择的不同年龄段的食蟹猴样本量有关。
3.3 高脂膳食诱导食蟹猴血清TC、LDL-C值与hs-CRP值的变化实验选择中年雄性食蟹猴进行高脂膳食诱导,诱导前和诱导后定期检测对照组和诱导组的TC与hs-CRP,检测结果见图 1,图 2。

|
|
图 1 高脂膳食诱导后食蟹猴总胆固醇值的变化
Fig. 1 Variation of TC concentration after high fat diet-induction
HF代表高脂诱导组, *表示与对照组相比差异有统计学意义(P<0.05), **表示差异有高度统计学意义(P<0.01);下图同。 HF represents the group induced by high-fat diet, * means significant difference and ** means extremely significant difference from the control group (P<0.01); the same below. |
|
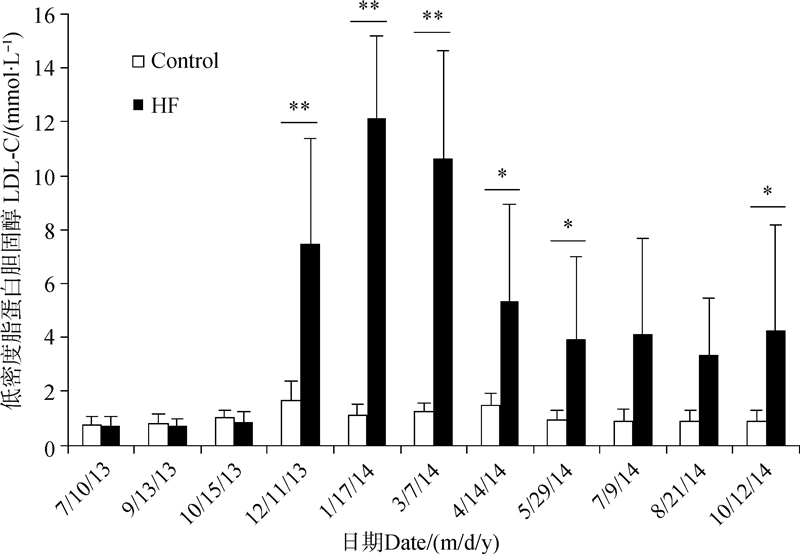
| 图 2 高脂膳食诱导后食蟹猴低密度脂蛋白胆固醇值的变化 Fig. 2 Variation of LDL-C concentration after high fat diet-induction |
图 1显示高脂膳食诱导初期食蟹猴的总胆固醇明显升高,与对照组有明显差异,且一直持续到后期。
图 2显示LDL-C与总胆固醇结果类似,高脂膳食诱导初期明显升高,与对照组的差异有高度统计学意义,且在实验结束的最后一次检测到的差异有统计学意义。
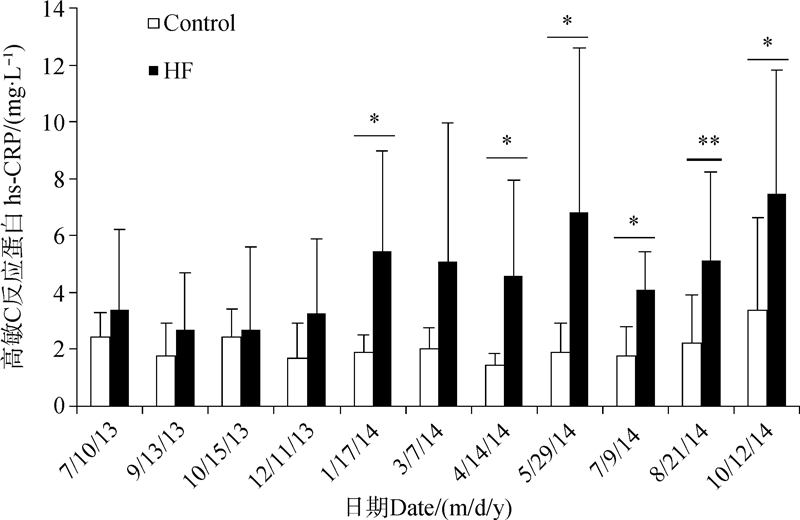
从图 3可以看出,随着血脂水平的升高,在高脂膳食诱导后的第2次血清检测(也即图上第5次血清检测)时hs-CRP水平显著高于对照组,随后阶段与对照组相比总体也维持在较高水平。
|
| 图 3 高脂膳食诱导后食蟹猴高敏C反应蛋白值的变化 Fig. 3 Variation of hs-CRP concentration after high fat diet-induction |
近年来的研究表明,AS是一个慢性炎症过程,是各类心脑血管疾病的病理基础。而C反应蛋白(C-reactive protein,CRP)是由肝脏产生的急性期反应物,其浓度低于10 mg·L-1时,常称为hs-CRP,是与AS的发生、演变和进展有关的促炎因子,是一个可以预测未来心血管事件发生危险的预警因子(Liu et al.,2013)。另外,有越来越多的证据表明CRP可能具有致心血管病发生的作用(Cozlea et al.,2013;Bian et al.,2014)。心血管疾病的一级和二级预防可以从降低CRP的治疗中受益,并期待能特异性阻断CRP结合并抑制其促炎效应的新型药物问世。因此,当前对CRP的研究及其应用成为针对AS、高脂血症及心血管病临床、机理和药物研发的一个热点。但很多前期及相关研究在人体并不能实现,所以选择合适的实验动物就显得尤为重要。无论是从遗传相似度、寿命范围,还是生理代谢等多方面都表明非人灵长类动物是理想的模型动物。而目前未见有对非人灵长类CRP的相关报道,因此对非人灵长类动物CRP的基础值的调查研究就显得尤为必要。
研究中调查了不同年龄段雄性食蟹猴的hs-CRP的大概正常值范围,确定雄性食蟹猴群体hs-CRP均值为3.19 mg·L-1±2.16 mg·L-1。而不同年龄段的hs-CRP值存在差异,老龄雄性食蟹猴的hs-CRP平均值高于中年和低龄食蟹猴(6.09 mg·L-1±2.06 mg·L-1 VS. 2.78 mg·L-1±1.48 mg·L-1 & 2.31 mg·L-1±1.52 mg·L-1),且差异有统计学意义(P<0.05)。表 2中的hs-CRP群体值与老年食蟹猴和中年食蟹猴的差异有统计学意义(P<0.05),进一步表明如果不分年龄层次随机选择动物进行动物实验时,某些重要的检测指标可能会不具备准确的参考、判断或应用价值。与临床上不同检测方法hs-CRP的正常值范围不同,本结果送广州金域医学检验中心检测得到结果,检测报告中给出的正常值范围为0~5 mg·L-1,正常雄性食蟹猴群体hs-CRP均值与低龄和中年食蟹猴均与此结果一致。但老年食蟹猴的均值超出此正常值范围,这可能与老年个体的内环境的自稳能力下降,器官功能老化受损而处于应激或炎症状态有关(傅朝平等,2005)。可进一步扩大雄性食蟹猴的检测样本数以进一步确定。
研究对8~9岁雄性食蟹猴经高脂膳食诱导后的TC、LDL-C与hs-CRP进行检测发现,高脂膳食诱导后随食蟹猴TC含量显著升高(P<0.05),LDL-C结果与TC结果类似,诱导后显著升高(P<0.05),hs-CRP与对照组比较也有明显升高(P<0.05)。TC前期的急剧上升可能与尚未启动体内的调节机制有关,经过一段时间的高脂膳食的适应期,后期进入稳定阶段并保持在一定的高值水平。指标检测结果显示hs-CRP水平的显著升高,时间上稍滞后于TC与LDL-C水平的显著升高,提示本研究中hs-CRP的显著升高可能与血清中的血脂水平升高有关,也表明在以后的检测中如果能单独检测到hs-CRP水平升高,则血清中的血脂水平也很可能高于正常,所以hs-CRP在动物相关研究中也可以考虑作为心血管病的独立危险因素加以应用,且准确性应高于血脂指标。
本研究初步测定了不同年龄段的雄性食蟹猴的hs-CRP正常值范围,并对高脂膳食诱导后的hs-CRP值的变化进行测定,为高脂血症、AS及心血管疾病等在涉及非人灵长类动物实验方面的相关研究提供相关的参考数据。但本研究只涉及了雄性食蟹猴hs-CRP的检测,后期研究中可对雌性食蟹猴进行检测,并与雄性比较,考察性别之间是否存在差异,另外,对已获得的数据也可以扩大样本量,或更细化的年龄分段进行比较,以期获得更为详实可靠的食蟹猴hs-CRP值范围。
| 傅朝平, 王新生, 胡舜英. 2005. 年龄、血糖与血脂、血压[J]. 中华临床医学杂志, 4(6):25-27. |
| 郝香芬, 万玉玲, 李学家, 等. 2011. 食蟹猴的基础血糖值调查[J]. 四川动物, 30(1):111-114. |
| 季芳, 饶军华, 刘晓明. 2006. 人工饲养恒河猴血液生化正常参考值的测定与分析[J]. 中国比较医学杂志, 16(6):345-349. |
| Bian F, Yang X, Zhou F, et al. 2014. C-reactive protein promotes atherosclerosis by in creasing LDL transcytosis across endothelial cell[J]. Br J Pharmacol, 171(10):2671-2684. |
| Cozlea DL, Farcas DM, Nagy A, et al. 2013. The impact of C reactive protein on global cardiovascular risk on patients with coronary artery disease[J]. Curr Health Sci Journal, 39(4):225-231. |
| Fernández MC. 2007. New perspectives in the measurement of cardiovascular risk:explorations to detect subclinical atherosclerosis and inflammation markers[J]. Med Clin, 128(9):344-351. |
| Juan S, María SM, Mervin C, et al. 2014. C-reactive protein:clinical and epidemiological perspectives[J]. Cardiol Res and Pract, 2(6):1-10. |
| Kahn R, Robertson RM, Smith R, et al. 2008. The impact of prevention on reducing the burden of cardiovascular disease[J]. Circulation, 118(5):576-585. |
| Liu SJ, Liu WH, Zhong Y, et al. 2013. Glycogen synthase kinase-3β is involoved in C-reactive protein-induced endothelial cell activation[J]. Biochemistry, 78(8):915-919. |
| Mendall MA, Patel P, Ballam L, et al. 1996. C reactive protein and its relation to cardiovascular risk factors:a population based cross sectional study[J]. BMJ Open, 312(7038):1061-1065. |
| Pasceri V, Willerson JT, Yeh ET. 2000. Direct proinflammatory effect of C-reactive protein on human endothelial cells[J]. Circulation, 102(18):2165-2168. |
| Yang SH, Dou KF, Song WJ. 2010. Prevalence of diabetes among men and women in China[J]. N Engl J Med, 362(25):2425-2426 |
| Yudkin JS, Stehouwer CDA, Emeis JJ, et al. 1999. C-reactive protein in healthy subjects:associations with obesity, insulin resistance, and endothelial dysfunction[J]. Arterioscler Thromb Vasc Biol, 19(4):972-978. |
 2015, Vol. 34(5)
2015, Vol. 34(5)




