扩展功能
文章信息
- 张秀娟, 陈金平, 张全军, 刘朝明, 刘晓明, 赖良学, 张守全
- ZHANG Xiujuan, CHEN Jinping, ZHANG Quanjun, LIU Zhaoming, LIU Xiaoming, LAI Liangxue, ZHANG Shouquan
- 重组人促卵泡激素剂量对食蟹猴卵泡发育和排卵同期化的影响
- Effects of rhFSH on Ovarian Follicular Development and Ovulation Synchronization in Macaca fascicularis
- 四川动物, 2015, 34: 407-410
- Sichuan Journal of Zoology, 2015, 34: 407-410
- 10.3969/j.issn.1000-7083.2015.03.015
-
文章历史
- 收稿日期:2014-05-20
- 接受日期:2015-01-23
2. 中国科学院广州生物医药与健康研究所, 广州 510530;
3. 华南农业大学动物科学学院, 广州 510642
2. Guangzhou Institutes of Biomedicine and Health, Chinese Academy of Sciences, Guangzhou 510530, China;
3. College of Animal Sciences, South China Agricultural University, Guangzhou 510642, China
非人灵长类动物(nonhuman primate,NHP)因与人有着最近的亲缘关系,且在生殖生理学、神经生物学和病理学等诸多方面最接近于人,因此是研究人类生命领域最高级的模式动物。NHP相关繁殖技术的优化不仅有助于提高动物繁殖效率,而且对提高转基因灵长类疾病模型制备效率具有重要的应用意义(Wolf,2004)。同时,NHP资源的匮乏和价格昂贵,使得繁殖技术的优化具有必要性。其中,食蟹猴Macaca fascicularis因体型小、性格温顺且常年均可繁殖和已完成基因组测序(Yan et al.,2011)等优势,近年来在转基因灵长类疾病模型制备研究中备受关注。然而食蟹猴个体平均月经周期天数差异大(26~34 d)(Sun et al.,2008),而导致胚胎移植程序中选择自然受体的生殖周期同步性差、准确性低,常常需要很大的观察群体和较高的同步性检测费用的投入,但同时胚胎移植受体的有效选择又是影响模型制备的关键因素(Yang et al.,2008;Niu et al.,2010),因此,本研究试图优化食蟹猴胚胎移植同步受体的处理技术。 1 材料与方法 1.1 研究对象与主要试剂
5~9岁月经周期正常的成年雌性食蟹猴37只,由广东蓝岛生物技术有限公司提供,动物许可证号SCXK(粤)2009-0010。实验猴采用单笼饲养,自动光控12 h光照与12 h黑暗,笼具中提供镜子和空心球供实验猴玩耍,每天观察月经情况并记录。
重组人促卵泡激素(recombinant human follicle stimulating hormone,rhFSH)和重组人绒毛膜促性腺激素(recombinant human chorionic gonadotropin,rhCG)为默克公司产品,聚乙烯吡咯烷酮(polyvinyl pyrrolidone,PVP)为Sigma公司产品,人雌二醇(E2)ELISA试剂盒为Cayman公司产品。 1.2 超数排卵和实验猴分组
食蟹猴群中连续3 d内同时观察到月经血的3~5只个体组成一实验批次。在出现月经血的第2~3天,每日肌注rhFSH,按超排剂量分2个实验组,超排供体组(n=13)于每日08∶00和20∶00注射25 IU/只rhFSH,超排受体组(n=6)采用30%聚乙烯吡咯烷酮(PVP)缓释技术(胡鹏飞等,2011),于每日晨08∶00注射25 IU/只rhFSH,其余为自然受体组(n=21)。连续注射rhFSH 7~8 d后,B超检测双侧卵巢超排反应和卵泡发育的大小和数量,并于次日晨08∶00注射rhCG 1000 IU/只。 1.3 食蟹猴卵母细胞的获取
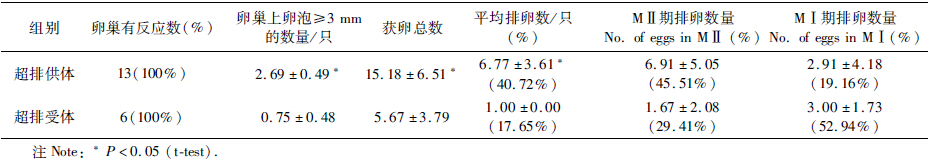
在无菌手术室手术法获取卵母细胞。要点是腹中线切口并暴露双侧卵巢,直尺测量左右侧超排后卵巢的直径,定义超排后卵巢的大小至少2 cm为反应良好;统计卵巢上直径≥3 mm的卵泡数量、平均获卵总数、平均排卵数及其中第二次减数分裂期(MⅡ)和第一次减数分裂期(MⅠ)卵数量。 1.4 E2的检测
血清样本的采集:rhFSH注射第6天起,连续4~5 d于早晨08∶00采集超排供体组、超排受体组和自然受体组个体的隐静脉血液1 mL,置于促凝管中,室温放置30 min,4000 r·min-1离心20 min分离血清,并立即-80 ℃保存备用。
按照人E2 ELISA试剂盒的检测说明书执行。绘制超排供体组、超排受体组和自然受体组的E2曲线。 1.5 排卵同期化评价
以超排供体组的E2曲线为参考标准,统计超排受体组与超排供体组排卵同期化的准确率和月经周期相差3 d以内的自然受体组排卵同期化的准确率。 1.6 统计分析
采用Excel和SPSS 17.0软件统计分析。 2 结果 2.1 rhFSH剂量对食蟹猴卵泡发育的影响
未经超排处理的食蟹猴卵巢大小如绿豆,而经超排处理后的卵巢显著增大,超排良好的食蟹猴卵巢平均大小在3 cm左右,其上布满大小不同的未排优势卵泡和少数排卵后形成的血体。
通过统计rhFSH剂量(即超排供体组和超排受体组)对食蟹猴卵泡发育的影响(表 1),结果表明2实验组超排后卵巢全部反应良好,B超检测超排供体组和超排受体组第8 天优势卵泡数(直径≥3 mm)分别为2.69个±0.49个和0.75个±0.48个(P<0.05),且获卵总数和平均排卵数分别为(15.18±6.51 VS. 5.67±3.79,6.77±3.61 VS. 1.00±0.00)(P<0.05);卵巢获得超排供体组中占45.51%比例的卵处于MⅡ期,而超排受体组52.94%比例的卵处于MⅠ期。
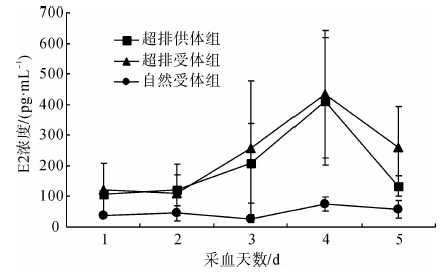
为了找到与超排供体组排卵周期同步的食蟹猴,检测每实验批次食蟹猴血清中E2浓度的变化(即E2曲线)来初步判断超排供体组有无排卵和有无排卵周期同步的受体食蟹猴。一般食蟹猴从注射rhFSH的第7天起,其体内E2的水平逐渐升高,并出现峰值,当天注射rhCG,引起E2急速下降,从而诱发排卵。从图 1可以看出,超排受体组和超排供体组的E2水平变化模式一致,2组水平浓度差异无统计学意义,于注射rhCG当日,E2浓度达到最高值(410.15 pg·mL-1±207.47 pg·mL-1 VS. 433.38 pg·mL-1±208.68 pg·mL-1),而自然受体组对照血清中各采样点E2水平偏低,峰值仅为75.42 pg·mL-1±22.32 pg·mL-1。
|
| 图 1 不同rhFSH剂量对食蟹猴血清E2浓度的影响 Fig. 1 The effect on E2 concentration in serum |
每实验批次中,以超排供体食蟹猴的E2曲线为参考标准,所有实验批次中超排受体组与超排供体组排卵同期化的准确率为5/6(83.33%),而月经周期相差3 d以内的自然受体组排卵同期化的准确率仅为9/21(42.85%)。 3 讨论
相关繁殖技术在NHP的应用已有20多年的历史,通常是体外卵母细胞/早期胚胎的获得和通过胚胎移植建立怀孕(Bavister,2004)。目前,NHP刺激卵泡发育研究主要集中在使用促性腺激素种类、注射时间和剂量方面。近来,在恒河猴M. mulatta中应用合成的人促性腺激素,如人促卵泡激素(human follicular stimulating hormone,hFSH)和人绒毛膜促性腺激素(human chorionic gonadotropin,hCG),获得了较好的超排效果(Schramm et al.,2002),提高了卵母细胞的质量和受精后早期胚胎的发育质量(Yang et al.,2007)。早期研究表明PVP缓释剂可提高奶牛排卵数量(Yamamoto et al.,1994),可使绵羊Ovis aries超排有效率达到80%,且卵巢上无大卵泡存留(曾培坚等,1996);本研究中应用30%的PVP溶解rhFSH单次注射方案对食蟹猴进行超排,超排受体全部有反应,表明PVP既促进了少量卵泡的发育,又能使超排受体及时排卵,其缓释促排作用在灵长类动物中可获得较好的应用效果。
在灵长类动物疾病转基因模型建立的过程中,如何准确把握受体的排卵时间是胚胎移植程序中最重要的技术环节。灵长类动物排卵受体内激素水平调控。MⅡ 期成熟的卵泡是在E2峰值出现后的24 h发生排卵反应的,而在排卵后约12 h,体内黄体素大量分泌,因此,常常使用分析灵长类动物血清中E2峰值的方法来评估排卵时间。Sun等(2008)研究结果暗示E2峰值出现后的24~36 h并伴随受体卵巢上黄体的出现是原核期胚胎移植的最佳时期,这就意味着超排供体和移植受体的排卵时间是一致的,或仅相差12 h左右。而在本研究中,采用30%的PVP溶解低剂量的rhFSH单次注射技术,可有效提高超排供体和超排受体排卵同期化的比例。
本研究表明以每日晨单次注射30%PVP溶解的rhFSH 25 IU/只剂量的方式,可获得与超排供体排卵同期化准确率较高的移植受体。
| 胡鹏飞, 张贵学, 于国庆, 等. 2011. 羔羊卵泡诱导发育、活体采卵和体外发育潜能研究[J]. 畜牧兽医学报, 42(2): 182-189. |
| 曾培坚, 石国庆, 皮文辉, 等. 1996. 用聚乙烯吡咯烷酮加FSH制剂对绵羊一次注射超排效果试验[J]. 中国养羊, 16(4): 26. |
| Bavister B. 2004. The role of animal studies in supporting human assisted reproductive technology[J]. Reprod Fertil Dev, 16(7): 719-728. |
| Niu Y, Yu Y, Bernat A, et al. 2010. Transgenic rhesus monkeys produced by gene transfer into early-cleavage-stage embryos using a simian immunodeficiency virus-based vector[J]. Proc Natl Acad Sci USA, 107(41): 17663-17667. |
| Schramm RD, Paprocki AM, Bavister BD. 2002. Features associated with reproductive ageing in female rhesus monkeys[J]. Hum Reprod, 17(6): 1597-1603. |
| Sun Q, Dong J, Yang W, et al. 2008. Efficient reproduction of cynomolgus monkey using pronuclear embryo transfer technique[J]. Proc Natl Acad Sci USA, 105(35): 12956-12960. |
| Wolf DP. 2004. Assisted reproductive technologies in rhesus macaques[J]. Reprod Biol Endocrinol, 2: 37. |
| Yamamoto M, Ooe M, Kawagychi M, et al. 1994. Superovulation in the cow with a single intramuscular injection of FSH dissolved in polyvinylpyrrolidone[J]. Theriogenology, 41(3): 747-755. |
| Yan G, Zhang G, Fang X, et al. 2011. Genome sequencing and comparison of two nonhuman primate animal models, the cynomolgus and Chinese rhesus macaques[J]. Nature Biotechnology, 29(11): 1019-1023. |
| Yang S, He X, Hildebrandt TB, et al. 2007. Effects of rhFSH dose on ovarian follicular response, oocyte recovery and embryo development in rhesus monkeys[J]. Theriogenology, 67(6): 1194-1201. |
| Yang SH, Cheng PH, Banta H, et al. 2008. Towards a transgenic model of Huntingtons disease in a non-human primate[J]. Nature, 453(7197): 921-924. |
 2015, Vol. 34
2015, Vol. 34