扩展功能
文章信息
- 徐菲, 龙振宇, 冉欣, 赵雪, 邱富源, 江廷磊, 冯江
- XU Fei, LONG Zhenyu, RAN Xin, ZHAO Xue, QIU Fuyuan, JIANG Tinglei, FENG Jiang
- 马铁菊头蝠对同种咀嚼声的反应研究
- Response to the Conspecific Chewing Sounds in Rhinolophus ferrumequinum
- 四川动物, 2015, 34(2): 181-186
- Sichuan Journal of Zoology, 2015, 34(2): 181-186
- 10.3969/j.issn.1000-7083.2015.02.004
-
文章历史
- 收稿日期:2014-06-19
- 接受日期:2014-10-17
咀嚼是哺乳动物食物吸收的重要组成部分,对动物的生存和繁殖极其重要。大多数哺乳动物咀嚼食物时都会发出一些低频的可听咀嚼声。目前,对哺乳动物咀嚼声的研究主要集中在人类,主要关注人类在咀嚼不同食物时咀嚼声的差异(De Belie et al.,2003),通过咀嚼声监测食物类型(Amft et al.,2005)和质地(Tanaka et al.,2011),以及咀嚼声的功能(Amos et al.,2006;Bethea,2013)等方面。此外,Schiffman和Warwick(1993)的研究表明倾听人类的咀嚼声可以增加自身或他人在就餐时的食欲和愉悦度。然而,除了人类,咀嚼声的研究在其他哺乳动物中还很少,特别是对于完全在夜间活动的蝙蝠。
蝙蝠具有复杂的社群结构,是哺乳动物中群居程度最高的类群(Barclay,1982;Fenton,2003;Fenton & Vonhof,2004)。它们主要依靠声学信号在黑暗环境中活动,不仅发出用于导航和定位的回声定位声波,还发出用于维持社群结构、高度复杂多样的交流声波(Davidson & Wilkinson 2004;Budenz et al.,2009),是声学和行为学研究的重要模式生物(Ma et al.,2008;Kobayasi et al.,2012)。
自20世纪40年代以来,蝙蝠声学研究一直集中在回声定位行为的发声、发育、功能和进化方面,并取得大量的创新性研究成果(Obrist,1995;Russo et al.,2001;Schnitzler et al.,2003;Russ et al.,2004)。此外,关于蝙蝠进食行为的研究表明,食物质地(Dumont,1999)、牙齿形状(Santana et al.,2011)对进食行为有显著的影响,然而关于蝙蝠咀嚼声的特征和功能仍不清楚。
马铁菊头蝠Rhinolophus ferrumequinum是翼手目中声纳系统较特殊、声脉冲形式和发声行为多样性较高的一个种类,也是蝙蝠回声定位声波和行为生态学的主要研究对象。但近几十年来,马铁菊头蝠的数量在世界范围内急剧下降(Bontadina,2002)。迄今为止,对马铁菊头蝠的研究主要集中在食性(Ma et al.,2008)、冬季活动和冬眠(Park et al.,2000)、系统地理学(Rossiter et al.,2007),以及繁殖和哺育行为(Rossiter et al.,2000)等诸多方面。目前尚未见马铁菊头蝠咀嚼声是否具有吸引同伴来进食功能的报道。
本研究以马铁菊头蝠为研究对象,通过录制其咀嚼声向其同伴回放,观察咀嚼声对马铁菊头蝠进食行为和回声定位声波的影响,研究结果试图证实以下假设:蝙蝠的咀嚼声对其他同种个体具有吸引作用,并会对蝙蝠的回声定位声波产生显著的影响。 1 材料与方法 1.1 样本的采集与蝙蝠的驯养
研究区域位于吉林省集安市治安村西侧。该区域林地主要由落叶林、次生落叶林和针叶林组成。主要乔木为紫椴Tilia amurensis、蒙古栎Quercus mongolica、辽东栎Quercus liaotungensis、核桃楸Juglans m and shurica Maxim、板栗Castanea mollissima和油松Pinu stabrlaeformis等。灌木和草本丰富(Sun et al.,2010)。在该区域内有3个蝙蝠栖息的山洞,它们分别是大砬子洞、蝙蝠洞和红军洞,马铁菊头蝠主要栖息在大砬子洞中。本实验主要在2013年7月到8月期间进行。之后,为了增加样本量,在2014年4月进行补充实验。黄昏的时候在这3个山洞利用雾网捕获蝙蝠,共捕获34只马铁菊头蝠,根据蝙蝠骺间距的融合程度区分成体和幼体。将成体蝙蝠带回当地废弃的老房子中(5 m×4 m×4 m)驯养。废弃的老房子能够自然地模仿当地山洞的环境,并且每天给蝙蝠喂养一定数量的面包虫和维生素,保证蝙蝠能够在老房子中健康成长。 1.2 形态学特征测量
采用直尺游标卡尺(0.01 mm)测量蝙蝠的前臂长、体长。并用天平(0.1 g)测量体质量。根据外生殖器的形态鉴别性别。 1.3 行为实验过程 1.3.1 咀嚼声的录制、编辑和分析
当蝙蝠已经适应房间环境后,从中挑选4只(2雌2雄)健康活跃的蝙蝠,在活动高峰期(20∶00—04∶00)将其放入笼子中,笼中的食盒提前放置80只面包虫,并安装超声波录制仪Avisoft Bioacoustics USG 116(Avisoft Bioacoustics,Berlin,Germany)和红外线摄像机(Sony HDR CX760E)同步录制蝙蝠进食时的咀嚼声。采样频率为100 kHz,分辨率为16 bit。
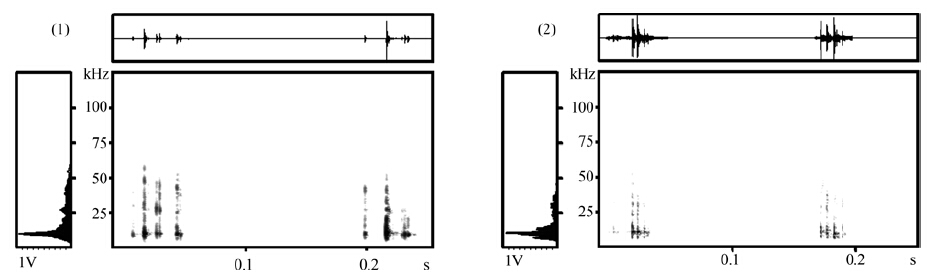
根据对应的视频,选择蝙蝠咀嚼时发出咀嚼声且信噪比较高的声波文件,通过专业的声波分析软件Avisoft SASLAB Pro 4.40(Avisoft Bioacoustics,Berlin,Germany)进行分析和编辑。分析内容包括声谱图(Spectrogram)、时域波型图(Oscillogram)和能量谱图(Power spectrum)(Hamming;FFT=1024)。分析声波参数包括持续时间、峰频、带宽和叫声速率。从每只蝙蝠发出的咀嚼声中,挑选出长度为3 s的高质量声波文件,每3只的咀嚼声合并为1个长度为9 s的声波文件,一共随机合成2个文件,分别进行标准化之后标记为1号和2号(图 1)。
|
|
图 1 马铁菊头蝠的咀嚼叫声
Fig. 1 The chewing sounds of Rhinolophus ferrumequinum
左为能量谱图,右上为时域波形图,右下为声谱图。 Left. Power spectrum,upper right. Oscillogram,lower right. Spectrogram. |
合成文件后,利用软件SPSS 16.0对咀嚼声声波各参数进行统计分析,经过正态分布检验后,采用Mann-Whitney U test检验峰频和叫声速率2个参数在1号文件和2号文件之间的差异。并采用双尾的独立样本T检验分析持续时间、带宽在不同文件下的差异。经过检验,1号文件和2号文件各参数之间差异均无统计学意义(持续时间T=2.012,P=0.055;峰频U=57.5,P=0.197;带宽T=1.012,P=0.321;叫声速率U=79.5,P=0.614)。 1.3.2 咀嚼声的回放以及回声定位声波和进食行为的录制
在饲养的34只蝙蝠中,每天随机挑选5只蝙蝠来进行咀嚼声回放实验,这样有助于最小化蝙蝠对食盒的记忆,减少实验误差。为了消除性别的影响,保证每5只蝙蝠中有雌有雄。为了区分个体,每组蝙蝠个体都用白色指甲油进行标记。1只涂在头上,1只涂在背上,1只涂在腹部,1只涂在头部和背部,1只不涂。
回放前,先将水盒放在笼子中间靠左的位置,食盒每天交换放在A位置或者B位置。在食盒一侧安装专业的超声波回放系统(USG Player 116,Avisoft Bioacoustics,Germany),在食盒另一侧安装超声波录制仪Avisoft Bioacoustics USG 116(Avisoft Bioacoustics,Berlin,Germany)和红外线摄像机(Sony HDR CX760E),同步录制蝙蝠的进食行为和回声定位声波(图 2)。每晚的咀嚼声回放文件按下列规则选择:双号日期回放1号文件,单号日期回放2号文件。回放实验从每晚20∶00开始到次日凌晨04∶00结束。20∶00—24∶00为一个阶段,24∶00—04∶00为另一个阶段。回放条件有2种:蝙蝠咀嚼声和空白对照。每个阶段的回放条件按以下规则进行:单号日期20∶00—24∶00回放蝙蝠咀嚼声,24∶00—04∶00进行空白对照试验,双号日期20∶00—24∶00进行空白对照试验,24∶00—04∶00回放蝙蝠咀嚼声。在整个实验期间,如果遇到雷雨大风天气,暂停实验。实验过程中录制的声波和视频都被同时保存在电脑中。

|
| 图 2 马铁菊头蝠咀嚼声回放实验设置示意图 Fig. 2 Illustration of experiment design of playback of the chewing sounds of Rhinolophus ferrumequinum |
通过捕食尝试和进食次数这2个参数来度量蝙蝠在不同回放条件下的进食行为。当蝙蝠爬向食盒,停留在垂直方向距离食盒底部12 cm的区域内或水平方向距食盒边缘5 cm处的区域内,定义蝙蝠表现一个捕食尝试。当蝙蝠头部伸进食盒并停留2 s以上定义为一次进食次数。根据上述定义,利用快播软件对每个晚上录制的视频进行分析,记录在2种回放条件下蝙蝠的捕食尝试和进食次数。 1.3.4 回声定位声波分析
在不同的回放条件下,选择信噪比较高的回声定位声波,并采用专业的声波分析软件Avisoft SASLAB Pro 4.40(Avisoft Bioacoustics,Berlin,Germany)分析声波。分析内容包括声谱图、时域波型图和能量谱图。分析声波参数包括峰频、脉冲持续时间、脉冲间隔和脉冲速率。 1.3.5 统计分析
经正态分布检验,持续时间、时间间隔、脉冲速率3个参数符合正态分布,而频率、捕食尝试、进食次数3个参数不符合。由于捕食尝试和进食次数为计数数据,且方差不具齐性,为了降低极端大变量对方差的影响,首先对其进行平方根转换。采用Mann-Whitney U test检验捕食尝试、进食次数和频率3个参数在不同回放条件下的差异。并采用双尾的独立样本T检验分析回声定位声波的其余3个参数(持续时间、脉冲速率、时间间隔)在不同条件下的差异。所有统计均在软件SPSS 16.0中进行。 2 结果
在整个实验阶段,在研究区域共采集了34只蝙蝠。在2013年8月和2014年4月,一共在21个晚上进行回放实验。因此,共回放了21次咀嚼声,进行了22次空白对照实验。 2.1 马铁菊头蝠对同种咀嚼声刺激下的进食行为
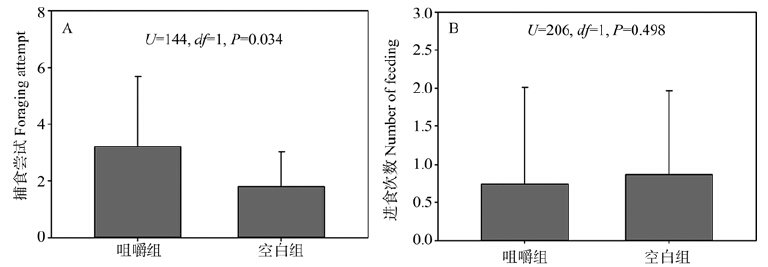
进食行为实测数值经过平方根转化后,结果表明,回放咀嚼声时,马铁菊头蝠的捕食尝试次数为3.22±2.46(n=21),进食次数为0.74±1.27(n=21);在空白条件下,马铁菊头蝠捕食尝试次数为1.85±1.25(n=22),进食次数为0.86±1.13(n=22)。Mann-Whitney U test检验结果表明进食次数在2种回放条件下差异无统计学意义(U=206,df=1,P=0.498),但捕食尝试在2种回放条件下的差异有统计学意义(U=144,df=1,P=0.034)(图 3)。
|
|
图 3 马铁菊头蝠捕食尝试(A)和进食次数(B)在2种不同回放条件下的比较
Fig. 3 Comparison of foraging attempt(A) and number of feeding(B)between two groups
在此图中,捕食尝试和进食次数都经过了平方根转换。 Note: Foraging attempt and number of feeding are transformed using square-root. |
回放咀嚼声条件下,马铁菊头蝠回声定位声波各参数值分别为:峰频69.20 kHz±0.22 kHz(n=34)、脉冲持续时间22.84 ms±4.68 ms(n=34)、脉冲间隔36.53 ms±11.36 ms(n=34)、脉冲速率19.17 ms-1±10.68 ms-1(n=34)。空白条件下,马铁菊头蝠回声定位声波各参数值分别为:峰频68.72 kHz±0.76 kHz(n=34)、脉冲持续时间18.12 ms±4.89 ms(n=34)、脉冲间隔39.19 ms±9.99 ms(n=34)、脉冲速率24.65 ms-1±8.35 ms-1(n=34)。在2种回放条件下,各参数除时间间隔差异无统计学意义(P=0.126)外,其余3个参数在不同回放条件下的差异均有统计学意义(持续时间P<0.001,频率P=0.039,脉冲速率P=0.029)(图 4)。即回放咀嚼声时,回声定位声波峰频显著增加,持续时间延长,脉冲速率减慢。

|
| 图 4 马铁菊头蝠回声定位声波在2种不同回放条件下的比较 Fig. 4 Comparison of echolocation call parameters between two groups |
本研究结果虽然显示马铁菊头蝠的进食次数在咀嚼声回放和空白对照条件下的差异无统计学意义,但在咀嚼声回放条件下,马铁菊头蝠的捕食尝试明显高于空白对照条件下的,且在不同回放条件下的差异有统计学意义(图 3)。因此,本研究结果表明马铁菊头蝠的咀嚼声对同种其他个体具有明显的吸引作用,这与人类咀嚼声的作用基本一致。
人类的咀嚼声可能增加自身或他人的食欲和就餐愉悦度(Schiffman & Warwick,1993;Bethea,2013)。然而,也有研究表明人类咀嚼声并没有如此的作用(Amos et al.,2006)。不管怎样,看见别人津津有味地进食,总会勾起自身想进食的欲望,这基本是人之常情。因此,本研究第一次报道了蝙蝠的咀嚼声也可能在一定程度上引起其他个体的进食动机和欲望。然而,虽然咀嚼声可能增加了哺乳动物的进食欲望,但并不一定增加动物的进食次数。本研究结果也表明,咀嚼声的刺激并不会增加蝙蝠的进食次数。
当人类在听见其他同伴的咀嚼声时,研究表明心血管系统会发生一系列生理反应,例如心跳加速、心脏泵血量增加等,从而刺激人类的食欲和增加就餐时的愉悦度(Schiffman & Warwick,1993;Amos et al.,2006)。对于蝙蝠,目前还不了解它们在听到同伴咀嚼声时的生理反应,也许和人类具有相似的反应。从行为生态的角度,大多蝙蝠是集群捕食的哺乳动物,彼此间的咀嚼声可能会增加它们的食欲,促使它们捕食更多的猎物,从而使其更好地生存和繁殖。当然,这些都需要将来的研究加以证实。
近来的研究证实,许多调频和恒频蝙蝠均具有明显的噪声躲避干扰反应(Bates et al.,2008;Tressler & Smotherman,2009),马铁菊头蝠在粉红噪声的干扰下能迅速地提高自己发声的频率和强度来适应噪声的干扰(Hage et al.,2013)。本研究中,在咀嚼声的刺激下,马铁菊头蝠会提高自身回声定位声波的峰频,以此来躲避咀嚼声的干扰。近年的研究也表明回声定位声波具有交流功能(Jones,2008;Kazial et al.,2008),但本研究中回声定位声波中是否包含食物信息,是否具有招引同伴来取食的功能还需要野外实验进一步证实。4 结论
本研究首次报道了蝙蝠咀嚼声对其同种个体有明显的吸引作用,这暗示蝙蝠倾听同伴的咀嚼声可能会增强自身的食欲,这为进一步阐明蝙蝠咀嚼声的功能和进化具有重要意义。同时,本研究也引出了很多值得研究的科学问题,例如,不同蝙蝠物种之间的咀嚼声是否具有相互吸引的作用,蝙蝠的咀嚼声是否包含食物的信息,以及咀嚼声是否会引起蝙蝠自身或其他个体生理上的反应等。
| Amft O, Stäger M, Lukowicz P, et al. 2005. Analysis of chewing sounds for dietary monitoring[C]./ Beigl M, Intille S, Rekimoto J, et al. UbiComp'05 proceedings of the 7th international conference on ubiquitous computing, Heidelberg: SpringerLecture Notes in Computer Science (including subseries Lecture Notes in Artificial Intelligence and Lecture Notes in Bioinformatics), 3660LNCS: 56-72. |
| Amos KE, Anari S, Buswell CA, et al. 2006. Does listening to the sound of yourself chewing increase your enjoyment of food?[DB/OL]. Annals of General Psychiatry 5. art. no. 22. |
| Barclay RMR. 1982. Interindividual use of echolocation calls: eavesdropping by bats[J]. Behavioral Ecology and Sociobiology, 10: 271-275. |
| Bates ME, Stamper SA, Simmons JA. 2008. Jamming avoidance response of big brown bats in target detection[J]. Journal of Experimental Biology, 211(1): 106-113. |
| Bethea C. 2013. The chewing sound and the fury: what if small, everyday noises ruined your life?[J]. New Republic, 244(11): 28-31. |
| Bontadina F, Schofield H, Naef-Daenzer B. 2002. Radio-tracking reveals that lesser horseshoe bats (Rhinolophus hipposideros) forage in woodland[J]. Journal of Zoology, 258(3): 281-290. |
| Budenz T, Heib S, Kusch J. 2009. Functions of bat social calls: the influence of local abundance, interspecific interactions and season on the production of pipistrelle (Pipistrellus pipistrellus) type D social calls[J]. Acta Chiropterologica, 11: 173-182. |
| Davidson SM, Wilkinson GS. 2002. Geographic and individual variation in vocalizations by male Saccopteryx bilineata (Chiroptera: Emballonuridae)[J]. Journal of Mammalogy, 83: 526-535. |
| Davidson SM, Wilkinson GS. 2004. Function of male song in the greater white-lined bat, Saccopteryx bilineata[J]. Animal Behaviour, 67(5): 883-891. |
| De Belie N, Sivertsvik M, De Baerdemaeker J. 2003. Differences in chewing sounds of dry-crisp snacks by multivariate data analysis[J]. Journal of Sound and Vibration, 266(3): 625-643. |
| Dumont ER. 1999. The effect of food hardness on feeding behaviour in frugivorous bats (Phyllostomidae): an experimental study[J]. Journal of Zoology, 248(2): 219-229. |
| Fenton MB, Vonhof MJ. 2004. Roost availability and population size of Thyroptera tricolor, a leaf-roosting bat, in north-eastern Costa Rica[J]. Journal of Tropical Ecology, 20: 291-305. |
| Fenton MB. 2003. Eavesdropping on the echolocation and social calls of bats[J]. Mammal Review, 33: 193-204. |
| Hage SR, Jiang TL, Berquist SW, et al. 2013. Ambient noise induces independent shifts in call frequency and amplitude within the Lombard effect in echolocating bats[J]. PNAS, 110: 4063-4068. |
| Jones G. 2008. Sensory ecology: echolocation calls are used for communication[J]. Current Biology, 18(1): 34-35. |
| Kazial KA, Pacheco S, Zielinski K. 2008. Information content of sonar calls of little brown bats (Myotis lucifugus): potential for communication[J]. Journal of Mammalogy, 89(1): 25-33. |
| Kobayasi KI, Hiryu S, Shimozawa R, et al. 2012. Vocalization of echolocation-like pulses for interindividual interaction in horseshoe bats (Rhinolophus ferrumequinum)[J]. Journal of the Acoustical Society of America, 132: EL417-EL422. |
| Ma J, Kobayasi K, Zhang S, et al. 2008. Vocal communication in adult greater horseshoe bats, Rhinolophus ferrumequinum[J]. Journal of Comparative Physiology A, 192: 535-550. |
| Obrist MK. 1995. Flexible bat echolocation: The influence of individual, habitat and conspecifics on sonar signal design[J]. Behavioral Ecology and Sociobiology, 36: 207-219. |
| Park KJ, Jones G, Ransome RD. 2000. Torpor, arousal and activity patterns of hibernating greater horse shoe bats (Rhinolophus ferrumequinum)[J]. Functional Ecology, 14: 580-588. |
| Rossiter SJ, Benda P, Dietz C, et al. 2007. Range-wide phylogeography in the greater horse shoe bat inferred from microsatellites: implications for population history, taxonomy and conservation[J]. Molecular Ecology, 16(22): 4699-4714. |
| Rossiter SJ, Jones G, Ransome RD, et al. 2000. Parentage, reproductive success and breeding behaviour in the greater horse shoe bat (Rhinolopus ferrumequinum)[J]. Proceedings of the Royal Society-Biological Sciences (Series BB), 267(1443): 545-551. |
| Russ JM, Jones G, Mackie IJ, et al. 2004. Interspecific responses to distress calls in bats (Chiroptera: Vespertilionidae): a function for convergence in call design?[J]. Animal Behaviour, 67: 1005-1014. |
| Russo D, Jones G, Mucedda M. 2001. Influence of age, sex and body size on echolocation calls of Mediterranean and Mehely's horseshoe bats, Rhinolophus euryale and R. mehelyi (Chiroptera: Rhinolophidae)[J]. Mammalia, 65: 429-436. |
| Santana SE, Strait S, Dumont ER. 2011. The better to eat you with: functional correlates of tooth structure in bats[J]. Functional Ecology, 25: 839-847. |
| Schiffman SS, Warwick ZS. 1993. Effect of flavour enhancement of foods for the elderly on nutritional status: food intake, biochemical indices, and anthropometric measures[J]. Physiol Behav, 53(2): 395-402. |
| Schnitzler HU, Moss CF, Denzinger A. 2003. From spatial orientation to food acquisition in echolocating bats[J]. Trends in Ecology and Evolution, 18: 386-394. |
| Sun KP, Feng J, Jing LR, et al. 2010. Discrimination based on echolocation calls parameters bat species inhabiting the same domain[J]. Northeast Normal University (Natural Science), 38(3): 157-162. |
| Tanaka H, Koizumi N, Uema Y, et al. 2011. Chewing jockey: augmented food texture by using sound based on the cross-modal effect[DB/OL]. SIGGRAPH Asia 2011 Emerging Technologies, SA'11 art. no. 18. |
| Tressler J, Smotherman MS. 2009. Context-dependent effects of noise on echolocation pulse characteristics in free-tailed bats[J]. Journal of Comparative Physiology A: Neuroethology, Sensory, Neural, and Behavioral Physiology, 195: 923-934. |
 2015, Vol. 34(2)
2015, Vol. 34(2)




