扩展功能
文章信息
- 黄小丽, 陈琳, 陈晨, 张蕾, 刘婉, 胡荣, 孔桂美, 卜平, 董小耘, 王隽
- HUANG Xiaoli, CHEN Lin, CHEN Chen, ZHANG Lei, LIU Wan, HU Rong, KONG Guimei, BO Ping, DONG Xiaoyun, WANG Jun
- 3种便秘模型的比较研究
- Comparison of Three Kinds of Type Constipation Model
- 四川动物, 2015, 34(1): 111-116
- Sichuan Journal of Zoology, 2015, 34(1): 111-116
- 10.3969/j.issn.1000-7083.2015.01.020
-
文章历史
- 收稿日期:2014-07-15
- 接受日期:2014-09-25
目前多数便秘患者对于已有的治疗药物并不满意(Li et al.,2014),对于治疗便秘的新型药物的研发成为医药工作者研究的当务之急,动物模型建造的成功与否在动物药效学实验中是较为关键的一个部分。目前,国内外相关的便秘模型较为繁多(巫全胜等,2007;Kakino et al.,2010;Wu et al.,2010;Neri et al.,2012),从选用动物来看小鼠、大鼠较多,但小鼠不同药物便秘模型目前报道较少(郑慧伶等,2013),小鼠和大鼠不同动物便秘模型优劣比较目前未见报道。同时,从国内外相关文献报道(Gwee & Setia,2012;Markland et al.,2013)中可了解到一般女性的便秘患病率要高于男性,而关于动物性别不同是否对便秘模型的建造效果有影响目前未见报道。本实验比较2种不同药物、不同性别小鼠造模以及和不同性别大鼠造模的优劣,现报道如下。1 材料和方法1.1 动物与分组
ICR小鼠48只,雌雄各半,SPF级,体质量25 g±3 g;Wistar大鼠24只,雌雄各半,SPF级,体质量200 g±5 g,由扬州大学比较中心提供(生产许可证号:SXCXK(苏)2012-0004;使用许可证号:SYXK(苏)2012-0029)。所有实验动物购回后,适应饲养7 d。48只ICR小鼠(雌雄各半)随机分为6组,每组8只,分别为雌性空白对照组(A)、雌性洛哌丁胺组(B)、雌性硫糖铝组(C)、雄性空白对照组(D)、雄性洛哌丁胺组(E)、雄性硫糖铝组(F);24只Wistar大鼠(雌雄各半)随机分为4组,每组6只,分别为雌性空白对照组(G)、雌性洛哌丁胺组(H)、雄性空白对照组(I)、雄性洛哌丁胺组(J)。动物饲养以组为单位,分笼饲养。1.2 主要药物与仪器
药物:洛哌丁胺(批号:130910300,西安杨森制药有限公司);硫糖铝(批号:1305222,江苏鹏瑶药业有限公司);硫酸钡(I型)干混悬剂(批号:130310,青岛东风化工有限公司生产,苏北人民医院放射科赠);复方地芬诺酯(批号:0512014,常州康普药业有限公司)。仪器:双目生物显微镜(型号:E200,尼康公司);切片机(型号:RM 2235,德国徕卡仪器公司)。1.3 模型的建立
动物正常饲养7 d后,参照文献(Lee et al.,2012;郑慧伶等,2013)方法加以改造进行模型建造,以洛哌丁胺9.38 mg·kg-1对雌性洛哌丁胺组、雄性洛哌丁胺组小鼠进行灌胃,首次给药量加倍,每天给药2次,分别在9∶00和17∶00;以硫糖铝16 mg·kg-1对雌性硫糖铝组、雄性硫糖铝组小鼠进行灌胃,首次给药量加倍,每天给药1次;以洛哌丁胺6.67 mg·kg-1对雌性洛哌丁胺组、雄性洛哌丁胺组大鼠进行灌胃,首次给药量加倍,每天给药2次,分别是9∶00和17∶00;雌性小鼠空白对照组、雄性小鼠空白对照组、雌性大鼠空白对照组、雄性大鼠空白对照组以磷酸盐缓冲液灌胃作为空白对照,上述给药过程连续10 d。停药后再连续观察7 d,以观察3种模型持续情况。1.4 检测指标1.4.1 一般状态
1)表观状态观察:每天2次观察各组动物活跃程度、毛色情况、精神状态等。2)体质量:从造模期到恢复期每天早上8∶30开始称量每只动物的质量并记录下来,分别计算比较造模期-恢复期和造模组-对照组之间差值有无统计学意义。3)饮水、进食量测定:利用饮水量、进食量差值法进行测定。每天早上同一时间用天平称取每组动物的食物质量和水的质量并记录,饮水量(进食量)用前一天初始的质量减去后一天剩余的质量。1.4.2 粪便参数
每天上午9∶00灌胃给药后,在中午12∶00收集3 h粪便称重,用电子天平称其质量(湿重)。每次收集的粪便称重之后放入烘箱中110 ℃下烘4 h,结束后称其干重,含水量=(湿重-干重)/湿重×100%。次日上午8∶50将每笼垫片换新(注垫片量不可过多)。1.4.3 口-肛传输时间
在每一阶段结束当日给予实验动物200%硫酸钡糊状液:小鼠0.5 mL/只、大鼠2 mL/只灌胃,灌胃后记录时间,当第1粒白色粪便排出时记录排出时间,以此计算出口-肛传输时间。1.4.4 组织学观察
在造模期、恢复期结束后,将实验动物处死,取出结肠后剪取距结肠10 mm左右的远端结肠8~10 mm,在PBS中轻轻震荡除去肠内容物,放入甲醛固定液中固定24 h以上。然后将组织进行包埋、切片、HE染色,在正置双目生物显微镜下观察远端结肠黏膜层厚度及结肠中细胞形态变化。1.5 统计学处理
将所有数据输入SPSS 11.0统计软件包及Excel软件进行处理,计量以均数±标准差(x±s)表示,统计数据多组间比较采用单因素方差分析。两组间差异比较采用t检验,检验水准α=0.05。2 结果2.1 一般状态2.1.1 表观状态观察情况
在整个实验过程中雌性小鼠空白对照组、雄性小鼠空白对照组、雌性大鼠空白对照组、雄性大鼠空白对照组一般表观状态正常,未见有异常。在小鼠这一动物模型组中,雌性洛哌丁胺组、雌性硫糖铝组与雌性空白对照组相比,活动量减少、毛色变暗、没有光泽,同时从粪便形态上看较为短小、干燥;雄性洛哌丁胺组、雄性硫糖铝组与雄性空白对照组相比,状态同上;大鼠动物模型中雌性洛哌丁胺组与雌性空白对照组、雄性洛哌丁胺组与雄性空白对照组相比,毛色较为暗淡并且易醒,粪便较为短小,有的近似小圆球状,同一时间段内排便量减少,但是I、J组中大鼠在实验期间易排稀便。2.1.2 各组动物体质量变化情况
造模期雌性洛哌丁胺组、雌性硫糖铝组与雌性空白对照组、雄性洛哌丁胺组、雄性硫糖铝组与雄性空白对照组相比,小鼠体质量差异具有高度统计学意义(P<0.01),B组与C组、E组与F组相比无统计学意义,即洛哌丁胺造模组体质量要轻于硫糖铝组,但是在正常范围内。在恢复期B、C组小鼠与A组相比体质量差异具有高度统计学意义(P<0.01),而B、C组之间体质量差异无统计学意义;E、F组与D组相比体质量差异具有高度统计学意义(P<0.01),而E、F组之间体质量差异无统计学意义。造模期雌性洛哌丁胺组与雌性空白对照组相比,大鼠体质量差异具有高度统计学意义(P<0.01),即雌性造模组与空白体质量相比在不断减轻;而雄性洛哌丁胺组与雄性空白对照组相比,体质量差异无统计学意义,即雄性大鼠造模组体质量虽然要轻于空白对照组,但是在正常范围内。恢复期H组与G组相比大鼠体质量差异具有高度统计学意义(P<0.01),说明雌性大鼠在恢复期中造模组体质量仍明显轻于正常组;J组与I组相比体质量差异具有高度统计学意义(P<0.01),雄性造模组大鼠在造模过程中常有稀便现象且到后期精神状态不是很佳,在恢复期造模组与正常组的差异较明显。
| 组别 | A | B | C | D | E | F |
| 造模期 | 29.0±0.5 | 27.4±0.5* | 27.5±0.2* | 34.3±0.6 | 32.3±0.3★ | 32.6±0.3★ |
| 恢复期 | 30.6±0.6 | 28.4±0.8☆ | 29.0±1.1☆ | 36.0±0.7 | 33.4±0.7☆ | 34.1±1.1☆ |
| 注: 造模期,与A组比较,*P<0.01; 与D组比较,★P<0.01; 恢复期,与A组比较,☆P<0.01。 Notes: Modeling period: compared with group A,*P<0.01; compared with group D,★P<0.01; Modeling post: compared with group A,☆P<0.01. | ||||||
| 组别 | G | H | I | J |
| 造模期 | 204.6±5.2 | 193±1.7* | 241.6±8.9 | 228.6±5.5 |
| 恢复期 | 226.1±4.1 | 199.5±6.7° | 263.2±5.3 | 226.7±5.8# |
| 注: 造模期,与G组比较,*P<0.01; 恢复期: 与G组比较,°P<0.01,与I组比较,#P<0.01。 Notes: Modeling period,compared with group G,*P<0.01; Modeling post: compared with group G,°P<0.01; compared with group I,#P<0.01. | ||||
进食情况:造模期雌性洛哌丁胺组、雌性硫糖铝组与雌性空白对照组相比,小鼠进食差异无统计学意义,雄性洛哌丁胺组、雄性硫糖铝组与雄性空白对照组相比,进食量差异具有统计学意义(P<0.05),B组与C组、E组与F组相比进食量差异无统计学意义。B组对应的恢复期与造模期相比,差异均具有统计学意
义(P<0.05),D、E、F各组差异显著(P<0.01),而A、C组对应的恢复期和造模期相比进食量差异无统计学意义(表 3)。造模期雌性洛哌丁胺与雌性空白对照组相比,大鼠进食量差异具有统计学意义(P<0.05),而雄性洛哌丁胺组与雄性空白对照组组相比进食量无统计学意义。恢复期与造模期相比,各组大鼠进食差异均无统计学意义(表 4)。
| 组别 | A | B | C | D | E | F |
| 造模期 | 36.8±3.1 | 34.6±1.6 | 35.0±2.5 | 44.9±3.4 | 40.5±1.4★ | 41.1±3.0★ |
| 恢复期 | 34.2±6.3 | 23.6±5.1° | 26.2±10.1 | 32.4±4.3☆ | 22.4±9.2☆ | 28.6±1.5☆ |
| 注: 与D组比较,★P<0.05; 与造模期比较,°P<0.05; 与造模期比较,☆P<0.01。 Notes: Compared with group D,★P<0.05; compared with modeling period,°P<0.05; compared with modeling period,☆P<0.01. | ||||||
| 组别 | G | H | I | J |
| 造模期 | 47.9±6.1 | 31.7±10.6* | 71.4±17.3 | 47.4±11.1 |
| 恢复期 | 37.9±14.8 | 22.1±6.0 | 42.6±24.3 | 34.8±9.8 |
| 注: 与G组比较,*P<0.05。 Note: Compared with group G,*P<0.05. | ||||
饮水情况:造模期雌性洛哌丁胺组、雌性硫糖铝组与雌性空白对照组、雄性洛哌丁胺组、雄性硫糖铝组与雄性空白对照组相比,小鼠饮水量差异无统计学意义,B组与C组、E组与F组相比饮水量差异也无统计学意义。但各组对应的恢复期和造模期相比,饮水量差异具有高度统计学意义(P<0.01)(表 5)。造模期雌性洛哌丁胺组与雌性空白对照组、雄性洛哌丁胺组与雄性空白对照组相比,大鼠饮水量差异无统计学意义。除H组外(P<0.01),各组大鼠对应的恢复期与造模期相比,大鼠饮水量差异无统计学意义(表 6)。
| 组别 | A | B | C | D | E | F |
| 造模期 | 75.1±6.6 | 73.2±6.3 | 75.5±5.6 | 76.1±5.6 | 68.6±6.0 | 69.1±4.5 |
| 恢复期 | 54.4±8.4☆ | 47.6±4.5☆ | 49.4±5.1☆ | 61.2±2.3☆ | 39.6±15.2☆ | 48.6±8.8☆ |
| 注: 与造模期比较,☆P<0.01。 Note: Compared with modeling period,☆P<0.01. | ||||||
| 组别 | G | H | I | J |
| 造模期 | 63.6±13.1 | 58.3±8.1 | 113.4±24.5 | 85.1±14.8 |
| 恢复期 | 57.2±25.3 | 42.6±8.1▲ | 81.5±26.0 | 64.0±13.7 |
| 注: 与造模期比较,▲P<0.01。 Note: Compared with modeling period,▲P<0.01. | ||||
造模期雌性洛哌丁胺组、雌性硫糖铝组与雌性空白对照组、雄性洛哌丁胺组、雄性硫糖铝组与雄性空白对照组相比,小鼠粪便含水量具有高度统计学意义(P<0.01),B组与C组、E组与F组相比含水量差异无统计学意义。恢复期与造模期相比各组粪便含水量差异无统计学意义。造模期雌性洛哌丁胺组与雌性空白对照组相比,大鼠粪便含水量差异具有统计学意义(P<0.05),而雄性洛哌丁胺组较雄性空白对照组相比,粪便含水量差异不显著。各组大鼠粪便含水量对应的恢复期与造模期相比差异无统计学意义(P>0.05)(表 8)。
| 组别 | A | B | C | D | E | F |
| 造模期 | 53.6±7.6 | 39.0±5.0* | 43.8±4.6* | 53.2±3.7 | 42.8±4.2★ | 44.3±4.2★ |
| 恢复期 | 49.2±7.6 | 39.0±13.2 | 41.8±10.3 | 47.0±8.4 | 43.6±6.9 | 42.6±9.6 |
| 注: 与A组比较,*P<0.01; 与D组比较,★P<0.01。 Notes: Compared with group A,*P<0.01; compared with group D,★P<0.01. | ||||||
| 组别 | G | H | I | J |
| 造模期 | 56.1±16.1 | 14.3±24.4* | 61.7±6.9 | 51.9±23.6 |
| 恢复期 | 51.2±15.7 | 30.1±13.3 | 53.5±11.9 | 38.4±21.4 |
| 注: 与G组比较,*P<0.05。 Note: Compared with group G,*P<0.05. | ||||
造模期雌性洛哌丁胺组、雌性硫糖铝组与雌性空白对照组相比,小鼠口-肛传输时间具有显著差异(P<0.01),并且B组和C组相比小鼠口-肛传输时间具有高度统计学意义(P<0.01),雄性洛哌丁胺组、雄性硫糖铝组与雄性空白对照组相比,小鼠口-肛传输时间差异具有统计学意义(P<0.05),E、F两组之间小鼠口-肛传输时间差异具有统计学意义(P<0.05)。而造模期与恢复期相比各组小鼠口-肛传输时间差异除F组有统计学意义(P<0.05)外,其余各组均无统计学意义(图 1)。造模期雌性洛哌丁胺组与雌性空白对照组相比,大鼠口-肛传输时间差异具有统计学意义(P<0.05),雄性洛哌丁胺组与雄性空白对照组相比无统计学差异。各组恢复期与造模期相比,其差异也无统计学意义(图 2)。
 |
| 图 1 小鼠口-肛传输时间 Fig. 1 Transfer time between mouth and anal of the mice 注: 与A组比较,*P<0.01; 与D组比较,#P<0.05; 与C组比较,&P<0.01; 与F组比较,★P<0.05。 Notes: Compared with group A,*P<0.01; compared with group D,#P<0.05; compared with group C,&P<0.01; compared with group F,★P<0.05. |
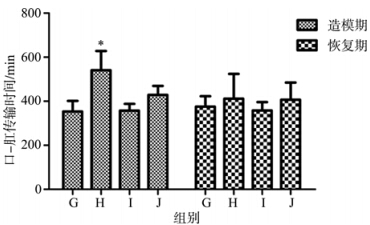 |
| 图 2 大鼠口-肛传输时间 Fig. 2 Transfer time between mouth and anal of the rats 注: 与G组比较,*P<0.01。 Note: Compared with group G,*P<0.01. |
远端结肠组织切片在10×物镜下进行观察。造模期雌性洛哌丁胺组、雌性硫糖铝组小鼠远端结肠黏膜层厚度明显小于雌性空白对照组,雄性洛哌丁胺组、雄性硫糖铝组远端结肠黏膜层厚度与雄性空白对照组相比无明显差异,但是黏膜层上细胞形态发生明显变化,由饱满、圆润向细长、干瘪状态变化(图 3)。而雌性洛哌丁胺组与雌性空白对照组相比,雄性洛哌丁胺组与雄性空白对照组相比,无论是在黏膜层厚度还是在细胞形态上均有明显差异,黏膜层厚度明显小于G、I组(图 4)。
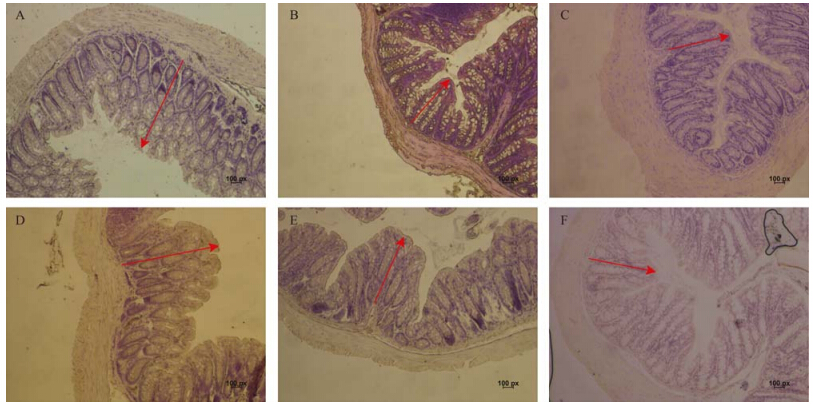 |
| 图 3 小鼠远端结肠HE染色 Fig. 3 The HE staining distal colon of mice 注: A. A组造模期,B. B组造模期,C. C组造模期,D. D组造模期,E. E组造模期,F. F组造模期; 红色箭头表示黏膜层厚度。 Notes: A. the modeling period of group A,B. the modeling period of group B,C. the modeling period of group C,D. the modeling period of group D,E. the modeling period of group E,F. the modeling period of group F; The red arrow indicates the thickness of mucosal layer. |
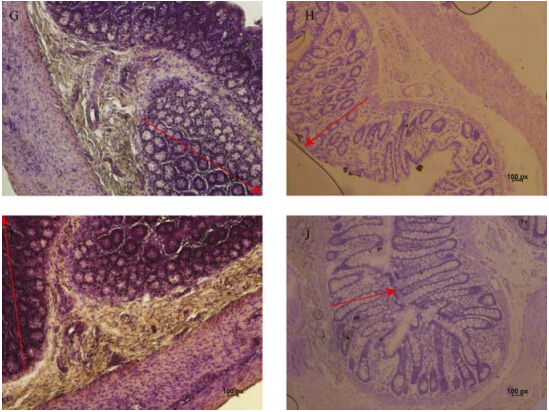 |
| 图 4 大鼠远端结肠HE染色 Fig. 4 The HE staining distal colon of rats 注: G. G组造模期,H. H组造模期,I. I组造模期,J. J组造模期。 Notes: G. the modeling period of group G,H. the modeling period of group H,I. the modeling period of group I,J. the modeling period of group J. |
便秘模型从造模方法角度可以分为限水法、冰水灌胃法、泻剂结肠法、药物造模法等。其中限水法形成便秘模型周期较短,但是易恢复并且长时间动物会因失水过多而死;泻剂结肠法效果较佳但是造模周期比较长;药物造模法中部分药品如吗啡等属于控制药品。在模型的建造中,研究人员应选择周期相对较短、模型持续时间较长、效果较佳、物品易得的方法,本研究采用2种不同药物建立了小鼠便秘模型,洛哌丁胺是常用的止泻剂,主要通过抑制肠道平滑肌的收缩,减少肠蠕动,使肠内容物通过延迟,致使实验动物出现排便减少或难排便、粪便豆样圆珠状表现,实验动物口-肛传输时间延长,含水量减少,肠黏膜层变薄,肠内细胞形态与正常对照组相比变得小而细长。而硫糖铝是一种应用已久的胃黏膜保护剂,其致便秘的主要机制是抑制肠推动作用以及肠水分吸收。在整个实验中小鼠实验动物组中洛哌丁胺组与硫糖铝组相比在体重、饮水、进食、粪便含水量上差异无统计学意义,但是雌性洛哌丁胺组小鼠的口-肛传输时间显著高于硫糖铝组(P<0.01),并且硫糖铝为片剂,灌胃之前需要研磨碾碎再溶解,而洛哌丁胺则无需研磨直接溶解。
从选用动物角度来说,现今已报道的用于便秘造模的动物有小鼠、大鼠、兔、猕猴、貂等,其中以小鼠、大鼠运用较多。猕猴、貂、兔等从价格上较大鼠、小鼠昂贵;从安全角度上来说,猕猴、貂相对于大鼠、小鼠更为危险;从造模便捷角度来说,小鼠、大鼠更为便捷且容易抓取。本研究就大鼠、小鼠2种动物进行便秘模型研究比较。从造模过程来说,小鼠更易抓取;从安全性角度说,小鼠较为安全、不易被咬伤;从造模效果上说,2种动物之间没有显著性差异。从药效实验角度来说,肛门、直肠给药的药效试验选用大鼠更为适宜,大鼠更便于塞入并且大鼠的抵抗力要强于小鼠,所以模型建造是选用大鼠还是小鼠应根据进行药效实验的药物及给药途径来确定。便秘模型从动物性别角度分析,据文献报道女性的便秘患病率普遍要高于男性。所以本研究就雌性、雄性何种性别的动物建模效果更好进行比较研究。发现雌性造模效果稍微优于雄性,实验小鼠模型中雌性小鼠造模组与对照组相比,口-肛传输时间差异性要比雄性更为明显。实验大鼠模型中,从体质量、进食量、粪便含水量、口-肛传输时间指标观察,雌性造模组与空白对照组差异性要比雄性更为显著。
本实验研究主要从体质量、饮水、进食、粪便含水量、口-肛传输时间、结肠黏膜层厚度及细胞形态等指标对造模效果进行评价,从而选取洛哌丁胺雌性大鼠便秘模型进行下一步药效学研究。在整个实验过程中仍有以下不足:首先,模型建造效果评价指标不足,在后续实验中应增加一氧化氮(NO)、结肠P物质(SP)、血电解质等指标的检测,这样对于造模效果的评价更为准确可靠;其次,在后续实验中应增加实验动物数量,使实验数据更精确;最后,为何雌性和雄性造模效果会有差异?可能是由于雌、雄动物中孕酮素的差异,该问题有待后续探究。
| 巫全胜, 吴曙光, 赵菊花, 等. 2007. 大鼠药物依赖性便秘模型的制作[J]. 实验动物科学, 24(4): 70-74. |
| 郑慧伶, 李艳霞, 张翠丽, 等. 2013. 四种小鼠便秘模型建立方法的比较[J]. 现代生物医学展, 13(28): 5456-5459. |
| Gwee KA, Setia S. 2012. Demographics and health care seeking behavior of Singaporean women with chronic constipation: implications for therapeutic management[J]. International Journal of General Medicine, 5: 287-302. |
| Kakino M, Hiroshi I, Ito T, et al. 2010. Agarwood induced laxative effects via acetylcholine receptors on loperamide-induced constipation in mice[J]. Biosci Biotechnol Biochem, 74(8): 1550-1555. |
| Lee HY, Kim JH, Jeung HW, et al. 2012. Effects of Ficus carica paste on loperamide-induced constipation in rats[J]. Food and Chemical Toxicology, 50: 895-902. |
| Li MK, Diana TF, Lorna L, et al. 2014. Complementary effects of auricular acupressure in relieving constipation symptoms and promoting[J]. Complementary Therapies in Medicine, 10: 1-34. |
| Markland AD, Goode PS, Palsson O, et al. 2013. Association of Low Dietary Intake of Fiber and Liquids with Constipation: Evidence from the National Health and Nutrition Examination Survey (NHANES)[J]. Am J Gastroenterol, 108(5): 796-803. |
| Neri F, Cavallari G, Tsivian M, et al. 2012. Effect of Colic Vein Ligature in Rats with Loperamide-Induced constipation[J]. Journal of Biomedicine and Biotechnology, 10: 1-5. |
| Wu DZ, Wang XH, Zhou JY, et al. 2010. Traditional Chinese formula, lubricating gut pill, improves loperamide-induced rat constipation involved in enhance of Cl secretion across distal colonic epithelium[J]. J Ethnopharmacol, 130(2): 347-353. |
 2015, Vol. 34(1)
2015, Vol. 34(1)




