扩展功能
文章信息
- 陈育, 魏巍, 许晓燕, 余梦瑶, 江南, 杨志荣, 罗霞
- CHEN Yu, WEI Wei, XU Xiaoyan, YU Mengyao, JIANG Nan, YANG Zhirong, LUO Xia
- 蛹虫草对腺嘌呤致肾阳虚证小鼠影响的实验研究
- Effects of Cordyceps militaris on Kidney-yang Deficiency Mice Induced by Adenine
- 四川动物, 2015, 34(4): 594-598
- Sichuan Journal of Zoology, 2015, 34(4): 594-598
- 10.11984/j.issn.1000-7083.2015.04.019
-
文章历史
- 收稿日期:2014-11-18
- 接受日期:2015-02-25
2. 四川省中医药科学院中药细胞与分子生物学实验室, 成都 610041
2. Traditional Chinese Medicine (TCM Cell and Molecular Lab, Sichuan Academy of Chinese Medicine Sciences, Chengdu 610041, China)
蛹虫草Cordyceps militaris (L.)Link,又叫北冬虫夏草或北虫草,属于子囊菌亚门Ascomycotina核菌纲Pyrenomycetes麦角菌目Clavicipitales麦角菌科Clavicipitaceae虫草属的模式种(卯晓兰,2009)。冬虫夏草Cordyceps sinensis作为名贵的中草药,性温,归肾、肺两经,中医认为其具有补肾助阳的功效(高学敏,2002;国家药典委员会,2010),现代药理研究发现其能增强性欲和修复生殖功能损伤(Ng & Wang,2005),具有十分重要的药用价值,但因天然药源匮乏,且价格昂贵,限制了冬虫夏草的使用。有研究发现蚕蛹虫草具有雄性激素样作用,并提出其可作为冬虫夏草的替代品用于临床(刘洁等,1994)。故本文采用腺嘌呤制备肾阳虚模型,考察实验室筛选出的具有雄性激素样作用(另文发表)的蛹虫草能否改善肾阳虚症状,以期为其成为冬虫夏草的替代品提供一定的实验基础。 1 材料与方法 1.1 材料 1.1.1 实验动物
昆明种清洁级雄性小鼠60只,质量35~37 g,购于成都达硕生物科技有限公司[合格证书号:SCXK(川)2013-24]。
1.1.2 药品及试剂腺嘌呤(Sigma公司,批号XX6-B2125),蛹虫草YCC2子实体(四川省中医药科学院细胞与分子生物学实验室提供),5.0 g·L-1的羧甲基纤维素钠(CMC-Na)混悬液,血清睾酮酶联免疫试剂盒与皮质醇酶联试剂盒(RapidBio公司,批号RB100,RB1028),腺苷(中国药品生物制品检定所,批号110879-200202),葡萄糖(天津市广成化学试剂有限公司,批号200508218)。陈育等:蛹虫草对腺嘌呤致肾阳虚证小鼠影响的实验研究 1.2 方法 1.2.1 蛹虫草新资源食品标准的检测
观察人工培育的蛹虫草YCC2子实体的性状,测定子实体中腺苷和多糖的含量。采用高效液相色谱分析法(high performance liquid chromatography,HPLC)(国家药典委员会,2010)测定蛹虫草子实体中腺苷的含量,色谱条件为:以十八烷基硅烷键合硅胶为填充剂,磷酸盐缓冲液(pH6.5)-甲醇(85∶15)为流动相,柱温30 ℃,流速为1 mL·min-1,检测波长260 nm;采用苯酚-硫酸法(王瑞华等,2011)测定蛹虫草子实体中多糖的含量,于486 nm处测定吸光度。
1.2.2 分组实验室条件下驯养3 d后,将60只雄性小鼠随机分成5组,每组12只,分别为正常对照组、肾阳虚模型组、蛹虫草低、中、高剂量组(1.25 g·kg-1、2.5 g·kg-1、5 g·kg-1)。
1.2.3 样品的制备称取人工栽培的蛹虫草YCC2的干燥子实体500 g,加500 mL蒸馏水蒸煮30 min,烘干,粉碎,过80目钢筛,获得人工栽培子实体细粉,将子实体细粉分别配制成3种不同剂量的蛹虫草子实体细粉悬液。
1.2.4 造模及给药腺嘌呤造模法(肖静等,2008),除正常对照组每天给予适量的5.0 g·L-1的羧甲基纤维素钠外,其余各组均每天给予适量的150 mg·kg-1的腺嘌呤,在此基础上给药组还分别灌胃给予适量的1.25 g·kg-1、2.5 g·kg-1、5 g·kg-1 3种剂量的蛹虫草子实体细粉悬液,所有小鼠均自由摄食。每周称量一次动物的体质量,同时观察其活动、毛色泽等情况,以评价造模效果,时间为28 d。
1.2.5 自主活动次数实验结束时采用避暗自主活动检测仪测定实验各组小鼠的自主活动次数,测定前每只小鼠先适应5 min,再测定5 min内的自主活动次数。
1.2.6 低温游泳时间测定实验结束时分别将各组小鼠放入水缸中,水温约15 ℃,观察小鼠低温游泳时间,平行测定,以小鼠下沉6 s不能冲出水面作为无力游泳的指标,记录从进水到无力游泳的时间。
1.2.7 血清睾酮和皮质醇浓度的测定末次给药1 h后,摘眼球取血,室温静置1 h,3000 r/min离心10 min,分离血清,-20 ℃保存,后按照睾酮和皮质醇酶联免疫试剂盒说明书步骤进行操作,测定各样品中睾酮和皮质醇的含量。
1.2.8 脏器湿重的测定断颈处死小鼠,剖开腹腔,剪取睾丸、肾脏、精囊腺和肾上腺,清除腺体上的全部脂肪,用分析天平迅速称量睾丸、肾脏、精囊腺和肾上腺等脏器的湿重。
1.2.9 睾丸形态的观察剪取睾丸(均取右侧),4%多聚甲醛固定,石蜡包埋,切片,苏木精-伊红(HE)染色,封片,光镜下观察睾丸组织的变化,并拍照记录。 1.3 统计学分析
记录的详细数据资料用SPSS 17.0进行统计学分析,实验数据以平均数±标准差表示,组间比较用单因素方差分析,P<0.05表示差异具有统计学意义。 2 实验结果 2.1 蛹虫草新资源食品标准的检测结果
蛹虫草YCC2子实体为金黄色(图 1),且子实体中腺苷和多糖含量远远高于新资源食品标准的规定含量(腺苷0.055%,多糖2.5%)(表 1)。

|
| 图 1 人工培养的蛹虫草YCC2 Fig. 1 Cordyceps militaris YCC2 of artificial cultivation |
| 成分 | 含量/% |
| 腺苷 | 0.57±0.01 |
| 多糖 | 22.14±0.38 |
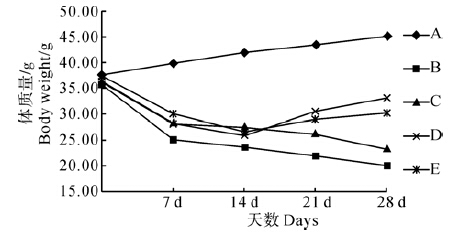
所有动物实验前精神好,动作灵活,毛发白而有光泽,摄食量和饮水量正常。实验结束后,正常对照组小鼠体质量明显增加(P<0.01),其他一般情况没有变化。肾阳虚模型组小鼠体毛疏松,蜷缩弓背,反应迟钝,畏寒扎堆,小便增多且体质量明显下降(P<0.01)。各给药组中,蛹虫草中剂量组和高剂量组小鼠肾阳虚症状有所改善,且小鼠体质量从第二周开始逐渐恢复,蛹虫草低剂量组小鼠肾阳虚症状较明显,且体质量仍持续降低(图 2)。
|
|
图 2 各组小鼠体质量的变化
Fig. 2 Change of body weight of mice in each group
注: A. 正常对照组,B. 肾阳虚模型组,C. 蛹虫草低剂量组,D. 蛹虫草中剂量组,E. 蛹虫草高剂量组。 Notes: A. Control group,B. Kidney-yang deficiency model group,C. Cordyceps militaris low-dose group,D. C. militaris middle-dose group,E. C. militaris high-dose group. |
与正常对照组相比,肾阳虚模型组小鼠自主活动次数明显减少(P<0.05),给予蛹虫草后,除蛹虫草低剂量组外,另两组小鼠自主活动次数均明显增多(P<0.01,P<0.05);与正常对照组相比,肾阳虚模型组小鼠低温游泳时间变短(P<0.01),给予蛹虫草后,除蛹虫草低剂量组外,另两组小鼠低温游泳时间均明显延长(P<0.01,P<0.05)(表 2)。
| 组别 | 自主活动 次数/(次/5 min) | 低温游泳 存活时间/min |
| 正常对照组 | 29.36±9.28 | 17.04±4.58 |
| 肾阳虚模型组 | 15.17±2.09* | 10.22±2.75** |
| 蛹虫草低剂量组 | 19.57±7.19 | 12.88±1.74 |
| 蛹虫草中剂量组 | 24.32±4.03## | 16.82±3.07## |
| 蛹虫草高剂量组 | 23.40±6.20# | 15.72±1.59# |
| 注: 与正常对照组比较,* P<0.05,** P<0.01; 与肾阳虚模型组比较,P#<0.05,P##<0.01; 下表同。 Note: compared with control group,* P<0.05,** P<0.01; compared with model group,# P<0.05,## P<0.01; the same below. | ||
与正常对照组小鼠相比,肾阳虚模型组小鼠肾脏、肾上腺、睾丸以及精囊腺等脏器湿重均明显下降(P<0.01,P<0.01,P<0.05,P<0.01);给予蛹虫草后,小鼠脏器湿重较模型组有一定的改善,其中蛹虫草中、高剂量组小鼠肾脏、肾上腺和睾丸湿重显著增加(P<0.01,P<0.05,P<0.05),蛹虫草中剂量组小鼠精囊腺湿重也显著增加(P<0.01)(表 3)。
| 组别 | 肾脏湿重/mg | 肾脏系数/% | 肾上腺 湿重/mg | 肾上腺 系数/% | 睾丸湿重/mg | 睾丸系数/% | 精囊腺 湿重/mg | 精囊腺 系数/% |
| 正常对照组 | 668.8±8.8 | 14.80±0.19 | 12.5±0.9 | 0.28±0.02 | 362.8±57.9 | 8.03±1.28 | 288.1±52.9 | 6.38±1.17 |
| 肾阳虚模型组 | 351.7±4.7** | 17.49±0.23 | 5.8±0.3** | 0.29±0.01 | 241.5±9.3* | 12.01±0.46 | 67.0±2.0** | 3.30±0.09 |
| 蛹虫草低剂量组 | 432.5±0.1 | 18.52±0.00 | 7.5±0.7 | 0.31±0.03 | 264.7±21.3 | 11.33±0.91 | 98.5±19.9 | 4.21±0.85 |
| 蛹虫草中剂量组 | 617.6±10.2## | 18.65±3.24 | 10.3±8.44# | 0.31±0.25 | 356.8±26.2# | 10.77±0.79 | 139.5±29.7## | 4.21±0.90 |
| 蛹虫草高剂量组 | 603.9±0.9## | 19.96±0.03 | 10.1±1.1# | 0.34±0.04 | 332.1±48.1# | 10.98±1.59 | 112.8±66.9# | 3.73±2.21 |
与正常对照组相比,肾阳虚模型组小鼠血清睾酮和皮质醇的含量均明显降低(P<0.01,P<0.01),给予蛹虫草后,小鼠激素含量较肾阳虚模型组有一定的升高,其中蛹虫草中剂量组小鼠睾酮水平明显升高(P<0.01),蛹虫草中、高剂量组小鼠皮质醇水平也显著增加(P<0.05,P<0.05)(表 4)。
| 组别 | 睾酮/ng·mL-1 | 皮质醇/ng·mL-1 |
| 正常对照组 | 8.8889±1.3860 | 14.1304±1.2076 |
| 肾阳虚模型组 | 3.4269±1.3780** | 8.2839±1.0259** |
| 蛹虫草低剂量组 | 4.7496±1.6215 | 11.0910±1.2579 |
| 蛹虫草中剂量组 | 7.4676±1.8053## | 11.7320±1.3201# |
| 蛹虫草高剂量组 | 6.1659±1.6959# | 11.6436±1.1615# |
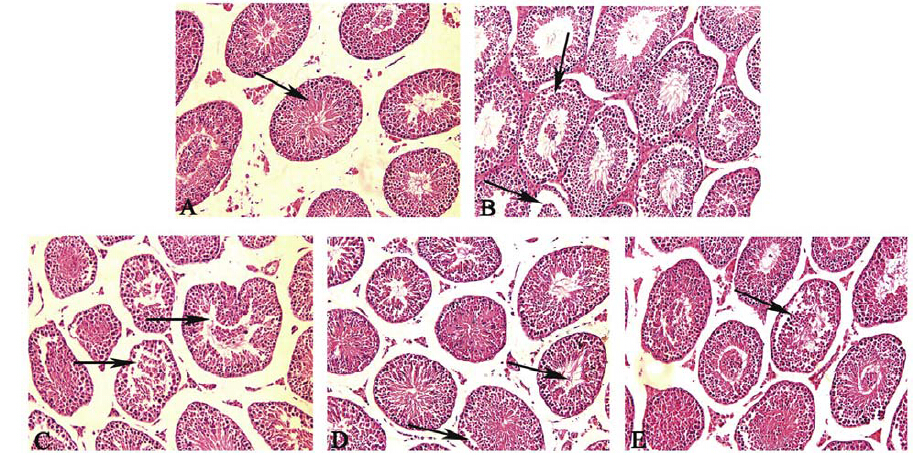
与正常对照组相比,肾阳虚模型组小鼠的曲细精管呈现明显退行性变化,管腔内生殖上皮变薄,各级生殖细胞萎缩出现空腔,排列紊乱,管腔较大。给予蛹虫草后,蛹虫草中、高剂量组小鼠睾丸损伤明显得到改善,各级生殖细胞萎缩减少,排列较规则,管腔较小。其中以蛹虫草中剂量组小鼠的睾丸损伤改善最明显,较接近正常对照组小鼠的睾丸形态(图 3)。
|
|
图 3 各组小鼠睾丸形态的比较(HE,×200)
Fig. 3 Comparison of testicular morphology of mice in each group(HE,×200)
注: A. 正常对照组,B. 肾阳虚模型组,C. 蛹虫草低剂量组,D. 蛹虫草中剂量组,E. 蛹虫草高剂量组。 Notes: A. Control group,B. Kidney-yang deficiency model group,C. Cordyceps militaris low-dose group,D. C. militaris middle-dose group,E. C. militaris high-dose group. |
蛹虫草作为药食两用菌,具有十分重要的药用价值,1999年版《中华本草》和1970年版《吉林中草药》分别有“滋肺补肾,治疗病后虚损和阳痿遗精”和“味甘、性温,归肾、肺两经”记载。刘洁等(1994)发现蚕蛹虫草水煎剂能增加去势大鼠精囊-前列腺质量,具有雄性激素样作用,其作用性质及强度与冬虫夏草相似。故本文考察能够促进睾丸间质细胞睾酮合成的具有雄性激素样作用的蛹虫草菌株对腺嘌呤造成的肾阳虚动物模型的防治作用,为其成为冬虫夏草的替代品提供更加完善的实验基础。
腺嘌呤是核酸的主要成分之一,当机体摄入大量的腺嘌呤后,异常高浓度的腺嘌呤在黄嘌呤氧化酶的作用下转变成极难溶解于水的2,8-二羟基腺嘌呤,其在肾内大量沉积形成结晶,造成肾功能损害,同时腺嘌呤代谢产物“毒性”作用,使肾组织中与糖、脂肪、蛋白质代谢有关的多种酶活性受抑制(Philips et al.,1990),影响了肾组织的能量代谢,进而出现一系列的阳虚表现。经腺嘌呤诱导后的动物模型可出现体质量下降、活动减少、反应迟钝、弓背蜷缩、畏寒、体毛疏松、多尿、泄泻等阳虚表现,符合中医学肾阳虚的典型体征,是可供科研和教学使用的较理想的肾阳虚动物模型(邵命海等,2008)。本实验中,给予腺嘌呤28 d后,模型组小鼠无论是外观状态,生理指标,激素水平,脏器质量和睾丸病理组织变化等均表明实验造模成功。本研究表明,与肾阳虚模型组相比,蛹虫草中、高剂量组小鼠的肾阳虚表征有明显改善,耐疲劳和耐寒能力提升,脏器湿重有显著的调整作用,血清睾酮和皮质醇含量升高,睾丸组织损伤减轻,这说明适当剂量的蛹虫草菌株YCC2对腺嘌呤致肾阳虚模型一定程度的改善作用。与前期考察该蛹虫草菌株能够促进睾酮的合成,具有雄性激素样的作用是相符的,这说明能够促进睾丸间质细胞睾酮合成的蛹虫草菌株确实对腺嘌呤致肾阳虚小鼠有防治作用,可以作为冬虫夏草的替代品进行进一步的研究开发。
| 高学敏. 2002. 中药学[M]. 北京: 中国中医药出版社: 530-531. |
| 国家药典委员会. 2010. 中华人民共和国药典[M]. 北京: 中国医药科技出版社: 106. |
| 刘洁, 杨旭, 陈正, 等. 1994. 蚕蛹虫草镇静及性激素样作用的研究[J]. 白求恩医科大学学报, 20(1): 14-16. |
| 卯晓兰. 2009. 中国蕈菌[M]. 北京: 科学出版社: 716. |
| 邵命海, 肖静, 王毅兴, 等. 2008. 从""肾主生殖""角度评价腺嘌呤与氢化可的松诱导的肾阳虚模型[J]. 上海中医药杂志, 42(2): 57-59. |
| 王瑞华, 杨昕, 涂秩平, 等. 2007. 人工蛹虫草子实体多糖的提取与含量测定[J]. 医药导报, 26(8): 843-845. |
| 肖静, 何立群, 高建东, 等. 2008. 腺嘌呤与氢化可的松大鼠肾阳虚模型造模方法比较[J]. 中国比较医学杂志, 18(3): 77-80. |
| Ng TB, Wang HX. 2005. Pharmacological actions of Cordyceps, a prized folk medicine[J]. J Pharmacal, 57: 1509-1519. |
| Philips FS, Thiersh JB, Bendic HA. 1990. Adenine intoxication in relation to in vivo formation and deposition of 2,8-dioxyadenine in renal tubules[J]. J Pharmacal Exp Ther, 104: 20-30. |
 2015, Vol. 34
2015, Vol. 34




