螺虫乙酯属季酮酸类杀虫剂,具有较强的内吸性,可在植物韧皮部和木质部上下双向传导,对刺吸性害虫具有较高活性[1];丁醚脲属硫脲类杀虫剂,广泛用于蔬菜、水果和茶树上防治蚜虫、粉虱和叶蝉等害虫。两者及其代谢物结构见图式 1。有研究显示,螺虫乙酯代谢物对雄性大鼠具有生殖毒性[2-3],而丁醚脲因其代谢物的毒性比母体更强,欧盟已全面禁止其使用[4]。中国已制定了螺虫乙酯和丁醚脲在部分作物上的临时限量[5]。鉴于其应用的广泛性和代谢物的高毒性,已开展两者正式限量标准制定项目。因此,建立螺虫乙酯、丁醚脲及其代谢物多残留的快速检测方法,将为制定两者正式限量标准、保障食品安全和国际贸易提供技术支撑。目前,关于螺虫乙酯和丁醚脲的测定方法主要是液相色谱-串联质谱法 (LC-MS/MS)[6-11],但均为螺虫乙酯或丁醚脲单一农药的测定方法,尚未见同时测定两者及代谢物多残留的分析方法。鉴于QuEchERS前处理方法简便、快速,本研究结合该前处理手段,利用超高效液相色谱-串联质谱建立了同时测定螺虫乙酯、丁醚脲及其代谢物(结构式见图式 1)在果蔬中的残留分析方法。
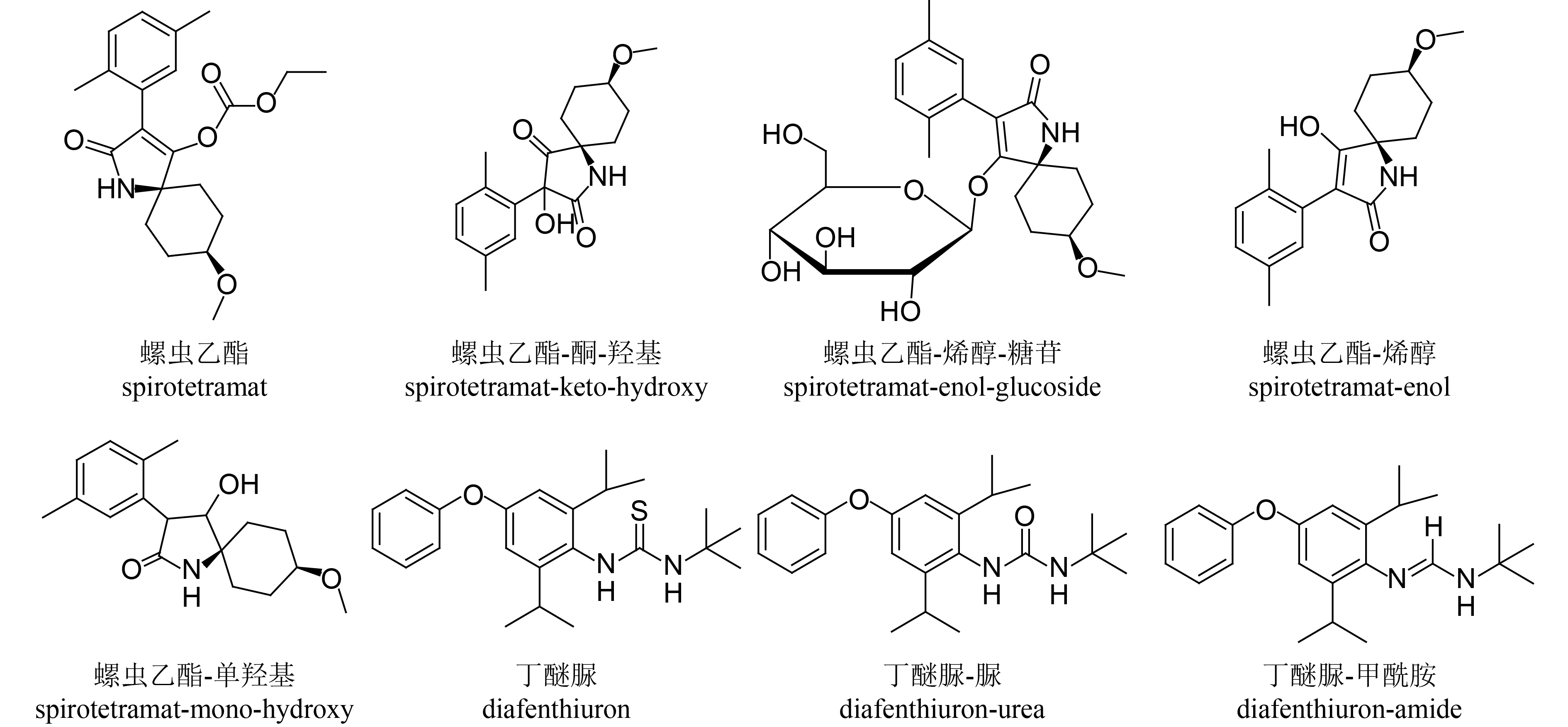
|
图式1 螺虫乙酯、丁醚脲及其代谢物的结构式 Scheme1 Structural formula of spirotetramat, diafenthiuron and their metabolites |
1 材料与方法 1.1 仪器与试剂
LC-MS 8040 超高效液相色谱-串联质谱仪 (日本岛津公司);SK-1 快速混匀器 (常州国华电器有限公司);UMV-1多管漩涡混匀器 (青云仪器设备有限公司);HX-PB965奥克斯破壁营养料理机 (佛山市海迅电器有限公司);BL610电子分析天平 (北京赛多利斯仪器系统有限公司);Milli-Q超纯水系统 (德国默克集团)。
99.5%螺虫乙酯 (spirotetramat)、98.6%螺虫乙酯-烯醇-糖苷 (spirotetramat-enol-glucoside,以下简称为S-glu,其余同)、98.2%螺虫乙酯-单羟基 (spirotetramat-mono-hydroxy,S-mono)、99.6%螺虫乙酯-烯醇 (spirotetramat-enol,S-enol)、94.8%螺虫乙酯-酮-羟基 (spirotetramat-keto-hydroxy,S-keto)和99.5%丁醚脲 (diafenthiuron),均购于德国Dr.Ehrenstorfer公司;99.7%丁醚脲-脲 (diafenthiuron-urea,D-urea)和99.1%丁醚脲-甲酰胺 (diafenthiuron-amide,D-amide),均购于日本林纯药工业株式会社;甲酸 (色谱级) 购于上海阿拉丁试剂有限公司;乙酸铵 (优级纯) 购于天津市科密欧化学试剂有限公司;甲醇 (质谱级) 购于上海安谱实验科技股份有限公司;定制QuEChERS净化管MQ1-2型 (青云实验耗材有限公司)
1.2 标准溶液配制标准工作溶液:准确称取适量的螺虫乙酯和丁醚脲标准品,用甲醇溶解,配成100 mg/L的标准储备液,再用甲醇逐级稀释成0.5、0.1、0.05、0.01和0.005 mg/L的系列混合标准工作溶液。
基质匹配标准溶液:用经提取、净化后获得的梨、葡萄、西瓜、芥蓝、芹菜和韭菜空白基质溶液分别将100 mg/L标准储备液稀释,配制成0.001、0.005、0.01、0.05、0.1和0.5 mg/L的基质匹配标准溶液。
标准工作溶液和基质匹配标准溶液配制过程中应避免使用一次性塑料吸管,以免抑制丁醚脲及其代谢物的离子化效率。
1.3 试验方法 1.3.1 样品前处理将样品切碎,四分法缩分后用料理机匀浆破壁。称取经破壁后的样品10 g(精确至0.01g) 于50 mL离心管中,加入10.0 mL乙腈和1.0 mL甲酸,涡旋提取10 min,再加入5~7 g氯化钠,涡旋提取2 min,于3 000 r/min下离心5 min;吸取4 mL上清液,加入5 mL QuEChERS净化管中,涡旋 20 s,挤压弃去净化管前端未被净化的提取液后,过0.22 μm尼龙滤膜,待分析。
1.3.2 检测条件色谱条件:shim-pack XR-ODS色谱柱 (75 mm × 2.0 mm,1.6 μm);柱温40 ℃;进样量1 μL。流动相A为体积分数为0.1%的甲酸水溶液,流动相B为甲醇;流速0.4 mL/min。梯度洗脱程序:10% B,保持0.2 min;9.8 min内调整为95%,恒定 4 min;1 min内调整为10%,保持2 min。
质谱条件:ESI+电离;多反应监测 (MRM) 模式;DL 管温度250 ℃;加热模块温度400 ℃;干燥气流速为15 L/min;碰撞气压力为230 kPa,接口电压+4.5 kV。优化的离子对、碰撞能量等信息详见表1。
|
|
表 1 8种化合物的相关质谱参数 Table 1 Mass spectrometry paprameters of the 8 compounds |
2 结果与分析 2.1 色谱条件的优化
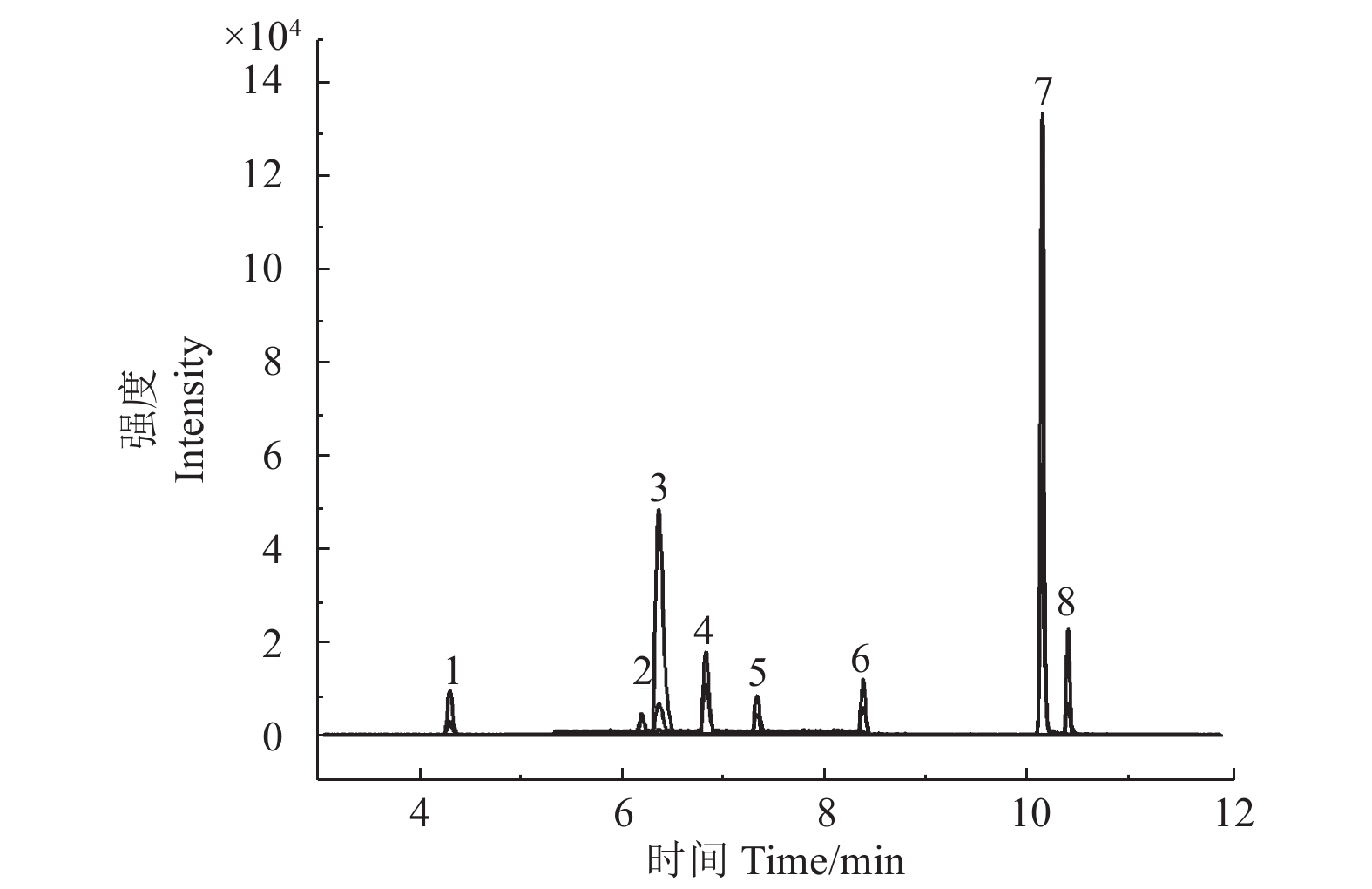
本研究中使用了实验室中常用的岛津XR C18色谱柱。鉴于螺虫乙酯、丁醚脲及其代谢物测定均采用ESI+ 电离模式,首选甲醇-水体系。考察了甲醇-水、甲醇-0.1%甲酸水溶液、甲醇-0.1%乙酸水溶液3种流动相对农药的色谱峰峰形和响应值的影响。结果表明:3种流动相条件下,各化合物的峰形均较好,但丁醚脲在甲醇-水、甲醇-0.1%乙酸水溶液2种流动相体系中会部分分解为丁醚脲代谢物,仅在甲醇-0.1%甲酸水溶液作流动相时相对稳定。因此,最终确定流动相为甲醇- 0.1%甲酸水溶液。8种化合物MRM色谱图如图1所示。
|
1. 螺虫乙酯-烯醇-糖苷;2. 螺虫乙酯-单羟基;3.丁醚脲-甲酰胺;4. 螺虫乙酯-烯醇;5. 螺虫乙酯-酮-羟基;6. 螺虫乙酯;7. 丁醚脲-脲;8. 丁醚脲。 1. S-glu; 2. S-mono; 3. D-amide; 4. S-enol; 5. S-keto; 6. spirotetramat; 7. D-urea; 8. diafenthiuron. 图 1 8种化合物的MRM色谱图(0.01 mg/L) Fig. 1 MRM chromatograms of the 8 compounds (0.01 mg/L) |
2.2 提取溶剂的选择
QuEChERS前处理方法中常用酸化乙腈作提取溶剂,本研究以黄瓜为试验对象,在 0.01 mg/kg添加水平下,分别比较了V (乙腈) : V (乙酸) = 100 : 1及V (乙腈) : V (甲酸) = 100 : 1、20 : 1、10 : 1对目标化合物的提取效率。结果 (表2) 表明: S-glu仅在V (乙腈) : V (甲酸) = 10 : 1提取条件下回收率在80%以上,而其余7种化合物在上述4种提取条件下均能达到农药残留检测要求[12]。兼顾丁醚脲、螺虫乙酯及其代谢物,最终确定以V (乙腈) : V (甲酸) = 10 : 1为提取溶剂。
|
|
表 2 黄瓜基质中8种化合物在不同酸化乙腈提取下的回收率 Table 2 Recoveries of the 8 compounds in cucumber matrix with different acidic acetonitrile |
2.3 基质效应、线性范围
采用公式ME = B/A × 100%评价基质效应 (其中:A和B分别表示溶剂标准溶液曲线和基质匹配标准溶液曲线的斜率)。当ME在80%~120%之间表明基质效应不明显,当ME在50%~80%和120%~150%之间时,应考虑消除基质效应[13]。本研究通过减缓流动相变化梯度 (见1.3.2节) 和进样1 μL的方式,考察了梨、葡萄、西瓜、芥蓝、芹菜和韭菜6种基质中的基质效应。从表3可知,8种化合物在6种果蔬中ME在83%~102%之间,基质效应不明显,可以忽略。
|
|
表 3 螺虫乙酯、丁醚脲及其代谢物线性范围和基质效应 Table 3 Linear ranges and matrix effects of spirotetramat, diafenthiuron and their metabolites |
以化合物质量浓度 (x, mg/L) 为横坐标,峰面积 (y) 为纵坐标得到线性方程。丁醚脲-脲 (D-urea) 和丁醚脲甲酰胺 (D-amide) 在0.001~0.1 mg/L范围内线性良好,其余化合物在0.005~0.5 mg/L范围内线性良好,R2 ≥ 0.999 3(表3)。
2.4 方法的准确度、精密度和定量限选取不含目标化合物的葡萄、梨、西瓜、韭菜、芥蓝和芹菜空白样品,通过添加回收试验,考察了方法的准确度和精密度 (n = 5)。结果 (表4) 表明:丁醚脲-脲和丁醚脲-甲酰胺在0.001、0.01和0.1 mg/kg添加水平下,其余化合物在0.005、0.05和0.5 mg/kg添加水平下,8种化合物的平均回收率在68%~94%之间,相对标准偏差在5.4%~15%之间,可以满足残留分析的要求[12]。根据添加回收试验确定丁醚脲-脲和丁醚脲-甲酰胺的定量限 (LOQ) 为0.001 mg/kg,其余化合物的LOQ均为0.005 mg/kg。
|
|
表 4 螺虫乙酯、丁醚脲及其代谢物的添加回收率和相对标准偏差 (n = 5) Table 4 Recoveries and relative standard deviations of spirotetramat, diafenthiuronand their metabolites(n = 5) |
2.5 实际样品测定
为评价方法的可行性,按所建立的方法对烟台市某市场抽取的220个水果及蔬菜样品进行分析测定。结果 (表5) 表明:有5个样品中检出丁醚脲及其代谢物残留,其残留量在0.012~0.11 mg/kg之间,检出率为2.3%;有8个样品检出螺虫乙酯及其代谢物残留,其残留量在0.005~0.22 mg/kg之间,检出率为3.6%。该结果表明本研究所建立的QuEChERS-超高液相色谱-串联质谱法适合果蔬中丁醚脲、螺虫乙酯及其代谢物残留量的测定。
|
|
表 5 果蔬中螺虫乙酯、丁醚脲及其代谢物残留量抽检结果 Table 5 The residues of spirotetramat, diafenthiuron and their metabolites in fruits and vegetables |
3 结论与讨论
建立了QuEChERS-超高效液相色谱-串联质谱法测定丁醚脲、螺虫乙酯及其代谢物残留。明确了方法中2个关键控制点:一是提取溶剂应采用V (乙腈) : V (甲酸) = 10 : 1;二是以甲醇-0.1%甲酸水溶液作流动相,可有效保护丁醚脲,减少其降解,同时提高对S-glu的提取效率。方法中确定了较佳的洗脱梯度、减少进样体积,降低了基质效应,避免了繁杂的基质匹配标准溶液配制过程。该方法简便、快速,灵敏度高,准确度和精密度均能达到农药残留的检测要求,可用于果蔬中两者及其代谢物残留的批量检测。虽然中国制定了丁醚脲和螺虫乙酯的限量标准值,但均为临时限量,且只规定了其在部分作物上的限量标准[5]。中国规定丁醚脲残留定义仅有丁醚脲。日本规定的丁醚脲限量标准中包括D-urea和D-amide 2个代谢物[14]。鉴于中国和日本的农产品贸易频繁,有必要在丁醚脲残留定义中包括此2种代谢物,否则两国口岸对农产品进行丁醚脲检测时,判定标准不一,容易出现贸易争端。近几年相关学者也关注过丁醚脲残留问题,研究中均包含此2种代谢物[6]。中国规定螺虫乙酯残留定义包括母体和烯醇类代谢物,与JMPR一致。但JMPR同时指出,如果考虑膳食摄入风险评估,螺虫乙酯残留定义应包括其母体及spirotetramat-enol-glucoside、spirotetramat-enol、spirotetramat-keto-hydroxy和spirotetramat-mono-hydroxy 4种代谢物[15],即本研究中的S-glu、S-enol、S-keto和S-mono。因此,开展螺虫乙酯限量标准制定或检测方法开发应考虑母体及以上4种代谢物。本研究在实际样品检测中,螺虫乙酯的4种代谢物和丁醚脲的2种代谢物均有检出。因此,建议开展丁醚脲和螺虫乙酯残留和风险评估研究应包括丁醚脲代谢物D-urea和D-amide,螺虫乙酯代谢物S-enol、S-keto、S-glu和S-mono,同时建议在修订两者残留定义时也应包含上述代谢物。
| [1] |
NAUEN R, RECKMANN U, THOMZIK J, et al. Biological profile of spirotetramat(Movento®)-a new two-way systemic(ambimobile) insecticide against sucking pest species
[J]. Bayer Crop Science Journal, 2008, 61(2): 245-278. |
| [2] |
吴慧明, 魏方林, 朱国念, 等. 螺虫乙酯在染毒雄性大鼠体内的分布与代谢[J]. 农药学学报, 2012, 14(4): 417-422. WU H M, WEI F L, ZHU G N, et al. Study on distribution and metabolism of spirotetramat in rat[J]. Chin J Pestic Sci, 2012, 14(4): 417-422. DOI:10.3969/j.issn.1008-7303.2012.04.10 |
| [3] |
Australian Pesticides and Veterinary Medicines Authority(APVMA). Evaluation of the New Active Spirotetramat in the Product MOVENTO 240 SC Insecticide[M]. Canberra: APVMA, 2009.
|
| [4] |
Official Journal of the European Communities. Commission Regulation(EC)[EB/OL]. (2002-11-20)[2018-10-10] . https://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=OJ:L:2002:319:0003:0011:EN:PDF
|
| [5] |
食品安全国家标准 食品中农药最大残留限量: GB 2763—2016[S]. 北京: 中国标准出版社, 2016. National food safety standard-Maximum residue limits for pesticides in food: GB 2763—2016[S]. Beijing: Standards Press of China, 2016. |
| [6] |
张新忠, 罗逢健, 刘光明, 等. 超高效液相色谱-串联质谱法测定茶叶和土壤中丁醚脲及其代谢物的残留[J]. 分析化学, 2011, 39(9): 1329-1335. ZHANG X Z, LUO F J, LIU G M, et al. Determination of diafenthiuron and its metabolites in tea and soil by ultra performance liquid chromatography-electrospray ionization tandem mass spectrometry[J]. Chin J Anal Chem, 2011, 39(9): 1329-1335. |
| [7] |
ZHU Y L, LIU X G, XU J, et al. Simultaneous determination of spirotetramat and its four metabolites in fruits and vegetables using a modified quick, easy, cheap, effective, rugged, and safe method and liquid chromatography/tandem mass spectrometry[J]. J Chromatogr A, 2013, 1299: 71-77. DOI:10.1016/j.chroma.2013.05.049 |
| [8] |
陈磊, 上官良敏, 付凤富. QuEChERS 预处理结合 HPLC-MS/MS 同时检测茶叶中 7 种农药残留[J]. 中国科学: 化学, 2016, 46(3): 302-308. CHEN L, SHANGGUAN L M, FU F F. Simultaneous determination of seven carbamates, neonicotinoids and diafenthiuron pesticide residues in tea by QuEChERS-HPLC-MS/MS[J]. Scientia Sinica(Chimica), 2016, 46(3): 302-308. |
| [9] |
LI S S, LIU X G, DONG F S, et al. Chemometric-assisted QuEChERS extraction method for the residual analysis of thiacloprid, spirotetramat and spirotetramat's four metabolites in pepper: Application of their dissipation patterns[J]. Food Chem, 2016, 192: 893-899. DOI:10.1016/j.foodchem.2015.07.122 |
| [10] |
易廷辉, 唐柏彬, 邹芸, 等. 超高效液相色谱-串联质谱法快速测定牛奶中螺虫乙酯及其代谢物残留[J]. 色谱, 2017, 35(7): 677-682. YI T H, TANG B B, ZOU Y, et al. Rapid determination of spirotetramat and its metabolite residues in milk by ultra performance liquid chromatography-tandem mass spectrometry[J]. Chin J Chromatogr, 2017, 35(7): 677-682. |
| [11] |
徐诚, 张圣虎, 张毅, 等. 超高效液相色谱-三重四极杆-离子阱质谱法检测柑橘中螺虫乙酯及其 4 种代谢产物[J]. 色谱, 2018, 36(4): 339-344. XU C, ZHANG S H, ZHANG Y, et al. Determination of spirotetramat and its four metabolites in citrus by ultra-high performance liquid chromatography-triple quadrupole-ion trap mass spectrometry[J]. Chin J Chromatogr, 2018, 36(4): 339-344. |
| [12] |
农药残留试验准则: NY/T 788—2004[S]. 北京: 中国农业出版社, 2004. Guideline on pesticide residue trials: NY/T 788—2004[S]. Beijing: China Agriculture Press, 2004. |
| [13] |
TAYLOR P J. Matrix effects: the achilles heel of quantitative high-performance liquid chromatography-electrospray-tandem mass spectrometry[J]. Clin Biochem, 2005, 38(4): 328-334. DOI:10.1016/j.clinbiochem.2004.11.007 |
| [14] |
The Japan Food Chemical Research Foundation. Maximum Residue Limits(MRLs) List of Agricultural Chemicals in Foods[EB/OL].[2018-12-29] . http://db.ffcr.or.jp/front/pesticide_comp.
|
| [15] |
Food and Agriculture Organization of the United Nations. Pesticide Evaluated by JMPR and JMPS[EB/OL].[2018-12-29] .http://www.fao.org/agriculture/crops/thematic-sitemap/theme/pests/lpe/lpe-s/en/.
|
 2019, Vol. 21
2019, Vol. 21


