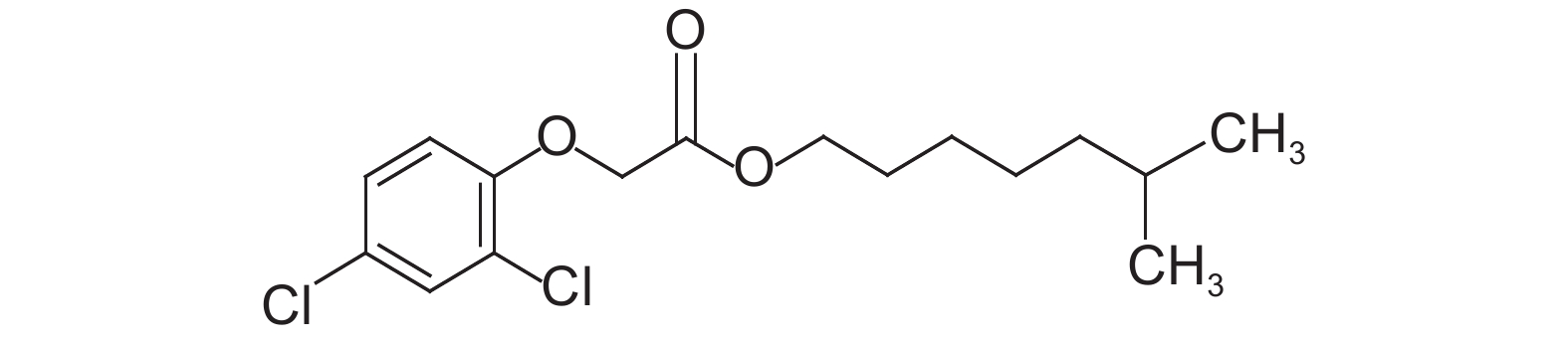
2,4-滴异辛酯 (2,4-D isooctyl ester) (结构式见图式 1) 是一种重要的苯氧羧酸酯类茎叶处理除草剂,主要用于防除小麦、大麦和玉米等禾本科作物田中的阔叶类杂草[1-2]。
笔者等[3]前期建立了2,4-滴异辛酯在土壤中的残留分析方法并得出其在土壤中的降解半衰期为12.83 d。农药在环境中的水解和光解是农药环境行为的重要组成部分,也是评价农药对生态环境影响及其在环境中残留特性的重要指标[4-5],但目前尚未见有关2,4-滴异辛酯在溶液中水解和光解特性的研究报道。为此,笔者采用室内模拟试验方法,就2,4-滴异辛酯的水解和光解特性及影响因素进行了研究。
|
图式1 2,4-滴异辛酯结构式 Scheme1 Structural formula of 2,4-D isooctyl ester |
1 材料与方法 1.1 仪器及试剂
Agilent 7890B气相色谱仪 (配ECD检测器)、Agilent 1290-6460液相色谱-串联三重四极杆质谱仪和MassHunter工作站软件 (Agilent公司,美国);BAS224S型电子天平 (精确到0.000 1 g,德国Sartorius公司);ZQZY-CF型恒温振荡培养箱 (上海知楚仪器有限公司);FE28 型pH计[梅特勒-托利多仪器 (上海) 有限公司];超纯水仪 (美国Millipore公司);YCYN-GHX-AC光化学反应仪 (上海郓曹电子科技有限公司)。
2,4-滴异辛酯 (2,4-D isooctyl ester) 标准品 (纯度96.8%,大连瑞泽有限公司);2,4-滴 (2,4-D) 标准品 (纯度99.4%,沈阳化工研究院);丙酮、乙腈为色谱纯,其余试剂为分析纯。
1.2 标准溶液配制及标准曲线绘制根据《化学农药环境安全评价试验准则》“第2 部分:水解试验”[6]及“第3 部分:光解试验”[7]要求,由于2,4-滴异辛酯难溶于水,故选择丙酮作为助溶剂。准确称取0.01 g (精确至0.00 01 g) 2,4-滴异辛酯标准品,用丙酮溶解并定容至100 mL,配制成100 mg/L的2,4-滴异辛酯标准储备液,于–20 ℃下避光保存,试验时再用丙酮逐级稀释,配制成0.01~5 mg/L的标准工作溶液,现用现配。以峰面积为纵坐标,进样质量浓度为横坐标绘制溶剂标准曲线。
1.3 检测条件 1.3.1 2,4-滴异辛酯检测条件色谱柱:Agilent HP-5毛细管柱 (30 m × 0.32 mm,0.25 µm);载气为氮气 (纯度99.999%);电子捕获检测器300 ℃;进样口250 ℃;进样量1 µL;不分流进样;隔垫吹扫流量为3 mL/min。程序升温:初始160 ℃,保持5 min;以6 ℃/min速率升至240 ℃,保持5 min;再以50 ℃/min速率降至160 ℃,保持5 min。在此条件下,2,4-滴异辛酯的保留时间为17.7 min。
1.3.2 2,4-滴异辛酯降解产物2,4-滴的检测条件色谱条件:Agilent Eclipse Plus C18色谱柱 (2.1 mm × 50 mm,1.8 µm),柱温40 ℃,进样体积1 µL;流动相A为甲醇,流动相B为体积分数0.2%的甲酸水溶液;流速0.4 mL/min。梯度洗脱程序:0 min, 10% A; 0 > ~ ≤ 1.5 min, 30% A ; 1.5 > ~ ≤ 3 min, 90% A; 3 > ~ ≤ 4 min, 90% A; 4 > ~ ≤5 min, 10% A。
质谱条件:电喷雾离子源 (ESI);干燥气为99.95%氮气,碰撞气为99.999%氮气;负离子多反应监测模式 (MRM);干燥气流速10.0 L/min,温度325 ℃;鞘气流速12.0 L/min,350 ℃;负极毛细管电压3 500 V,喷嘴电压0 V;裂解电压70 V;定性离子对m/z 218.9/124.6,碰撞能28 V;定量离子对m/z 218.9/160.8,碰撞能9 V。在此条件下,2,4-滴的保留时间为3.2 min。
1.4 缓冲溶液配制pH=4 的缓冲溶液:乙酸 (冰醋酸) 18.86 mL,乙酸铵 4.62 g;pH=7 的缓冲溶液:磷酸二氢钾 12.9 g,三水磷酸氢二钾13.68 g;pH=9 的缓冲溶液:碳酸氢钠 89.61 g,碳酸钠 6.36 g。均用蒸馏水定容至100 mL,现用现配,使用前灭菌并重新校准。
1.5 水解试验根据试验准则[6]要求,参考文献[8]中的方法并略有改进:配制5 mg/L的2,4-滴异辛酯标准工作溶液,分别考察其在不同温度 (15、25和35 ℃) 以及pH值 (4、7和9) 下的水解;分别采用蒸馏水 (pH 7.16)、自来水 (pH 6.52)、稻田水 (pH 7.29) 和河水 (pH 7.23) 配制5 mg/L的2,4-滴异辛酯标准品水溶液,考察其在不同水体中的水解;采用pH = 7的缓冲溶液配制初始质量浓度分别为1、3和5 mg/L的2,4-滴异辛酯标准工作溶液,考察其在不同初始质量浓度下的水解。于0、0.17、0.33、0.5、1、6、12、24、72、120、168及240 h后分别取样,通过GC-ECD检测2,4-滴异辛酯的残留量。每处理3次重复。
1.6 光解试验根据试验准则[7]要求,参考文献[8]中的方法,并依照1.5节水解试验设计进行2,4-滴异辛酯的光解试验。其中,2,4-滴异辛酯在不同pH值、不同水体和不同初始质量浓度下的光解试验均采用300 W (照度为30 000 lx) 汞灯在光化学反应仪中进行光照;另分别采用300 W汞灯 (30 000 lx)、500 W汞灯 (50 000 lx) 以及500 W氙灯 (10 500 lx) 光照,考察2,4-滴异辛酯在不同光源下的光解。
2 结果与分析 2.1 方法的准确性和精密度外标法定量。结果表明:在0.01~5 mg/L范围内,2,4-滴异辛酯的峰面积与进样质量浓度间呈良好线性关系,回归方程为y = 12 512x – 123.19,R2 = 1;在0.01~1 mg/L添加水平下,2,4-滴异辛酯的平均回收率在99%~102%之间,日内相对标准偏差 (RSD1) 在2.9%~5.1%之间 (n = 5),日间相对标准偏差 (RSD2) 在3.4%~4.8%之间 (n = 15);根据最低添加浓度得到该方法的定量限 (LOQ) 为0.01 mg/L。表明所用分析方法能够满足2,4-滴异辛酯的残留检测要求[9]。
2.2 影响2,4-滴异辛酯水解的因素 2.2.1 温度和pH值的影响结果 (表1) 表明,高温条件有利于其水解,而中性条件不利于其水解。在pH值为7时,温度越高水解速率越快;25 ℃时,不同pH值条件下的水解速率从大到小依次为:酸性>碱性>中性。
|
|
表 1 2,4-滴异辛酯在不同温度和不同pH 值条件下的水解动力学参数 Table 1 Hydrolysis kinetics parameters of 2,4-D isooctyl ester solutions under different temperatures and pH values |
温度对2,4-滴异辛酯的水解速率影响显著,每升高10 ℃,其水解速率平均增加1.79倍。这是由于水解属于热反应,温度升高,分子运动速度加快,碰撞频率加快,从而增大了分子碰撞产生的活化能,使水解反应速率加快[10-11]。
pH值对2,4-滴异辛酯水解的影响也比较明显。由于其酯键断裂需要强酸、强碱的催化,因此在中性 (pH 7) 条件下,2,4-滴异辛酯的水解半衰期较长,水解难以发生。
2.2.2 水体的影响由表2可知:2,4-滴异辛酯在自来水中的水解速率相对较快,可能是由于该水体呈弱酸性 (pH 6.52) 所致;在蒸馏水、稻田水和河水中的水解速率由快到慢依次为:稻田水>河水>蒸馏水。由于自然水体中含有大量的溶解性物质、微量元素、悬浮颗粒物和微生物等[8],2,4-滴异辛酯在稻田水和河水中的水解必然受其影响,其中微生物降解可能是其在稻田水和河水中半衰期比在蒸馏水中明显缩短的重要影响因素。
|
|
表 2 2,4-滴异辛酯在不同水体中的水解动力学参数 Table 2 Hydrolysis kinetics parameters of 2,4-D isooctyl ester solutions in different types of water quality |
2.2.3 初始浓度的影响
由表3可看出,随初始浓度增大,2,4-滴异辛酯的水解速率常数逐渐增大,半衰期逐渐缩短。与刘晓旭[12]对嘧菌酯水解的研究结果一致。其原因可能是由于随着2,4-滴异辛酯初始浓度增大,水解过程中中心原子给电子的能力增强,反应速率随之加快[13]。
|
|
表 3 不同初始浓度下2,4-滴异辛酯的水解动力学参数 Table 3 Hydrolysis kinetics parameters of 2,4-D isooctyl ester solutions with different initial concentration |
2.3 影响2,4-滴异辛酯光解的因素 2.3.1 pH值的影响
2,4-滴异辛酯在不同pH值缓冲溶液中的光解均符合一级反应动力学方程。相同浓度的2,4-滴异辛酯在不同pH值缓冲溶液中的光解半衰期差异显著 (表4),光解速率依次为:pH =4 > pH= 7 > pH= 9。
|
|
表 4 2,4-滴异辛酯在不同pH值缓冲溶液中的光解动力学参数 Table 4 Photolysis kinetics parameters of 2,4-D isooctyl ester solutions in buffer solutions with different pH values |
由于不同自然水体间酸碱度存在差异,因此研究2,4-滴异辛酯在不同pH值缓冲溶液中的光解行为具有重要意义。研究表明,不同pH缓冲溶液中存在的H+ 和OH– 会不同程度地催化降解反应[14],但H+ 和OH– 对2,4-滴异辛酯光解的影响机制还需要进一步研究。
2.3.2 水体的影响300 W汞灯照射下,2,4-滴异辛酯在不同水体中的光解均符合一级反应动力学方程,其在4种水体中的光解速率依次为:河水>稻田水>自来水>蒸馏水 (表5)。由于不同水体中所含有的吸收和传导光能的物质不同,所以农药在不同水体中的光解速率通常会存在一定差异[15]。
|
|
表 5 2,4-滴异辛酯在不同水体中的光解动力学参数 Table 5 Photolysis kinetics parameters of 2,4-D isooctyl ester solutions in different types of water quality |
2.3.3 光源的影响
不同光源下,2,4-滴异辛酯的光解半衰期依次为500 W氙灯>300 W汞灯>500 W汞灯 (表6),其在汞灯照射下的光解速率比氙灯下快了近2倍。由于汞灯的发射光谱主要集中在短波长的近紫外部分,与氙灯相比其波长短且强度大,故而使得药剂的光解速率明显加快,且汞灯光强越大,光解速率越快[16]。因此,2,4-滴异辛酯在长波长光源下相对稳定,不易光解;而在短波长的光源下相对较为活跃,易被光解[12]。
|
|
表 6 2,4-滴异辛酯在不同光源下的光解动力学参数 Table 6 Photolysis kinetics parameters of of 2,4-D isooctyl ester solutions under different light sources |
2.3.4 初始浓度的影响
300 W汞灯照射下,不同初始质量浓度2,4-滴异辛酯的光解半衰期依次为:1 mg/L > 3 mg/L > 5 mg/L ( 表7),表明2,4-滴异辛酯的光解速率随初始浓度的增大而加快,与刘晓旭[12]对嘧菌酯光解的研究结果一致。这可能与其光解自由基反应机理有关,即2,4-滴异辛酯在汞灯照射下形成高能量的氧化态自由基,从而进一步引发了光降解反应[17],高浓度的2,4-滴异辛酯由于单位分子量增加,接受光能发生光降解的分子数量也增加,从而使得总体光解速率加快。具体还有待进一步研究。
|
|
表 7 不同初始浓度下2,4-滴异辛酯的光解动力学参数 Table 7 Photolysis kinetics parameters of 2,4-D isooctyl ester solutions with different initial concentrations |
3 2,4-滴异辛酯降解产物测定
农药最大允许残留限量国家标准[18]中指出,2,4-滴异辛酯的降解产物为2,4-滴。因此,本研究采用液相色谱-串联质谱 (HPLC-MS/MS) 方法,同时检测了2,4-滴异辛酯水解及光解样品中2,4-滴的含量。
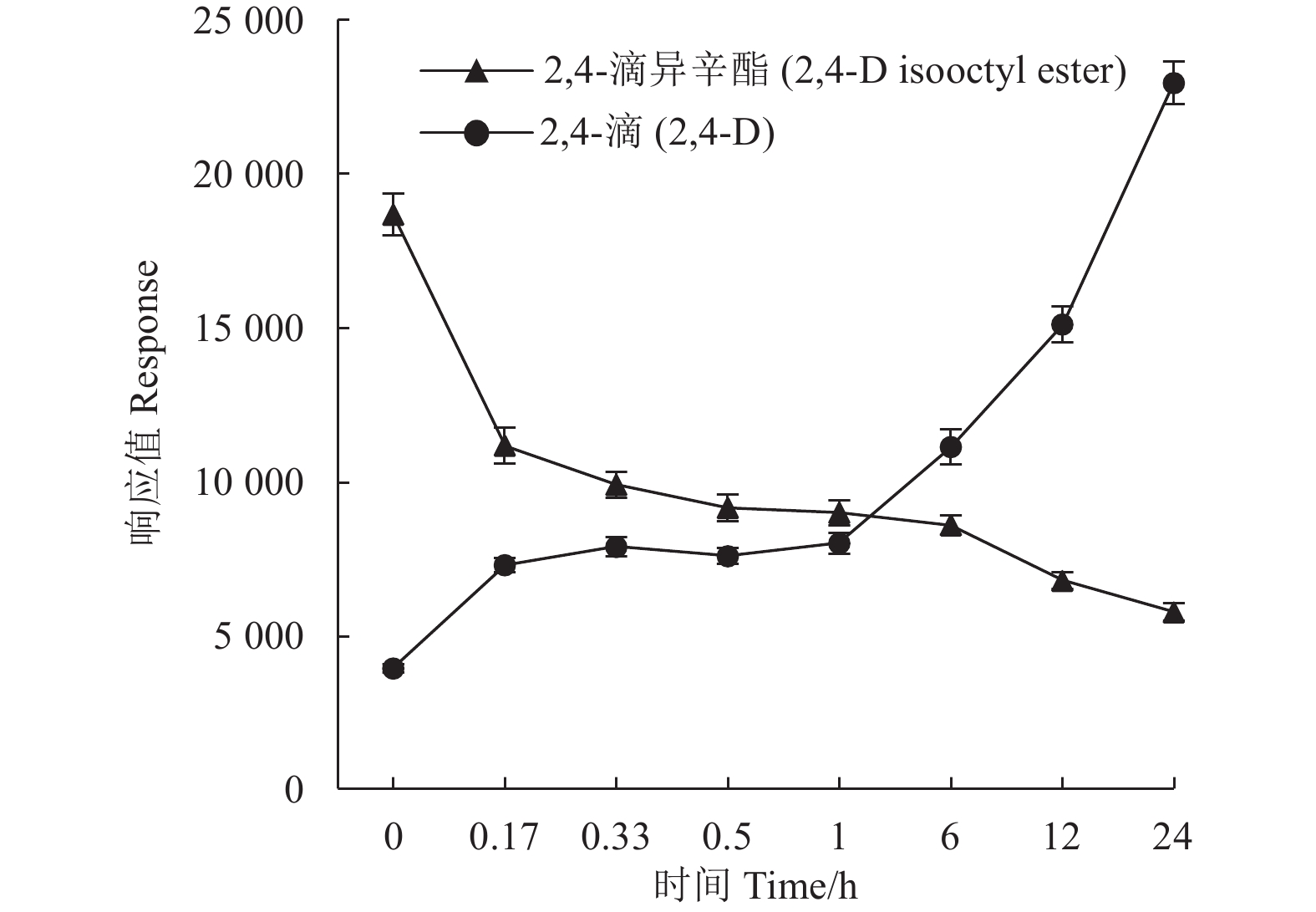
以2,4-滴异辛酯在35 ℃、pH=9的缓冲溶液中的水解为例,随时间推移,样品中2,4-滴异辛酯的含量逐渐减少,而2,4-滴的含量逐渐增加 (图1),表明2,4-滴异辛酯水解及光解后的主要产物是2,4-滴,该过程为酯水解反应 (图2)。目前,农药残留联合专家会议 (JMPR) 和欧洲食品安全局 (EFSA) 等的报告中均未提及2,4-滴异辛酯的酯水解,关于其酯水解生成2,4-滴和7-甲基庚醇的研究也未见报道,因此尚有待深入研究。
|
图 1 2,4-滴异辛酯和2,4-滴随时间变化曲线 Fig. 1 The variation curve of 2,4-D isooctyl ester and 2,4-D with time |

|
图 2 2,4-滴异辛酯酯水解反应方程式 Fig. 2 Hydrolysis reaction of 2,4-D isooctyl ester |
关于2,4-滴异辛酯降解产物2,4-滴的降解特性已有诸多报道,如吴星卫等[19]关于2,4-滴水解、光解及在土壤中的降解特性研究,以及Venkatesh等[20]的2,4-滴在玉米叶上的光降解研究等。依据农药特性数据库 (PPDB)[21],2,4-滴的主要代谢产物为2,4-二氯苯酚、2,4-二氯甲氧基苯和对氯苯酚,水解和光解后也会生成部分1, 2,4-苯三酚;EFSA报告[22]中指出,2,4-滴的代谢产物为二氯苯胺和二氯苯酚;JMPR报告[23]中指出,2,4-滴可代谢成多种组分,主要为亲本2,4-滴和2,4-二氯苯酚的共轭产物,其他代谢物的转化率低于5%。因此可以断定,2,4-滴的主要降解产物为2,4-二氯苯酚。
4 结论目前尚未见有关2,4-滴异辛酯在环境中化学行为的深入研究报道。本研究表明:2,4-滴异辛酯在不同环境条件下的水解和光解均符合一级反应动力学方程。其在酸性及碱性条件下的水解速率快于在中性条件下;其水解速率随温度升高而明显加快;2,4-滴异辛酯在稻田水和自来水中的水解速率高于其在蒸馏水和河水中;初始浓度越高其水解速率越快。
2,4-滴异辛酯的光解速率随pH值升高而减慢;其在稻田水和河水中的光解速率高于其在蒸馏水和自来水中;不同光源下的光解速率依次为500 W汞灯 > 300 W汞灯 > 500 W氙灯;初始浓度越高,2,4-滴异辛酯的光解速率越快。
影响农药在环境中水解和光解的因素很多,除了文中探讨的温度、溶液pH值、水质、光源和初始浓度外,主要还有腐殖酸、有机溶剂、金属离子和表面活性剂等[24-25],因此,为全面了解2,4-滴异辛酯在环境中的水解和光解特性,还需进行更广泛深入的研究。此外,为了系统评价2,4-滴异辛酯对环境的安全性,还需要对其本身及其水解和光解产生的各种代谢物的毒性和环境毒理等进行深入研究。
| [1] |
吴淑华, 张兰云, 聂乐兴, 等. 2,4-滴异辛酯·莠去津 51% 悬浮剂防除夏玉米田杂草药效与安全性评价[J]. 农药科学与管理, 2008, 30(9): 35-37. WU S H, ZHANG L Y, NIE L X, et al. Efficacy and security test of 2,4-D-ethylhexyl·atrazine 51% SC for control of weeds in summer maize field[J]. Pestic Sci Admin, 2008, 30(9): 35-37. DOI:10.3969/j.issn.1002-5480.2008.09.012 |
| [2] |
朱春杰. 90% 2,4-滴异辛酯乳油防除玉米田、大豆田阔叶类杂草效果评价[J]. 辽宁农业科学, 2013(5): 71-73. ZHU C J. 90% 2,4-D isooctyl ester EC for evaluation of control effect of broad-leaved weeds in corn and soybean fields[J]. Liaoning Agric Sci, 2013(5): 71-73. DOI:10.3969/j.issn.1002-1728.2013.05.021 |
| [3] |
张双, 刘娜, 程功, 等. 利用 QuEChERS-GC-ECD 法测定 2,4-滴异辛酯在土壤中的残留及消解[J]. 农药, 2018, 57(4): 290-293. ZHANG S, LIU N, CHENG G, et al. Determination of 2,4-D isooctyl ester residues in soil and dissipation process in soil by QuEChERS-GC-ECD[J]. Agrochemicals, 2018, 57(4): 290-293. |
| [4] |
PROSEN H, ZUPANČIČ-KRALJ L. Evaluation of photolysis and hydrolysis of atrazine and its first degradation products in the presence of humic acids[J]. Environ Pollut, 2005, 133(3): 517-529. |
| [5] |
ATKINSON S K, MARLATT V L, KIMPE L E, et al. Environmental factors affecting ultraviolet photodegradation rates and estrogenicity of estrone and ethinylestradiol in natural waters[J]. Arch Environ Contam Toxicol, 2011, 60(1): 1-7. |
| [6] |
化学农药环境安全评价试验准则 第 2 部分: 水解试验: GB/T 31270. 2—2014[S]. 北京: 中国标准出版社, 2015. Test guidelines on environmental safety assessment for chemical pesticides, part 2: hydrolysis: GB/T 31270. 2—2014[S]. Beijing: Standards Press of China, 2015. |
| [7] |
化学农药环境安全评价试验准则 第 3 部分: 光解试验: GB/T 31270. 3—2014[S]. 北京: 中国标准出版社, 2015. Test guidelines on environmental safety assessment for chemical pesticides, part 3: phototransformation: GB/T 31270. 3—2014[S]. Beijing: Standards Press of China, 2015. |
| [8] |
KWON J W, ARMBRUST K L, GREY T L. Hydrolysis and photolysis of flumioxazin in aqueous buffer solutions[J]. Pest Manag Sci, 2004, 60(9): 939-943. DOI:10.1002/(ISSN)1526-4998 |
| [9] |
农药残留试验准则: NY/T 788—2004[S]. 北京: 中国农业出版社, 2004. Guideline on pesticide residue trials: NY/T 788—2004[S]. Beijing: China Agriculture Press, 2004. |
| [10] |
陈锡岭, 徐新明, 樊德方. 温度和 pH 值对雷克拉水解速率的影响[J]. 农业环境保护, 1999, 18(6): 275-277. CHEN X L, XU X M, FAN D F. The effect of temperature and pH value on carbetamide hydroysis rate[J]. Agro-Environ Prot, 1999, 18(6): 275-277. |
| [11] |
HONG F, PEHKONEN S O, BROOKS E. Pathways for the hydrolysis of phorate: product studies by 31P NMR and GC-MS[J]. J Agric Food Chem, 2000, 48(7): 3013-3017. DOI:10.1021/jf990558u |
| [12] |
刘晓旭. 嘧菌酯的水解和光解特性研究[D]. 长春: 吉林农业大学, 2013. LIU X X. Study on the hydrolysis and photolytic characteristic of azoxystrobin[D]. Changchun: Jilin Agricultural University, 2013. |
| [13] |
欧晓明. 农药在环境中的水解机理及其影响因子研究进展[J]. 生态环境, 2006, 15(6): 1352-1359. OU X M. Hydrolysis and its influencing factors of pesticides in environment: a review[J]. Ecol Environ, 2006, 15(6): 1352-1359. DOI:10.3969/j.issn.1674-5906.2006.06.044 |
| [14] |
梁菁, 郭正元, 冯丽萍, 等. 农药在环境中光化学降解的影响因素[J]. 农业环境科学学报, 2007, 26(增刊1):668-673. LIANG J, GUO Z Y, FENG L P, et al. The influence factors of pesticides photodegradation in the environment[J]. J Agro-Environ Sci, 2007, 26(Suppl.1): 668-673. |
| [15] |
李芫慧. 胺唑草酮的水解与光解特性研究[D]. 长春: 吉林农业大学, 2015. LI Y H. The Study of amicarazone hydrolysis and photolysis characteristics[D]. Changchun: Jilin Agricultural University, 2015. |
| [16] |
殷花. 联苯肼酯的水解及光解行为研究[D]. 重庆: 西南大学, 2015. YIN H. Study on the hydrolysis and the photodegradation of bifenazate[D]. Chongqing: Southwestern University, 2015. |
| [17] |
贾娜, 施海燕, 王鸣华. 2,4-D 丁酯的水解与光解特性研究[J]. 农业环境科学学报, 2011, 30(6): 1082-1086. JIA N, SHI H Y, WANG M H. Hydrolysis and photolysis of 2,4-D butylate[J]. J Agro-Environ Sci, 2011, 30(6): 1082-1086. |
| [18] |
食品安全国家标准 食品中农药最大残留限量: GB 2763—2016[S]. 北京: 中国标准出版社, 2017. National food safety standard: maximum residue limits for pesticides in food: GB 2763—2016[S]. Beijing: Standards Press of China, 2017. |
| [19] |
吴星卫, 单正军, 薛韵涵. 2,4-D 的水解、光解及在土壤中的降解特性研究[J]. 安徽农业科学, 2011, 39(16): 9711-9713. WU X W, SHAN Z J, XUE Y H. Photolysis, hydrolysis of 2,4-dicholrophenoxyacetic acid and its degradation characteristics in soils[J]. J Anhui Agric Sci, 2011, 39(16): 9711-9713. DOI:10.3969/j.issn.0517-6611.2011.16.095 |
| [20] |
VENKATESH R, HARRISON S K. Photolytic degradation of 2,4-D on Zea mays leaves
[J]. Weed Sci, 1999, 47(3): 262-269. |
| [21] |
Pesticide Properties DataBase (PPDB). 2,4-D. Key metabolites and other known metabolites for 2,4-D[EB/OL]. (2018-08-23)[2018-11-28]. http://sitem.herts.ac.uk/aeru/ppdb/en/Reports/4.htm.
|
| [22] |
EFSA. Conclusion on the peer review of the pesticide risk assessment of the active substance 2,4-D[EB/OL]. (2017-03-21)[2018-11-29]. http://www.efsa.europa.eu/en/efsajournal/pub/3812.
|
| [23] |
JMPR. 2017 (R) report, evaluation[EB/OL]. [2018-11-29].http://www.fao.org/agriculture/crops/core-themes/theme/pests/lpe/en/.
|
| [24] |
SUNDA W, HUNTSMAN S. Effect of pH, light, and temperature on Fe-EDTA chelation and Fe hydrolysis in seawater[J]. Mar Chem, 2003, 84(1-2): 35-47. |
| [25] |
LOFTIN K A, ADAMS C D, MEYER M T, et al. Effects of ionic strength, temperature, and pH on degradation of selected antibiotics[J]. J Environ Qual, 2008, 37(2): 378-386. DOI:10.2134/jeq2007.0230 |
 2019, Vol. 21
2019, Vol. 21


