三唑酰草胺 (ipfencarbazone,图式 1) 是由日本北兴化学工业株式会社研制的一种三唑啉酮类除草剂,对于较难防除的禾本科杂草具有持效长、防效高及对水稻高度安全等优点。三唑酰草胺被植物根或茎部吸收后,可阻碍脂肪酸合成及代谢,抑制植物细胞分裂和生长,达到防除效果[1]。
农药在土壤中的降解特性是评价其对生态环境影响的重要指标之一[2]。随着药剂施用后的迁移和转化,农药在土壤中持留时间愈长,对生态环境的潜在威胁越大[3-4]。目前,三唑酰草胺的相关制剂仅在日本和韩国获准登记,用于水稻直播田防除一年生或多年生杂草,在中国则暂无相关登记资料。日本规定三唑酰草胺在糙米及鱼中的最大残留限量 (MRL) 值分别为0.05和0.04 mg/kg,韩国规定糙米中的MRL值为0.05 mg/kg。中国已有关于三唑酰草胺分析方法的研究报道[5],但尚未见有关其残留及环境行为等方面的研究。由于三唑酰草胺水溶性弱,且土壤对其吸附性强,在施用后主要分布在表层土壤中[6],因此,对三唑酰草胺在土壤中的残留转化规律进行研究十分必要。笔者采用室内模拟方法,研究了三唑酰草胺在不同类型土壤中的降解特性及影响因素,以期为其环境风险评估提供参考。

|
图式1 三唑酰草胺结构式 Scheme1 Structural formula of ipfencarbazone |
1 材料与方法 1.1 主要仪器及试剂
Agilent 1200高效液相色谱仪 (配紫外检测器,美国安捷伦公司);BSP-250生化培养箱 (上海博迅实业有限公司医疗设备厂);HWS-P智能恒温恒湿培养箱 (华德利科学器材公司);ESJ 200-4电子天平 (精确到0.000 1 g,深圳市新朗普电子科技有限公司);ZD-85气浴恒温振荡器 (江苏金坛中大仪器厂);ALPHAI-2 真空冷冻干燥机 (德国Christ公司)。
98.88%三唑酰草胺 (ipfencarbazone) 原药,由日本北兴化学工业株式会社提供;分析纯试剂:乙腈、氯化钠、无水硫酸镁及PSA吸附剂;色谱纯试剂:乙腈;水为屈臣氏蒸馏水。
1.2 供试土壤采集3 种有代表性的新鲜农田耕作层土壤:吉林黑土(采自吉林省白山市长白山)、江西红土 (采自江西省抚州市余江县) 及安徽水稻土 (采自安徽省长丰县),除去植株根系、石块等杂质,风干后物理粉碎,过2 mm筛,于4 ℃保存备用,土壤保存期不超过半年。土壤基本理化性质见表1。
|
|
表 1 供试3种土壤的基本理化性质 Table 1 Physical and chemical properties of three types of soil tested |
1.3 检测方法
色谱柱:Agilent HC-C18,4.6 mm × 250 mm,5 μm;流动相:V乙腈 : V水 = 65 : 35;检测波长220 nm;柱温40 ℃;流速1.0 mL/min;进样量20 μL;外标法定量。在此检测条件下,三唑酰草胺的保留时间为11.6 min。
1.4 样品前处理方法将土壤样品冷冻干燥后,准确称取20 g置于三角瓶中,加入10 mL蒸馏水及20 mL乙腈,振荡提取40 min;加入4~5 g氯化钠,振摇5 min,将提取液用滤纸过滤至50 mL离心管;移取2 mL滤液至预先装有100 mg无水硫酸镁及100 mg PSA的10 mL离心管中,涡旋1 min,于5 000 r/min下离心3 min;取上清液过0.22 mm有机系滤膜,待测。
1.5 标准溶液配制及标准曲线绘制准确称取0.050 6 g 三唑酰草胺标准品,以色谱纯乙腈超声溶解并定容至5 mL,配制成10 000 mg/L的标准储备液,于 –20 ℃下避光保存。试验时再用色谱纯乙腈逐级稀释,分别配成10、5、1、0.5、0.1及0.02 mg/L的三唑酰草胺标准工作溶液。外标法定量,以峰面积为纵坐标、进样质量浓度为横坐标绘制标准曲线。
1.6 添加回收试验向3种土壤空白样品中分别添加0.05、1及10 mg/kg 3个水平的三唑酰草胺标准工作溶液,每个水平重复5次,按上述方法进行样品前处理及测定,计算添加回收率和相对标准偏差 (RSD)。
1.7 三唑酰草胺在土壤中的降解试验 1.7.1 好氧及厌氧条件下土壤的预培养在25 ℃室温下,分别称取适量土壤样品于不锈钢托盘内 (好氧及厌氧条件试验各取2 kg左右),喷水润湿后混合均匀 (加水量为土壤饱和持水量的40%),置于25 ℃恒温箱中鼓风避光培养14 d (实测温度24.8~25.2 ℃)。将预培养的土壤带盘称重,培养过程中及时调节土壤内水分含量,以保持原有持水状态。水稻土的饱和持水量为23%,红土为21%,黑土为30%。
1.7.2 供试物水溶液配制取10 000 mg/L的三唑酰草胺标准储备液,用蒸馏水稀释,配成100 mg/L的水溶液,待用。
1.7.3 好氧条件下降解试验分别称取20 g土壤 (精确到0.01 g) 于250 mL棕色锥形瓶中,移取2 mL、100 mg/L的三唑酰草胺水溶液,均匀点滴于土层表面,静置。待土壤润湿后,振摇混匀,使土壤的初始含药量为10 mg/kg。加水将土壤含水量调节到饱和持水量的60%用透气硅胶塞封口,置于25 ℃恒温箱中鼓风避光培养 (实测温度24.8~25.2 ℃),分别于0、2、6 h及1、3、5、7、14、21、30、45、60、90、120 d取样,每次取2个平行样,测定土壤中三唑酰草胺的残留量。
1.7.4 厌氧条件下降解试验分别称取20 g土壤 (精确到0.01 g) 于250 mL棕色锥形瓶中,移取100 mg/L三唑酰草胺水溶液2 mL,均匀点滴于土层表面,静置。待土壤润湿后,振摇混匀,使土壤初始含药量为10 mg/kg。加水将土壤含水量调节到饱和持水量的60%,以透气硅胶塞封口,置于25 ℃恒温箱中,鼓风避光培养30 d (实测温度24.8~25.2 ℃);加入1~3 cm高水层并通入惰性气体 (氮气) 使系统处于厌氧环境,置于25 ℃、相对湿度60%的恒温恒湿培养箱中避光培养 (实测温度24.8~25.2 ℃,相对湿度58%~62%),于0、2、6 h及1、3、5、7、14、21、30、45、60、90、120 d分别取样,每次取2个平行样,测定土壤中三唑酰草胺的残留量。
1.7.5 水稻田厌氧条件下降解试验在25 ℃室温下,分别称取50 g土壤样品 (精确到0.01 g) 于250 mL棕色锥形瓶中,加水至土壤表面存有0.5~1 cm高水层并通入氮气使系统处于厌氧环境,置于25 ℃、相对湿度60%的恒温恒湿培养箱中避光培养14 d。用注射器向土层中缓慢移动注入100 mg/L的三唑酰草胺水溶液2 mL,使土壤的初始含药量为4 mg/kg,继续培养,分别于0、2、6 h及1、3、5、7、14、21、30、45、60、90、120、150 d取样,每次取2个平行样,测定土壤中三唑酰草胺的残留量。
以上试验培养过程中需及时调节锥形瓶内水分含量,以保持原有持水状态。均以添加等体积蒸馏水的土壤样品为空白对照。
1.8 数据处理三唑酰草胺在土壤中的降解可按一级动力学方程ct = c0e–kt进行拟合,降解半衰期按t1/2 = ln2/k计算。样品以基质匹配标准溶液定量,计算残留结果。
1.9 土壤中降解特性等级划分三唑酰草胺在土壤中的降解特性等级参照《化学农药环境安全评价试验准则》[7]进行划分 (表2)。
2 结果与分析 2.1 方法的线性范围、准确度及精密度
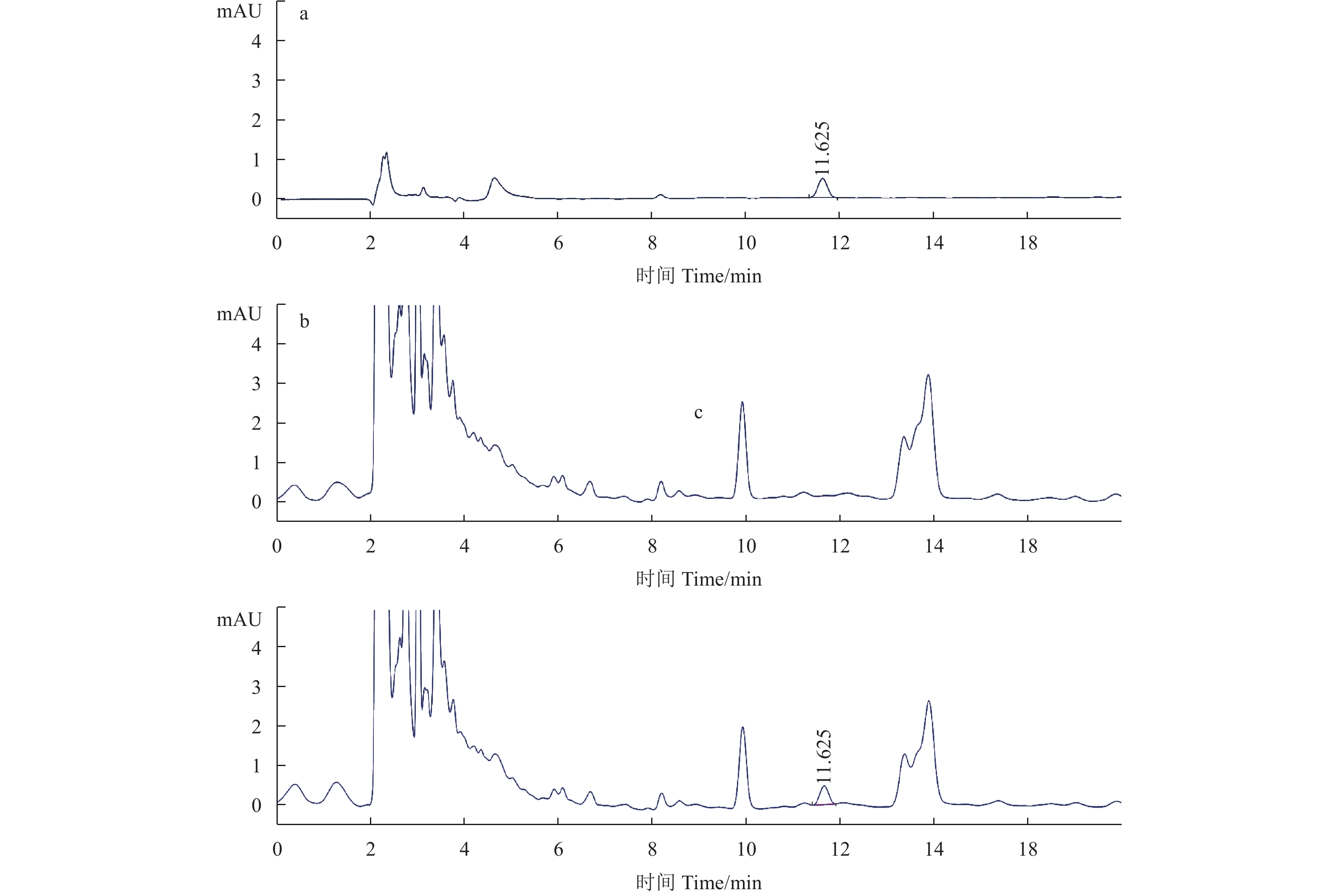
结果见表3。在0.02~10 mg/L范围内,三唑酰草胺的峰面积与对应质量浓度间呈良好线性关系,其线性方程为y = 63.826 8x – 0.172 6,R2 = 1.0。在0.05~10 mg/kg添加水平下,三唑酰草胺在土壤中的平均回收率为85%~91%,相对标准偏差为0.2%~7.6% (典型色谱图见图1)。三唑酰草胺在3种土壤中的最小检出量为1.0 ng,以3倍信噪比计算得仪器的检出限 (LOD) 为0.02 mg/kg,以10倍信噪比计算得方法的定量限 (LOQ) 为0.05 mg/kg。样品前处理及检测方法均满足残留试验准则要求[8]。
|
|
表 3 三唑酰草胺在土壤样品中的添加回收率及相对标准偏差 (n = 5) Table 3 Recoveries and RSDs of ipfencarbazone in soil (n = 5) |
|
a: 三唑酰草胺标准溶液 (0.05 mg/L); b:黑土空白; c: 黑土中添加0.05 mg/kg三唑酰草胺。 a: ipfencarbazone standard sample (0.05 mg/L); b: blank black soil; c: black soil spiked with 0.05 mg/kg of ipfencarbazone. 图 1 三唑酰草胺标准溶液及添加回收样品的典型色谱图 Fig. 1 Chromatograms of ipfencarbazone standard and spiked samples |
2.2 好氧条件下三唑酰草胺在土壤中的降解特性
好氧条件下,三唑酰草胺在土壤中的降解动态曲线符合一级动力学方程 (表4),其在黑土、红土及水稻土中的降解半衰期分别为86.5、106和91.4 d,降解速率依次为黑土 > 水稻土 > 红土;培养120 d后,三唑酰草胺在3种土壤中的降解率均小于70% ( 表5)。试验中3种供试土壤的pH值属弱酸性或近中性,随土壤有机质及黏粒含量升高,三唑酰草胺的降解速率呈增快趋势。
|
|
表 4 好氧条件下三唑酰草胺在土壤中的降解动力学参数 Table 4 Degradation kinetic parameters of ipfencarbazone in soil under aerobic conditions |
|
|
表 5 好氧条件下三唑酰草胺在土壤中的降解动态 Table 5 Degradation dynamics of ipfencarbazone in soil under aerobic conditions |
目前有关三唑酰草胺母体降解的研究报道较少,且尚未有其降解产物的登记资料。有资料表明,稻田环境中三唑酰草胺的半衰期为8.5~34.4 d[6]。在自然环境下,三唑酰草胺经化学或生物作用逐步分解,最后矿化生成二氧化碳[6]。相对于复杂的稻田自然环境,室内试验的影响因素较少。农药在土壤中的降解主要受土壤有机质含量、pH值及粒径分布等因素的影响,通常在黏粒及有机质含量较少的砂质土壤中,农药的移动性较强,而在黏粒与有机质含量高的土壤中则不易移动[9]。同时土壤中有机质含量高还能促进微生物的繁殖,进一步加速农药在土壤中的降解[10]。
2.3 厌氧条件下三唑酰草胺在土壤中的降解特性厌氧条件下,三唑酰草胺在黑土、红土及水稻土中的降解速率整体较好氧条件下有所减慢,其在3种土壤中的降解半衰期分别为106、130及127 d (表6),比好氧条件下仅延长18.4%~ 28.0%,差异不明显,且土壤类型与降解速率的关系与好氧条件下一致。在厌氧条件下培养120 d后,三唑酰草胺在3种土壤中的降解率均低于60% (表7)。土壤在保持适当湿度条件下进行好氧培养,以保持土壤中好氧微生物的生物活性,而后加入1~3 cm高的水层并通入惰性气体使其处于厌氧环境,此时土壤含水量增多、透气能力变差,且持续通入的氮气使得土层和水层表面氧气含量衰减,好氧微生物的活性减弱,三唑酰草胺的降解趋势亦随之减弱。有研究表明,避光条件下土壤中农药的降解很大程度上是微生物降解和水解共同作用的结果[11-12]。
|
|
表 6 厌氧条件下三唑酰草胺在土壤中的降解动力学参数 Table 6 Degradation kinetic parameters of ipfencarbazone in soil under anaerobic conditions |
|
|
表 7 厌氧条件下三唑酰草胺在土壤中的降解动态 Table 7 Degradation dynamics of ipfencarbazone in soil under anaerobic conditions |
2.4 三唑酰草胺在水稻田厌氧土壤中的降解特性
在室内模拟水稻田环境进行试验,三唑酰草胺的降解半衰期明显延长,其在黑土、红土和水稻土中的半衰期分别为162、219及188 d (表8),培养150 d后,三唑酰草胺在3种土壤中的降解率均低于50% (表9)。积水厌氧条件下,土壤中好氧微生物活性受到限制,影响了土壤微生物对农药的降解能力,从而减慢了三唑酰草胺的降解速率[13-14]。由于3种土壤的有机质含量、pH值及粒径等均存在差异,故在相同的积水厌氧条件下,三唑酰草胺在不同类型土壤中的降解速率亦有所不同。此时,土壤粒径对农药的吸附性能影响较大,土壤pH值对农药的水解作用也有一定的影响[15]。
|
|
表 8 水稻田厌氧条件下三唑酰草胺在土壤中的降解动力学参数 Table 8 Degradation kinetic parameters of ipfencarbazone under anaerobic conditions in paddy fields |
|
|
表 9 水稻田厌氧条件下三唑酰草胺在土壤中的降解动态 Table 9 Degradation dynamics of ipfencarbazone under anaerobic conditions in paddy fields |
3 结论
研究表明:好氧、厌氧及水稻田厌氧条件下,三唑酰草胺在3种不同类型土壤中的残留量均随时间延长而逐渐降低,半衰期在86.5~219 d之间,其降解动态符合一级动力学方程,且在3种条件下,三唑酰草胺均是在黑土中降解最快,在红土中最慢。
参考文献[7]对三唑酰草胺在土壤中的降解特性进行归类,结果表明:好氧条件下三唑酰草胺在黑土中属中等降解,在红土及水稻土中属较难降解;厌氧条件下其在黑土、红土及水稻土中均属较难降解;水稻田厌氧条件下,三唑酰草胺在黑土中属较难降解,在红土及水稻土中属难降解。整体来看,三唑酰草胺在水稻田厌氧条件下的降解速率明显慢于其他2种试验条件下。室内条件下三唑酰草胺在土壤中残存时间较长,可能与室内条件影响其降解的因素单一有关。关于其在情况较复杂的稻田自然环境中的降解特性仍需深入研究。
| [1] |
刘长令. 世界农药大全: 杀菌剂卷[M]. 北京: 化学工业出版社, 2006: 84-86. LIU C L. Pesticide in worldwide, fungicide volume[M]. Beijing: Chemical Industry Press, 2006: 84-86. |
| [2] |
朴秀英, 陶传江, 姜辉, 等. 烯酰吗啉顺反异构体在土壤中的降解动态研究[J]. 农药学学报, 2011, 13(2): 169-173. PIAO X Y, TAO C J, JIANG H, et al. Study on degradation dynamics of Z-and E-isomers of dimethomorph in soils [J]. Chin J Pest Sci, 2011, 13(2): 169-173. DOI:10.3969/j.issn.1008-7303.2011.02.12 |
| [3] |
马山山, 孔祥吉, 郭敏, 等. 代森联在几种典型土壤中的降解特性研究[J]. 中国农学通报, 2014, 30(26): 159-164. MA S S, KONG X J, GUO M, et al. Studies on the degradation characteristic of metiram in different kinds of soils[J]. Chin Agric Sci Bull, 2014, 30(26): 159-164. DOI:10.11924/j.issn.1000-6850.2013-3041 |
| [4] |
袁野, 李璇, 王娇, 等. 唑虫酰胺在土壤中的降解特性[J]. 农药, 2017, 56(2): 129-130. YUAN Y, LI X, WANG J, et al. Degradation characteristics of tolfenpyrad in soil[J]. Agrochemicals, 2017, 56(2): 129-130. |
| [5] |
孙启霞, 姜宜飞, 李友顺, 等. 三唑酰草胺 2.5% 颗粒剂的高效液相色谱分析[J]. 农药科学与管理, 2012, 33(12): 50-52. SUN Q X, JIANG Y F, LI Y S, et al. Analysis of ipfencarbazone in 2.5% GR by HPLC[J]. Pest Sci Admin, 2012, 33(12): 50-52. DOI:10.3969/j.issn.1002-5480.2012.12.020 |
| [6] |
叶萱. 水稻田除草剂三唑酰草胺[J]. 世界农药, 2016, 38(6): 54-58. YE X. Rice field herbicide ipfencarbazone[J]. World Pest, 2016, 38(6): 54-58. |
| [7] |
化学农药环境安全评价试验准则第 1 部分 土壤降解试验: GB/T 31270. 1—2014[S]. 北京: 中国标准出版社, 2014. Test guidelines on environmental safety assessment for chemical pesticides—part 1: transformation in soils: GB/T 31270.1—2014[S]. Beijing: Chinese Standards Press, 2014. |
| [8] |
农药残留试验准则: NY/T 788—2004[S]. 北京: 中国农业出版社, 2004. Guideline on pesticide residue trials: NY/T 788—2004[S]. Beijing: Chinese Agricultural Press, 2004. |
| [9] |
王俊伟, 周春江, 杨建国, 等. 农药残留在环境中的行为过程、危害及治理措施[J]. 农药科学与管理, 2018, 39(2): 30-34. WANG J W, ZHOU C J, YANG J G, et al. Behavior process, harm and treatment of pesticide residues in environment[J]. Pest Sci Admin, 2018, 39(2): 30-34. DOI:10.3969/j.issn.1002-5480.2018.02.010 |
| [10] |
宋宁慧, 单正军, 石利利, 等. 多重环境因子对氟胺磺隆在土壤中降解的影响[J]. 环境科学, 2012, 33(12): 4400-4405. SONG N H, SHAN Z J, SHI L L, et al. Effects of multiple environmental factors on triflulsulfuron-methyl degradation in soils[J]. Environ Sci, 2012, 33(12): 4400-4405. |
| [11] |
石利利, 单正军, 蔡道基. 三唑磷农药在土壤中的降解与吸附特性研究[J]. 农业环境科学学报, 2006, 25(3): 733-736. SHI L L, SHAN Z J, CAI D J. Degradation and adsorption characteristics of triazophos in soils[J]. J Agro-Environ Sci, 2006, 25(3): 733-736. DOI:10.3321/j.issn:1672-2043.2006.03.037 |
| [12] |
孔德洋, 吴文铸, 许静, 等. 毒草胺在环境中的降解特性研究[J]. 生态环境学报, 2012, 21(7): 1325-1328. KONG D Y, WU W Z, XU J, et al. Photolysis, hydrolysis of propachlor and its degradation in soils[J]. Ecol Environ Sci, 2012, 21(7): 1325-1328. |
| [13] |
KUROLA J, SALKINOJA-SALONEN M. Potential for biodegradation of anthropogenic organic compounds at low temperature in boreal soils[J]. Soil Biol Biochem, 2007, 39(5): 1206-1212. DOI:10.1016/j.soilbio.2006.11.005 |
| [14] |
许静, 王娜, 孔德洋, 等. 磺胺类药物在土壤中的降解性[J]. 环境化学, 2013, 32(12): 2349-2356. XU J, WANG N, KONG D Y, et al. Degradation of sulfonamides in soils[J]. Environ Chem, 2013, 32(12): 2349-2356. DOI:10.7524/j.issn.0254-6108.2013.12.019 |
| [15] |
孔德洋, 葛峰, 许静, 等. 3 种烟碱类杀虫剂在土壤中的降解吸附特性及对地下水的影响[J]. 农业环境科学学报, 2011, 30(11): 2237-2241. KONG D Y, GE F, XU J. The degradation and absorption of neonicotinoid pesticides in soils and its effect to groundwater[J]. J Agro-Environ Sci, 2011, 30(11): 2237-2241. |
 2019, Vol. 21
2019, Vol. 21


