2. 山东临沂烟草有限公司,山东 临沂 276400
2. Shandong Linyi Tobacco Company Ltd., Linyi 276400, Shandong Province, China
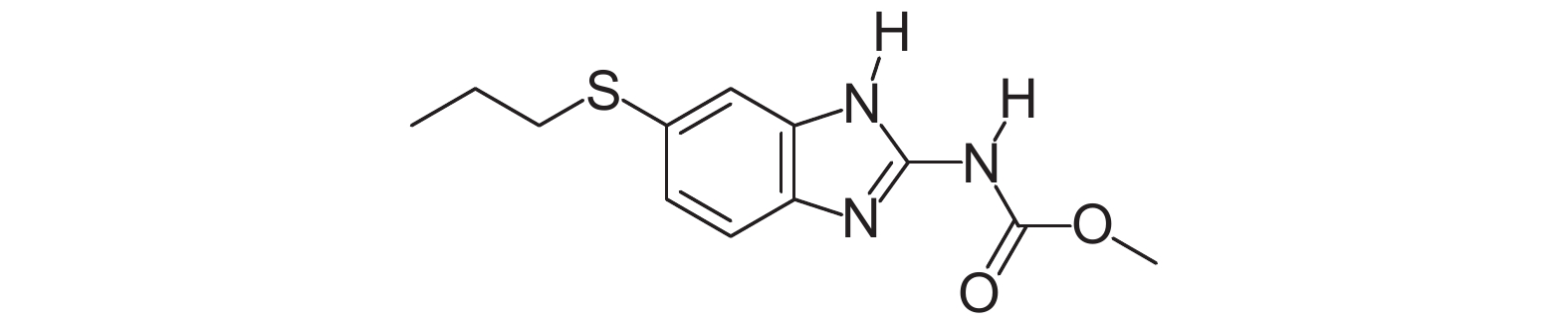
内吸性丙硫唑类为新一代农用杀菌剂,兼具兽用杀虫活性和农作物杀菌活性,通过诱导作物自身产生抗体,增强作物抗病能力,具有预防保护、内吸治疗和渗透传导作用[1]。其中丙硫咪唑 (结构式见图式1) 具有广谱的杀菌作用,对水稻、小麦和黄瓜等多种作物的白粉病等多种病害均具有良好的防治效果[1-3]。
|
图式1 丙硫咪唑化学结构式 Scheme1 The structural formula of albendazole |
烟草在生长过程中主要通过喷施化学农药防治常见病虫害,但农药的大量使用,为烟叶中农药残留管控带来了挑战。由于烟草内含物质丰富,对烟草中农药残留的检测也提出了更高的要求,需要开发高效、科学的农药残留前处理方法,去除和分离烟草自身的多种化学成分对目标物的干扰。QuEChERS (Quick, Easy, Cheap, Effective, Rugged and Safe) 方法具有快速、高效、简便且成本低的优点,已成为欧洲标准委员会认可的快速检测方法[4]。QuEChERS与HPLC-MS/MS技术联用,已被广泛运用于水果、蔬菜等基质中农药残留的检测分析,近年来也在烟草、茶叶等复杂基质中得到了应用[5-6],但用该方法开展烟草中丙硫咪唑农药残留检测的研究尚未见报道。目前,有关丙硫咪唑残留的检测方法主要有气相色谱-串联质谱、液相色谱-串联质谱和高效液相色谱-串联质谱等[7-10],但其在作物上的消解和残留特征尚不明确。本研究利用QuEChERS前处理方法,结合HPLC-MS/MS建立了烟草中丙硫咪唑残留的分析方法,验证了方法的准确度、精密度和灵敏度。通过田间施用15%丙硫唑•戊唑醇悬浮剂,研究了烟叶中丙硫咪唑的消解动态和最终残留水平,以此结果提出丙硫咪唑在烟草中的残留限量,旨在为该农药的合理使用和残留监管提供基础数据。
1 材料与方法 1.1 仪器、药剂与试剂高效液相色谱-串联三重四极杆质谱仪 (HPLC-MS/MS)(THERMO-FISHER TSQ QUANTUM ULTRA,美国Thermo公司),涡旋混匀器 (Crystal HYQ-3110,美国Crystal公司),高速离心机 (Sigma 3K15,美国Sigma公司),千分之一电子天平 (SHIMADZU-UW 420 H,瑞士赛多利斯公司),万分之一电子天平 (ER-182 A,瑞士赛多利斯公司)。
丙硫咪唑 (albendazole) 标准品 (纯度99.0%,贵州道元科技有限公司);15%丙硫唑•戊唑醇悬浮剂 (丙硫咪唑有效成分含量5%,戊唑醇有效成分含量为10%;贵州道元科技有限公司);甲酸和乙腈 [分析纯,国药集团 (上海) 化学试剂有限公司]。
1.2 样品前处理方法称取适量样品 (鲜烟叶5 g,干烟叶2 g) 于50 mL塑料离心管中,加入20 mL V (乙腈) :V (0.1%甲酸水溶液) = 3 : 1混合溶液,涡旋提取2 min,于4 000 r/min下离心10 min。移取1 mL上清液至盛有30 mg C18的1.5 mL离心管中,涡旋2 min,于10 000 r/min 下离心2 min。取上清液过0.22 μm微孔滤膜,待HPLC-MS/MS检测。
1.3 HPLC-MS/MS检测条件色谱条件:以乙腈和0.1%甲酸水溶液为流动相,对ThermoHypersil GOLD C18色谱柱 (2.1 mm × 100 mm, 3.0 µm) 进行线性梯度洗脱。梯度洗脱程序:乙腈初始体积比10%,0.5 min内调整为90%,恒定6 min,2 min内调整为10%,保持2 min。流速0.25 mL/min;柱温25 ℃;进样量10 μL。
质谱条件:电喷雾正离子 (ESI+) 模式;喷雾电压3 000 V;毛细管温度300 ℃;鞘气压力115.2 kPa;辅助气压力46.2 kPa;多重反应监测 (MRM) 模式。其他质谱条件见表1。
|
|
表 1 丙硫咪唑HPLC-MS/MS检测条件 Table 1 HPLC-MS/MS parameters of albendazole |
1.4 田间试验
田间试验分别于2015年和2016年在山东省青岛市及四川省西昌市试验基地进行。参照《农药登记残留田间试验标准操作规程》[11]和《农药残留试验准则》[12],设计农药消解动态试验和最终残留试验。供试药剂为15%丙硫唑•戊唑醇悬浮剂 (推荐剂量为有效成分45~90 g/hm2)。
1.4.1 消解动态试验按有效成分135 g/hm2的剂量施药,于烟草旺长后期整株均匀喷雾,分别在施药后1 h及1、3、5、7、14、21、28、35、42 d采集烟叶,每处理小区采样不少于50片,切碎混匀,留样300 g,于 –20 ℃保存。
1.4.2 最终残留试验于烟草现蕾期-成熟期,分别按有效成分90和135 g/hm2 的剂量于叶面喷雾3次,施药间隔期7 d。分别于距最后1次施药后7、14和21 d采集成熟烟叶,采用三段式工艺烘烤,烤后烟叶去除主脉,粉碎,过2 mm筛,缩分留样200 g,于 –20 ℃保存。小区面积30 m2,重复3次,喷雾量900 L/hm2,设空白对照,处理间设保护带。所有操作符合良好农业操作规程要求[12]。
2 结果与分析 2.1 仪器条件和样品前处理方法的优化 2.1.1 仪器条件的优化用乙腈配制1.0 mg/L的丙硫咪唑标准溶液,分别采用电喷雾正离子 (ESI+) 模式和负离子 (ESI–) 模式进行母离子扫描。结果表明:当使用ESI+ 模式扫描时,丙硫咪唑的分子离子峰 [M+H] 响应值较高,故采用ESI+ 模式,m/z 266.12为丙硫咪唑的母离子。进一步对子离子、碎裂电压和碰撞能量等参数进行优化,选出响应值最高的3组离子对、最优锥孔电压和碰撞能量,将响应值最大的1组离子对设为定量离子对,另2组离子对设为定性离子对,确定最终质谱条件见表1。
采用乙腈-水作为流动相,对目标物进行梯度洗脱,获得合适的保留时间。在水相中添加适量的甲酸,不仅可以改善色谱峰形,还可提高农药的离子化效率,从而提高检测的灵敏度[13]。经过试验验证,在水相中加入体积分数为0.1%的甲酸检测效果最佳。
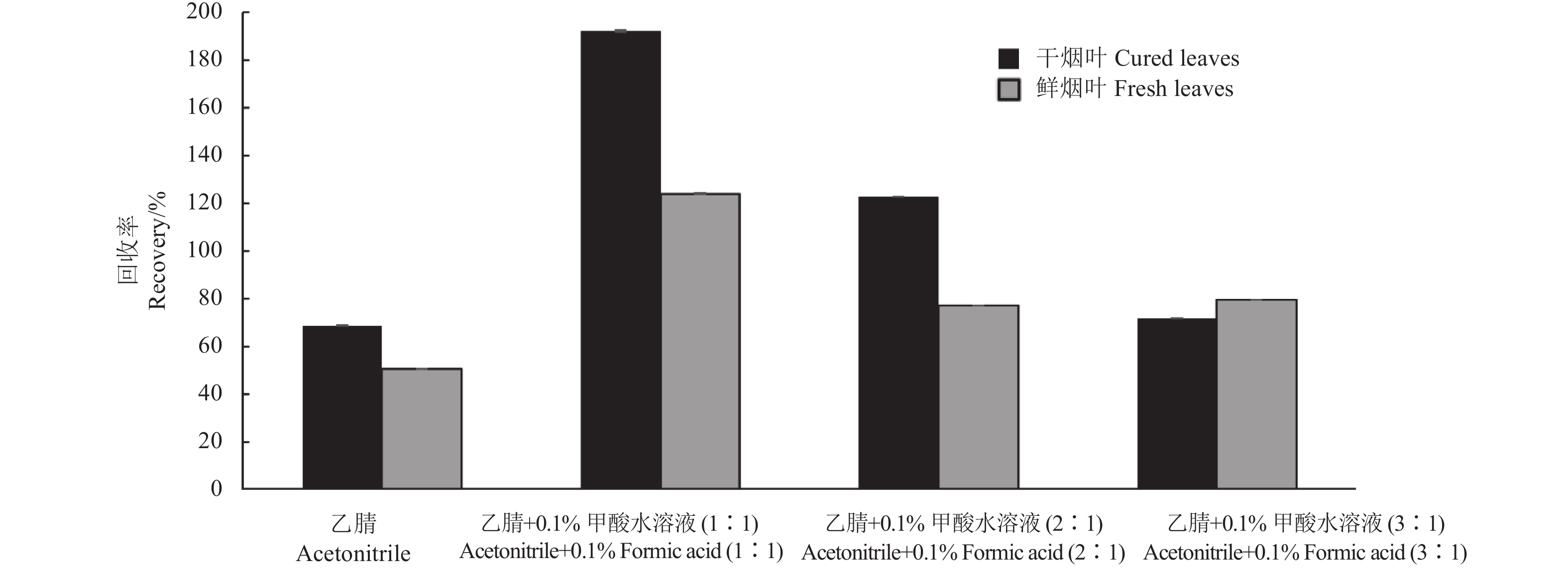
2.1.2 样品前处理方法的优化根据《农药残留试验准则》要求[12],结合目标化合物的性质,比较了V (乙腈) ∶V (0.1%甲酸水溶液) = 1 : 0、3 : 1、2 : 1和1 : 1对目标农药的提取效率。结果 (图1) 表明:当采用V (乙腈) ∶V (0.1%甲酸水溶液) = 3 : 1混合溶液提取时,目标农药回收率在70%~110%范围内,符合农药残留检测要求[12],因此采用该混合溶液作为最佳提取溶液。
|
图 1 烟叶中丙硫咪唑在不同提取条件下的回收率 Fig. 1 Recovery rate of albendazole using different extraction conditions |
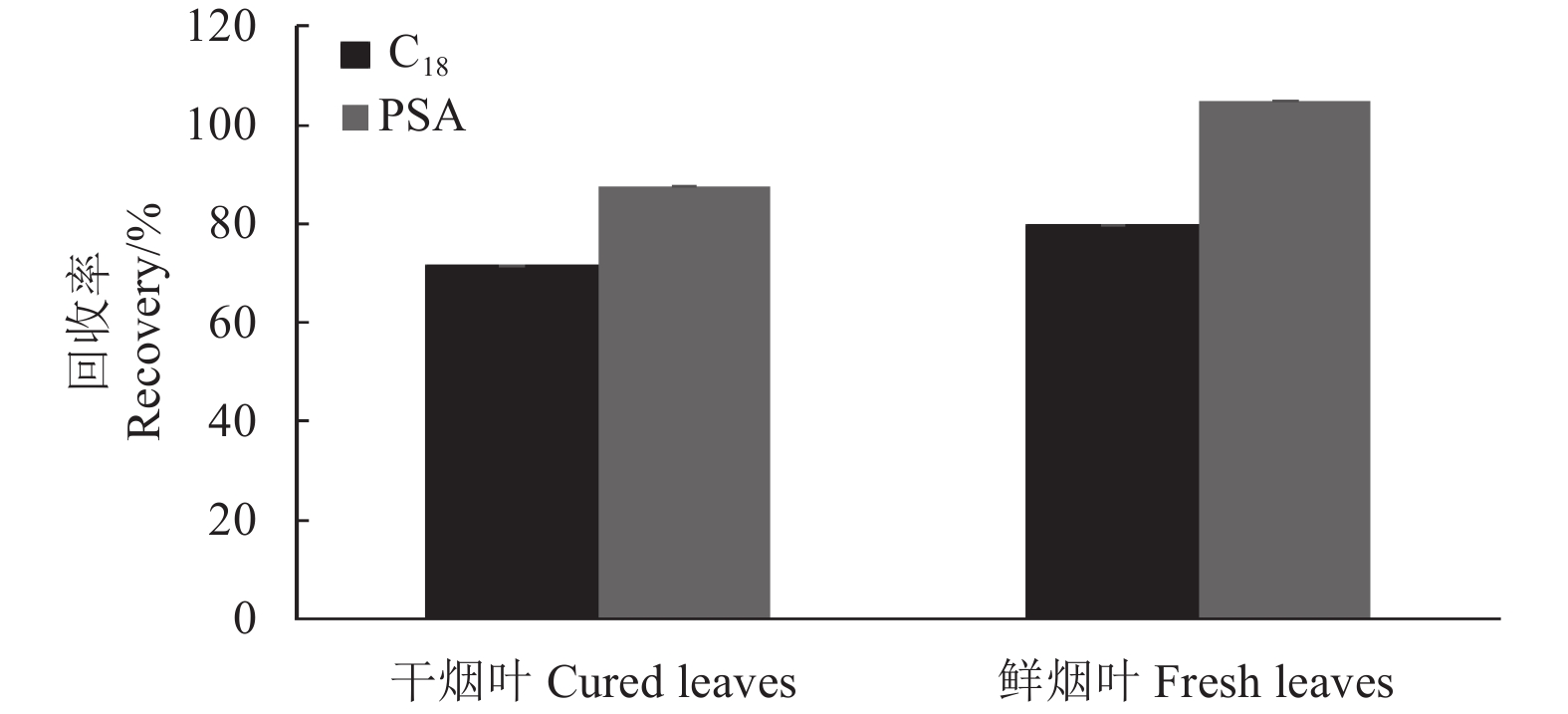
分别以30 mg PSA和C18为分散固相萃取的吸附剂,考察了不同吸附剂对上清液的净化效果。结果 (图2) 显示:采用2种吸附剂,目标农药回收率均符合农药残留检测要求,但使用C18为吸附剂时,净化后上清液颜色较浅,且C18成本比较低,从色素干扰和成本角度考虑,选用C18作为吸附剂。
|
图 2 烟叶中丙硫咪唑在不同净化条件下的回收率 Fig. 2 Recovery rate of albendazole using different purification conditions |
2.1.3 方法性能指标 2.1.3.1 方法的线性及检出限
称取丙硫咪唑标准品 (精确至0.01 mg),用乙腈溶解并定容,配制成100 mg/L的标准储备液,采用基质空白溶液将该储备液进行逐级稀释,配制所需浓度的基质匹配标准工作液。
在0.001~1 mg/L范围内,丙硫咪唑在鲜烟叶和干烟叶中的质量浓度与色谱峰面积间呈良好线性关系,线性方程为:y = 174 990 586 x + 1 188 252,决定系数 (R2) 为0.998 0 (鲜烟叶);y = 100 464 975 x + 1 153 403,R2为0.999 2 (干烟叶)。以3倍信噪比产生的信号所对应的农药量作为方法的检出限 (LOD),丙硫咪唑的LOD值为0.005 ng;以检测出待测物在样品中的最低含量作为方法的定量限 (LOQ),干烟叶、鲜烟叶中的LOQ分别为0.01和0.02 mg/kg。
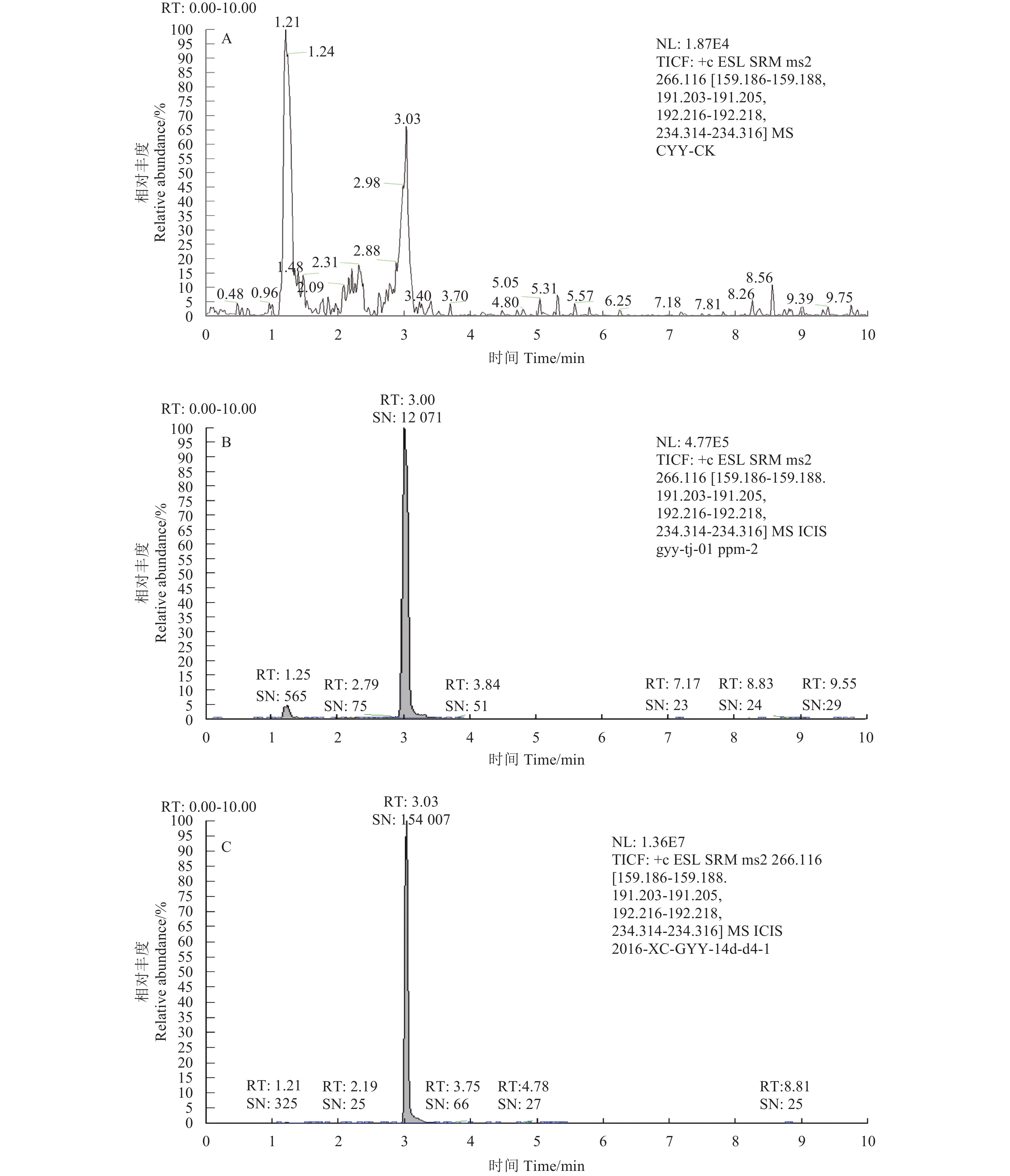
2.1.3.2 方法的准确度和精密度准确称取5 g鲜烟叶或2 g干烟叶空白样品进行添加回收试验,分别添加3个水平的丙硫咪唑标准溶液,静置30 min 后按1.2节的条件处理样品。每个添加水平重复5 次,计算回收率和相对标准偏差。结果 (表2) 表明:丙硫咪唑在干烟叶中添加回收率和相对标准偏差 (RSD) 分别为85%~104%和2.0%~8.1%,在鲜烟叶中的添加回收率和RSD分别为94%~99%和1.2%~2.7%,满足农药残留分析的要求[12]。典型色谱图见图3。
|
|
表 2 丙硫咪唑在烟叶中的添加回收率和相对标准偏差 (n = 5) Table 2 Recoveries and RSDs of albendazole in fresh tobacco leaves and cured tobacco leaves (n = 5) |
|
A. 干烟叶空白样品;B. 干烟叶添加样品 (0.1 mg/kg);C. 干烟叶最终残留样品 (四川, 14 d)。 A. Blank cured tobacco leaves; B. Cured tobacco leaves spiked at the concentration of 0.1 mg/kg; C. Real cured tobacco leaves (Sichuan, 14 d). 图 3 目标农药典型色谱图 Fig. 3 Typical HPLC-MS/MS chromatograms of albendazole in tobacco leaves |
2.2 丙硫咪唑在烟叶中的消解动态和最终残留 2.2.1 丙硫咪唑在鲜烟叶中的消解动态
丙硫咪唑消解动力学方程见表3。山东试验点,丙硫咪唑在烟叶中的原始沉积量为0.67~2.40 mg/kg,5 d时消解率为11.6%~55.7%,21 d时消解率为49.4%~73.3%,理论半衰期为5.4~8.6 d。四川试验点,丙硫咪唑原始沉积量为0.57~1.34 mg/kg,3 d时消解率接近50%,42 d时消解率为86.2%~96.7%,理论半衰期为9.1~16.1 d。不同试验地点和试验年份,消解速率有一定差异。
|
|
表 3 丙硫咪唑在鲜烟叶中的消解动态 Table 3 Dissipation dynamic of albendazole in fresh tobacco leaves |
2.2.2 丙硫咪唑在干烟叶中的最终残留量
山东、四川2年2地试验结果 (表4) 表明:总体上看,随施药剂量增大和施药次数增多,残留量呈升高趋势,随采收间隔期的延长,残留量降低,但也出现了2015年山东点14 和21 d高剂量处理比低剂量处理的农药残留量反而略低的情况,经分析和比较2个试验点的气象资料,发现2015年山东试验点在施药后遇到降雨等天气情况,可能是雨水对烟叶表面农药冲刷作用的干扰,影响了残留农药在不同处理叶片中的分布,加上取样均匀性的差异,导致烟叶中农药残留出现了无规律性波动。
|
|
表 4 丙硫咪唑在干烟叶中的最终残留量 Table 4 The terminal residue of albendazole in cured tobacco leaves |
3 讨论
丙硫咪唑早期作为一种新型的高效、广谱和低毒的苯咪唑类抗蠕虫药,因其在预防保护、内吸治疗、渗透传导等方面的独特功效,近几年开始应用于植物病害防治[14-15]。在动物源产品中进行残留检测时,多采用乙酸乙酯、乙腈的酸溶液等有机溶剂进行反复提取,辅以固相萃取进行净化,操作程序繁琐,有机溶剂消耗量大,试验成本较高,废弃溶剂处理环保风险大;另外,文献报道的检测方法大多为HPLC检测,为保证方法的灵敏度,需要氮吹、旋转蒸发等步骤进行浓缩,试验效率低[16]。本研究采用QuEChERS前处理与高灵敏度和选择性的HPLC-MS/MS联用,不仅能够实现烟草中丙硫咪唑的快速灵敏检测,而且大大减少了有机溶剂的消耗,保证了方法的检测灵敏度。
半衰期是判定农药降解速率的关键指标。本研究中,2016年,丙硫咪唑在山东和四川2地的消解速率接近,半衰期分别为8.6和9.1 d,2015年,四川鲜烟叶中的消解半衰期为16.1 d,明显高于山东的5.4 d。通过对比气象资料数据,发现不同的光照度及降雨量都会影响烟叶中的农药残留。此外,不同试验地点和试验年度也是影响烟叶中农药残留降解速率的重要因素。
最终残留数据显示,按照推荐剂量和1.5倍推荐剂量施药后,丙硫咪唑在烟叶中的最终残留量在0.23~3.00 mg/kg之间。烟叶中最终残留水平与施药剂量、采收间隔期等有关,随着安全间隔期延长,农药残留量显著降低。目前,国际烟草合作研究中心 (CORESTA) 的指导性残留限量 (guideline residue limit, GRL) 标准中,规定了多菌灵和戊菌唑等苯丙咪唑类农药的GRL值为2 mg/kg[17],暂未制定丙硫咪唑在烟叶中的GRL值。丙硫咪唑与这2种农药性质类似,防治对象相同,按照比例推算法[18],残留限量可同等考虑。以此为标准,按照推荐剂量和1.5倍推荐高剂量用药,施药后7 和14 d烟叶中最大残留值 (HR) 高于GRL值 (2 mg/kg),施药21 d后则均未超过2 mg/kg的残留限量。另外,干烟叶收获后,还需要经过2~3年的储存醇化过程,在此过程中,农药残留还会进一步降解[19]。在燃吸过程中,农药残留迁移率也较低[4]。因此在合理使用条件下,农药残留风险可控。
4 结论本研究建立了QuEChERS前处理与HPLC-MS/MS仪器手段相结合,检测烟草中丙硫咪唑残留的方法,该方法具有快速、准确和灵敏的特点,适用于烟草中丙硫咪唑残留的检测。丙硫咪唑在烟草上消解较快,半衰期为5.4~16.1 d;在GAP条件下,末次施药后21 d,丙硫咪唑在干烟叶中的残留量低于多菌灵等苯丙咪唑类杀菌剂2 mg/kg的GRL限量标准。
| [1] |
李靖, 夏丽娟, 彭成林, 等. 50% 丙硫菌唑•戊唑醇悬浮剂防治黄瓜白粉病效果研究[J]. 四川农业科技, 2017(5): 28-29. LI J, XIA L J, PENG C L, et al. Study on the effect of 50% prothioconazole•tebuconazole suspension in controlling cucumber powdery mildew[J]. Sichuan Agric Sci Technol, 2017(5): 28-29. DOI:10.3969/j.issn.1004-1028.2017.05.012 |
| [2] |
黄志. 10% 丙硫唑悬浮剂防治水稻穗颈瘟田间药效示范试验[J]. 现代农业科技, 2018(5): 98. HUANG Z. A demonstration experiment on the efficacy of 10% albendazole suspension in the control of rice panicles in the field[J]. Mod Agric Sci Technol, 2018(5): 98. DOI:10.3969/j.issn.1007-5739.2018.05.061 |
| [3] |
毛奇, 闵红. 15% 丙硫唑•戊唑醇悬浮剂防治小麦赤霉病试验研究[J]. 河南农业, 2018(31): 37. MAO Q, MIN H. Experimental study on the control of wheat scab by 15% albendazole•tebuconazole suspending agent[J]. Henan Agric, 2018(31): 37. |
| [4] |
ANASTASSIADES M, LEHOTAY S J, ŠTAJNBAHER D, et al. Fast and easy multiresidue method employing acetonitrile extraction/partitioning and " dispersive solid-phase extraction” for the determination of pesticide residues in produce[J]. J AOAC Int, 2003, 86(2): 412-431. |
| [5] |
隋程程, 尤祥伟, 李义强, 等. QuEChERS 与高效液相色谱-串联质谱联用快速检测动物源产品中苯并烯氟菌唑残留[J]. 农药学学报, 2017, 19(5): 659-664. SUI C C, YOU X W, LI Y Q, et al. Rapid analysis of benzovindiflupyr in animal-origin food using QuEChERS coupled with high performance liquid chromatography-tandem mass spectrometry[J]. Chin J Pestic Sci, 2017, 19(5): 659-664. |
| [6] |
陈磊, 上官良敏, 付凤富. QuEChERS 预处理结合 HPLC-MS/MS 同时检测茶叶中 7 种农药残留[J]. 中国科学: 化学, 2016, 46(3): 302-308. CHEN L, SHANGGUAN L M, FU F F. Simultaneous determination of seven carbamates, neonicotinoids and diafenthiuron pesticide residues in tea by QuEChERS-HPLC-MS/MS[J]. Chin Sci: Chem, 2016, 46(3): 302-308. |
| [7] |
王纪晶, 苗虹. 食品中苯并咪唑类农药残留检测方法研究进展[J]. 食品安全质量检测学报, 2013, 4(3): 636-644. WANG J J, MIAO H. Research progress on detection of benzimidazole fungicides in foods[J]. J Food Saf Qual, 2013, 4(3): 636-644. |
| [8] |
李俊, 蔡滔, 杜楠, 等. QuEChERS-气相色谱-串联质谱法测定茶青中28种农药残留[J]. 农药学学报, 2017, 19(3): 366-373. LI J, CAI T, DU N, et al. Determination of 28 pesticide residues in fresh tea leaves using QuEChERS-gas chromatography-tandem mass spectrometry[J]. Chin J Pestic Sci, 2017, 19(3): 366-373. |
| [9] |
周杨全, 徐金丽, 徐光军, 等. 液相色谱-串联质谱法检测吲唑磺菌胺在烟叶中的残留及消解动态[J]. 农药学学报, 2015, 17(5): 585-589. ZHOU Y Q, XU J L, XU G J, et al. Residue and dissipation of amisulbrom in tobacco leaves by liquid chromatography-tandem mass spectrometry[J]. Chin J Pestic Sci, 2015, 17(5): 585-589. DOI:10.3969/j.issn.1008-7303.2015.05.12 |
| [10] |
烟草及烟草制品 多种农药残留量的测定 第 1 部分: 高效液相色谱-串联质谱法: YC/T405. 1—2011[S]. 北京: 中国标准出版社, 2011. Tobacco and tobacco products-determination of multi-pesticide residues, part 1: high performance liquid chromatography-tandem mass spectrometry method: YC/T405. 1—2011[S]. Beijing: Standards Press of China, 2011. |
| [11] |
王运浩. 农药登记残留田间试验标准操作规程[M]. 北京: 中国标准出版社, 2007. WANG Y H. Standard operating procedures on pesticide registration residue field[M]. Beijing: Standards Press of China, 2007. |
| [12] |
农药残留试验准则: NY/T 788—2004[S]. 北京: 中国农业出版社, 2004. Guideline on pesticide residue trials: NY/T 788—2004[S]. Beijing: China Agricultural Press, 2004. |
| [13] |
李娜, 张玉婷, 李辉, 等. 超高效液相色谱-串联质谱法测定 6 种中药材中110种农药残留[J]. 农药学学报, 2012, 14(6): 619-628. LI N, ZHANG Y T, LI H, et al. Determination of 110 pesticide residues in six Chinese herbal medicines by ultra performance liquid chromatography-tandem mass spectrometry[J]. J Pestic Sci, 2012, 14(6): 619-628. DOI:10.3969/j.issn.1008-7303.2012.06.06 |
| [14] |
吴宁鹏, 彭丽, 孟蕾, 等. 高效液相色谱-荧光法测定牛羊组织中阿苯达唑及其代谢物的残留量[J]. 中国兽药杂志, 2017, 51(2): 35-39. WU N P, PENG L, MENG L, et al. Determination of albendazole and its main metabolites residues in cattle and ovine tissues by HPLC-FLD[J]. Chinese Journal of Veterinary Drug, 2017, 51(2): 35-39. |
| [15] |
郑爱华,黄金占,陈祖国.合成阿苯达唑的研究进展[J].浙江化工, 2018, 49(12): 1-5. ZHENG A H, HUANG J Z, CHEN Z G. Research progress in the synthesis of albendazole[J].Zhejiang Chemical Industry, 2018, 49(12): 1-5. |
| [16] |
李慧萍, 毕文岩, 郭恒, 等. 牛肉中阿苯达唑及其代谢产物残留的检测[J]. 中国奶牛, 2011(8): 62-64. LI H P, BI W Y, GUO H, et al. The determination of albendazole and its main metabolites residues in bovine skeletal muscle[J]. China Dairy Cattle, 2011(8): 62-64. |
| [17] |
CORESTA guidance No.1-2016: The concept and implementation of CPA guidance residue level[DB/OL]. (2016-07). http://www.coresta.org/Guides/Guide-No01-GRLs(4th-Issue-July2016).pdf.
|
| [18] |
徐军, 简秋, 董丰收, 等. 比例推算法在国际食品法典农药最大残留限量评估中的应用[J]. 农药学学报, 2014, 16(2): 115-118. XU J, JIAN Q, DONG F S, et al. Development on the use of proportionality concept to estimate codex maximum residue limits for pesticides[J]. Chin J Pestic Sci, 2014, 16(2): 115-118. DOI:10.3969/j.issn.1008-7303.2014.02.01 |
| [19] |
王津军, 文国松, 丁金玲, 等. 烟草农药残留研究进展及降低烟叶农药残留的探讨[J]. 云南农业大学学报, 2006, 21(3): 329-332. WANG J J, WEN G S, DING J L, et al. The research progress of the residues of pesticides of tobacco and the discussion of reduce the residues of pesticides of tobacco leaf[J]. J Yunnan Agric Univ, 2006, 21(3): 329-332. DOI:10.3969/j.issn.1004-390X.2006.03.013 |
 2019, Vol. 21
2019, Vol. 21


