随着人们对食品安全意识的提高,大米中农药残留检测越来越引起社会的关注。目前大米中农药残留检测方法有气相色谱法[1-2] (GC)、高效液相色谱法[3-5] (HPLC)、气相色谱-质谱法[6-8] (GC-MS),气相色谱-串联质谱法[9] (GC-MS/MS) 以及液相色谱-串联质谱法[10-18] (LC-MS/MS)。其中,GC和HPLC一般灵敏度较低,且不适用于难挥发和无紫外吸收化合物的检测。随着检测技术的发展,农药多残留检测技术逐渐以色谱-质谱联用技术为主导,但由于农药种类繁多,极性差异显著,有些极性较强的农药不适合采用气-质联用检测。而液-质联用技术不仅弥补了单一技术的不足,还可对强极性农药进行检测,最后通过多反应离子监测模式进行准确的分析和定量。与之相适应的样品净化技术也快速发展,凝胶色谱 (GPC)、QuEChERS方法、固相萃取 (SPE) 在检测领域得到广泛应用[10-18]。中国国家标准[10]中采用了凝胶渗透色谱净化经液-质联用技术检测粮谷中的486种农药;江泽君等[16]、李增梅等[17]和段婷婷等[18]均采用液-质联用技术检测了稻米中单一品种农药的残留。而针对上海市近4年重点推荐的农药品种 (粮油) 名录中水稻田常用的甲氨基阿维菌素苯甲酸盐、茚虫威等15种农药在大米中多残留的同时检测尚未见报道。鉴于此,本研究针对这15种常用农药,优化质谱参数和色谱条件,考察提取溶剂类型、提取方法、基质效应以及5种不同净化方法对其回收率的影响,拟建立一种大米中15种农药超高效液相色谱-串联质谱同时检测的方法,以期为大米安全食用提供检测技术保障。
1 材料与方法 1.1 仪器设备与药剂Agilent 6460 三重四极杆液相色谱-质谱联用仪 (美国Aglient公司);IKA T25匀浆机 (德国IKA公司);TYXH-II旋涡混合器 (上海比朗仪器有限公司);TDL-5-A离心机 (上海安亭科学仪器厂);Milli-Q Advantage A10 (美国Millipore公司)。
15种农药标准品:吡蚜酮 (pymetrozine)(纯度99%,上海市农药研究所);呋虫胺 (dinotefuran)、烯啶虫胺 (nitenpyram)、吡虫啉 (imidacloprid)、噻虫胺 (clothianidin)、三环唑 (tricyclazole)、氯虫苯甲酰胺 (chlorantraniliprole)、嘧菌酯 (azoxystrobin)、噻呋酰胺 (thifluzamide)、戊唑醇 (tebuconazole)、甲氨基阿维菌素苯甲酸盐 (emamectin benzoate)、茚虫威 (indoxacarb) 和噻嗪酮 (buprofezin)(纯度均为98%,上海市农药研究所);噻虫嗪 (thiamethoxam)(纯度98.6%,上海市农药研究所);多杀霉素 (spinosad A/D)(纯度94.8%,德国Dr. Ehrenstorfer公司)。C18(博纳艾杰尔公司);N-丙基乙二胺 (PSA)(美国Aglient公司);硫酸镁 (德国CNW科技公司);NH2净化柱、Florisil净化柱、PSA净化柱及C18净化柱 (美国Aglient公司);乙腈、甲醇 (色谱纯,霍尼韦尔公司)、氯化钠 (分析纯)。
1.2 检测条件色谱条件:Poroshell 120 EC-C18色谱柱 (3.0 mm × 100 mm,2.7 μm);柱温30 ℃;进样体积2.0 μL;流速0.4 mL/ min。流动相A相为体积分数为0.1%甲酸水溶液,B相为甲醇;梯度洗脱程序:0~6 min,10%~70%B;6~9 min,70%~85%B;9~11 min,85%~95%B;11~13 min,95%B。后运行时间2 min。
质谱条件:电喷雾离子源正离子扫描 (ESI+);多反应监测模式 (MRM);毛细管电压4 000 V;雾化气压力275.6 kPa;碰撞气为氮气;干燥气温度300 ℃;鞘气温度350 ℃;鞘气流速12 L/min;其他质谱参数见表1。
|
|
表 1 15种农药质谱采集参数 Table 1 Mass spectrum acquisition parameters of 15 pesticides |
1.3 样品提取及净化 1.3.1 提取
称取粉碎后的大米样品10 g于100 mL离心管中,加入20 mL混合溶剂 [V (乙腈) : V (丙酮) : V (水) = 16 : 2 : 2],于14 000 r/min下提取1 min,加入2~3 g氯化钠,涡旋1 min,于4 000 r /min下离心5 min,待净化。
1.3.2 净化取2 mL待净化的样品提取液置于装有100 mg C18、100 mg PSA和300 mg 硫酸镁的15 mL离心管中,涡旋1 min,于4 000 r/min下离心5min,取上清液过0.22 μm有机系滤膜,待测。高浓度添加需稀释后再检测。
1.4 标准溶液配制与标准曲线绘制准确称取15种农药各10 mg (精确至0.01 mg),用甲醇溶解并定容至10 mL,配成质量浓度为1 000 mg/L的标准母液;取适量标准母液用甲醇稀释成0.005、0.01、0.05、0.1、0.5和1 mg/L的系列质量浓度的标准溶液,再用空白样品溶液稀释,配成系列同溶剂标准样品浓度的基质标准溶液,按1.2节的条件测定。分别以质量浓度为横坐标,峰面积为纵坐标绘制标准曲线。
1.5 添加回收试验选用大米空白样品,通过添加回收试验考察方法的准确度和精密度。添加水平为0.01、0.1、1和4 mg/kg,每个水平重复5次,计算添加回收率及相对标准偏差。
1.6 实际样品检测从上海浦东、奉贤、崇明和金山区县合作社随机购买10个大米品种的20个批次样品,按本研究建立的方法,对15种目标农药进行检测,评价方法的实用性和15种农药的残留水平。
2 结果与讨论 2.1 色谱与质谱条件优化本试验采用正离子扫描,单针自动进样分析15种目标农药标准溶液的质谱条件,根据化合物的响应,进入一级质谱后,可产生稳定的[M+H]+离子,以准分子离子为母离子,在SIM模式下,再进行二级质谱扫描,对Fragmentor (碎裂电压) 进行优化;在Product ion(子离子)模式下,对CE (碰撞能量) 进行优化,找到两个响应信号稳定的子离子作为定性子离子,其中响应信号较强的子离子作为定量子离子,最终确定优化后15种农药在多反应监测 (MRM) 模式下的质谱采集参数见表1。
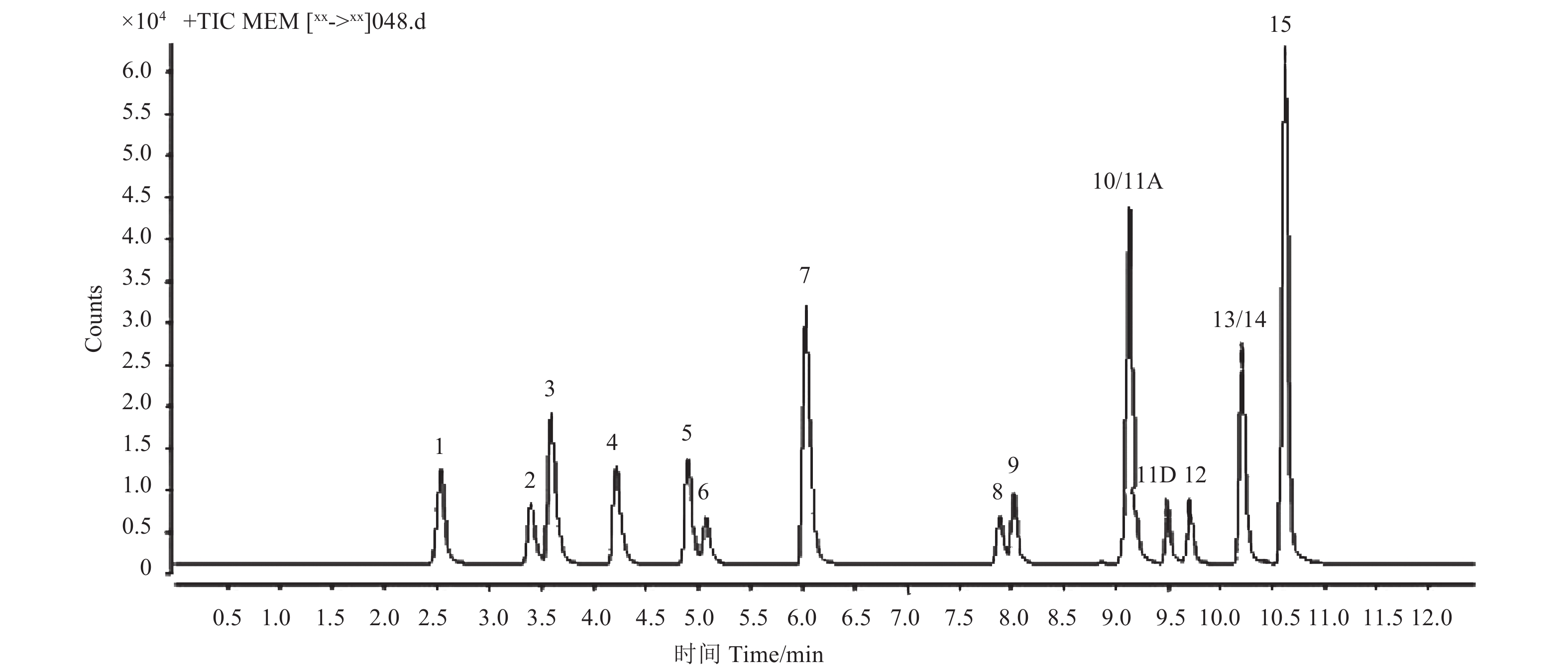
参考李文明等的方法[15],分别考察了0.1%甲酸-水/甲醇、0.1%甲酸-水/乙腈两种体系下梯度洗脱 (见1.2节的色谱条件) 对15种目标农药分离效果和灵敏度的影响。结果显示:两种条件下15种农药的响应强度差异不显著,但乙腈体系下吡蚜酮会有杂质峰干扰 (图1B),因此最终选择0.1%甲酸-水/甲醇体系。在此条件下,15种目标农药可在13 min内完成分离与检测。图2为15种农药的总离子流图。

|
图 1 0.1%甲酸-水/甲醇 (A) 和0.1%甲酸-水/乙腈 (B) 体系下吡蚜酮提取色谱图 Fig. 1 Extraction chromatogram of pymetrozine in 0.1% formic acid-water/methanol (A) and 0.1% formic acid-water/acetonitrile (B) |
|
1-吡蚜酮pymetrozine;2-呋虫胺dinotefuran;3-烯啶虫胺nitenpyram;4-噻虫嗪thiamethoxam;5-吡虫啉imidacloprid;6-噻虫胺clothianidin;7-三环唑tricyclazole;8-氯虫苯甲酰胺chlorantraniliprole;9-嘧菌酯azoxystrobin;10-噻呋酰胺thifluzamide;11A-多杀霉素A spinosad A;11D-多杀霉素D spinosad D;12-戊唑醇tebuconazole;13-甲氨基阿维菌素苯甲酸盐emamectin benzoate;14-茚虫威indoxacarb;15-噻嗪酮buprofezin。 图 2 15种农药总离子流图 Fig. 2 Total ion chromatogram (TIC) of the 15 pesticides |
2.2 样品前处理方法优化 2.2.1 提取溶剂的选择
比较了乙腈、丙酮、V (乙腈): V (丙酮) = 8:1以及V (乙腈) : V (丙酮) : V (水) = 16 : 2 : 2共4种提取溶剂对大米 (添加浓度为0.1 mg/kg) 中15种目标农药回收率影响及方法显著差异性 (图3)。从图3可以看出,4种提取溶剂在吡蚜酮、甲氨基阿维菌素苯甲酸盐、嘧菌酯以及烯啶虫胺上存在显著差异性。当分别采用乙腈、丙酮和V (乙腈) : V (丙酮) = 8 : 1为提取溶剂时,部分农药的回收率低于70%;而采用V (乙腈) : V (丙酮) : V (水) = 16 : 2 : 2时,15种农药回收率均在80%以上。综合考虑,最终选择V (乙腈) : V (丙酮) : V (水) = 16 : 2 : 2作为提取溶剂,同时对比一般干样制品常规先加水后添加有机溶剂,本试验一次性将水添加到提取有机溶剂中,15种农药添加回收率都满足农药残留试验准则[20]要求。

|
1-吡虫啉imidacloprid;2-吡蚜酮pymetrozine;3-A多杀霉素A spinosad A;3-D多杀霉素D spinosad D;4-呋虫胺dinotefuran;5-甲氨基阿维菌素苯甲酸盐emamectin benzoate;6-氯虫苯甲酰胺chlorantraniliprole;7-嘧菌酯azoxystrobin;8-噻虫胺clothianidin;9-噻虫嗪thiamethoxam;10-噻呋酰胺thifluzamide;11-噻嗪酮buprofezin;12-三环唑tricyclazole;13-戊唑醇tebuconazole;14-烯啶虫胺nitenpyram;15-茚虫威indoxacarb。 图 3 不同提取溶剂下15种目标农药在大米中回收率对比结果 (添加水平为0.1 mg/kg) Fig. 3 The comparison of the recoveries of 15 pesticides in rice under the different solvent conditions (spiked 0.1 mg/kg) |
2.2.2 提取方法的选择
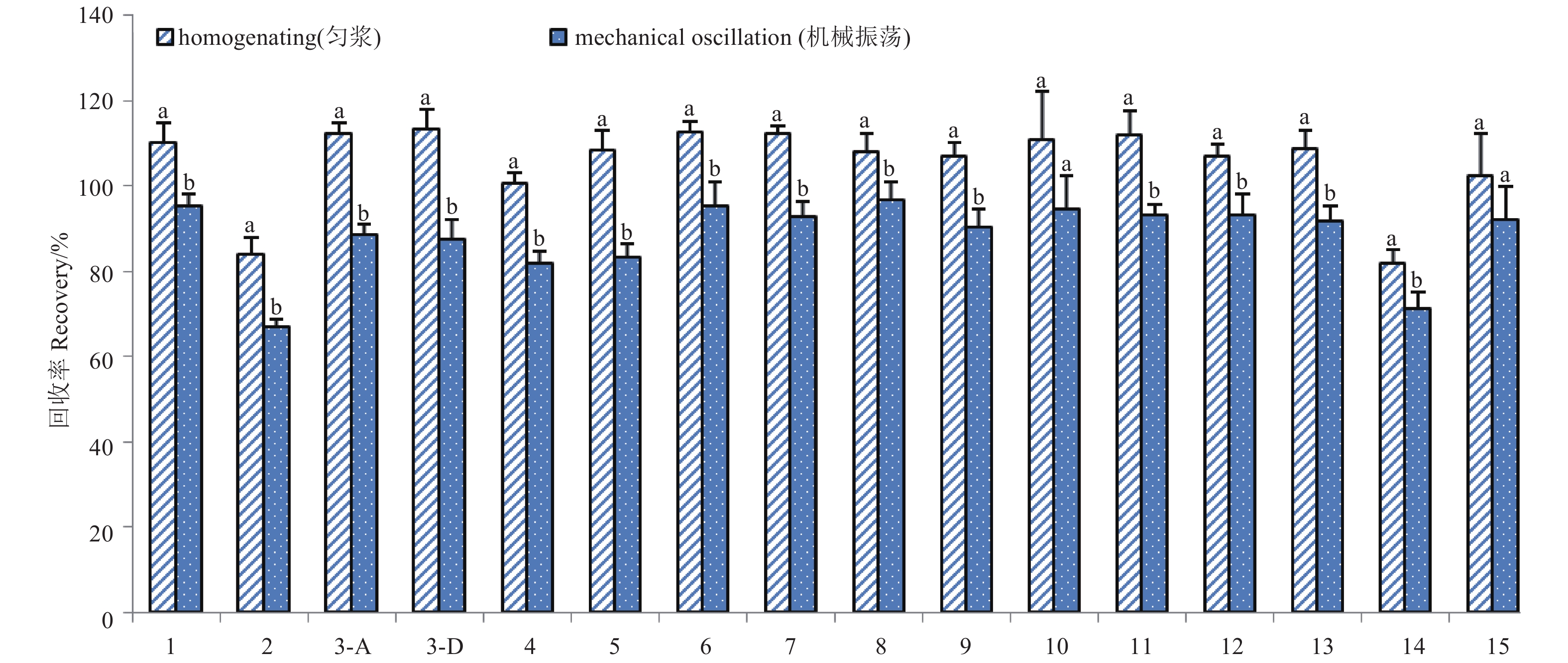
分别比较了机械振荡1 h和匀浆两种提取方法对大米 (添加水平为0.1 mg/kg) 中15种目标农药回收率影响及方法显著差异性 (图4)。从图4可以看出,除噻呋酰胺和茚虫威外,其他农药在两种方法上存在差异性。当采用机械振荡提取时,吡蚜酮和烯啶虫胺回收率均低于80%,而采用匀浆提取时,15种农药的回收率均在80%~120%之间,同时匀浆用时短,因此最终选择匀浆提取作为本研究的提取方法。
|
1-吡虫啉imidacloprid;2-吡蚜酮pymetrozine;3-A多杀霉素A spinosad A;3-D多杀霉素D spinosad D;4-呋虫胺dinotefuran;5-甲氨基阿维菌素苯甲酸盐emamectin benzoate;6-氯虫苯甲酰胺chlorantraniliprole;7-嘧菌酯azoxystrobin;8-噻虫胺clothianidin;9-噻虫嗪thiamethoxam;10-噻呋酰胺thifluzamide;11-噻嗪酮buprofezin;12-三环唑tricyclazole;13-戊唑醇tebuconazole;14-烯啶虫胺nitenpyram;15-茚虫威indoxacarb。 图 4 不同提取方法下15种目标农药在大米中回收率对比结果 (添加水平为0.1 mg/kg) Fig. 4 The comparison of the recoveries of 15 pesticides in rice under the different extractionconditions (spiked 0.1 mg/kg) |
2.2.3 净化条件的优化
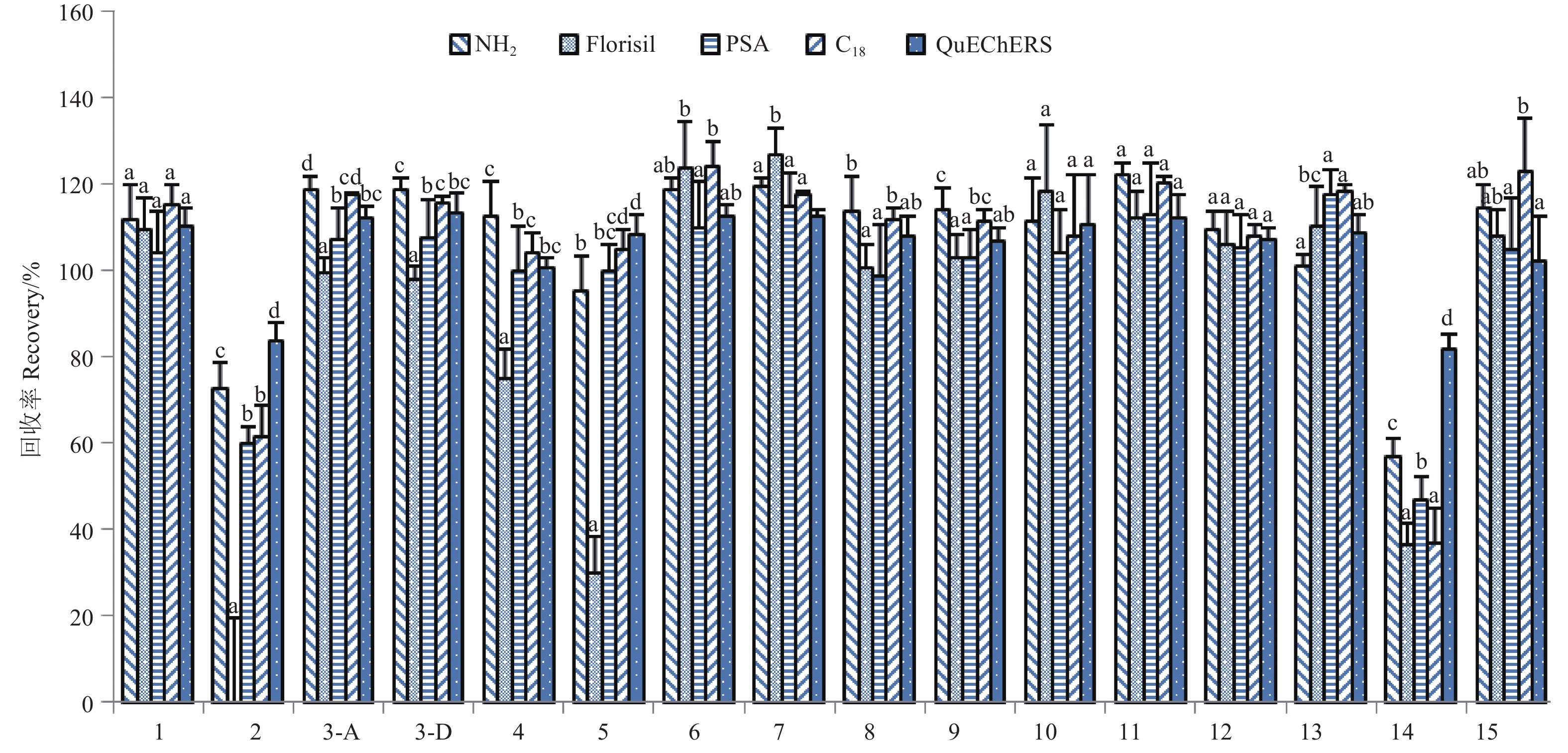
比较了NH2净化柱、Florisil净化柱、PSA净化柱、C18净化柱和QuEChERS共5种净化方法对大米中15种农药回收率影响及方法显著差异性 (图5)。按1.3.1节的提取步骤,除QuEChERS方法外,其余4种净化方法均采用V (二氯甲烷) : V(甲醇) = 95 : 5作为洗脱剂,淋洗体积15 mL,分3次淋洗。结果表明:在QuEChERS净化方法下,15种农药的回收率在80%~120%之间,而其余4种净化方法下吡蚜酮和烯啶虫胺的回收率均低于80%。另外,在Florisil净化柱条件下呋虫胺的回收率也低于80%,吡蚜酮的回收率几乎为零,甲氨基阿维菌素苯甲酸盐和烯啶虫胺的回收率均在40%以下,这主要与Florisil净化柱在正相条件下从非极性基质中强烈吸附极性分析物有关,而吡蚜酮、甲氨基阿维菌素苯甲酸盐、烯啶虫胺都存在强极性基团,因此未能被洗脱;同时通过SPSS数据分析,与其他4种方法相比,QuEChERS方法在吡蚜酮和烯啶虫胺上具有显著差异性 (图5);再综合15种农药净化后回收率结果以及QuEChERS方法时间短、使用试剂少等优点,最终选择QuEChERS作为净化方法。
|
1-吡虫啉imidacloprid;2-吡蚜酮pymetrozine;3-A多杀霉素A spinosad A;3-D多杀霉素D spinosad D;4-呋虫胺dinotefuran;5-甲氨基阿维菌素苯甲酸盐emamectin benzoate;6-氯虫苯甲酰胺chlorantraniliprole;7-嘧菌酯azoxystrobin;8-噻虫胺clothianidin;9-噻虫嗪thiamethoxam;10-噻呋酰胺thifluzamide;11-噻嗪酮buprofezin;12-三环唑tricyclazole;13-戊唑醇tebuconazole;14-烯啶虫胺nitenpyram;15-茚虫威indoxacarb 图 5 5种不同净化方法对15种目标农药回收率的影响 (添加水平为0.1 mg/kg) Fig. 5 The effect of five different purification methods on the recoveries of 15 pesticides (spiked 0.1 mg/kg) |
2.3 基质效应考察
基质与溶剂标准曲线斜率的比值反应基质效应的强弱。在大米基质中,吡蚜酮、呋虫胺、烯啶虫胺、噻虫嗪、吡虫啉、噻虫胺、嘧菌酯、噻呋酰胺、戊唑醇、甲氨基阿维菌素苯甲酸盐和茚虫威均有明显基质效应 (表2),因此本研究采取补偿措施[19],基质标准溶液校正法定量。
2.4 方法的线性范围及检出限为提高定量的准确度和可靠性,本研究采用空白基质添加不同浓度的目标化合物混合标准溶液,在0.005~1 mg/L范围内已优化的色谱和质谱条件下,15种农药的峰面积与其质量浓度间呈线性关系,标准线性方程、相关系数以及15种农药的检出限见表2。根据添加回收试验,在上述仪器条件下,15种农药的定量限均为0.01 mg/kg。
|
|
表 2 溶剂和基质标准样品的标准曲线、检出限及斜率比值 Table 2 Standards curves and LODs of 15 pesticides in solvent and matrix and their slope ratios |
2.5 方法的准确度和精密度
结果 (表3) 表明:在0.01、0.1、1和4 mg/kg 4个添加水平下,15种农药在大米中的平均回收率在82%~116%之间;相对标准偏差在1.2%~12%之间。方法的准确度和精密度均符合农药残留检测要求[20]。
|
|
表 3 15种农药在大米中的平均添加回收率和相对标准偏差 Table 3 The average recoveries and relative standard deviations (RSDs) of 15 pesticides in rice at 4 spiked levels |
2.6 实际样品分析
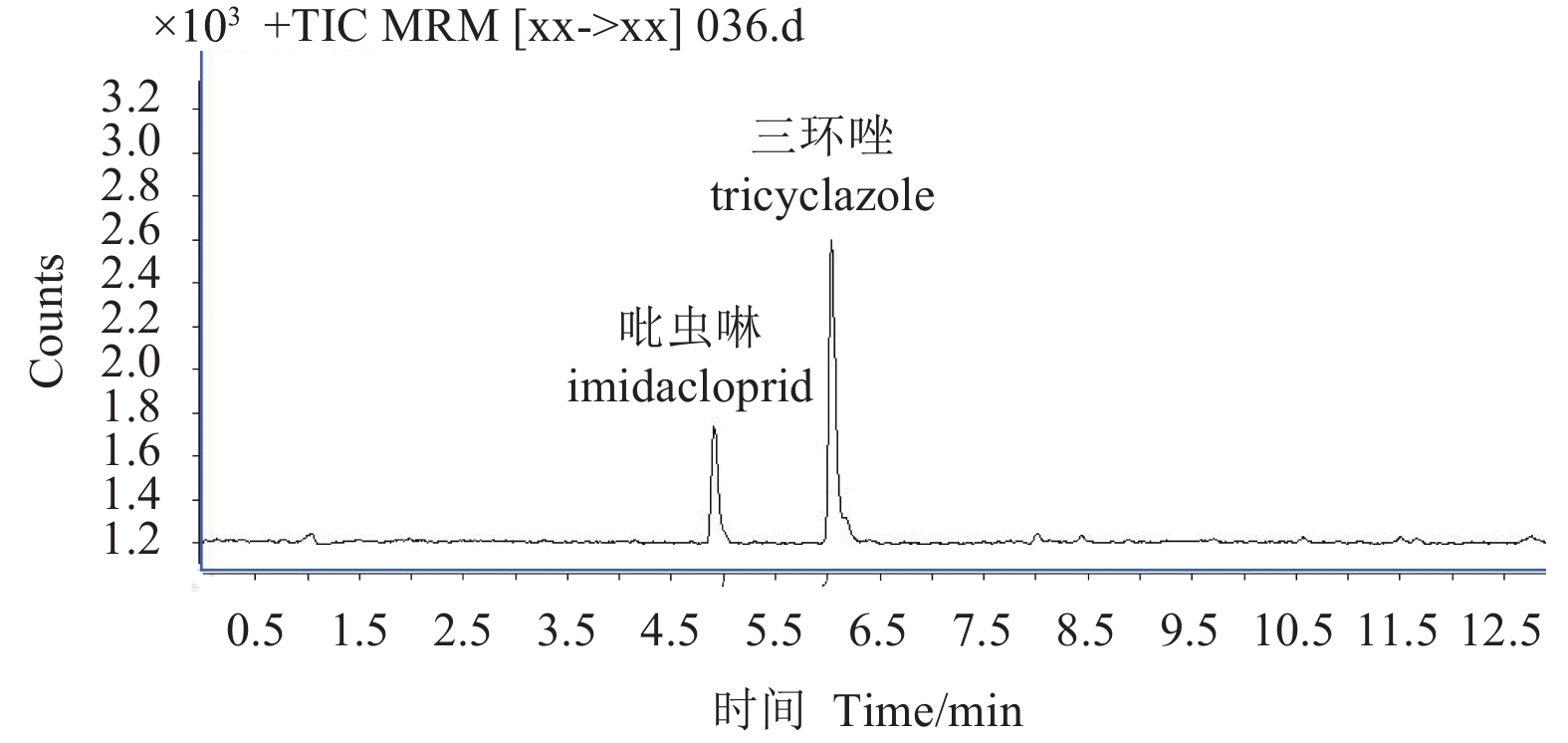
结果 (表4) 显示:从市场抽检20个批次的10个品种大米样品中,共检出吡虫啉和三环唑两种农药,检出率分别为30%和20%,其余农药均未检出。依据食品安全国家标准[21],检出的两种农药均未超出其最大残留限量值 (MRL)。典型样品总离子流色谱图见图6。
|
|
表 4 15种目标农药在大米实际样品中的残留量 Table 4 Analytical results of 15 pesticides residues in rice samples |
|
图 6 大米实际样品中吡虫啉和三环唑的总离子流图 Fig. 6 Total ion chromatogram of imidacloprid and tricyclazole in a real rice sample |
3 结论
本研究采用QuEChERS净化方法,建立了大米中15种常用农药的超高效液相色谱-串联质谱 (UPLC-MS/MS) 检测方法。方法以V(乙腈) : V (丙酮) : V (水) = 16:2:2作为提取溶剂,匀浆提取1 min,经MgSO4、PSA和C18混合净化剂净化,UPLC-MS/MS测定。该方法简便快捷、实用性强,方法回收率和精密度均符合农药残留试验准则的要求,可满足大米中农药多残留的日常检测。
| [1] |
靳保辉, 谢丽琪, 吴卫东, 等. 大米与大豆中8种二苯醚除草剂残留量气相色谱测定方法研究[J]. 分析试验室, 2008, 27(6): 75-77. JIN B H, XIE L Q, WU W D, et al. Determination of 8 diphenyl ether herbicides in cereals and oilseeds by GC[J]. Chin J Anal Lab, 2008, 27(6): 75-77. |
| [2] |
张莹, 黄志强, 陈新焕. 气相色谱法测定大米中吡氟氯禾灵农药的残留量[J]. 色谱, 2004, 22(1): 95. ZHANG Y, HUANG Z Q, CHEN X H. Dertermination of residue in cereals by GC[J]. Chin J Chromatogr, 2004, 22(1): 95. |
| [3] |
王和兴, 黎源倩, 雍莉, 等. 固相萃取-高效液相色谱法同时测定大豆和大米中的磺酰脲类和二苯醚类除草剂残留[J]. 色谱, 2007, 25(4): 536-540. WANG H X, LI Y Q, YONG L, et al. Simultaneous determination of sulfonylurea and diphenylether herbicide residues in soybean and rice by high performance liquid chromatography[J]. Chin J Chromatogr, 2007, 25(4): 536-540. |
| [4] |
QI R F, JIANG H C, LIU S X, et al. Preconcentration and determination of pesticides with graphene-modified polymer monolith combined with high performance liquid chromatography[J]. Anal Methods, 2014, 6(5): 1427-1434. DOI:10.1039/c3ay41688g |
| [5] |
VICHAPONG J, BURAKHAM R. Novel ultrasound-assisted mixed anionic-cationic surfactant-enhanced emulsification microextraction combined with HPLC for the determination of carbamate pesticides[J]. Anal Methods, 2012, 4(7): 2101-2108. DOI:10.1039/c2ay25139f |
| [6] |
刘芃岩, 刘庆学, 马育松, 等. 大米中多种残留农药的固相萃取-气相色谱-质谱分析[J]. 色谱, 2006, 24(3): 228-234. LIU P Y, LIU Q X, MA Y S, et al. Analysis of pesticide multiresidues in rice by gas chromatography-mass spectrometry coupled with solid phase extraction[J]. Chin J Chromatogr, 2006, 24(3): 228-234. |
| [7] |
食品安全国家标准 粮谷中475种农药及相关化学品残留量的测定 气相色谱-质谱法: GB23200.9—2016[S]. 北京: 中国标准出版社, 2009. National food safety standards-Determination of 475 pesticides and related chemicals residues in grains gas chromatography-mass spectrometry: GB23200.9—2016[S]. Beijing: Standards Press of China, 2009. |
| [8] |
阮华, 荣维广, 马永建, 等. QuEChERS-在线凝胶色谱-气相色谱-质谱法测定大米、黍子和小麦中34种农药残留[J]. 色谱, 2013, 31(12): 1211-1217. RUAN H, RONG W G, MA Y J, et al. Determination of 34 pesticide residues in rice, proso millet and wheat with QuECHERS-on line gel permeation chromatography-gas chromatography-mass spectrometry[J]. Chin J Chromatogr, 2013, 31(12): 1211-1217. |
| [9] |
陈溪, 董振霖, 孙玉玉, 等. 气相色谱-串联质谱法检测大米中20种农药残留[J]. 分析测试学报, 2016, 35(4): 394-399. CHEN X, DONG Z L, SUN Y Y, et al. Determination of 20 kinds of pesticide residues in rice by gas chromatography-tandem mass spectrometry[J]. J Instum Anal, 2016, 35(4): 394-399. |
| [10] |
粮谷中486种农药及相关化学品残留量的测定 液相色谱-串联质谱法: GB/T20770—2008[S]. 北京: 中国标准出版社, 2009. Determination of 486 pesticides and related chemicals residues in grains-LC-MS-MS method: GB/T20770—2008[S]. Beijing: Standards Press of China, 2009. |
| [11] |
李育左, 张睿, 王海涛, 等. 高效液相色谱串联质谱法对大米中26种三嗪类除草剂多残留的检测[J]. 分析测试学报, 2009, 28(3): 315-318. LIU Y Z, ZHANG R, WANG H T, et al. Determination of multi-residues of triazine herbicides residues in rice by HPLC-tandem MS/MS[J]. J Instrum Anal, 2009, 28(3): 315-318. |
| [12] |
曹赵云, 牟仁祥, 陈铭学. 液相色谱-串联质谱法测定稻米中的草甘膦和氨甲基膦酸残留[J]. 色谱, 2010, 28(8): 743-748. CAO Z Y, MOU R X, CHEN M X. Determination of glyphosate and aminomethylphosphonic acid in rice by using liquid chromatography-tandem mass spectrometry[J]. Chin J Chromatogr, 2010, 28(8): 743-748. |
| [13] |
粟有志, 李芳, 于晶晶, 等. QuEChERS-高效液相色谱-串联质谱法测定植物源食品中氯啶菌酯和丙炔恶草酮残留[J]. 色谱, 2016, 34(6): 577-582. SU Y Z, LI F, YU J J, et al. Determination of triclopyricarb and oxadiargyl residues in vegetative foods by QuEChERS-high performance liquid chromatography-tandem mass spectrometry[J]. Chin J Chromatogr, 2016, 34(6): 577-582. |
| [14] |
WANG X, WANG S J, CAI Z W. The latest developments and applications of mass spectrometry in food-safety and quality analysis[J]. TrAC Trends Anal Chem, 2013, 52: 170-185. DOI:10.1016/j.trac.2013.08.005 |
| [15] |
李文明, 乔成奎, 陈晓旭, 等. 高效液相色谱-串联质谱法测定水稻中的多杀霉素的残留及消解动态[J]. 农药学学报, 2012, 14(3): 298-304. LI W M, QIAO C K, CHEN X X, et al. Study on decline and residue of spinosad in paddy using high performance liquid chromatography-tandem mass spectrometry[J]. Chin J Pestic Sci, 2012, 14(3): 298-304. |
| [16] |
江泽军, 石梦琪, 刘广洋, 等. 液相色谱-串联质谱法测定21种植物源性食品中茚虫威残留[J]. 分析测试学报, 2015, 34(8): 867-873. JIANG Z J, SHI M Q, LIU G Y, et al. Determination of indoxacarb in 21 plant-derived foods by liquid chromatography tandem mass spectrometry[J]. J Instrum Anal, 2015, 34(8): 867-873. |
| [17] |
李增梅, 赵善仓, 梁京芸, 等. 超高效液相色谱-串联质谱法测定水稻田中甲氨基阿维菌素苯甲酸盐的残留量[J]. 分析测试学报, 2014, 33(1): 78-82. LI Z M, ZHAO S C, LIANG J Y, et al. Determination of emamectin benzoate in paddy field by ultra performance liquid chromatography-tandem mass spectrometry[J]. J Instrum Anal, 2014, 33(1): 78-82. |
| [18] |
段婷婷, 张盈, 魏进, 等. 超高效液相色谱-串联质谱快速检测精米、玉米与土豆样品中噻呋酰胺残留[J]. 分析测试学报, 2014, 33(5): 598-601. DUAN T T, ZHANG Y, WEI J, et al. Determination of thifluzamide residues in rice, corn and potato using UPLC-MS/MS[J]. J Instrum Anal, 2014, 33(5): 598-601. |
| [19] |
WATANABE E, KOBARA Y, BABA K, et al. Aqueous acetonitrile extraction for pesticide residue analysis in agricultural products with HPLC-DAD[J]. Food Chem, 2014, 154: 7-12. DOI:10.1016/j.foodchem.2013.12.075 |
| [20] |
农药残留试验准则: NY/T 788—2004[S]. 北京: 中国农业出版社, 2004. Guideline on pesticide residue trials: NY/T 788—2004[S]. Beijing: China Agriculture Press, 2004. |
| [21] |
食品安全国家标准 食品中农药最大残留限量: GB 2763—2016[S]. 北京: 中国标准出版社, 2017. National food safety standard-maximum residue limits for pesticides in food: GB 2763—2016[S]. Beijing: Standards Press of China, 2017. |
 2018, Vol. 20
2018, Vol. 20


