阿维菌素B2是广谱性杀虫剂阿维菌素8个异构体中的一种组分,其提取制备专利于2013年公开[1],杀虫谱不同于广泛使用的阿维菌素B1a(其中Bla不低于90%、Bla/Blb > 20)。冯龙等的研究结果表明,其对根结线虫作用突出,5%阿维菌素B 2乳油对番茄根结线虫的防效显著优于1.8%阿维菌素B1a乳油[2]。李人杰等研究表明,阿维菌素B2在土壤中的消解半衰期为2 d左右,属土壤易降解化合物[3]。虽然易降解农药可以降低其残留量,但往往需多次施药方可有效控制有害生物,相比之下农药缓释剂对于防治地下有害生物更加方便、有效,既可降低农药使用量,提高农药利用率,又可降低对环境的压力,对人畜更加安全[4]。因此,为了提高阿维菌素B2的农药利用率,笔者拟采用复凝聚法制备阿维菌素B2海藻酸钠-壳聚糖包埋颗粒剂。
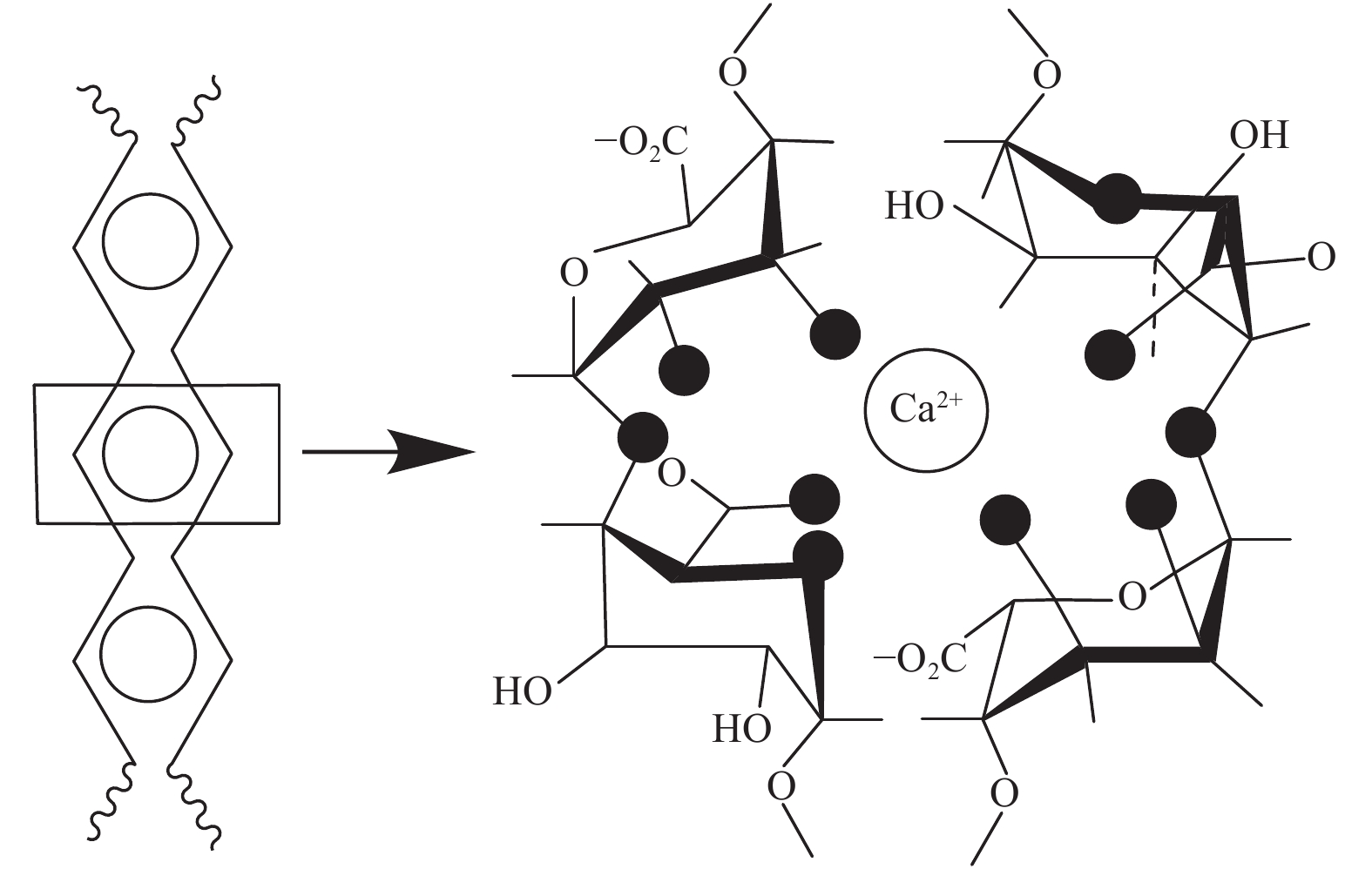
复凝聚法 (complex coacervation) 是以带相反电荷的两种高分子聚合物作为复合载体,将有效成分分散在高分子聚合物水溶液中,介质的改变促使带相反电荷的高分子聚合物发生静电作用[5],带相反电荷的高分子聚合物相互吸引后,使溶解度降低并产生相分离,聚合物与有效成分凝聚成球[6]。海藻酸钠 (sodium alginate,SA) 是从褐藻类的海带或马尾藻中提取碘和甘露醇之后的多糖副产物,当有Ca2+、Ba2+ 等阳离子存在时,其中G单元上的Na+与二价阳离子发生离子交换反应形成交联网络结构,从而形成水凝胶[7](图1),但形成的网络结构较疏松,水凝胶不够致密。海藻酸钠为天然的聚阴离子化合物,分子链上含有大量的羧基;壳聚糖 (chitosan,CS) 分子链上含有大量的伯氨基,为天然聚阳离子化合物。海藻酸钠与壳聚糖可以通过正、负电荷吸引形成聚电解质络合物[8](图2)。利用壳聚糖的络合作用可改善海藻酸盐水凝胶的致密度,不仅有利于强化对药物等活性成分的缓释作用,而且有助于改善海藻酸盐在碱性条件下的稳定性,防止其溶解;同时,壳聚糖自身在酸性条件下的稳定性也得到改善。因此,采用海藻酸盐和壳聚糖经适当方式制备复合微/纳米凝胶成为研究的热点[9-11]。
|
图 1 海藻酸钠与钙离子形成的水凝胶结构 Fig. 1 The hydrogel structure formed by sodium alginate and calcium ions |

|
图 2 壳聚糖与海藻酸钠的复凝聚反应 Fig. 2 Complex coacervation of chitosan and sodium alginate |
颗粒剂 (GR) 是指有效成分均匀吸附或分散在载体表面,具有一定粒径范围并可直接使用的、自由流动的粒状制剂[12]。常规崩解型颗粒剂的载体仅具有分散或吸附作用,无持效性,非崩解型颗粒剂具有一定的缓释作用,但载体在环境中不易降解,而高分子聚合物载体不但具有优良的缓释性能,且在环境中可生物降解,对环境友好[4]。鉴于此,本研究以高分子海藻酸钠和壳聚糖为复合载体,采用复凝聚法将阿维菌素B2包埋于组合载体中,获得了具缓释作用的阿维菌素B2海藻酸钠-壳聚糖包埋颗粒剂 (为了与传统颗粒剂进行区分将其命名为包埋颗粒剂)。对其结构及物理形态进行了表征,并对其在土壤中的缓释性能进行了研究。
1 材料与方法 1.1 药剂与仪器阿维菌素B2原药 (abamectin B2,纯度91.1%,石家庄市兴柏生物工程有限公司);海藻酸钠 (化学纯)、壳聚糖 (生化试剂,脱乙酰度80.0%~95.0%)、二甲苯 (分析纯)、Tween-20 (分析纯)、二水合柠檬酸三钠 (分析纯) 和碳酸氢钠 (分析纯)(国药集团化学试剂有限公司);无水氯化钙 (分析纯,广东汕头市西陇化工厂),乙酸 (分析纯,北京化工厂)。
79-1磁力加热搅拌器 (常州国华电器有限公司);Agilent 1200 Infinity高效液相色谱仪 (安捷伦科技有限公司);AA-200型万分之一电子天平[赛多利斯科学仪器 (北京) 有限公司];SHB-III循环水式多用真空泵 (郑州长城科工贸有限公司);MPZ-01实验室微量进样泵 (金华市婺城区欣卡电子产品商行);FW80微型高速万能粉碎机 (北京中兴伟业仪器有限公司);150 μm、300 μm标准试验筛 (浙江上虞市肖金标准筛具厂);Nicolet 6700红外光谱仪 (美国Nicolet公司);SU8010场发射扫描电子显微镜 (日本日立公司)。
1.2 阿维菌素B2海藻酸钠-壳聚糖包埋颗粒剂制备将阿维菌素B2溶于二甲苯中,加入乳化剂Tween-20,混合均匀为油相;将油相缓慢加入海藻酸钠水溶液 (水相) 中,磁力搅拌 (1 000 r/min) 乳化15 min。将乳液置于带有6#针头 (内径为0.6 mm) 的注射器中,使用微量进样泵将乳液滴加至由壳聚糖和氯化钙水溶液组成的交联相中,滴加完毕后交联反应20 min。过滤,于54 ℃烘箱中干燥,过夜后收集包埋颗粒产物。
制备的初始过滤干燥后产物经过微型高速万能粉碎机粉碎,分别过150 μm、300 μm标准试验筛,获得3种不同粒径( < 150 μm、150~300 μm及 > 300 μm)的包埋颗粒剂。
1.3 包埋颗粒剂载药量与包埋率测定 1.3.1 包埋颗粒剂破球解聚方法由于海藻酸钠-壳聚糖与氯化钙交联形成的颗粒不能通过超声溶解于甲醇和乙腈中,而使用物理方法离心破球又不能提取全部有效成分,故本研究参照文献[13]中的方法,采用0.2 mol/L碳酸氢钠与0.06 mol/L柠檬酸三钠溶液进行超声破球解聚,其中海藻酸钠与钙离子形成的水凝胶结构可被柠檬酸根破坏,海藻酸钠与壳聚糖之间的静电凝聚可被碳酸氢钠破坏。
1.3.2 高效液相色谱分析方法取0.1 g包埋颗粒剂,置于由碳酸氢钠和柠檬酸三钠组成的解聚液中,超声解聚后转移至容量瓶中,用流动相定容,过0.45 μm有机滤膜,使用高效液相色谱仪测定阿维菌素B2的质量分数,分别采用 (1) 和 (2) 式计算载药量和包埋率。
| ${\text{载药量}}/{\%} = \frac{\text{包埋颗粒剂中有效成分质量}}{\text{包埋颗粒剂质量}} \times 100$ | (1) |
| ${\text{包埋率}}/{\%} = \frac{{\text{载药量} \times \text{包埋颗粒剂质量}}}{\text{投入有效成分质量}} \times 100$ | (2) |
高效液相色谱分析条件:流动相为V (甲醇) : V (乙腈) : V (水) = 40 : 40 : 20,流速l.0 mL/min;Waters sunfire-C18色谱柱 (4.6 mm × 150 mm,5 μm);紫外检测器波长254 nm;柱温30 ℃;进样体积5 μL。阿维菌素B2保留时间:8.5 min。
1.4 单因素试验设计设乳液中海藻酸钠的质量分数为1.5%,乳化剂Tween-20的质量分数为0.75%;m (油相) : m (水相) = 1 : 20;投药量m (阿维菌素B2) : m (海藻酸钠) = 1 : 2,交联相中壳聚糖的质量分数为1.0%。试验均重复3次。
1.5 正交试验设计选取单因素试验中对包埋率有显著影响的因素作为正交试验设计的因子,根据正交试验结果获得理论较优配方,最后通过验证获得制备阿维菌素B2海藻酸钠-壳聚糖包埋颗粒剂的优选配方。
1.6 包埋颗粒剂结构表征用扫描电镜和红外光谱表征包埋颗粒剂的表面形态和结构。取经粉碎机粉碎的包埋颗粒剂干粉适量,均匀撒布在双面胶带上,经离子镀膜仪喷金后采用扫描电子显微镜 (SEM) 观察其表面形态。取适量溴化钾分别与干燥的阿维菌素B2原药、空白颗粒剂和阿维菌素B2海藻酸钠-壳聚糖包埋颗粒剂混合均匀,压片,采用傅里叶变换红外光谱仪进行分析。
1.7 包埋颗粒剂在土壤中的释放性能评价参照文献[14]的土壤包埋法进行。供试土壤取自中国农业科学院植物保护研究所 (黏粒7.53%,粉砂粒72.62%,砂粒19.85%),试验期间最高气温平均31.4 ℃,最低气温平均21.0 ℃,平均相对湿度66%,采用干燥法测得土壤湿度为13%。将装有新鲜土壤的花盆置于室外。为使包埋颗粒剂与土壤充分接触,将所制备的3种不同粒径的包埋颗粒剂约30 mg包裹于孔径大小接近各自最小粒径的尼龙网中,粒径 > 300 μm的包埋颗粒剂使用孔径300 μm尼龙网,粒径在150~300 μm之间的使用孔径150 μm尼龙网,粒径 < 150 μm的使用孔径75 μm尼龙网。将装有包埋颗粒剂的尼龙网埋于花盆中部,分别于10、20、30、40、50、60、70、80 d时取出,置烘箱中干燥,通过高效液相色谱仪测定回收载药量,按 (3) 式计算有效成分释放率。
| ${\text{释放率}}/{{\% }} = \frac{{\text{回收包埋颗粒剂质量} \times \text{回收载药量}}}{{\text{初始包埋颗粒剂质量} \times \text{初始载药量}}} \times 100$ | (3) |
将3种不同粒径包埋颗粒剂在土壤中的释放曲线与药物常用释放动力学模型—零级动力学模型、一级动力学模型、Higuchi模型和Weibull模型进行拟合分析[15]。
2 结果与分析 2.1 单因素试验 2.1.1 海藻酸钠用量对包埋颗粒剂载药量和包埋率的影响由于海藻酸钠可作增稠剂使用,浓度过大时难以配制溶液,并且乳液黏度过大会影响注射器的滴加,因此本研究以乳液中海藻酸钠的质量分数2%作为上限,分别设定海藻酸钠在乳液中的质量分数为0.5%、1.0%、1.5%和2.0%,采用1.2节方法,分别制备阿维菌素B2海藻酸钠-壳聚糖包埋颗粒剂,测定其载药量和包埋率。结果 (表1) 表明:乳液中海藻酸钠的质量分数对包埋颗粒剂的载药量有显著影响,其中当其质量分数分别为1.5%和2.0%时,包埋颗粒剂的载药量和包埋率均显著高于其质量分数分别为0.5%与1%的水平。这是由于海藻酸钠浓度越高,其与钙离子交联形成的水凝胶越牢固、致密,而交联固化程度越高,载体包埋原药的效率越高,载药量越大,包埋率也随之增加。当海藻酸钠浓度较低时,形成的水凝胶较松散,导致所形成的颗粒不规则,粘连严重。海藻酸钠质量分数为2.0%时的载药量和包埋率与其质量分数为1.5%时的差异不显著,说明大部分药物已被载体包埋,继续增加载体浓度并未提高包埋率,反而会造成载体的浪费,因此最终选用海藻酸钠质量分数为1.5%作为该载体的最佳水平。
|
|
表 1 海藻酸钠质量分数、投药量、油水比对包埋颗粒剂载药量和包埋率的影响 Table 1 Effect of mass fraction of sodium alginate, dosage and oil to water ratio on drug loading and entrapment efficiency of embedding granules |
2.1.2 投药量对包埋颗粒剂载药量和包埋率的影响
鉴于在包埋颗粒剂的制备过程中,海藻酸钠作为主载体,因此投药量仅以原药与海藻酸钠 (下称载体) 的质量比作为投药量的研究因素。分别设定原药与载体的质量比为1:1、1:1.5、1:2、1:3和1:4,采用1.2节方法分别制备阿维菌素B2颗粒剂,测定其载药量和包埋率。结果 (表1) 表明:载药量随原药与载体质量比的降低而降低,而包埋率除原药与载体的质量比为1:1时较低外,其余投药量对包埋率的影响差异均不显著,这与一般以高分子载体制备缓释微球的结果有所差异,如郑玉制备吡唑醚菌酯PLGA微球,随着有效成分质量分数的增大包埋率显著降低[16]。本研究结果表明阿维菌素B2原药与载体结合较好。原药与载体质量比为1:1时包埋率较低的原因,可能是由于原药的质量分数过高,载体不能将其充分包埋。由本研究结果可以看出,当原药与载体质量比在1:1.5~1:4之间时,均可制备载药量在10%~25%之间的阿维菌素B2包埋颗粒剂,并可保证其包埋率接近90%,但考虑到当原药与载体比例较高时可能会造成一定程度的突释[17],因此最终选用原药与载体的质量比为1:2进行其他影响因素的研究。
2.1.3 油水比对包埋颗粒剂载药量和包埋率的影响按照以上试验筛选获得的最佳条件,分别设定油水质量比为1:20 、1:10和1: 5制备包埋颗粒剂,测定其载药量及包埋率。结果 (表1) 表明:油水比例对包埋颗粒剂的载药量影响不显著,但对包埋率影响显著。当油水比由1:20增加到1:5时,包埋率下降了3%,这可能是因为随着油相的增加,乳状液黏度增大,乳液粘壁增多损耗增大,乳液滴加不匀,交联不充分,导致包埋率下降。最终选用的油水比为1:20,此时包埋率最高。
2.1.4 乳化剂Tween-20用量对包埋颗粒剂载药量和包埋率的影响采用以上试验筛选获得的最佳条件,设定乳化剂Tween-20在乳液中的质量分数为0.50%、0.75%、1.00%、1.25%和1.50%,采用1.2节方法分别制备包埋颗粒剂,测定其经过滤、干燥后产物的质量、载药量及包埋率。由表2可见,随着Tween-20用量的增加,包埋颗粒剂的载药量显著下降,包埋率也随之下降。Tween-20形成乳液后一部分附着于颗粒表面,一部分溶于水相中,附着在颗粒表面的增加的部分乳化剂并不会随着过滤、干燥而失去,而投入的有效成分质量不变,因此过滤干燥后产物质量增加导致载药量下降。而包埋率的下降可能是由于Tween-20用量过大时,部分Tween-20会溶于水相中形成胶束,进而会对农药有效成分产生增溶作用,导致原药溶于其中,从而使包埋率下降[18]。本研究发现,虽然当Tween-20质量分数为0.50%时所制备的包埋颗粒剂包埋率较高,但配制乳液时有微量析出物,而乳化剂质量分数为0.75%可满足乳化要求,包埋率与Tween-20为0.50%时的无显著差异,因此确定乳化剂的质量分数为0.75%。
|
|
表 2 Tween-20及壳聚糖质量分数对包埋颗粒剂质量、载药量及包埋率的影响 Table 2 Effect of mass fraction of Tween-20 and chitosan on mass, drug loading and entrapment efficiency of embedding granules |
2.1.5 壳聚糖用量对包埋颗粒剂载药量和包埋率的影响
按照以上试验所筛选的最佳条件,设定壳聚糖在交联相中的质量分数分别为0%、0.5%、1%、2%和3%,采用1.2节方法分别制备包埋颗粒剂,测定其经过滤、干燥后产物的质量、载药量及包埋率。结果 (表2) 表明:与以壳聚糖和海藻酸钠为复合载体制备的载药颗粒剂相比,不添加壳聚糖,仅以海藻酸钠为单一载体制备的包埋颗粒剂,产物质量和包埋率显著降低,虽然载药量略高,但差距不大。说明单用海藻酸钠形成的水凝胶不够致密,壳聚糖的加入可以形成更致密的海藻酸钠-壳聚糖聚电解质络合物[8]。随着壳聚糖质量分数的增加,包埋颗粒剂的载药量与包埋率均呈现先增加后降低的趋势,表明适量的壳聚糖可以提高凝聚物的致密程度,但随着壳聚糖质量分数的增加,交联相的黏度也会显著增加,黏度过高会阻碍交联反应充分进行。最终选取壳聚糖的质量分数为1%。
2.2 正交试验设计选取海藻酸钠质量分数、Tween-20质量分数、油水比和壳聚糖质量分数作为正交试验设计的试验因素,各取4个水平,采用L16(45) 正交表设计试验 (表3)。结果见表4。
|
|
表 3 正交试验因素与水平 Table 3 Factors and levels of orthogonal test |
|
|
表 4 正交试验结果 Table 4 Results of orthogonal test |
由方差分析结果 (表5) 可以看出:各因素的影响顺序为FA > > FB > FC > FD,海藻酸钠质量分数与其他因素差异极显著,表明海藻酸钠的质量分数对包埋率的影响最大,其他3个因素差异不显著,其中壳聚糖的质量分数影响最小。采用SAS的均值进行比较,结果表明:A3 > A 4 > A 2 > A 1,即海藻酸钠的质量分数以1.5%为佳;B1 > B 2 > B 3 > B 4,Tween-20的质量分数以0.75%为佳;C1 > C 3 > C 2 > C 4,油水质量比以1:20为佳;D4 > D 3 > D 1 > D 2,壳聚糖的质量分数以3%为佳。
|
|
表 5 正交试验方差分析结果 Table 5 Variance analysis of orthogonal test |
根据正交试验结果得到的最优组合为A3B1C1D4,即海藻酸钠和Tween-20的质量分数分别为1.5%和0.75%,油水质量比为1:20,壳聚糖质量分数为3%。选取正交试验最优组合与单因素试验时包埋率较高的试验组合进行验证试验,结果见表6。
|
|
表 6 正交试验验证结果 Table 6 Verification results of orthogonal test |
结果表明,包埋率由高到低的试验组合为A3B1C3D4 > A 3B1C1D2 > A 3B1C3D2 > A 3B1C1D4,尽管A3B1C3D4包埋率略高于A3B1C1D2,但从原材料使用量考虑,前者壳聚糖的用量与二甲苯的用量均高于后者,而包埋率并未显著高于后者,因此推荐A3B1C1D2为最优配方,即海藻酸钠质量分数为1.5%,Tween-20质量分数为0.75%,油水质量比为1:20,壳聚糖质量分数为1%。
2.3 采用优化配方制备的阿维菌素B2壳聚糖-海藻酸钠包埋颗粒剂称取91.1%阿维菌素B2原药0.75 g溶于3 g二甲苯中,加入0.75 g乳化剂Tween-20,搅拌混合均匀为油相。称取海藻酸钠1.5 g,加蒸馏水至100 g(油水质量比为1:20,油水总质量为100 g),搅拌溶解为水相。称取壳聚糖0.5 g,乙酸0.5 g,氯化钙1 g,溶于50 g蒸馏水中,加热搅拌、溶解为交联相。将油相缓慢加入水相中乳化15 min (搅拌速度1 000 r/min),直至为均匀的乳状液。将乳化均匀的乳液置于注射器中 (0.6 mm针头),使用注射泵将乳液滴加至交联相中 (滴加速度为1 mL/min),滴加完毕后交联反应20 min。过滤滤去水相,收集产物置于54 ℃烘箱中干燥,获得阿维菌素B2壳聚糖-海藻酸钠包埋颗粒剂。经高效液相色谱仪测定得知,其载药量为22.38% ± 0.25%,包埋率为95.26% ± 0.61%。
2.4 不同粒径包埋颗粒剂的载药量初始过滤干燥颗粒经过机械粉碎后获得的3种不同粒径包埋颗粒剂的载药量测定结果见表7。
|
|
表 7 不同粒径的阿维菌素B2包埋颗粒剂载药量 Table 7 The drug loading of different particle sizes of abamectin B2 embedding granules |
由表7可见,随着粒径的减小,颗粒内部 (包埋) 载药量降低,颗粒外部 (附着颗粒表面) 载药量增加,但总载药量变化不大。这是由于颗粒越细,比表面积越大,分布在颗粒表面的有效成分越多,因此所粉碎粒径越小,裸露于颗粒表面有效成分增多,而被包埋在颗粒内部的有效成分质量分数随之降低。
2.5 扫描电子显微镜 (SEM) 观察结果结果 (图3) 显示,经粉碎后得到的包埋颗粒剂 (< 150 μm) 形状不规则,并且在其致密表面附着有棒状阿维菌素B2原药晶体。

|
图 3 阿维菌素B2包埋颗粒剂扫描电镜图 Fig. 3 SEM photo of abamectin B2 embedding granules |
2.6 红外光谱分析结果
由图4可见,对于阿维菌素B2原药,3 523 cm–1处的吸收峰是由-OH伸缩振动引起的,2 931~2 967 cm–1处的吸收峰是由C-H伸缩振动引起的 (-CH3与-CH2),1 716 cm–1处的吸收峰是由C=O伸缩振动引起的,1 144 cm–1处的吸收峰是由C-O-C伸缩振动引起的,986 cm–1处吸收峰是由C=C上的C-H面外弯曲振动引起的。而对于以海藻酸钠-壳聚糖为载体形成的未载药颗粒剂 (空白颗粒剂),3 446 cm–1处的吸收峰是由海藻酸钠与壳聚糖 -OH伸缩振动与壳聚糖N-H伸缩振动叠加而成,1 622 cm–1处吸收峰是由海藻酸钠中COO–受到壳聚糖中氨基的影响发生反对称振动形成的[18],1 108 cm–1处吸收峰是海藻酸钠与壳聚糖C–O伸缩振动引起。与空白颗粒剂相比,阿维菌素B2包埋颗粒剂在3 420、1 608和1 107 cm–13处特征吸收峰均出现了蓝移,即向短波长方向移动,并且强度增强,这是由于这3处吸收峰除海藻酸钠与壳聚糖外还受到了阿维菌素B2对应位置相同基团 -OH伸缩振动、C=O、C–O伸缩振动的影响。由于空白颗粒剂中无C=C,因此在载药颗粒剂987 cm–1处出现的由C=C中C–H面外弯曲振动引起吸收峰,验证了阿维菌素B2已成功包埋在海藻酸钠-壳聚糖复合载体中。

|
图 4 阿维菌素B2原药、海藻酸钠-壳聚糖空白颗粒剂、阿维菌素B2海藻酸钠-壳聚糖包埋颗粒剂红外光谱图 Fig. 4 IR spectra of abamectin B2, alginate-chitosan embedding granules, abamectin B2 alginate-chitosan embedding granules |
2.7 不同粒径包埋颗粒剂在土壤中的模拟释放性能研究
3种不同粒径的包埋颗粒剂在土壤中的模拟释放曲线见图5。由图中可见,随着粒径的减小,有效成分释放速率明显加快,粒径 > 300 μm、150~300 μm、< 150 μm的颗粒剂80 d时有效成分释放率依次为45.10%、74.67%和79.20%。这是因为颗粒越细,表面上吸附的有效成分越多,颗粒表面上的有效成分由于无载体包覆而优先向外释放,且颗粒越细,比表面积越大,有效成分向外释放的阻力越小,载体降解加快,因而释放速率越快。在试验的前30 d内,3种粒径的颗粒剂均出现了速度较快的突释,> 300 μm、150~300 μm、< 150 μm 3种颗粒在土壤中30 d时释放率分别占到80 d总释放率的79.2%、61.7%和75.3%,占80 d总释放量的60%以上;在30~80 d之间,粒径 > 300 μm的颗粒剂与其他两种相比,释放曲线较平缓,在后50 d中,有效成分的释放量仅增加了9.4%,表明颗粒越大,载体降解的速率越慢,仅仅依靠载体孔隙向外释放的压力降低,从而有效成分释放缓慢。
常用的模拟释放的数学模型有零级动力学方程、一级动力学方程、Higuchi方程和Weibull方程等。本研究使用Orign 9.0软件对释放数据进行方程拟合。由决定系数R2得到3种粒径包埋颗粒剂的最优拟合度,释放模型见表8。结果表明:粒径 > 300 μm包埋颗粒剂拟合较好的为一级动力学方程与Weibull方程,但用Weibull模型拟合时虽然其 R2 最高,拟合曲线较为接近,但分析显示拟合没有收敛,超过迭代最大次数,因此该模型不适用,所对应的一级动力学方程应为 > 300 μm颗粒剂最适宜拟合方程;粒径150~300 μm的包埋颗粒剂拟合较好的为一级动力学方程与Higuchi方程,二者差异较小,R2均大于0.95,拟合程度均很高;粒径 < 150 μm的包埋颗粒剂,其拟合较好的模型为Higuchi方程,R2为0.93。综合考虑,粒径150~300 μm和 > 300 μm的包埋颗粒剂在土壤中的模拟释放均符合一级动力学方程,粒径150~300 μm和 < 150 μm的包埋颗粒剂在土壤中的模拟释放亦符合Higuchi方程。

|
图 5 3种粒径阿维菌素B2包埋颗粒剂在土壤中模拟释放曲线 Fig. 5 The simulated release curves of three kinds of abamectin B2 embedding granules in the soil |
|
|
表 8 3种粒径包埋颗粒剂在土壤中释放曲线方程拟合 Table 8 Fitting equation of release curve of three kinds of embedding granules in the soil |
3 结论与讨论
使用复凝聚法制备了阿维菌素B2海藻酸钠-壳聚糖包埋颗粒剂,并通过单因素试验研究了海藻酸钠质量分数、投药量、油水比、乳化剂质量分数及壳聚糖质量分数对包埋颗粒剂载药量和包埋率的影响,并以对包埋率影响显著的因素作为正交试验设计的因子进行正交试验。经过配方优化获得的阿维菌素B2海藻酸钠-壳聚糖包埋颗粒剂优选配方为:海藻酸钠质量分数为1.5%,Tween-20质量分数为0.75%,二甲苯质量分数为3%,以上组分均为乳液中的质量分数;壳聚糖质量分数为1%,氯化钙质量分数为2.0%,以上组分均为交联相中质量分数);投料量为1:2(阿维菌素B2为0.75% × 91.1%=0.68%,乳液中的质量分数);油水质量比为1:20。所制备的包埋颗粒剂经高效液相色谱仪测定,其载药量为22.38% ± 0.25%,包埋率为95.26% ± 0.61%。
一般常规剂型在生产工艺上全进全出,产出基本没有损耗,产出率很高,例如固体剂型可湿性粉剂一般可达到98%以上,液体剂型乳油、微乳剂等可达到100%。而缓释剂型由于有效成分与载体发生相互作用,不可能完全被包埋或包封,一般达到80%以上即为成功的制备方法,例如宋丽敏制备的高效氯氰菊酯凝胶微球的包埋率仅为76%[20]。本研究所制备的包埋颗粒剂经过单因素及正交试验的配方工艺优化,获得了高包埋率的产品,包埋率高达95%以上,这可与常规农药剂型的产出率相媲美,极大降低了缓释制剂的生产成本 (假设缓释制剂的包埋率为80%,则由于有效成分的损耗而提高原药成本20%),也表明阿维菌素B2包埋颗粒剂的工艺优化达到较高水平。
文献报道,采用复凝聚法制备的海藻酸钠-壳聚糖微囊,粒径均较小,如Natrajan等以O/W乳液制备的香精油海藻酸钠-壳聚糖微囊,其粒径小于300 nm[21],李凤红等以大豆油为油相,海藻酸钠质量分数为2%,以W/O乳液制备了海藻酸钠-壳聚糖纳米微球,其粒径最小为364.4 nm,最大为1 171 nm[22]。而本研究所制备的阿维菌素B2包埋颗粒剂的粒径较大,初始过滤干燥后的颗粒粒径大于0.6 mm。在W/O乳液中海藻酸钠水溶液作为分散相处于界面膜内,界面膜外被连续相大豆油包覆,海藻酸钠与交联相中的壳聚糖并未直接接触,交联缓慢,乳液有充分时间分散为小液滴,因此其粒径较小,而在O/W乳液中,海藻酸钠水溶液作为连续相处于阿维菌素B2油珠颗粒的界面膜外,将乳液滴加至由壳聚糖和氯化钙组成的交联相中后,海藻酸钠与钙离子快速形成水凝胶,且与壳聚糖快速凝聚成聚电解质络合物而高浓度的海藻酸钠乳液在分散之前即迅速被交联固化,因此本研究所制备的包埋颗粒粒径较大。Natrajan等使用的海藻酸钠的质量分数仅为0.03%,而本研究使用海藻酸钠质量分数为1.5%,为前者的50倍,之所以选用高浓度的海藻酸钠,是为了使制备工艺获得较高的效率和收率,便于农药制剂的工业化生产。
通过添加壳聚糖对包埋颗粒剂的载药量及包埋率的影响表明单用海藻酸钠形成的水凝胶不够致密,壳聚糖的加入可以形成更致密的聚电解质络合物。适量的壳聚糖可以提高凝聚物的致密程度,但过量的壳聚糖由于黏度过高而影响交联反应的充分进行,而且对降低制剂的成本很有优势,海藻酸钠工业品每吨约为1万元,而壳聚糖工业品每吨超过10万,以海藻酸钠为载体主要成分可大幅度降低制剂成本。
一般缓释剂具有优异的持效性,而相应的速效性较差,而本研究中3种粒径的包埋颗粒剂在土壤中的模拟释放研究表明:其具有明显的突释效应,该效应对于缓释剂获得一定的速效性意义重大 (颗粒表面附着的有效成分优先释放,亦具有一定的速效性),使之既具有一定的速效性,亦有良好的持效性。释放速率与包埋颗粒粒径呈负相关,即颗粒粒径越小,越易释放,持效期越短。包埋颗粒剂中有效成分与载体均匀混合包埋,机械粉碎不破坏包埋颗粒剂的结构,仅对内外的载药量有影响,可根据防治靶标的实际需要 (不同靶标所需药剂的持效期不同),通过不同标准的筛网获得不同粒径的包埋颗粒剂,达到真正控制释放的目的。3种粒径的包埋颗粒剂在土壤中的模拟释放曲线拟合结果表明,其符合均匀包埋的缓释剂释放动力学[23]。
对缓释剂释放性能的研究一般在水介质中进行模拟研究,而在土壤中进行模拟释放研究并不多见[24]。本研究制备的阿维菌素B2包埋颗粒剂专用于防治蔬菜根结线虫,通常在土壤中使用,若在水介质中进行模拟释放研究,由于使用环境差异太大而实际意义不大。本研究最初曾尝试按照Sarkar等介绍的方法[24](缓释剂直接埋在装有土壤的烧杯中,用有机溶剂淋洗土壤,测定淋洗出的有效成分) 进行试验,结果很快就将大部分有效成分从土壤中淋洗出来 (当天进行回收率试验,粒径 < 150 μm的包埋颗粒剂有95.11%的有效成分被淋洗出来,> 300 μm的包埋颗粒剂回收率也达到83.78%),无法研究其缓释性能。最终参考《液体制剂》介绍的土壤包埋法 [14]展开缓释剂在土壤中的模拟释放研究,取得了初步的结果,为在土壤中使用的缓释剂的模拟释放研究提供了一种新的尝试。由于土壤环境与大气环境差异较大,土壤湿度、温度、土壤微生物、土壤pH值均对包埋颗粒剂的释放有重要影响,因此这些因素对其释放性能的影响有待于后续进一步研究。
在土壤中的模拟释放采用包埋法,虽然包埋颗粒剂与土壤通过尼龙网相对隔离,但是土壤中的水分或微生物通过尼龙网的网孔影响包埋颗粒剂中有效成分的释放。参照缓释剂的释放机理[23],可以假设包埋颗粒剂在土壤中的释放机理:首先,附着在表面的有效成分通过尼龙网优先释放到土壤中;其次在土壤水分的作用下,尼龙网中的包埋颗粒剂吸水膨胀,产生孔隙,有效成分通过孔隙往外释放;第三,随着土壤微生物对载体的降解,有效成分随即释放出来,这是包埋颗粒剂降解的主要途径。在测定过程中,不仅取出来的尼龙网中的包埋颗粒剂载药量降低,而且尼龙网中的包埋颗粒剂质量也在减少,表明有效成分与降解的载体均往外释放。
通过高效液相色谱测定尼龙网中回收的包埋颗粒剂的载药量,来计算阿维菌素B2的释放量切实可行。虽然阿维菌素B2在土壤中的半衰期约为2 d,属于易降解的农药有效成分,但将其包埋在载体中 (用尼龙网包裹埋在土壤中),有效成分与土壤还是形成相对的物理隔离,且测定的是尼龙网中的包埋颗粒剂的载药量,把每次取回的包埋颗粒剂有效成分的减少量作为累积释放量,而无需考虑阿维菌素B2在土壤中的降解因素。
| [1] |
张海航, 王琳慧, 暴连群, 等. 一种阿维菌素 B2a 的提取制备方法: CN102977168A[P]. 2013-03-20.
ZHANG H H, WANG L L, BAO L Q, et al. Method for extraction and preparation of avermectin B2a: CN102977168A[P]. 2013-03-20. |
| [2] |
冯龙, 暴连群, 鲁森. 阿维菌素 B2 乳油防治番茄根结线虫的田间试验
[J]. 农药, 2015, 54(6): 448–449.
FENG L, BAO L Q, LU S. Control efficacy of abamectin B2 EC against Meloidogyne incognita [J]. Agrochemicals, 2015, 54(6): 448–449. |
| [3] |
李人杰, 暴连群, 张海航, 等. 阿维菌素 B2 在番茄和土壤中的消解动态及最终残留
[J]. 农药, 2016, 55(6): 437–440.
LI R J, BAO L Q, ZHANG H H, et al. The degradation dynamics and final residues of avermectin B2 in tomato and soil [J]. Agrochemicals, 2016, 55(6): 437–440. |
| [4] |
陈福良. 农药新剂型加工与应用[M]. 北京: 化学工业出版社, 2015: 219, 225-226.
CHEN F L. Processing and application of pesticide new formulation[M]. Beijing: Chemical Industry Press, 2015: 219, 225-226. |
| [5] | FU J C, SCHLENOFF J B. Driving forces for oppositely charged polyion association in aqueous solutions: enthalpic, entropic, but not electrostatic[J]. J Am Chem Soc, 2016, 138(3): 980–990. doi:10.1021/jacs.5b11878 |
| [6] | SPRUIJT E, WESTPHAL A H, BORST J W, et al. Binodal compositions of polyelectrolyte complexes[J]. Macromolecules, 2010, 43(15): 6476–6484. doi:10.1021/ma101031t |
| [7] |
高春梅, 柳明珠, 吕少瑜, 等. 海藻酸钠水凝胶的制备及其在药物释放中的应用[J]. 化学进展, 2013, 25(6): 1012–1022.
GAO C M, LIU M Z, LV S Y, et al. Preparation of sodium alginate hydrogel and its application in drug release[J]. Progr Chem, 2013, 25(6): 1012–1022. |
| [8] | LI X X, XIE H G, LIN J Z, et al. Characterization and biodegradation of chitosan alginate polyelectrolyte complexes[J]. Polym Degrad Stab, 2009, 94(1): 1–6. doi:10.1016/j.polymdegradstab.2008.10.017 |
| [9] | LUCINDA-SILVA R M, SALGADO H R N, EVANGELISTA R C. Alginate chitosan systems: in vitro controlled release of triamcinolone and in vivo gastrointestinal transit [J]. Carbohydr Polym, 2010, 81(2): 260–268. doi:10.1016/j.carbpol.2010.02.016 |
| [10] | AGNIHOTRI S A, MALLIKARJUNA N N, AMINABHAVI T M. Recent advances on chitosan-based micro-and nanoparticles in drug delivery[J]. J Control Rel, 2004, 100(1): 5–28. doi:10.1016/j.jconrel.2004.08.010 |
| [11] | DEKA C, DEKA D, BORA M M, et al. Synthesis of peppermint oil-loaded chitosan/alginate polyelectrolyte complexes and study of their antibacterial activity[J]. J of Drug Delivery Sci Tech, 2016, 35: 314–322. doi:10.1016/j.jddst.2016.08.007 |
| [12] |
中华人民共和国农业部. 农药剂型名称及代码: GB/T 19378—2003[S]. 北京: 中国标准出版社, 2004.
Ministry of Agriculture of the People's Republic of China. Nomenclature and codes for pesticide for formulations: GB/T 19378—2003[S]. Beijing: China Standards Press, 2004. |
| [13] |
薛伟明, 于炜婷, 刘袖洞, 等. 载细胞海藻酸钠/壳聚糖微胶囊的化学破囊方法研究[J]. 高等学校化学学报, 2004, 25(7): 1342–1346.
XUE W M, YU W T, LIU X D, et al. Chemical method of breaking the cell-loaded sodium alginate/chitosan microcapsules[J]. Chem J Chin Univ, 2004, 25(7): 1342–1346. |
| [14] |
郭武棣. 液体制剂[M]. 3版. 北京: 化学工业出版社, 2004: 303.
GUO W D. Liquid pesticide preparation[M]. 3rd ed. Beijing: Chemical Industry Press, 2004: 303. |
| [15] | DASH S, MURTHY P N, NATH L, et al. Kinetic modeling on drug release from controlled drug delivery systems[J]. Acta Pol Pharm, 2010, 67(3): 217–223. |
| [16] |
郑玉. 吡唑醚菌酯 PLGA 微球的研制及其性能研究[D]. 北京: 中国农业科学院, 2014.
ZHENG Y. The preparation of pyraclostrobin PLGA microsphere and research on its property[D]. Beijing: Chinese Academy of Agricultural Sciences, 2014. |
| [17] | KAMALY N, YAMEEN B, WU J, et al. Degradable controlled-release polymers and polymeric nanoparticles: mechanisms of controlling drug release[J]. Chem Rev, 2016, 116(4): 2602–2663. doi:10.1021/acs.chemrev.5b00346 |
| [18] |
朱欣妍. 甲维盐聚乳酸微球的研制及其缓释性能研究[D]. 北京: 中国农业科学院, 2013.
ZHU X Y. Study on ememactin benzoate PLA microsphere and its controlled-release property[D]. Beijing: Chinese Academy of Agricultural Sciences, 2013. |
| [19] | LAWRIE G, KEEN I, DREW B, et al. Interactions between alginate and chitosan biopolymers characterized using FTIR and XPS[J]. Biomacromolecules, 2007, 8(8): 2533–2541. doi:10.1021/bm070014y |
| [20] |
宋丽敏, 李明, 倪雅欣, 等. 高效氯氰菊酯/海藻酸钠/壳聚糖凝胶微球的制备[J]. 应用化工, 2016, 45(11): 2118–2120.
SONG L M, LI M, NI Y X, et al. Preparation of beta-cypermethrin/sodium alginate/chitosan hydrogel microspheres [J]. Appl Chem Indust, 2016, 45(11): 2118–2120. |
| [21] | NATRAJAN D, SRINIVASAN S, SUNDAR K, et al. Formulation of essential oil-loaded chitosan–alginate nanocapsules[J]. J Food Drug Anal., 2015, 23(3): 560–568. doi:10.1016/j.jfda.2015.01.001 |
| [22] |
李凤红, 相丽英, 宣天义, 等. 反相乳液法制备海藻酸钠/壳聚糖纳米微球[J]. 化工新型材料, 2016, 44(12): 106–108.
LI F H, XIANG L Y, XUAN T Y, et al. Preparation of sodium alginate/chitosan nanosphere in reverse emulsion[J]. New Chem Mater, 2016, 44(12): 106–108. |
| [23] | SIEPMANN J, SIEPMANN F. Mathematical modeling of drug delivery[J]. Int J Pharm, 2008, 364(2): 328–343. doi:10.1016/j.ijpharm.2008.09.004 |
| [24] | SARKAR D J, KUMAR J, SHAKIL N A, et al. Release kinetics of controlled release formulations thiamethoxam employing nano-ranged amphiphilic PEG and diacid based block polymers in soil[J]. J Environ Sci Health, Part A, 2012, 47(11): 1701–1712. doi:10.1080/10934529.2012.687294 |
 2017, Vol. 19
2017, Vol. 19


