2. 浙江大学 原子核农业科学研究所, 杭州 310029
2. Institute of Nuclear Agricultural Sciences, Zhejiang University, Hangzhou 310029, China
毒氟磷 (Dufulin) 是贵州大学精细化工研究开发中心创制的具有知识产权的新型植物抗病毒剂品种,于2015年12月在中国获得正式登记[1-3],其属于含氟α-氨基膦酸酯类化合物,对烟草、水稻、黄瓜和番茄等植物的病毒病具有良好防效[3]。毒氟磷可能是通过激活HrBP1蛋白而触发水杨酸信号通路,从而激活植物宿主的抗病毒反应[4]。30%毒氟磷可湿性粉剂对鱼类、蜂类、鸟类和家蚕均为低毒[5]。关于毒氟磷在植物中的吸收、分布、转移、残留及其在水体和土壤中环境行为等研究,目前仅限于色谱法或色谱-质谱联用法对母体化合物的检测,而极少涉及其代谢/降解物[6-10]。迄今,对毒氟磷的代谢过程和环境行为等仍缺乏深入的研究。
在国际新农药的创制过程中,对新药的代谢途径、作用机理、环境行为与归宿等研究,大多借助了放射性同位素示踪技术。放射性同位素示踪技术具有痕量精准、溯源追踪和直观简便等独特优势,是其他任何技术所不可替代的[11]。因此,在国际经合组织、欧盟、美国、日本等国家或组织的农药代谢和残留评价方法中均明确指出:农药代谢降解研究需首先考虑同位素示踪法[12-14]。
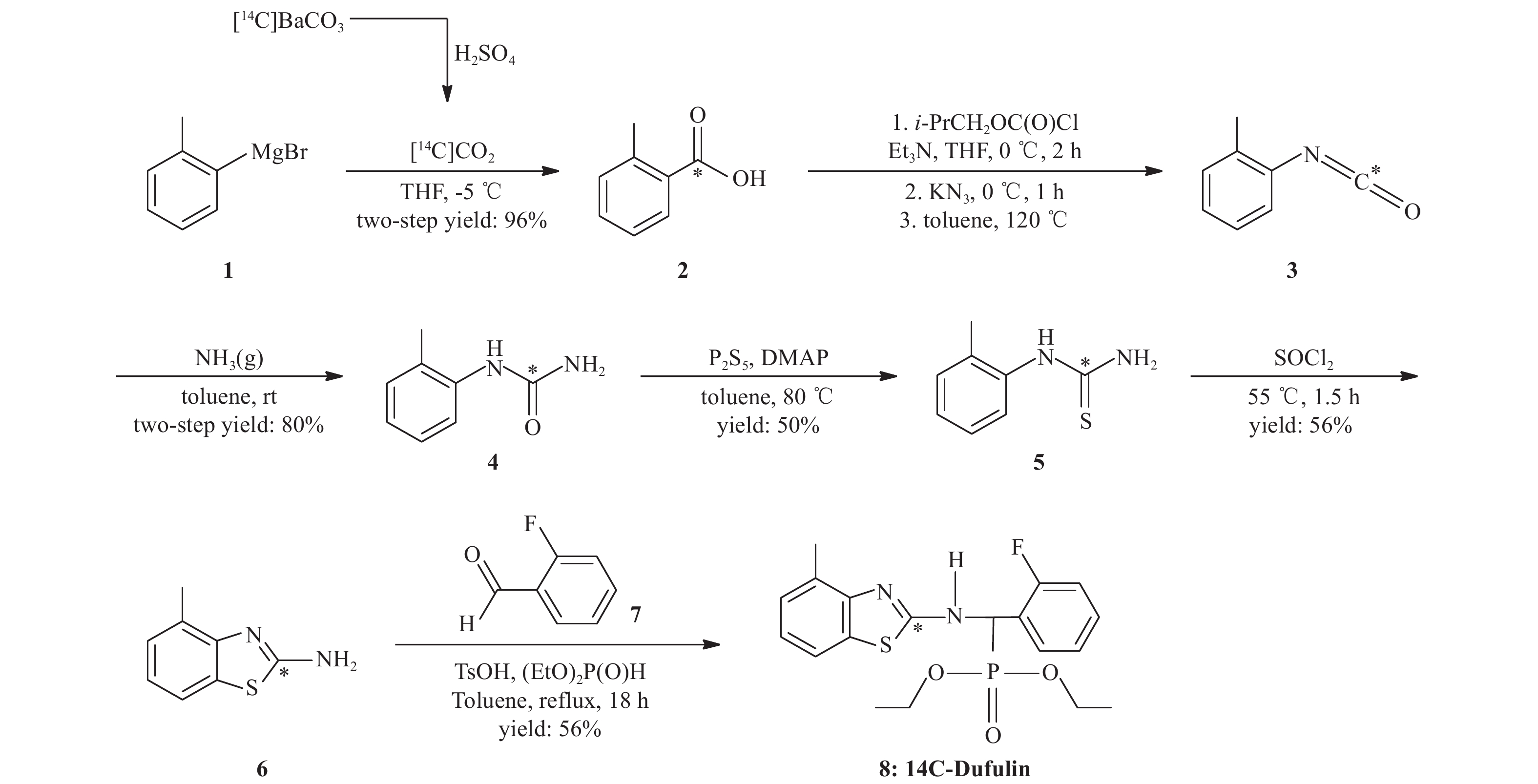
为满足国际农药安全评判试验标准和登记要求,助推毒氟磷走向国际市场,开展毒氟磷在生物 (植物、哺乳动物和家禽) 体内的代谢及其在土壤中的环境行为等研究,必须借助于放射性同位素示踪技术,而放射性同位素标记的毒氟磷是开展上述示踪研究所必需的示踪剂。本文首次报道作为示踪剂使用的用放射性同位素碳-14标记的毒氟磷的设计、合成与分析 (见图式 1)。
|
图式1 放射性同位素碳-14标记毒氟磷 (8) 的合成路线 (*表示碳-14标记位置) Scheme1 Synthetic route of radioisotope carbon-14 labelled Dufulin (8, * indicates carbon-14 labelled site) |
1 实验部分 1.1 试剂与仪器
放射性[14C]碳酸钡 (比活度58.0 mCi/mmol,放化纯度99.9%),美国ARC公司;闪烁体2,5-二苯基鰁唑 (HPLC纯度 > 99.0%) 和1,4-双 (5-苯基-2-鰁唑) 苯 (HPLC纯度 > 98.0%),均购自日本TCI公司;闪烁液Optiphase HiSafe 3,美国PE公司;HPLC和HPLC-MS用甲醇、乙腈分别为色谱级和质谱级,美国Fisher Scientific公司;毒氟磷 (Dufulin) 标样,用工业品经多次重结晶自行制备,由上海启甄环境科技有限公司代谢安全评价中心GLP实验室分析认可;其他试剂均为市售分析纯,溶剂按照文献方法纯化[15]。
Varian 400 MHz核磁共振仪 (以TMS为内标);安捷伦7890B-5977B气相色谱-质谱联用系统;Waters Alliance e2695 HPLC-Acquity QDa MS/2489 UV联用系统;Waters Alliance e2695 HPLC-AIM ν.ARC FSA/Waters 2998 PDA/Waters Acquity QDa MS联用系统 (FSA与PDA并联;MS串联于PDA后);Waters 2545 HPLC-2998 PDA制备液相色谱系统;Waters fraction collector III; PerkinElmer Tri-Carb 4910TR液体闪烁测量仪;Typhoon FLA9500 IP多功能激光成像仪;Milli-Q Reference S. Kit (18.2 MΩ/cm, 25 ℃) 超纯水制备系统;Sartorius BSA22 4S-CW (1 mg) 和BT25S (0.01 mg) 电子天平。以上仪器均通过3Q认证和上海市计量测试技术研究院校准。
1.2 放射性同位素标记化合物的合成 1.2.1 邻甲基苯[14C]甲酸 (2)在氩气保护下,将干燥的集成式微型放射性二氧化碳反应系统 (包含二氧化碳发生器、气体压力缓冲器、微型干燥器、二氧化碳反应器、微型气体循环泵、玻璃旋塞和连接管线等功能单元) 固定在铁架上。向二氧化碳发生器中加入[14C]碳酸钡 (434 mg,126.3 mCi,58.0 mCi/mmol);最后将系统所有管口密封严实。
将反应系统中各功能单元加热 (250 ℃),反复抽真空-充氩气操作5次。排除空气完毕,在加热条件下用油泵抽真空至反应系统内压力 (0.07 Pa) 不再下降,关闭系统的所有旋塞,使系统处于高真空状态,自然冷却至室温。
向二氧化碳反应器中加入含邻甲苯基溴化镁的四氢呋喃 (THF) 溶液 (1, 1 mol/L, 4.4 mL) 和无水THF(14 mL)。将二氧化碳发生器和二氧化碳反应器分别冷却至 –10 ℃,启动电磁搅拌,向二氧化碳发生器中缓慢滴加脱除CO2的浓硫酸 (8 mL),产生的[14C]CO2经微型干燥器 (P2O5) 干燥后进入二氧化碳反应器与格氏试剂 (1) 反应。待二氧化碳反应器液面无明显气泡溢出时,接通二氧化碳反应器和二氧化碳发生器之间气体回路上的旋塞,启动微型气体循环泵,将二氧化碳发生器升温至50 ℃;向系统补充适量的干燥氩气,以运载系统中残余的[14C]CO2与格氏试剂反应。经气相色谱-质谱 (GC-MS) 和气体放射性检测,氩气循环2 h后[14C]CO2彻底消耗。以氢氧化钠溶液淬灭反应,调节溶液pH至13,在45 ℃下减压脱除反应混合液中的THF,余液加水至80 mL,用甲基叔丁基醚 (60 mL) 萃取除去杂质。以盐酸调节水相pH至2~3,乙酸乙酯萃取 (80 mL × 6),合并有机相,用饱和食盐水洗涤,无水硫酸钠干燥,过滤,减压浓缩得白色固体 (2,288 mg,121.1 mCi,两步反应收率为96%)。重复该反应2次;共累积865 mg/360.0 mCi邻甲基苯[14C]甲酸 (2)。1H NMR (400 MHz,DMSO-d6),δ:12.80 (s, 1H), 7.82 (d, J = 7.6 Hz, 1H), 7.45 (t, J = 7.4 Hz, 1H), 7.29 (t, J = 8.3 Hz, 2H), 2.52 (s, 3H)。ESI-MS,m/z:139[M+H]+,161[M+Na]+。
1.2.2 [异氰基-14C]异氰酸邻甲苯酯 (3)在氩气保护下,将含邻甲基苯[14C]甲酸 (2, 281 mg, 118.1 mCi) 的无水THF溶液 (10 mL) 冷却至0~5 ℃,搅拌,加入无水三乙胺 (253 mg,2.5 mmol) 和氯甲酸异丁酯 (342 mg, 2.5 mmol),搅拌2 h, 体系变为白色浑浊[16]。用高效液相色谱-流动液体闪烁测量/二极管阵列检测器/质谱联用分析 (HPLC-FSA/PDA/MS,缩写为HFPM) 监测显示化合物2已完全转化;化合物2在HPLC-FSA色谱图、HPLC-UV色谱图中的保留时间 (因两者一致,故下文不再区分) 均为12.898 min。色谱条件:Diamonsil C18柱 (5 μm, 4.6 mm × 150 mm,美国迪马公司),流速0.80 mL/min,波长254 nm,进样量10 μL;梯度洗脱 (min/%A) 控制:0/10, 5/10, 18/100, 20/100。A为甲醇,B为0.1%甲酸水溶液。
在避光和0~5 ℃下,向白色浑浊液中加入饱和KN3 (260 mg,3.2 mmol) 水溶液 (1 mL),搅拌1 h。向反应体系加入碎冰-水 (50 mL),以甲基叔丁基醚(MTBE)萃取 (60 mL × 5),合并有机相,用饱和食盐水洗涤,无水硫酸钠充分干燥,抽滤。滤液减压浓缩至2~3 mL,向其中加入无水甲苯 (15 mL),在35 ℃水浴中继续减压浓缩直至体积不再减少。HFPM监测表明,无水甲苯溶液中放射性物质仅有酰基叠氮化合物。
在避光、氩气保护和搅拌下,将浓缩液升温至120 ℃,逸出N2,搅拌2 h。HFPM监测显示酰基叠氮化合物完全转化。将产物[异氰基-14C]异氰酸邻甲苯酯 (3) 无水甲苯溶液冷却后直接用于下一步反应。
1.2.3 邻甲苯基[14C]脲 (4)在室温下,用干燥氨气充分置换1.2.2节中得到[异氰基-14C]异氰酸邻甲苯酯 (3) 无水甲苯溶液装置中的气体,化合物3与氨气在搅拌下迅速反应而析出白色固体,再搅拌1 h[17]。HFPM监测显示,反应体系仅有1个放射性组分 (4),其保留时间为6.477 min。色谱条件:梯度洗脱 (min/%A) 控制:0/20, 5/20, 10/100, 20/100;其余条件同1.2.2节。过滤反应液,以正戊烷 (10 mL × 3) 洗除滤饼中残留的甲苯,滤饼用甲醇 (0 ℃) 溶解后抽滤,减压浓缩得白色固体 (4,254 mg,96.9 mCi,两步反应收率为80%)。重复由 (2) 制备 (4) 2次;共累积722 mg/275.5 mCi邻甲苯基[14C]脲 (4)。1H NMR (400 MHz, DMSO-d6),δ:7.78 (d, J = 8.1 Hz, 1H), 7.66 (s, 1H), 7.14-7.04 (m, 1H), 6.92-6.83 (m, 1H), 5.99 (s, 2H), 2.18 (s, 3H)。ESI-MS,m/z: 153[M+H]+。
1.2.4 邻甲苯基[14C]硫脲 (5)在氩气保护和搅拌下,将邻甲苯基[14C]脲 (4, 240 mg, 91.6 mCi)、DMAP(98 mg, 0.8 mmol)、P2S5(860 mg, 3.84 mmol) 和无水甲苯 (10 mL) 的混合物升温至80 ℃,搅拌5 h[18]。HFPM监测显示化合物4彻底消耗,目标物5的保留时间为7.316 min,色谱条件同1.2.3节。将体系温度降低至室温,加入碎冰-水 (70 mL),用乙酸乙酯萃取 (80 mL × 4),无水硫酸钠干燥,过滤,减压浓缩得粗产品,经硅胶柱层析 [V(二氯甲烷) : V(甲醇) = 40 : 1] 得淡黄色固体 (5, 132 mg, 45.6 mCi, 50%)。重复该反应2次;共累积353 mg/121.9 mCi邻甲苯基[14C]硫脲 (5)。1H NMR (400 MHz, DMSO-d6),δ:9.21 (s, 1H), 7.27-7.12 (m, 2H),2.18 (s, 3H)。ESI-MS,m/z: 169[M+H]+。
1.2.5 2-氨基-4-甲基苯并[2-14C]噻唑 (6)在氩气保护下,将邻甲苯基[14C]硫脲 (5, 351 mg, 121.2 mCi) 和重蒸二氯亚砜 (4 mL) 混合物升温至55 ℃,搅拌2 h。HFPM监测显示化合物5彻底消耗,目标物6的保留时间为4.401 min,色谱条件同1.2.3节。反应降至室温,加入碎冰-水 (70 mL),再缓慢加入碳酸氢钠粉末至水相呈碱性,乙酸乙酯萃取 (50 mL × 4);所得有机相依次用稀盐酸 (0.05 mol/L, 50 mL)、水 (40 mL × 3) 反萃取;以碳酸氢钠粉末调节所得水相pH至9~10,乙酸乙酯萃取 (50 mL × 4),无水硫酸钠干燥,过滤,减压浓缩得白色固体 (6, 195 mg, 68.1 mCi, 56%)。1H NMR (400 MHz, CDCl3),δ:7.44 (d,J = 7.8 Hz,1H),7.15-7.10 (m,1H),7.07-7.00 (m,1H)。5.53 (s, 2H)。2.56 (s, 3H)。ESI-MS,m/z: 167[M+H]+。
1.2.6 N-[2-(4-甲基苯并[2-14C]噻唑基)]-2-氨基-2-氟代苯基-O, O-二乙基甲基膦酸酯 (8, 14C-毒氟磷)在氩气保护下,将2-氨基-4-甲基苯并[2-14C]噻唑 (6, 194 mg, 67.8 mCi) 无水甲苯 (8 mL) 溶液、邻氟苯甲醛 (220 mg, 1.77 mmol) 和亚磷酸二乙酯 (278 mg, 2.01 mmol) 依次加入无水硫酸钠 (1 344 mg, 9.46 mmol, 在350 ℃预干燥2 h)、无水对甲苯磺酸 (12 mg, 0.06 mmol) 和无水甲苯 (8 mL) 的混合物中,搅拌,升温至120 ℃,回流16 h[3]。HFPM监测显示化合物6彻底消耗,目标物8的保留时间为16.448 min,色谱条件同1.2.2节。将反应冷却至室温,过滤,滤饼用无水甲醇洗涤至无明显放射性。滤液减压浓缩得粗品,采用高效液相色谱纯化得白色固体 (8, 271 mg,38.3 mCi, 56 %)。色谱条件:xBridge Prep C18柱 (10 μm, 150 mm × 19 mm; Waters Co., MA, USA),流速9.00 mL/min,波长254 nm,进样量600 μL;梯度洗脱 (min/%A) 控制:0/60, 5/60, 10/100, 15/100, 20/60, 25/60;A为乙腈,B为水。收集保留时间为11.48~13.72 min组分 (8)。1H NMR (400 MHz, CDCl3),δ:7.65-7.54 (m, 1H), 7.38 (d, J = 7.7 Hz, 1H), 7.32-7.26 (m, 1H), 7.17-7.04 (m, 3H), 6.98 (t, J = 7.5 Hz, 1H), 5.77 (d, J = 22.7 Hz, 1H), 4.31-4.16 (m, 2H), 4.07-3.96 (m, 1H), 3.92-3.79 (m, 1H), 2.52 (s, 3H), 1.33 (d, J = 7.0 Hz, 2H), 1.13 (t, J = 6.8 Hz, 3H)。ESI-MS,m/z: 411[M+H]+,433[M+Na]+。
1.3 同位素标记化合物的质量指标分析 1.3.1 放化纯度的测定准确称取5.10 mg标记物8,用甲醇溶解并在50.00 mL容量瓶中配成质量浓度为102 μg/mL的溶液,然后分别稀释至10和0.01 μg/mL保存备用。另配制毒氟磷标样20 μg/mL丙酮溶液。
1.3.1.1 TLC-IIA法将标记物8的甲醇溶液 (2.00 mL,10 μg/mL) 转至浓缩管,转入氮吹仪浓缩至干,再以1mL丙酮溶解作为试样。将试样和毒氟磷标样在硅胶薄板 (5 cm × 20 cm) 底端约1 cm高度处在4 个位置依次均匀点样 (试样、标样、试样、标样),保持斑点直径不超过3 mm。将此硅胶板在层析缸中展开[V(乙酸乙酯) : V(石油醚) = 1 : 2]后,挥干溶剂,将硅胶板在多功能激光成像仪中进行同位素成像分析 (IIA, Isotope Imaging Analysis)[19]。据此计算化合物8的放化纯度。
1.3.1.2 HPLC-LSC法取标记物8溶液 (10 μL, 0.01 μg/mL) 进行HPLC-PDA分析,洗脱液用自动收集器收集于闪烁瓶;收集16.650~17.330 min洗脱组分。向收集洗脱液中加入10 mL闪烁液 (按照文献方法配置,避光保存24 h后使用),混匀,避光12 h后以液体闪烁测量仪 (LSC, Liquid Scintillation Counter) 测量其放射性活度 (Ae)[19]。重复6次。取标记物8溶液 (10 μL, 0.01 μg/mL) 加入闪烁瓶,同法加10 mL闪烁液后测定其放射性活度 (A0)。重复6次。色谱条件:波长270 nm,流速1.00 mL/min,梯度洗脱 (min/%A) 控制:0/35, 18/100, 20/100, 23/35, 25/35. A为甲醇,B为0.1%甲酸水溶液;其余条件同1.2.2节。标记物8的保留时间为16.860 min。
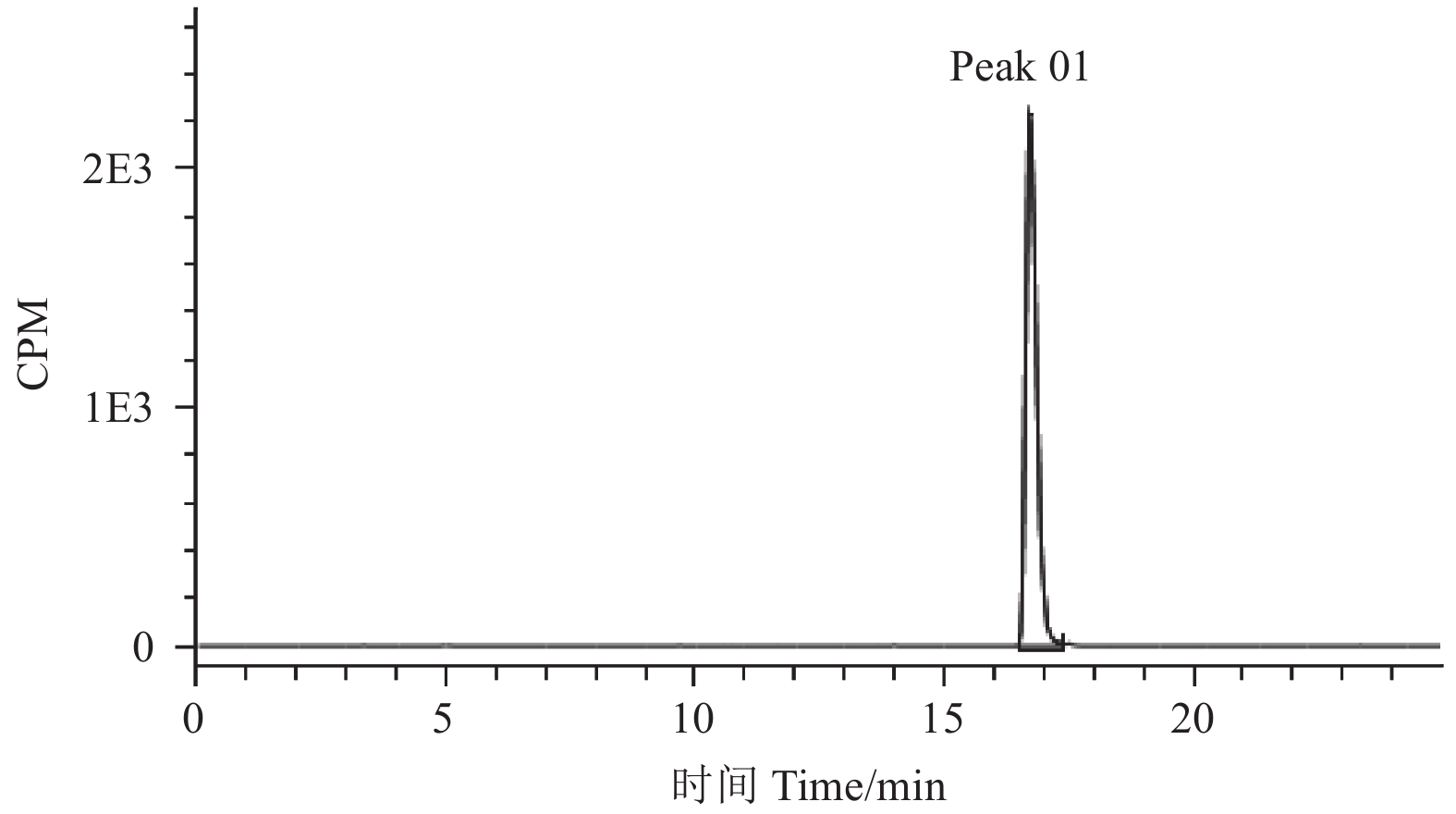
1.3.1.3 HPLC-FSA法将标记物8溶液进行HFPM分析。HPLC柱后洗脱液分别进入流动液体闪烁测量仪 (FSA, Flow Scintillation Analyzer) 和PDA检测器,分流比为1 : 1;进入FSA检测器中洗脱液与Optiphase HiSafe 3闪烁液的流速比为1 : 8。分析结果见图1和2。根据HPLC-FSA色谱图以面积归一法计算8的放化纯度。色谱条件同1.3.1.2节。
|
图 1 目标物碳-14标记毒氟磷 (8) 的HPLC-FSA色谱图 Fig. 1 HPLC-FSA chromatogram of the carbon-14 labelled Dufulin (8) |
|
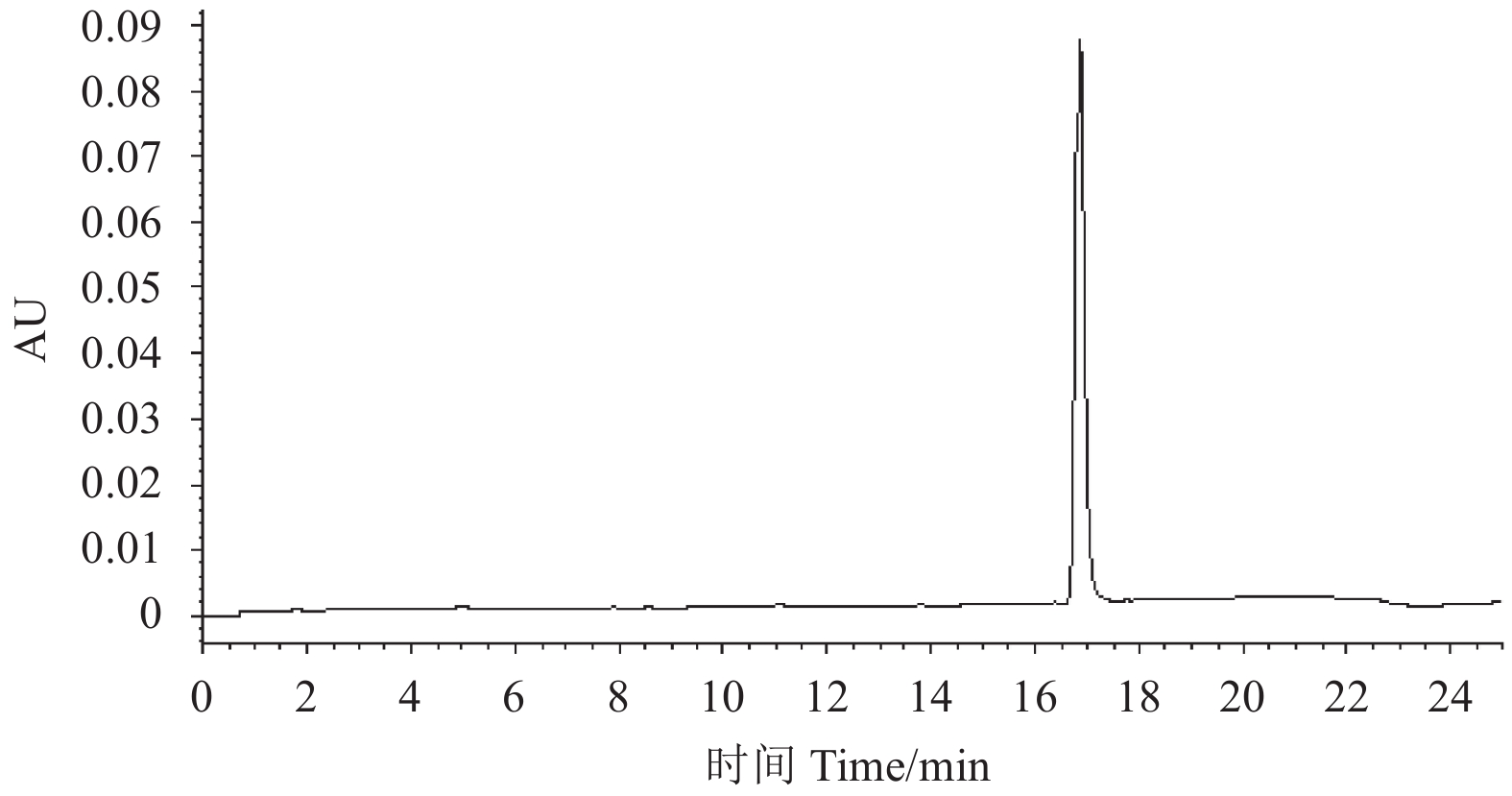
图 2 目标物碳-14标记毒氟磷 (8) 的HPLC-UV图 (270 nm) Fig. 2 HPLC-UV chromatogram of the carbon-14 labelled Dufulin (8, 270 nm) |
1.3.2 化学纯度的测定
根据1.3.1.3节中所得HPLC-UV色谱图 (图2),以面积归一法计算标记物8的化学纯度。
1.3.3 比活度的测定用微量注射器精确移取标记物8溶液 (10 μL, 0.01 μg/mL) 加入闪烁瓶中,再加入10 mL闪烁液,混匀;重复6次。将闪烁瓶避光保存24 h后用LSC测量其放射性活度,据此计算 (8) 的比活度[19]。
2 结果与讨论在前期冷反应条件下优化反应工艺和摸索放射性毒氟磷合成试验的基础上,以[14C]碳酸钡为放射性原料,通过格氏反应、Curtius重排、亲核加成、硫代、关环等7步反应,制备了高比活度标记物8纯品,7步反应的放化收率/化学收率为10%。标记物8的 1H NMR分析数据与毒氟磷的结构相符;其ESI-MS分析数据显示,8的相对分子质量为410,比毒氟磷的相对分子质量大2,这也与8的结构相符。表明标记物8就是14C-毒氟磷 (N-[2-(4-甲基苯并[2-14C]噻唑基)]-2-氨基-2-氟代苯基-O, O-二乙基甲基膦酸酯)。HPLC-FSA色谱图中放射性色谱峰 (保留时间16.79 min,图1) 与HPLC-UV色谱图中8对应的色谱峰 (保留时间16.847 min,ESI-MS,m/z : 411[M+H]+;图2) 一致,这进一步验证了标记物8即14C-毒氟磷。
为了确保标记物8质量指标的可靠性,本研究分别采用TLC-IIA、HPLC-LSC和HPLC-FSA 3种方法对其放化纯度进行了测定,所得结果分别为100%、98.4%和99.2%。HPLC-PDA分析表明,8的化学纯度为98.7%;LSC分析表明,8的比活度为58.0 mCi/mmol。因而,所得标记物8的质量指标满足下游同位素示踪的要求,可作为放射性示踪剂,用于毒氟磷的代谢和环境行为等研究。
在农药放射性同位素标记合成时,首先要考虑标记位置和标记原子的选择。用于农药代谢和环境行为等研究的同位素示踪剂通常标记在标记原子不易脱落的位置,且优先考虑以碳-14标记[19-22]。毒氟磷分子含2个芳环片段,从化学稳定性、代谢稳定性和毒理学重要性的角度考虑,最理想的标记位置是对毒氟磷分子中2个苯环分别以碳-14标记;但这两种标记物对应的合成路线较长,费用极高,合成周期很长,风险高。毒氟磷分子中噻唑环属于芳香环,具有一定稳定性,故本研究选择噻唑环中2位碳原子标记。该方案以便宜易得的[14C]碳酸钡为放射性同位素原料,合成路线相对较短,因而具有一定的可行性。
本研究以[14C]碳酸钡为起始原料,实验过程中放射性物质用量较大,受国家辐射安全与防护标准的限制,部分高活度放射性物质参与的反应须分批进行。在本研究中,将[14C]碳酸钡高效地转化为邻甲基苯[14C]甲酸 (2) 是制备14C-毒氟磷 (8) 的关键。在此反应中,必须将[14C]碳酸钡完全转化为[14C]CO2,并确保剧毒[14C]CO2与格氏试剂 (1) 在足够小的反应器中被彻底转化。为确保安全和减少放射性物质损失,笔者在前期设计制作的微型放射性二氧化碳反应系统基础上,改进并制作了集成式微型放射性二氧化碳反应系统,新系统容积更小 (48 mL),有效减少了放射性物质挂壁损失。利用新系统以96%产率获得了邻甲基苯[14C]甲酸 (2)。
在制备异氰酸酯时,通常将羧酸转化为酰氯或者混酐,以叠氮化试剂将其转化为酰基叠氮化合物,或者将羧酸用叠氮磷酸二苯酯直接转化为酰基叠氮化合物;酰基叠氮化合物在避光、加热条件下脱氮气转化为异氰酸酯。结合放射合成的特点和要求,通过在冷反应条件下对上述反应方法的筛选及反应条件优化,利用氯甲酸异丁酯将化合物2转化为混酐,再与叠氮化钾反应转化为较稳定的酰基叠氮化合物,经加热转化为活泼的[异氰基-14C]异氰酸邻甲苯酯 (3),与氨气迅速反应转化为邻甲苯基[14C]脲 (4)[16]。
中间体4的硫化是影响14C-毒氟磷合成总收率的主要反应。在冷反应条件下,P2S5能高效地将邻甲苯基脲硫化,而Lawesson试剂、三氯硫磷等反应效果较差,不适合用于标记合成[18]。在放射合成中,P2S5将化合物4成功转化为邻甲苯基[14C]硫脲 (5)。
3 结论以[14C]碳酸钡为放射性同位素原料,通过7步反应制备了放射性同位素碳-14标记的毒氟磷 (N-[2-(4-甲基苯并[2-14C]噻唑基)]-2-氨基-2-氟代苯基-O, O-二乙基甲基膦酸酯,38.3 mCi),反应的总放化收率/化学收率为10%。标记物的化学纯度、放化纯度均超过98%,其比活度为58.0 mCi/mmol。该标记物可作为放射性示踪剂,用于毒氟磷的代谢和环境行为等研究。
| [1] |
第八届全国农药登记评审委员会第十八次全体会议纪要[J]. 今日农药, 2016(2): 11-13.
The summary of the 18th plenary meeting of the 8th national pesticide registration review committee[J]. Agrochem Today, 2016(2): 11-13. |
| [2] |
陈卓, 杨松. 自主创制抗植物病毒新农药: 毒氟磷[J]. 世界农药, 2009, 31(2): 52–53.
CHEN Z, YANG S. Dufulin: a novle plant antiviral agent developed independently[J]. World Pestici, 2009, 31(2): 52–53. |
| [3] | SONG B A, JIN L, YANG S, et al. Environment-friendly antiviral agents for plants[M]. Beijing: Chemical Industry Press, 2010: 207. |
| [4] | CHEN Z, ZENG M J, SONG B A, et al. Dufulin activates HrBP1 to produce antiviral responses in tobacco[J]. PLoS One, 2012, 7(5): e37944. doi:10.1371/journal.pone.0037944 |
| [5] |
范会涛, 李向阳, 陈卓, 等. 30%毒氟磷可湿性粉剂对环境生物的毒性与安全性评价[J]. 农药, 2011, 50(1): 48–50, 52.
FAN H T, LI X Y, CHEN Z, et al. Toxicity and safety evaluation of Dufulin 30% WP to the environmental biology[J]. Agrochemicals, 2011, 50(1): 48–50, 52. |
| [6] |
向章敏. 毒氟磷消旋体及R(S)对映体在烟草上的吸收、分布和转移[D]. 贵阳: 贵州大学, 2008.
XIANG Z M. The uptake, distribution and translation of Dufulin racemate and R(S)-enantiomer in Nicotiana tabacum[D]. Guiyang: Guizhou University, 2008. |
| [7] |
丁立平, 方祥, 吴文凡. 固相萃取-气相色谱-质谱联用法测定黄瓜和番茄中毒氟磷的残留及其裂解机理[J]. 农药学学报, 2013, 15(5): 523–527.
DING L P, FANG X, WU W F. Determination of Dufulin residues in cucumber and tomato by gas chromatography-mass spectrometry with solid phase extraction and its fragmentation mechanism[J]. Chin J Pestic Sci, 2013, 15(5): 523–527. |
| [8] |
卢平, 李艳娇, 丁晓燕. 新型抗植物病毒剂毒氟磷的酶联免疫分析方法[J]. 农药, 2014, 53(11): 802–805.
LU P, LI Y J, DING X Y. The Immunoassay method for the detection of Dufulin[J]. Agrochemicals, 2014, 53(11): 802–805. |
| [9] |
樊玲娥. 新农药毒氟磷的水环境化学行为研究[D]. 贵阳: 贵州大学, 2008.
FANG L E. Study on the chemical behavior of Dufulin in water[D]. Guiyang: Guizhou University, 2008. |
| [10] | WANG H Z, ZUO H G, DING Y J, et al. Biotic and abiotic degradation of pesticide Dufulin in soils[J]. Environ Sci Pollut Res, 2014, 21(6): 4331–4342. doi:10.1007/s11356-013-2380-8 |
| [11] | VOGEL H G, MAAS J, GEBAUER A. Drug discovery and evaluation: methods in clinical pharmacology[M]. Berlin: Springer, 2011. |
| [12] |
经济合作与发展组织化学品测试准则编译委员会. 经济合作与发展组织化学品测试准则[M]. 北京: 中国农业出版社, 2013: 1367.
Compilation and translation committee of OECD guidelines for the testing of chemicals. OECD guidelines for the testing of chemicals[M]. Beijing: China Agriculture Press, 2013: 1367. |
| [13] |
贾明宏, 李本昌. 农药学研究的重要手段——放射性同位素示踪技术[J]. 农药科学与管理, 1996(4): 14–19.
JIA M H, LI B C. Important method for research pesticide science-radioisotope tracer techniques[J]. Pestic Sci Admin, 1996(4): 14–19. |
| [14] | IAEA. Quantification nature and bioavailability of bound 14C-pesricide residue in soil, plants and food[M]. Vienna: International Atomic Energy Agency, 1986: 155-182. |
| [15] | ARMAREGO W L F, CHAI C L L. Purification of laboratory chemicals[M]. 7th ed. Boston: Butterworth-Heinemann, 2012. |
| [16] | TROUCHE N, WIECKOWSKI S, SUN W M, et al. Small multivalent architectures mimicking homotrimers of the tnf superfamily member CD40L: delineating the relationship between structure and effector function[J]. J Am Chem Soc, 2007, 129(44): 13480–13492. doi:10.1021/ja073169m |
| [17] | SANABRIA C M, DO CASAL M T, DE SOUZA R B A, et al. Highly regioselective iodination of N-phenylureas with iodine/trichloroisocyanuric acid [J]. Synthesis, 2016, 49(7): 1648–1654. doi:10.1055/s-0036-1588370 |
| [18] | ALAWODE O E, ROBINSON C, RAYAT S. Clean photodecomposition of 1-methyl-4-phenyl-1H-tetrazole-5(4H)-thiones to carbodiimides proceeds via a biradical [J]. J Org Chem, 2011, 76(1): 216–222. doi:10.1021/jo1019859 |
| [19] |
杨征敏, 叶庆富, 唐庆红, 等. 新型除草剂丙酯草醚A环 14C均标记合成和鉴定
[J]. 化学学报, 2005, 63(21): 1999–2003.
YANG Z M, YE Q F, TANG Q H, et al. Radiolabeled synthesis and identification of a novel herbicide, propyl 4-[2-(4, 6-dimethoxy-2-pyrimidinyloxy)benzylamino]benzoate with all six benzoic ring carbons labeled by 14C [J]. Acta Chimica Sinica, 2005, 63(21): 1999–2003. doi:10.3321/j.issn:0567-7351.2005.21.010 |
| [20] | YANG Z M, YE Q F, LU L. Synthesis of herbicidal ZJ0273 labeled with tritium and carbon-14[J]. J Label Compd Radiopharm, 2008, 51(4): 182–186. doi:10.1002/(ISSN)1099-1344 |
| [21] | YANG Z M, WANG W, HAN A L, et al. Determination of herbicide ZJ0273 residue in rapeseed by radioisotopic tracing method[J]. Food Chem, 2009, 114(1): 300–305. doi:10.1016/j.foodchem.2008.08.095 |
| [22] | YANG Z M, JI Z Q, YE Q F, et al. Synthesis of 6β-([1-14C]propoxy)celangulin V [J]. J Label Compd Radiopharm, 2008, 51(2): 109–112. doi:10.1002/(ISSN)1099-1344 |
 2017, Vol. 19
2017, Vol. 19


