三嗪类除草剂为均三氮苯类除草剂,广泛应用于预防杂草生长。目前,中国茶园中登记的三嗪类除草剂有西玛津、扑草净、莠去津等,由于该类除草剂用量较大、水溶性较强、化学性质稳定且残留时间较长,使用后可能会对农作物、土壤、水源等造成污染 [1-4]。有研究发现,莠去津、西玛津等三嗪类除草剂能干扰和破坏生物体的内分泌系统及免疫系统[5]。近年来,随着对食品安全要求的提高,中国对植物源食品中三嗪类除草剂的残留制定了严格的限量标准,规定西玛津、莠去津等三嗪类除草剂的最大残留限量 (MRL) 值为20~500 μg/kg[6]。
多壁碳纳米管 (MWCNTs) 是由多个碳六元环组成的类似石墨的纳米级中空管,与石墨化碳相比比表面积更大,改性后的多壁碳纳米管在有机溶剂中具有良好的分散性。目前,多壁碳纳米管在农药、兽药残留分析检测中已有应用[7-8],采用多壁碳纳米管作为净化剂,以改进的QuEChERS方法净化,与传统的前处理方法相比,能够提高净化效率、节约成本。目前,三嗪类除草剂残留分析方法主要有气相色谱法、气相色谱-串联质谱法、液相色谱法及液相色谱-串联质谱法[9-16]。其中,气相色谱法和液相色谱法对于分离检测多种农药存在困难,液相色谱-串联质谱的成本较高,普及率较低,操作相对复杂。因此,开发一种高效、高灵敏度、成本较低的除草剂检测方法十分必要。本研究以多壁碳纳米管、N-丙基乙二胺 (PSA)、C18和MgSO4作为净化剂,以改进的QuEChERS方法萃取去除共提取物杂质,结合气相色谱-串联质谱检测技术,拟建立乌龙茶及土壤中10种三嗪类除草剂 (西玛津、莠去津、扑灭津、特丁津、敌草净、环丙津、西草净、莠灭净、扑草净和特丁净) 残留的分析方法。
1 材料与方法 1.1 仪器、药剂与试剂Shimadzu GC-MS/MS TQ8040气相色谱-串联质谱仪 (日本岛津公司);KQ-500DE超声仪 (昆山市超声仪器有限公司);Anke TDL-5-A离心机 (上海安亭科学仪器厂);涡旋振荡器 (德国IKA公司)。
西玛津 (simazine)、莠去津 (atrazine)、扑灭津 (propazine)、特丁津 (terbuthylazine)、敌草净 (desmetryn)、环丙津 (cyprazine)、西草净 (simetryn)、莠灭净 (ametryn)、扑草净 (prometryn) 和特丁净 (terbutryn) 标准品,纯度均 ≥ 96%,均购自Dr. Ehrenstorfer公司 (德国)。
乙腈、乙酸乙酯均为色谱纯 (Dikma,中国);丙酮 (色谱纯,国药集团化学有限公司);多壁碳纳米管 (直径10~20 nm,长度10~30 μm,纯度98%),(北京德科岛金公司);N-丙基乙二胺、C18(博纳艾杰尔科技公司)。
乌龙茶 (干样) 及土壤样品均采自福建安溪茶园,样品经粉碎后过20目筛,密封,备用。
1.2 试验方法1.2.1 标准溶液的配制及标准曲线的绘制
单标储备液:分别准确称取10 mg (精确至0.01mg) 各药剂标准品,用丙酮溶解并定容于10 mL容量瓶中,配成1 000 mg/L的单标储备液,于 –20 ℃保存。
混合标准工作液:分别移取0.1 mL单标储备液,用丙酮稀释并定容于10 mL容量瓶中,配成10 mg/L的混合标准工作液,于 –20 ℃保存。
空白基质匹配标准工作溶液:准确移取一定量的混合标准工作液,用空白样品提取液稀释为5、10、50、100、200、500 μg/L的系列工作液,配制成系列空白基质匹配标准溶液,现配现用。外标法定量。以峰面积为纵坐标,溶液质量浓度为横坐标,绘制工作曲线。
1.2.2 样品前处理 准确称取1.00 g样品于50 mL离心管中,依次加入3 mL饱和氯化钠溶液和5 mL乙腈,涡旋振荡后超声提取30 min,于5 000 r/min下离心5 min;取上清液,重复提取1次,合并上清液;取1 mL上清液于2 mL净化管 (包含15 mg MWCNTs、30 mg PSA、30 mg C18、150 mg MgSO4),漩涡振荡10 min,于5 000 r/min下离心5 min;取上清液,过0.22 μm滤膜,待GC-MS/MS分析。
1.2.3 色谱与质谱检测条件 色谱条件:Rxi-5 Sil MS色谱柱 (30 m × 0.25 mm, 0.25 μm);进样口温度250 ℃;柱温:柱温箱初始温度为60 ℃,以15 ℃/min升至200 ℃,保持2 min,再以10 ℃/min升至280 ℃,保持5 min;不分流进样;进样量1 μL;载气为高纯氦气 (99.999%),流速1 mL/min。
质谱条件:电子轰击离子源 (EI源);离子源电压70 eV;离子源温度200 ℃;接口温度250 ℃;溶剂延迟2.5 min;多反应监测模式 (MRM)。每种药剂分别选择1个定量离子对,2个定性离子对。10种待测组分的保留时间、定量离子、定性离子见表1。
|
|
表 1 10种三嗪类除草剂质谱信息 Table 1 Mass spectrum information for 10 triazine herbicides |
1.2.4 添加回收试验 称取样品,加入适量混合标准工作液,混匀静置10 min后,按1.2.2和1.2.3节的步骤进行样品前处理和分析测定。添加水平为 5、50 和 100 ug/kg,每个水平重复6次,并设空白对照。计算回收率和相对标准偏差 (RSD)。
2 结果与讨论 2.1 色谱、质谱检测方法的建立色谱条件的变化对分析物的峰形和灵敏度有影响。将单标溶液通过全扫模式逐一全扫后,确定各组分保留时间,采用程序升温,尽量将各种农药的保留时间分开,以消除相互干扰,进行不同时段的离子对扫描,以提高稳定性及重现性。对于保留时间相近的药剂,采用MRM模式进行扫描后,通过对离子对进行区分,可以实现对未完全分离的目标农药的定性与定量分析。
质谱条件的优化主要包括母离子、碰撞能量、扫描时间等。首先,将各个标准物质扫描后,选择响应较强、高质量端的碎片离子作为母离子,随后通过Smart Database MRM优化工具确定各组分的碎片离子信息及最优的碰撞电压,建立多反应监测模式 (MRM)。其次,选择合适的分段扫描窗口,根据保留时间设定每一分段的起始时间和结束时间,每个分段时间内尽量不要选择过多扫描通道,增加相应的采集点数,以提高分析准确性。最终创建了10种三嗪类除草剂的GC-MS/MS检测方法。10种除草剂的色谱-质谱图见图1,质谱信息见表1。
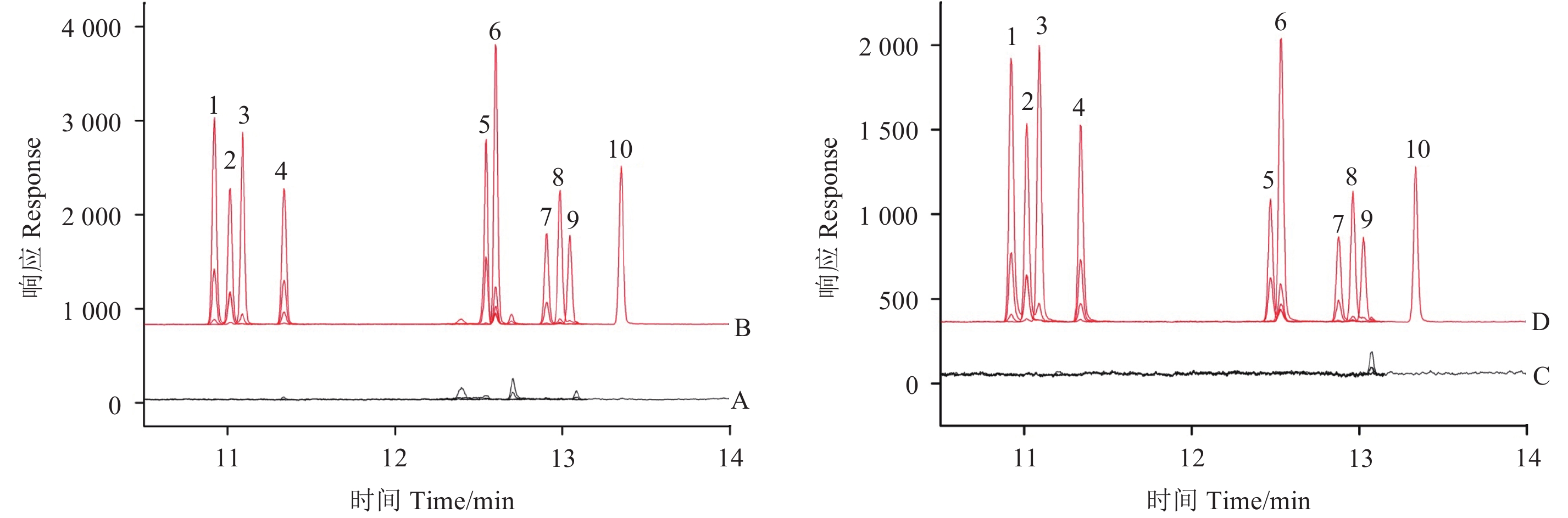
|
1. 西玛津simazine; 2. 莠去津atrazine; 3. 扑灭津propazine; 4. 特丁津terbuthylazine; 5. 敌草净desmetryn; 6. 环丙津cyprazine; 7. 西草净simetryn; 8. 莠灭净ametryn; 9. 扑草净prometryn; 10. 特丁净terbutryn 图 1 茶叶空白 (A)、茶叶空白样品添加 (10 μg/kg,B)、土壤空白 (C)、土壤空白样品添加 (10 μg/kg,D) 的总离子流色谱图 Fig. 1 TIC chromatogram of blank tea (A),the spiked blank tea samples (10 μg/kg,B),blank soil (C) and the spiked blank soil samples (10 μg/kg,D) |
2.2 前处理方法的优化
2.2.1 提取溶剂的优化 目前常用的农药提取溶剂主要有乙腈、丙酮、乙酸乙酯及其混合溶液等,三嗪类除草剂的极性较强,因此选择极性中等及以上的提取溶剂提取。本研究分别考察了乙腈、V (乙腈) : V (丙酮) = 1 : 1、V (乙腈) : V (乙酸乙酯) = 1 : 1和V (丙酮) : V (乙酸乙酯) = 1 : 1共4种不同提取溶剂在茶叶和土壤基质中对目标农药的提取效率,结果如图2所示。
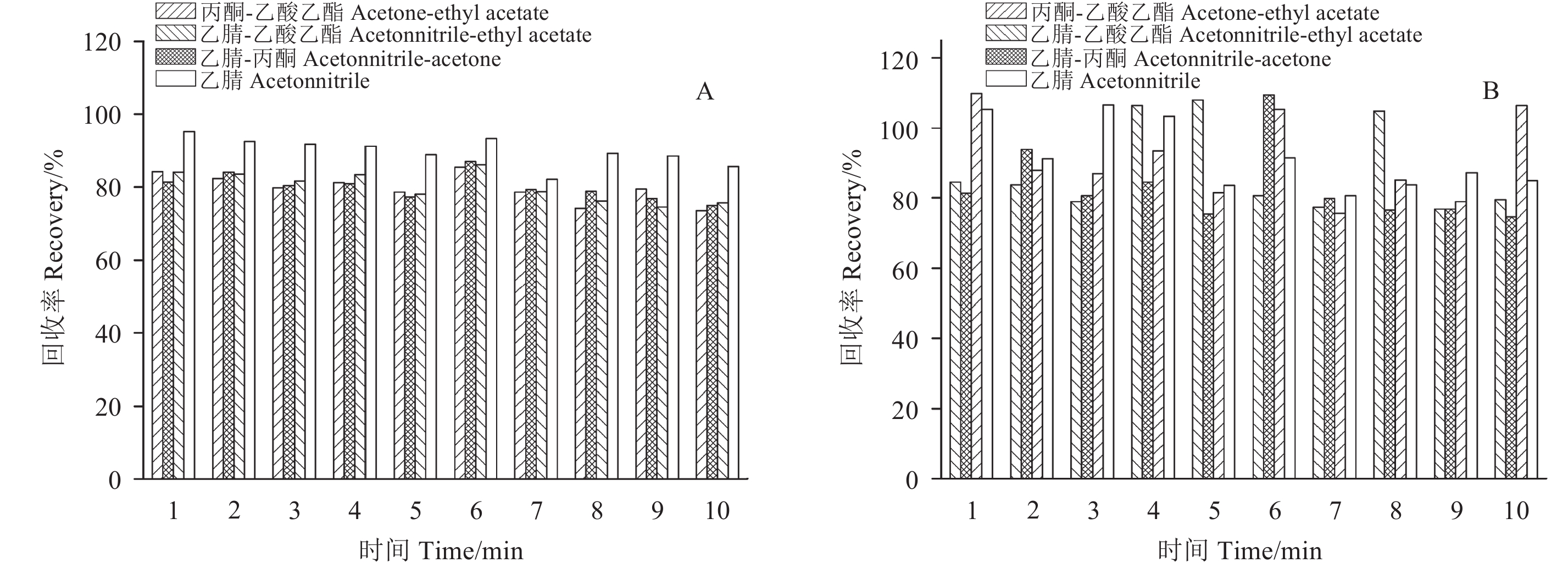
|
1. 西玛津simazine; 2. 莠去津atrazine; 3. 扑灭津propazine; 4. 特丁津terbuthylazine; 5. 敌草净desmetryn; 6. 环丙津cyprazine; 7. 西草净simetryn; 8. 莠灭净ametryn; 9. 扑草净prometryn; 10. 特丁净terbutryn 图 2 不同提取溶剂对茶叶 (A) 及土壤 (B) 中10种三嗪类除草剂添加回收率的影响 Fig. 2 Spiked recoveries of 10 triazine herbicides in the tea (A) and soil (B) samples extracted with different extraction solvents |
从图2可以看出:以乙腈为提取溶剂时,10种三嗪类除草剂在茶叶及土壤基质中的平均回收率在80%~120%之间,这可能是由于乙腈对此类农药的溶解度较大,且共提取物较少,故提取效果较好;而其余3种提取溶剂的提取效率均偏低,可能是这些提取溶剂的共提取物较多,产生了较强的基质效应,从而对目标物的响应产生抑制。综合考虑,最终选择乙腈为提取溶剂。
2.2.2 净化条件的优化 乌龙茶及其土壤基质比较复杂,含有大量杂质,对目标组分的定性与定量分析有干扰,因此需要对样品进行净化。PSA是弱阴离子交换吸附剂,可以去除样品基质中的脂肪酸、有机酸、酚类等,但其吸附色素能力有限;改性的MWCNTs比表面积大,吸附能力较高,可以有效吸附色素、脂肪酸等基质干扰成分;C18填料主要用于去除样品基质中脂类等弱极性干扰物等;GCB能够有效吸附色素、甾醇等干扰物[7];无水MgSO4能充分吸收基质中的水分。
为了有效去除有机酸、色素等杂质,本研究对MWCNTs、PSA、C18、GCB的含量进行了优化。固定离心管中无水硫酸镁的含量 (150 mg),在离心管中分别加入不同含量的MWCNTs、PSA、C18及GCB,得到含有不同净化剂的组合。
组合A:10 mg MWCNTs+30 mg PSA + 30 mg C18 + 150 mg MgSO4
组合B:15 mg MWCNTs+30 mg PSA + 30 mg C18 + 150 mg MgSO4
组合C:20 mg MWCNTs+30 mg PSA + 30 mg C18 + 150 mg MgSO4
组合D:15 mg GCB+30 mg PSA + 30 mg C18 + 150 mg MgSO4
组合E:15 mg MWCNTs + 150 mg MgSO4
组合F:30 mg PSA + 30 mg C18 + 150 mg MgSO4
按照1.2.2节的方法进行茶叶样品提取,提取液分别用以上组合净化。结果显示:茶叶样品经组合F净化后的提取液颜色最深,净化效果差;经组合A、D和E净化后的溶液颜色相差不大,但回收率明显低于组合B和C;经组合B和C净化后的溶液颜色及回收率相差不大,但组合B中MWCNTs的用量相对较少。土壤样品分别经上述6种组合净化后的溶液颜色差别不大。从图1可以看出,样品经净化后,在目标物出峰处基本无干扰。综合考虑,最终选择组合B (15 mg MWCNTs + 30 mg PSA + 30 mg C18 + 150 mg MgSO4) 作为净化剂。
2.3 方法的线性范围与灵敏度结果 (表2) 表明:西草净和扑草净在10~500 μg/kg ,其余8种药剂在5~500 μg/kg范围内线性关系良好,相关系数 (r) 均大于0.99,10种三嗪类除草剂的LOQ在5.0~10 μg/kg之间。
|
|
表 2 10 种三嗪类除草剂的线性方程、相关系数及定量限 Table 2 Linear equation, correlation, and LOQ of 10 triazine herbicides |
2.4 方法的准确度及精密度
从表3可以看出:在5~100 μg/kg 3个添加水平下,平均回收率在75%~111%之间,相对标准偏差 (RSD)(n = 6) 在3.1%~8.7%之间。表明该方法的准确度与精密度均能满足于农药残留分析检测的要求[6]。
|
|
表 3 10种三嗪类除草剂添加回收率及相对标准偏差(n=6) Table 3 Recoveries and relative standard deviations (RSD) of 10 triazine herbicides (n=6) |
2.5 实际样品分析
利用本研究建立的方法,分别对市场上随机抽取的10份乌龙茶样品及土壤样品进行上述10种三嗪类除草剂的检测。结果显示:茶叶样品中均未检出三嗪类除草剂残留;其中一份土壤样品检测出莠去津,为45.9 μg/kg。
3 结论本研究建立了乌龙茶及土壤中10种三嗪类除草剂 (西玛津、莠去津、扑灭津、特丁津、敌草净、环丙津、西草净、莠灭净、扑草净和特丁净) 残留的气相色谱-串联质谱 (GC-MS/MS) 测定方法。以乙腈为提取溶剂,通过采用改进QuEChERS方法进行净化,以15 mg MWCNTs + 30 mg PSA + 30 mg C18 + 150 mg MgSO4为净化剂,能够有效去除色素、有机酸等杂质,提取及净化均取得理想效果。10种三嗪类除草剂在5~500 μg/kg范围内线性关系良好,回收率、重现性、灵敏度均能满足痕量分析检测的要求。MWCNTs有望作为一种新型的净化吸附剂,应用于农药残留检测。本研究所建立的方法,提取效率高、检测灵敏度高,样品处理操作简单,能够满足于乌龙茶及土壤中三嗪类除草剂残留的分析测定。
| [1] | KÖCK-SCHULMEYER M, GINEBREDA A, GONZÁLEZ S, et al. Analysis of the occurrence and risk assessment of polar pesticides in the Llobregat River Basin (NE Spain)[J]. Chemosphere, 2012, 86(1): 8–16. doi:10.1016/j.chemosphere.2011.08.034 |
| [2] | PICHON V, CHEN L, HENNION M C, et al. Preparation and evaluation of immunosorbents for selective trace enrichment of phenylurea and triazine herbicides in environmental waters[J]. Anal Chem, 1995, 67(14): 2451–2460. doi:10.1021/ac00110a021 |
| [3] | DE ARMAS E D, MONTEIRO R T R, ANTUNES P M, et al. Diagnóstico espaço-temporal da ocorrência de herbicidas nas águas superficiais e sedimentos do rio Corumbataí e principais afluentes[J]. Quim Nova, 2007, 30(5): 1119–1127. doi:10.1590/S0100-40422007000500013 |
| [4] | MARTIN E T, MCGUIRE C M, MUBARAK M S, et al. Electroreductive remediation of halogenated environmental pollutants[J]. Chem Rev, 2016, 116(24): 15198–15234. doi:10.1021/acs.chemrev.6b00531 |
| [5] | HINCAPIÉ M, MALDONADO M I, OLLER I, et al. Solar photocatalytic degradation and detoxification of EU priority substances[J]. Catal Today, 2005, 101(3-4): 203–210. doi:10.1016/j.cattod.2005.03.004 |
| [6] |
食品安全国家标准 食品中农药最大残留限量: GB 2763—2016[S]. 北京: 中国标准出版社, 2017.
National food safety standard-Maximum residue limits for pesticides in food: GB 2763—2016[S]. Beijing: Standards Press of China, 2017. |
| [7] |
荣杰峰, 韦航, 李亦军, 等. 羟基化多壁碳纳米管分散固相萃取-气相色谱-质谱法测定茶叶中21种有机磷农药[J]. 色谱, 2016, 34(2): 194–201.
RONG J F, WEI H, LI Y J, et al. Determination of 21 organophosphorus pesticides in tea by gas chromatography-mass spectrometry coupled with hydroxylated multi-walled carbon nanotubes based on dispersive solid-phase extraction[J]. Chin J Chromatogr, 2016, 34(2): 194–201. |
| [8] |
曹慧, 陈小珍, 朱岩, 等. 多壁碳纳米管固相萃取技术同时测定蜂蜜中多类兽药残留[J]. 高等学校化学学报, 2013, 34(12): 2710–2715.
CAO H, CHEN X Z, ZHU Y, et al. Simultaneous determination of multi-veterinary drug residues in honey by ultra performance liquid chromatography-tandem mass spectrometry and multiwalled carbon nanotubes cleaning[J]. Chem J Chin Univ, 2013, 34(12): 2710–2715. doi:10.7503/cjcu20130764 |
| [9] | TOLEDANO R M, CORTÉS J M, ANDINI J C, et al. Large volume injection of water in gas chromatography-mass spectrometry using the through oven transfer adsorption desorption interface: application to multiresidue analysis of pesticides[J]. J Chromatogr A, 2010, 1217(28): 4738–4742. doi:10.1016/j.chroma.2010.05.011 |
| [10] |
周利, 罗逢健, 张新忠, 等. 纳米竹炭分散固相萃取/超高效液相色谱-串联质谱法测定绿茶中的农药多残留[J]. 分析测试学报, 2014, 33(6): 642–647.
ZHOU L, LUO F J, ZHANG X Z, et al. Determination of multi-pesticide residues in green tea by nano bamboo charcoal-dSPE/Ultra high performance liquid chromatography-tandem mass spectrometry[J]. J Instrum Anal, 2014, 33(6): 642–647. |
| [11] |
张华威, 刘慧慧, 田秀慧, 等. 凝胶色谱-固相萃取-气相色谱-串联质谱法测定水产品中9种三嗪类除草剂[J]. 质谱学报, 2015, 36(2): 177–184.
ZHANG H W, LIU H H, TIAN X H, et al. Determination of 9 triazine herbicides in aquatic products by GPC-SPE-GC-MS/MS[J]. J Chin Mass Spectrom Soc, 2015, 36(2): 177–184. doi:10.7538/zpxb.youxian.2014.0054 |
| [12] |
彭金云, 韦良兴, 农克良, 等. 基质固相分散气相色谱法测定甘蔗中三嗪类除草剂[J]. 分析试验室, 2010, 29(6): 49–52.
PENG J Y, WEI L X, NONG K L, et al. Matrix solid-phase dispersion and gas chromatography for the determination of triazine herbicides in sugarcane[J]. Chin J Anal Lab, 2010, 29(6): 49–52. |
| [13] |
祁彦, 占春瑞, 张新忠, 等. 高效液相色谱法测定大豆中13种三嗪类除草剂多残留量[J]. 分析化学, 2006, 34(6): 787–790.
QI Y, ZHAN C R, ZHANG X Z, et al. Simultaneous determination of thirteen triazine herbicides residues in soybeans by high performance liquid chromatography[J]. Chin J Anal Chem, 2006, 34(6): 787–790. |
| [14] |
田宏哲, 白雪松, 苑馨方, 等. 气相色谱-电子捕获检测器同时测定瓜果类蔬菜中15种除草剂残留[J]. 农药学学报, 2016, 18(5): 625–632.
TIAN H Z, BAI X S, YUAN X F, et al. Simultaneous determination of fifteen herbicides in cucurbitaceous and solanaceous vegetables by gas chromatography with electron caption detector[J]. Chin J Pestic Sci, 2016, 18(5): 625–632. |
| [15] |
郭立群, 徐军, 董丰收, 等. 分散固相萃取-超高效液相色谱-串联质谱法同时检测玉米及其土壤中烟嘧磺隆、莠去津及氯氟吡氧乙酸残留[J]. 农药学学报, 2012, 14(2): 177–184.
GUO L Q, XU J, DONG F S, et al. Simultaneous determination of nicosulfuron, atrazine and fluroxypyr in soil and corn by ultraperformance liquid chromatography-mass spectrometry[J]. Chin J Pestic Sci, 2012, 14(2): 177–184. |
| [16] |
张新忠, 马晓东, 张伟国, 等. 气相色谱化学电离二级质谱法测定土壤中16种三嗪类除草剂的残留[J]. 分析化学, 2008, 36(6): 781–787.
ZHANG X Z, MA X D, ZHANG W G, et al. Determination of sixteen triazine herbicide residues in soil by gas chromatography-chemical Ionization tandem mass spectrometry[J]. Chin J Anal Chem, 2008, 36(6): 781–787. |
 2017, Vol. 19
2017, Vol. 19


