避蚊胺 (diethyltoluamide,以下简称 DEET) 是酰胺类化学合成驱避剂,具有广谱性、高效性和安全低毒等特点,已被广泛应用 60 余年[1]。但由于 DEET 本身具有亲油性,水中溶解性差,所以市售避蚊胺大多以乙醇作溶剂,主要用作熏蒸趋避目的,如果直接涂抹在身上,产品易挥发,对皮肤刺激也强,且实际驱蚊效果一般只有 4~6 h,不能提供长时间的有效保护,因此,有必要制备一种安全的水溶性 DEET 缓释产品。
β-环糊精 (β-cyclodextrin,以下简称 β-CD) 是由 α-1,4-糖苷键连接 7 个葡萄糖组成的无毒环状寡糖,具有疏水性内部空腔和亲水性外部结构[2-4]。这一独特结构允许客体 (疏水分子或疏水部分) 通过非共价键被包合进空腔而形成水溶性包合物,进而起到增溶、缓释和增加稳定性的作用[5]。O-羧甲基壳聚糖 (O-carboxymethyl chitosan,以下简称 O-CMC) 是壳聚糖的两性乙醚衍生物,由于其具有无毒性、生物可降解性及生物相容性而被关注[6-8]。此外,O-CMC 在中性及碱性环境下水溶性好,安全性高,由其所制备的纳米胶囊具有较好的缓释作用[9]。基于此,本研究采用饱和溶液法先制备 DEET/β-CD 包合物,再采用离子交联法将其包入 O-CMC 与交联剂氯化钙 (CaCl2) 形成的纳米胶囊内,制备了 DEET/β-CD/O-CMC 亲水性纳米胶囊,对其结构进行表征,并进行了缓释性能研究,以期实现 DEET 更安全和长效的释放。
1 材料与方法 1.1 材料与仪器O-羧甲基壳聚糖 (O-CMC),青岛弘海生物技术有限公司 (取代度 > 80%);DEET (纯度 > 98%),Aladdin Reagent;β-CD (纯度 > 99%),成都市科龙化工试剂厂。其余试剂均为分析纯。
T6 系列紫外-可见分光光度计,北京普析通用仪器有限公司;Zetasizer Nano ZS90 激光粒度分析仪,英国马尔文公司;DSC 404 F3 差示扫描量热仪 (DSC) 和 XRD6000 X-射线衍射仪,日本岛津制作所;Tecrai 10 扫描电子显微镜 (SEM),日本日立制作所。
1.2 试验方法1.2.1 DEET 标准曲线的绘制 准确称取 0.01 g (精确至 0.000 1 g) DEET,用质量分数为 80% 的乙醇溶液定容至 100 mL,即得质量浓度为 0.1 mg/mL 的 DEET 储备液。分别量取 DEET 储备液 1.0、1.5、2.0、2.5 和 3.0 mL 至 10 mL 容量瓶中,用质量分数为 80% 乙醇溶液定容,混合均匀得 10.0、15.0、20.0、25.0 和 30.0 μg/mL 的 DEET 标准溶液。以 80% 乙醇溶液为参比溶液,在 265 nm 波长处,分别测定不同浓度 DEET 标准溶液的紫外吸光度值,以 DEET 质量浓度为横坐标,以吸光度为纵坐标,绘制 DEET 的标准曲线。
1.2.2 β-CD 对 DEET 的增溶作用测定 准确称取 2.775 g β-CD,溶于 150 mL 蒸馏水中,获得 β-CD 储备液。分别向含有 15.0、20.0、25.0、30.0 和 35.0 mL β-CD 储备液的 50 mL 烧杯中加入 0.998 g DEET,每个烧杯均补水至 35 mL,置于 30 ℃ 水浴恒温振荡器中振荡 48 h。分别取出 5.0 mL 样品过滤后测定紫外吸光度值,根据标准曲线绘制相溶解度图,并研究 β-CD 的增溶作用。
1.2.3 DEET/β-CD 包合物的制备 采用饱和溶液法[10]制备。准确称取 0.925 0 g β-CD 于 50 mL 蒸馏水中配制成饱和溶液,在搅拌下加入由相溶解度图确定的 DEET 乙醇溶液,置于恒温 30 ℃ 磁力搅拌器上搅拌 3 h,于 4 ℃ 冷藏 12 h,12 000 r/min 下离心,分离沉淀,冷冻干燥,即得 DEET/β-CD 包合物。
1.2.4 DEET/β-CD 包合物的表征
1.2.4.1 包封率和载药量的测定 将 DEET/β-CD 包合物于 12 000 r/min 下离心,收集上清液,于紫外-可见分光光度计下测定吸光度值,通过标准曲线计算上清液中 DEET 的含量 (mB)。按公式 (1) 和 (2) 计算包合物载药量 (Lc) 及包封率 (Ee)。
| ${L_{\rm{c}}}/\text{%} = \frac{{{m_{\rm A}} - {m_{\rm B}}}}{{{m_{\rm S}}}} \times 100$ | (1) |
| ${E_{\rm e}}/ \text{%}= \frac{{{m_{\rm A}} - {m_{\rm B}}}}{{{m_{\rm A}}}} \times 100 $ | (2) |
式中:mA 为初始投药量,mB 为上清液中含药量,mS 为冷冻干燥后的包合物的质量。
1.2.4.2 DEET/β-CD 包合物的 DSC 分析 分别对 β-CD、DEET、DEET 与 β-CD 的物理混合物和 DEET/β-CD 包合物进行 DSC 表征,扫描范围为 T = 40~360 ℃。
1.2.4.3 DEET/β-CD 包合物的 XRD 分析 用 XRD 对 β-CD、DEET/β-CD 包合物进行表征,扫描范围为 2θ = 2°~45°。
1.2.5 DEET/β-CD/O-CMC 亲水性纳米胶囊的制备 采用离子交联法制备[11]。取 2 mg/mL 的 O-CMC 溶液 20 mL,用 0.1 mol/L 的盐酸溶液调节 pH 为 7.4,加入 1.96 mL DEET/β-CD 包合物溶液 [m(DEET) : m (O-CMC) = 3:20],滴加 4 mg/mL 的交联剂 CaCl2 溶液 2.5 mL (m (CaCl2) : m (O-CMC) = 1 : 4),搅拌 30 min 后得到纳米胶囊混悬液,于 12 000 r/min 下离心,得到沉淀,冷冻干燥,即得纳米胶囊。
1.2.6 纳米胶囊的表征
1.2.6.1 包封率和载药量的测定 DEET/β-CD/O-CMC 纳米胶囊混悬液的处理及载药量 (Lc)、包封率 (Ee) 的计算公式同 1.2.4 节。
1.2.6.2 粒径、PDI 以及 Zeta 电位的测定 用粒径电位仪测定纳米胶囊混悬液的粒径、PDI 和 Zeta 电位。
1.2.6.3 表面形态观察 适当用蒸馏水稀释纳米胶囊混悬液,滴在单晶硅片上,晾干后用 SEM 观察其形态。
1.2.7 载药缓释性能研究 分别将 DEET、DEET/β-CD 包合物和 DEET/β-CD/O-CMC 纳米胶囊溶于 0.05 mol/L 的 Tris-HCl (pH = 7.4) 缓冲液中,置于 37 ℃ 恒温振荡器中振荡,定时取样,测定吸光度值,按 (3) 式计算 DEET 的累积释放率 (Er)[12]。
| ${E_{\rm r}}/\text{%} = \frac{{{V_{\rm e}}\mathop \sum \nolimits_{i = 1}^{n - 1} {C_i} + {V_0}{C_n}}}{{{m_{\rm {drug}}}}} \times 100$ | (3) |
式中:Er 表示累积释放率,Ve 为每次取样体积,V0 为总体积,Cn 为 DEET 取样浓度,mdrug 为 DEET 总量。
2 结果与讨论 2.1 DEET 的标准曲线测定结果表明,DEET 在质量浓度 (ρ) 为 10.0~30.0 μg/mL 范围内与吸光度 (A) 呈较好的线性关系,其线性回归方程为 A = 0.020 22ρ–0.003,决定系数 R2 = 0.999 0。
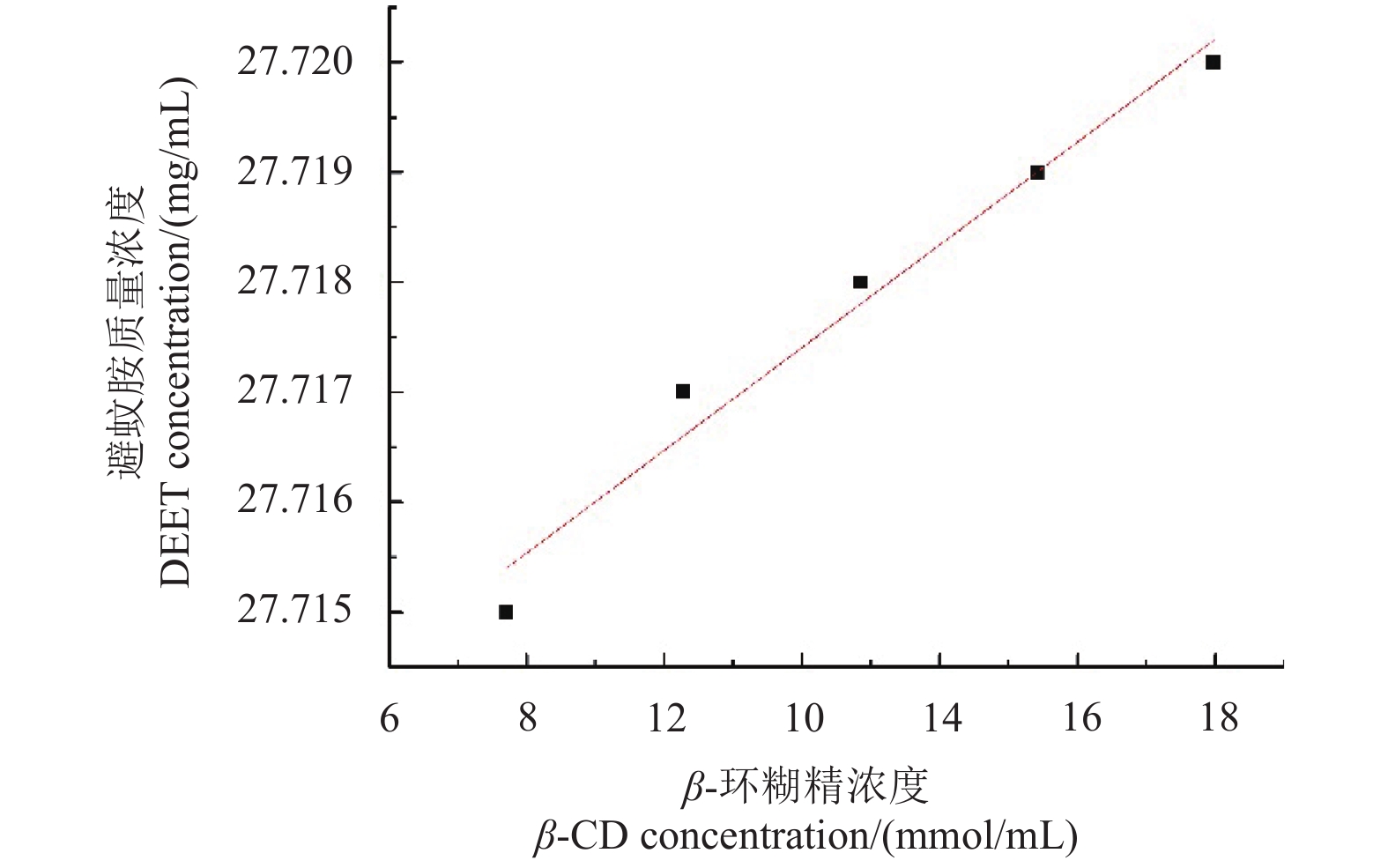
2.2 β-CD 对 DEET 的增溶作用由图 1 可知,DEET 的溶解度与 β-CD 的浓度呈线性关系,即随着 β-CD 浓度的增加,DEET 的溶解度增大。据文献[13]报道,相溶解度图呈现 AL 型,这表明包合物的形成是 DEET 与 β-CD 以 1 : 1 的物质的量之比进行了包埋。
|
图 1 β-CD 对 DEET 溶解度的影响 Fig. 1 Effect of β-CD on the solubility of DEET |
DEET 在水中的溶解度约为 0.99 mg/mL,按 1.2.3 节饱和溶液法制备的 DEET/β-CD 包合物 (DEET 与 β-CD 物质的量之比为 1 : 1),其溶解度增加至 27.70 mg/mL,表明 β-CD 的加入,使 DEET 溶解度增加了约 27 倍。
2.3 DEET/β-CD 包合物的表征2.3.1 包封率和载药量 结果表明,本研究所制备的 DEET/β-CD 包合物的包封率为 (81.69 ± 1.07)%,载药量为 (20.60 ± 0.33)%。
2.3.2 DEET/β-CD 包合物的 DSC 分析 图 2 为 DEET (a)、β-CD (b)、β-CD 与 DEET 物理混合物 (物质的量之比 1 : 1)(c) 及 DEET/β-CD 包合物 (物质的量之比 1 : 1)(d) 的 DSC 图。可以看出:纯 DEET (a) 在 166.2 ℃ 有一个强吸收峰,纯 β-CD (b) 在 119.9 ℃ 处有一个很强的吸收峰;二者的物理混合物 (c) 在 166.2 ℃ 和 112.8 ℃ 出现强吸收峰,基本是 β-CD 和 DEET 吸收峰的叠加;而 DEET/β-CD 包合物 (d) 在 166.2 ℃ 处的吸收峰完全消失。表明 DEET 通过非共价键进入了 β-CD 空腔形成水溶性包合物,破坏了原来的 DEET 晶形结构。

|
图 2 DEET (a)、β-CD (b)、β-CD 与 DEET 物理混合物 (c) 及 DEET/β-CD 包合物 (d) 的 DSC 图 Fig. 2 DSC thermograms of DEET (a), β-CD (b), physical mixture of DEET and β-CD (c), and DEET/β-CD inclusion compound (d) |
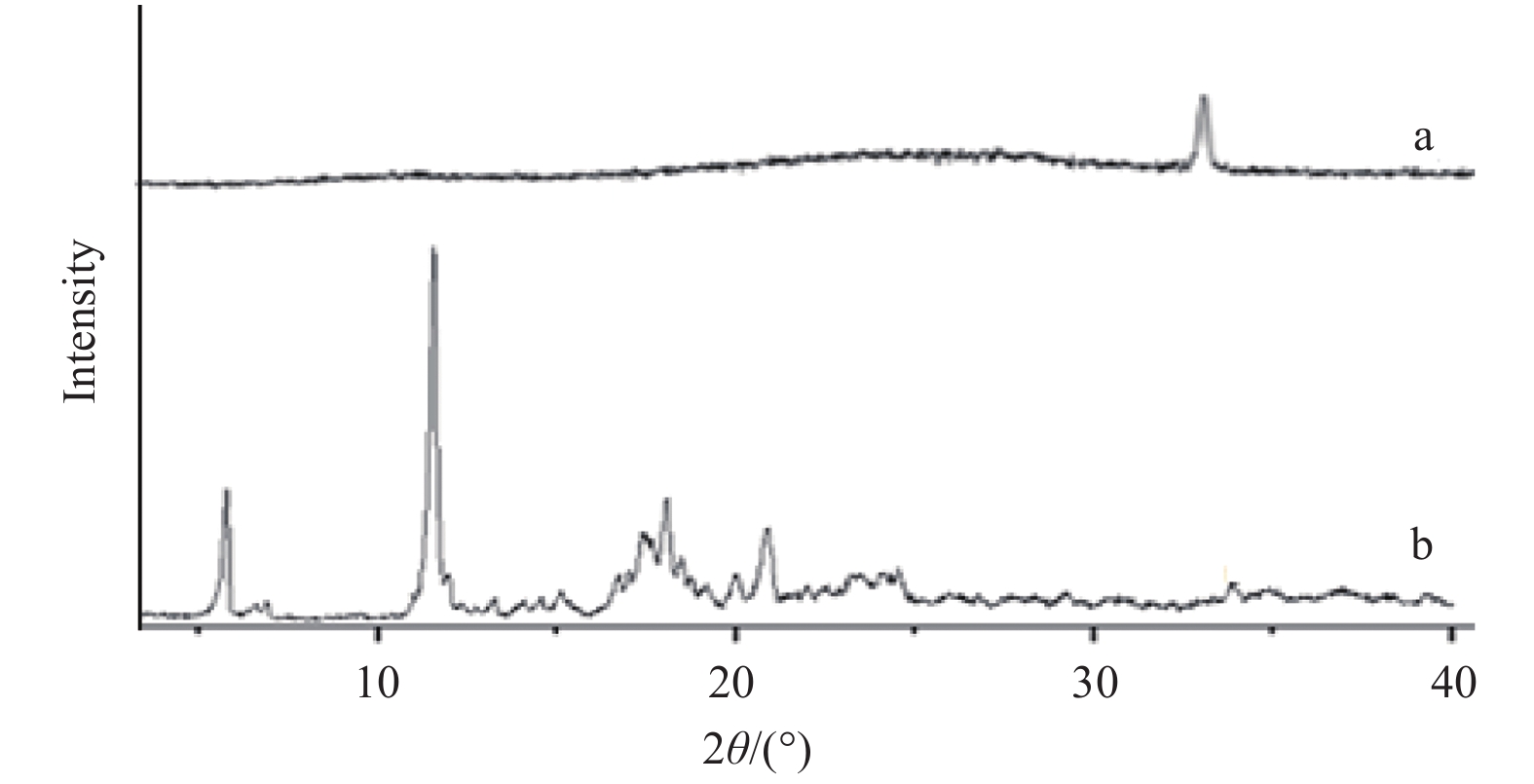
2.3.3 DEET/β-CD 包合物的 XRD 分析 由图 3 可以看出:β-CD (a) 在 2θ = 32.5° 处有强烈的尖峰;而 DEET/β-CD 包合物 (b) 的衍射峰有明显变化,在 2θ=5.6°、10.8°、17.5° 和 20.4° 处均有尖峰存在,这表明 DEET 与 β-CD 之间不是发生了简单包埋,也可能发生了一定的相互作用。
|
图 3 β-CD (a)、DEET/β-CD 包合物 (b) 的 XRD 图谱 Fig. 3 XRD patterns of β-CD (a) and DEET/β-CD inclusion compound (b) |
2.3.4 DEET/β-CD/O-CMC 纳米胶囊的表征
2.3.4.1 包封率和载药量 通过离子交联法制备得到的 DEET/β-CD/O-CMC 纳米胶囊的包封率为 (79.93 ± 2.08) %,载药量为 (12.11 ± 0.09) %。
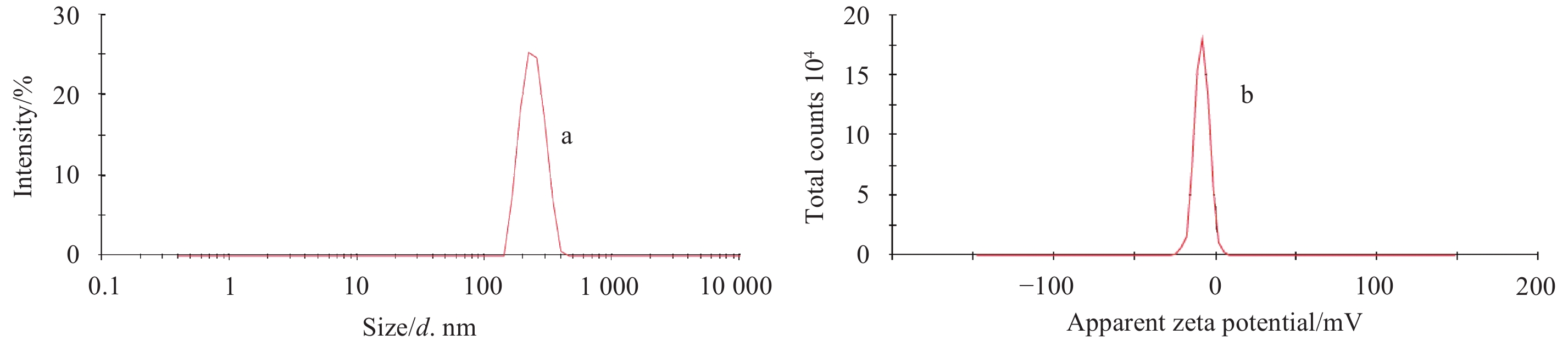
2.3.4.2 纳米胶囊粒径、PDI 及 Zeta 电位 从图 4 可以看出,该纳米胶囊平均粒径为 (230.50 ± 11.34) nm,Zeta 电位为 (–19.08 ± 0.99) mV,PDI 为 0.055。说明所得纳米胶囊粒径分布较窄,而且纳米胶囊稳定性良好。
|
图 4 DEET/β-CD/O-CMC 纳米胶囊粒径 (a) 及 Zeta 电位分布图 (b) Fig. 4 Particles size and Zeta potential distribution of DEET/β-CD/O-CMC nanocapsules |
2.3.4.3 纳米胶囊 SEM 观察 SEM 观察发现,DEET/β-CD/O-CMC 纳米胶囊呈椭圆形,平均粒径在 200~300 nm (图 5),这与激光粒度仪所得结果相符合。

|
图 5 DEET/β-CD/O-CMC 纳米胶囊的 SEM 图 Fig. 5 SEM micrographs of DEET/β-CD/O-CMC nanocapsules |
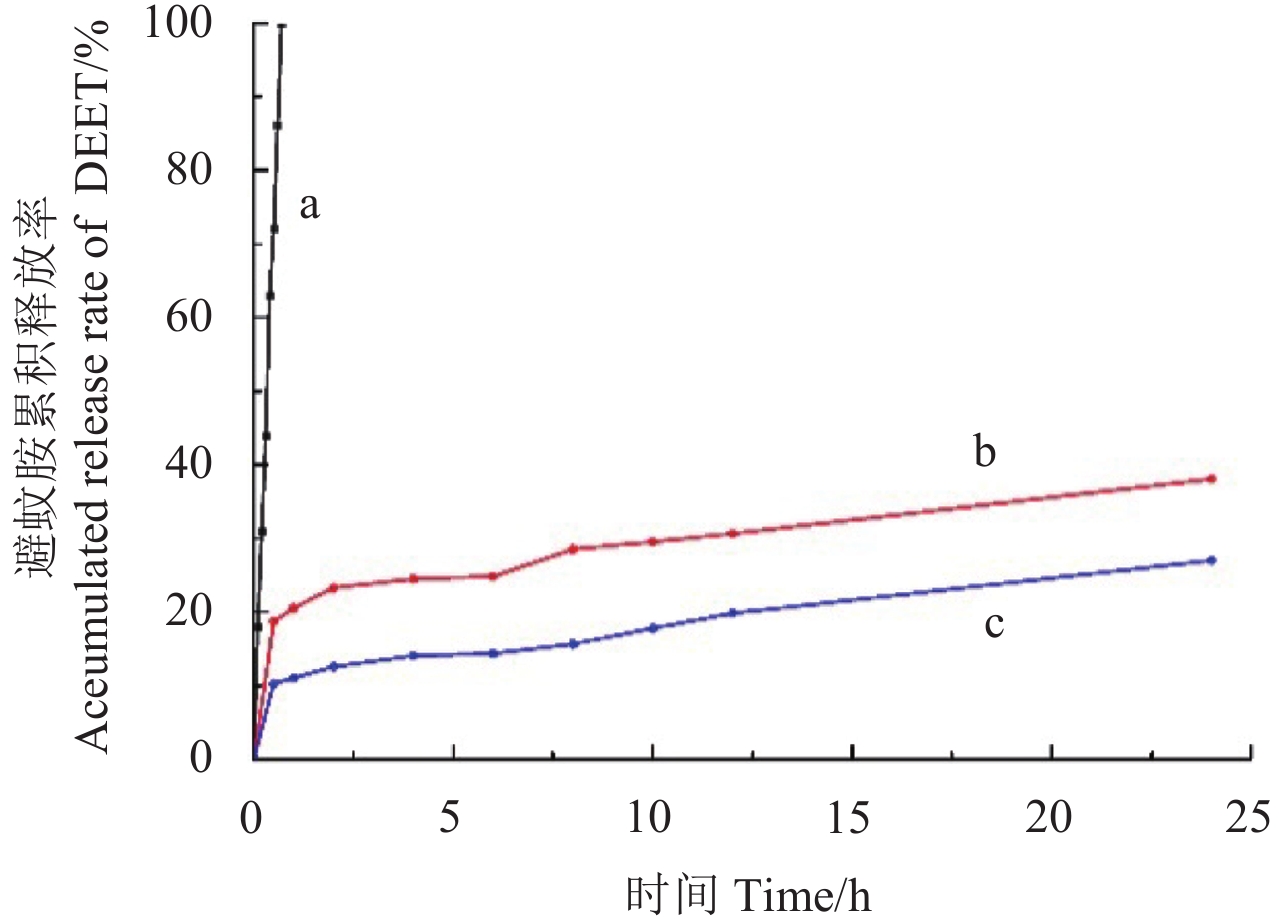
2.3.5 载药缓释性能研究 图 6 为 DEET、DEET/β-CD 包合物和 DEET/β-CD/O-CMC 纳米胶囊的缓释行为。可以看出:纯 DEET (a) 在 40 min 时已完全释放;而 DEET/β-CD 包合物 (b) 和 DEET/β-CD/O-CMC 纳米胶囊 (c) 中的 DEET,在 6 h 时的累积释放率分别为 24.87% 和 14.39%,12 h 时分别为 30.67% 和 19.86%,24 h 时分别为 38.10% 和 27.04%。可见相较于 DEET/β-CD 包合物,DEET/β-CD/O-CMC 纳米胶囊具有更好的缓释性。
|
图 6 Tris-HCl 缓冲液下纯 DEET (a)、DEET/β-CD 包含物 (b) 及 DEET/β-CD/O-CMC 纳米胶囊 (c) 里 DEET 的累积释放率 Fig. 6 Accumulated release rate of DEET (a), DEET/β-CD inclusion compound (b), DEET/β-CD/O-CMC nanocapsules (c) in Tris-HCl |
3 结论
本研究采用饱和溶液法制备了 DEET/β-CD 包合物,并通过离子交联法制备了 DEET/β-CD/O-CMC 纳米胶囊。DSC、XRD 分析结果表明,DEET 已成功包合进入 β-CD 空腔中,而且通过 β-CD 的增溶作用,可使 DEET 在水中的溶解度增加约 27 倍。所制备的 DEET/β-CD/O-CMC 纳米胶囊的包封率和载药量分别为 (79.93 ± 2.08) % 和 (12.11 ± 0.09) %,且分散性和稳定性良好,粒径为 (230.50 ± 11.34) nm。体外释放 24 h 发现,包合物和纳米胶囊中 DEET 累积释放率分别为 38.10% 和 27.04%。表明 DEET/β-CD/O-CMC 纳米胶囊具有很好的缓释性。
| [1] |
陶波, 张大伟. 蚊虫驱避剂的研究进展[J]. 东北农业大学学报, 2014, 45(2): 123–128.
TAO B, ZHANG D W. Research advance of mosquito repellents[J]. J Northeast Agric Univ, 2014, 45(2): 123–128. |
| [2] | ROMI R, NOSTRO P L, BOCCI E, et al. Bioengineering of a cellulosic fabric for insecticide delivery via grafted cyclodextrin[J]. Biotechnol Progr, 2005, 21(6): 1724–1730. doi:10.1021/bp050276g |
| [3] | ZHANG J Q, WU D, JIANG K M, et al. Preparation, spectroscopy and molecular modelling studies of the inclusion complex of cordycepin with cyclodextrins[J]. Carbohydr Res, 2015, 406: 55–64. doi:10.1016/j.carres.2015.01.005 |
| [4] | SINGH R, TØNNESEN H H, VOGENSEN S B, et al. Studies of curcumin and curcuminoids. XXXVI. The stoichiometry and complexation constants of cyclodextrin complexes as determined by the phase-solubility method and UV–Vis titration[J]. J Inclusion Phenom Macrocycl Chem, 2010, 66(3-4): 335–348. doi:10.1007/s10847-009-9651-5 |
| [5] | FIGUEIRAS A, SARRAGUÇA J M G, CARVALHO R A, et al. Interaction of omeprazole with a methylated derivative of β-cyclodextrin: phase solubility, NMR spectroscopy and molecular simulation [J]. Pharm Res, 2007, 24(2): 377–389. doi:10.1007/s11095-006-9161-8 |
| [6] | ANITHA A, MAYA S, DEEPA N, et al. Efficient water soluble O-carboxymethyl chitosan nanocarrier for the delivery of curcumin to cancer cells [J]. Carbohydr Polym, 2011, 83(2): 452–461. doi:10.1016/j.carbpol.2010.08.008 |
| [7] | MOHAMED R R, SABAA M W. Synthesis and characterization of antimicrobial crosslinked carboxymethyl chitosan nanoparticles loaded with silver[J]. Int J Biol Macromol, 2014, 69: 95–99. doi:10.1016/j.ijbiomac.2014.05.025 |
| [8] | UPADHYAYA L, SINGH J, AGARWAL V, et al. The implications of recent advances in carboxymethyl chitosan based targeted drug delivery and tissue engineering applications[J]. J Controlled Release, 2014, 186: 54–87. doi:10.1016/j.jconrel.2014.04.043 |
| [9] | MAI T T T, HA P T, PHAM H N, et al. Chitosan and O-carboxymethyl chitosan modified Fe3O4 for hyperthermic treatment [J]. Adv Nat Sci, 2012, 3(1): 015006. |
| [10] |
赵国巍, 廖正根, 梁新丽, 等. 饱和溶液法制备木香挥发油/β-环糊精包合物
[J]. 江西中医药, 2009, 40(8): 73–75.
ZHAO G W, LIAO Z G, LIANG X L, et al. Preparation of volatile oil/β-cyclodextrin inclusion compound of woody by saturated solution method [J]. Jiangxi J Tradit Chin Med, 2009, 40(8): 73–75. |
| [11] |
何慧, 季金苟, 刘月华, 等. β-环糊精/O-羧甲基壳聚糖纳米粒对光敏性药物的联合保护
[J]. 高分子材料科学与工程, 2016, 32(1): 105–109.
HE H, JI J G, LIU Y H, et al. β-cyclodextrin/O-carboxymethyl chitosan nanoparticles in combine protected photosensitive drugs [J]. Polym Mater Sci Eng, 2016, 32(1): 105–109. |
| [12] | LI J J, GUO S Z, WANG M, et al. Poly(lactic acid)/poly(ethylene glycol) block copolymer based shell or core cross-linked micelles for controlled release of hydrophobic drug[J]. RSC Adv, 2015, 5(25): 19484–19492. doi:10.1039/C4RA14376K |
| [13] | ZINGONE G, RUBESSA F. Preformulation study of the inclusion complex warfarin-β-cyclodextrin [J]. Int J Pharm, 2005, 291(1-2): 3–10. doi:10.1016/j.ijpharm.2004.11.013 |
 2017, Vol. 19
2017, Vol. 19


