2. 农业部农产品质量安全风险评估实验室(昆明),昆明 650223;
3. 云南省大理市农产品质量安全检测站,云南 大理 671000
2. Laboratory of Quality & Safety Risk Assessment for Agro-Products (Kunming), Ministry of Agriculture, Kunming 650223, China;
3. Quality and Safety Inspection Station of Agricultural Products in Dali City, Dali 671000, Yunnan Province, China
2,4-滴,即2,4-二氯苯氧乙酸,是一种人工合成的植物外源激素,能够发挥与生长素相似的生理效应。早在1942年就有文献报道了2,4-滴在低于30 mg/kg时可用作植物生长调节剂,主要用于防止番茄、棉花、菠萝、香蕉等作物的落花落果及形成无子果实等[1-2]。
近年来,2,4-滴在香蕉的种植过程中使用较为普遍,但过量的2,4-滴会在果蔬中残留并对动物具有慢性毒性[3-4],可能引起基因突变和染色体异常等[5-6],但到目前为止尚未被证实。中国国家标准中只对水果中的柑橘类、仁果类、核果类、浆果和其他小粒水果中的2,4-滴进行了最大残留限量 (MRL) 的规定[7],尚未对香蕉的MRL值进行规定,而欧盟、日本、英国等发达国家和地区均对2,4-滴在香蕉中的MRL值进行了规定[8]。
目前已经报道的关于2,4-滴残留检测的方法主要包括气相色谱法[9]、液相色谱-质谱联用法[10]、免疫学的方法[11-12]和分子印迹[13]等,但这些方法的样品前处理均较为复杂,且灵敏度较低。近年来,随着超高效液相色谱-三重四极杆串联质谱仪 (UPLC-MS/MS) 的普及,利用UPLC-MS/MS对2,4-滴在果蔬中残留的检测也变得简单和高效,且灵敏度相对于其他方法可提高多个数量级[14-15]。目前,对于香蕉中2,4-滴的残留还缺乏快速、准确的检测方法,同时对于2,4-滴在香蕉中的残留动态及最大残留限量也没有明确的基础数据。因此,本研究采用UPLC-MS/MS建立了香蕉中2,4-滴残留的快速测定方法,并利用该方法研究了2,4-滴在香蕉中的残留消解动态,以期为2,4-滴在香蕉中的合理使用提供科学依据。
1 材料与方法 1.1 材料与试剂香蕉品种为巴西蕉 (云南省西双版纳傣族自治州);2,4-滴标准品 (CAS:94-75-7,100 μg/mL),中国百灵威科技有限公司;2,4-滴原药 (纯度98%),江苏辉丰农化股份有限公司;乙腈和甲醇,均为色谱纯,德国merck公司;氯化钠 (分析纯),国药集团化学试剂北京有限公司;纯净水,杭州娃哈哈集团。
1.2 仪器与设备API4000三重四极杆质谱仪 (配有电喷雾离子源及Analysis数据处理系统),美国AB公司;1290超高效液相色谱仪和ZORBAX RRHD色谱柱 (2.1 mm × 50 mm,1.8 μm),美国Agilent公司;AE-100电子分析天平 (精度 0.1 mg),瑞士METTLER TOLEDO公司;涡旋振荡器,美国Thermo Scientific公司;TGL-15B高速台式离心机,上海安亭科学仪器厂;HY-5回旋式振荡仪,江苏省金坛市环宇科学仪器厂;HR7625匀浆机,荷兰飞利浦公司;WBS-16农用背负式手动喷雾器,浙江海盐农邦机械有限公司。
1.3 试验方法 1.3.1 田间试验设计残留消解动态试验施药剂量为有效成分53 mg/kg;最终残留试验设低、中、高3个剂量,分别为为有效成分23、35和53 mg/kg;另设空白对照组。
小区面积:每小区2棵香蕉树,每处理重复3次,4个处理共12个小区,顺序排列。
1.3.2 田间试验方法残留消解动态试验于香蕉断蕾抹花后7~14 d (冬夏季略有调整),即香蕉上扬时为最佳施药时期;用喷雾器于香蕉果指喷雾,用水量为75 kg/hm2,施药次数为1次,分别在施药后2 h、8 h以及1、2、5、7、10、14、21和28 d采样。测定消解率,消解率计算方法为:消解率 = (第0天样品原始残留量 – 第n次采样样品中的残留量)/第0天样品原始残留量[16]。
最终残留试验的施药方法同残留消解动态试验;施药次数为1次,于施药60 d后一次性采样。
样品采集及处理:每穗果分上、中、下不同方位采集8~10个香蕉果指,每次每小区 (2棵树) 共采集16~20个果,用塑料袋封装,于–20 ℃保存,备用。
1.3.3 标准溶液配制准确吸取0.1 mL 2,4-滴标准品,用甲醇稀释成1 μg/mL的标准储备液。准确量取0.01、0.02、0.04、0.08和0.1 mL的2,4-滴标准储备溶液,用甲醇分别稀释配成1、2、4、8和10 μg/L的系列标准工作溶液,于–20 ℃下保存,备用。
1.3.4 样品前处理香蕉样品经四分法缩分和匀浆机匀浆后,准确称取10 g香蕉样品于50 mL离心管中,加入20 mL乙腈,振荡30 min,加入2 g氯化钠,于3 000 r/min下涡旋30 s,5 000 r/min下离心3 min后,吸取上层乙腈提取液1 mL,过0.22 μm滤膜,待UPLC-MS/MS分析。
1.3.5 检测条件色谱条件:以甲醇–0.1%甲酸水溶液作为流动相,流速0.2 mL/min;柱温35 ℃;进样量1 μL,梯度洗脱参数见表1。
|
|
表 1 梯度洗脱参数 Table 1 The parameters of gradient elution |
质谱条件:参照文献[17]中的相关质谱条件并根据仪器的实际情况稍作改进,即ESI离子源;负离子扫描;多反应监测模式 (MRM)。扫描条件:GS1雾化气55 L/h;GS2辅助加热气55 L/h;气帘气20 L/h;喷雾电压–5 500 V;辅助加热气温度550 ℃;2,4-滴定量离子对m/z 219.0/160.8,定性离子对m/z 219.0/124.9;去簇电压–27 V/–27 V,碰撞能量–22 V/–35 V。
1.3.6 添加回收试验以云南省昆明市市场上销售的香蕉空白基质作为添加回收试验对象,根据2,4-滴的定量限,分别以1倍、5倍和10倍定量限作为添加浓度进行回收试验,每水平重复6次,考察方法的准确度和精密度。
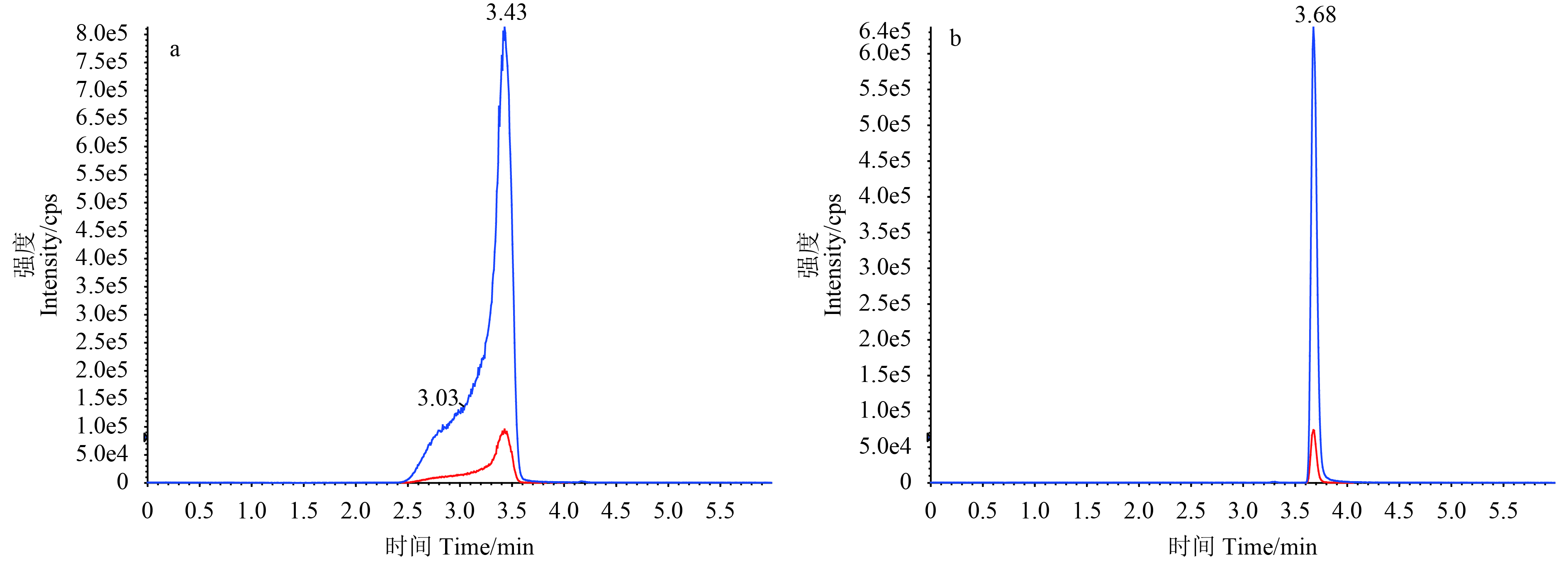
2 结果与分析 2.1 仪器条件的优化选择分别考察了以甲醇-水、甲醇–0.1%甲酸水溶液及甲醇–0.1%氨水溶液作为流动相时2,4-滴的色谱峰情况。结果表明:以甲醇-水作为流动相时,2,4-滴的色谱峰拖尾严重,峰形较宽 (图1a);以甲醇–0.1%甲酸水溶液作为流动相时,峰形较好,无拖尾现象 (图1b);而在甲醇中添加氨水,2,4-滴的色谱峰也存在一定的拖尾现象,与甲醇-水作为流动相的峰形类似。本研究中采用超高效液相色谱仪,以甲醇–0.1%甲酸水溶液为流动相,极大地提高了色谱分离的效率,整个分析过程可在6 min内完成,其中2,4-滴的保留时间为3.68 mim,达到了香蕉中2,4-滴残留快速高效分析测定的目的。
|
a. 甲醇-水溶液;b. 甲醇–0.1%甲酸水溶液。 a. methanol-water solutions; b. methanol –0.1% formic acid water solutions. 图 1 2,4-滴在不同流动相中的色谱图 (0.5 μg/mL) Fig. 1 The chromatogram of 2,4-D in different mobile phase (0.5 μg/mL) |
2.2 方法的线性范围和检出限
结果表明:在1.0~10 μg/L范围内,2,4-滴的质量浓度与对应的色谱峰面积间线性关系较好,R2=0.999 7,检出限 (S/N=3) 为0.001 5 mg/kg,定量限 (S/N=10) 为0.005 mg/kg,表明利用本方法对于香蕉中的2,4-滴检测的灵敏度较好。
|
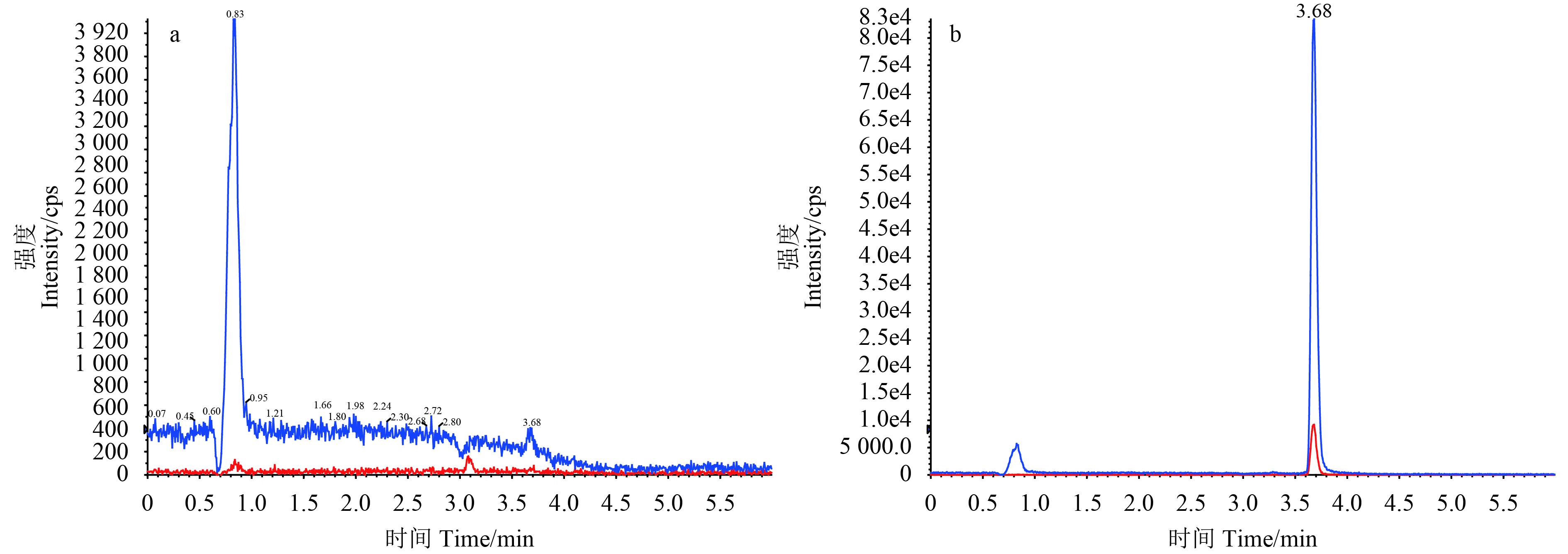
图 2 香蕉空白(a)和香蕉添加2,4-滴 (b,0.05 mg/kg) 的色谱图 Fig. 2 The chromatogram of banana blank matrix (a) and blank matrix spiked 2,4-D (b, 0.05 mg/kg) |
2.3 方法的准确度和精密度
结果显示:在0.005、0.05和0.5 mg/kg 3个添加水平下,2,4-滴的回收率为93%~99%,相对标准偏差为2.5%~3.0%,能够准确测定香蕉中2,4-滴的残留,可满足《农药残留试验准则》的要求[18]。添加色谱图见图2。
2.4 2,4-滴在香蕉中的残留消解动态消解动态试验结果见表2。由表2可见,施药后2,4-滴的消解率不断增大,施药后5 d的消解率大于50%,消解较快,施药后21 d时,消解率超过90%。
|
|
表 2 2,4-滴在香蕉中的消解动态 Table 2 Residual dynamic of 2,4-D in bananas |
2,4-滴的消解回归方程为ct = 0.305e–0.27t (R2 = 0.787),符合一级反应动力学方程。由回归方程可知,2,4-滴的半衰期为5.4 d,小于30 d,属易降解农药[19],但从动态残留数据中可以发现,2,4-滴在大部分时间内的消解较快,半衰期较短,但在21 d时在香蕉中仍有少量残留,提示2,4-滴虽属易降解农药,但是其降解速率较慢,在制定安全采收期和最大残留限量值时应引起重视。
2.5 2,4-滴在香蕉中的最终残留量最终残留试验结果表明,低、中和高浓度的2,4-滴在香蕉中的最终残留量均 < LOQ。中国国家标准中虽未规定香蕉中2,4-滴的最大残留限量,但对香蕉中农药残留测定部位要求为全蕉[7],即测定时将香蕉皮与果肉混合后测定,但在日常膳食中香蕉皮不食用,因此,在香蕉食用前的剥皮步骤可以将采收后香蕉中微量2,4-滴残留风险降到最低。
3 结论本研究建立了超高效液相色谱-串联质谱快速测定香蕉中2,4-滴残留的方法。结果表明,采用负离子模式,MRM监测模式,在1.0~10 μg/L范围内,2,4-滴的质量浓度与对应的峰面积间线性关系较好,检出限 (S/N=3) 为0.001 5 mg/kg,定量限 (S/N=10) 为0.005 mg/kg。在0.005、0.05和0.5 mg/kg 3个添加水平下,2,4-滴的回收率为93%~99%,相对标准偏差为2.5%~3.0%。该方法灵敏度高,精密度好,分析速度快,可满足香蕉中2,4-滴残留检测的要求。
田间试验结果表明,2,4-滴在香蕉中的消解半衰期为5.4 d,属易降解农药,但2,4-滴在21 d时仍有少量残留,在施药时应引起重视。
| [1] | PAZMIÑO D M, ROMERO-PUERTAS M C, SANDALIO L M. Insights into the toxicity mechanism of and cell response to the herbicide 2,4-D in plants[J]. Plant Signal Behav, 2012, 7(3): 425–427. doi:10.4161/psb.19124 |
| [2] | VAN OVERBEEK J. Plant hormones and regulators[J]. Science, 1966, 152(3723): 721–731. doi:10.1126/science.152.3723.721 |
| [3] | HANSEN W H, QUAIFE M L, HABERMANN R T, et al. Chronic toxicity of 2,4-dichlorophenoxyacetic acid in rats and dogs[J]. Toxicol Appl Pharmacol, 1971, 20(1): 122–129. doi:10.1016/0041-008X(71)90096-2 |
| [4] | GARABRANT D H, PHILBERT M A. Review of 2,4-dichlorophenoxyacetic acid (2,4-D) epidemiology and toxicology[J]. Crit Rev Toxicol, 2002, 32(4): 233–257. doi:10.1080/20024091064237 |
| [5] | PURCELL M, NEAULT J F, MALONGA H, et al. Interactions of atrazine and 2,4-D with human serum albumin studied by gel and capillary electrophoresis, and FTIR spectroscopy[J]. Biochim Biophys Acta, 2001, 1548(1): 129–138. doi:10.1016/S0167-4838(01)00229-1 |
| [6] | PAVLICA M, PAPEŠ D, NAGY B. 2,4-Dichlorophenoxyacetic acid causes chromatin and chromosome abnormalities in plant cells and mutation in cultured mammalian cells[J]. Mutat Res Lett, 1991, 263(2): 77–81. doi:10.1016/0165-7992(91)90063-A |
| [7] |
食品中农药最大残留限量: GB 2763—2016[S]. 北京: 中国标准出版社, 2017.
Maximum residue limits for pesticides in food: GB 2763—2016[S]. Beijing: Standards Press of China, 2017. |
| [8] |
食品伙伴网. 农兽药数据库[DB/OL]. [2017-07-06]. http://db. foodmate.net/pesticide/.
Food Mate Network. Agricultural and veterinary drugs Database [DB/OL]. [2017-07-06]. http://db.foodmate.net/pesticide/. |
| [9] |
常宇文, 吴晓宗, 李伟, 等. 凝胶渗透色谱-气相色谱法测定豆芽中2,4-二氯苯氧乙酸残留量[J]. 食品工业科技, 2008, 28(12): 203–205.
CHANG Y W, WU X Z, LI W, et al. Determination of residues of 2,4-dichlorophenoxyacetic in bean sprout by gas chromatography and gel permeation chromatography[J]. Sci Technol Food Ind, 2008, 28(12): 203–205. |
| [10] | BEESON M D, DRISKELL W J, BARR D B. Isotope dilution high-performance liquid chromatography/tandem mass spectrometry method for quantifying urinary metabolites of atrazine, malathion, and 2,4-dichlorophenoxyacetic acid[J]. Anal Chem, 1999, 71(16): 3526–3530. doi:10.1021/ac990130u |
| [11] | DZANTIEV B B, ZHERDEV A V, YULAEV M F, et al. Electrochemical immunosensors for determination of the pesticides 2,4-dichlorophenoxyacetic and 2,4, 5-tricholorophenoxyacetic acids[J]. Biosens Bioelectron, 1996, 11(1-2): 179–185. doi:10.1016/0956-5663(96)83725-0 |
| [12] |
余若祯, 何苗, 施汉昌, 等. 间接竞争ELISA方法测定水中2,4-D的研究[J]. 生态毒理学报, 2006, 1(1): 88–92.
YU R Z, HE M, SHI H C, et al. Development of indirect ELISA for the determination of 2,4-D in water[J]. Asian J Ecotoxicol, 2006, 1(1): 88–92. |
| [13] | HAUPT K, DZGOEV A, MOSBACH K. Assay system for the herbicide 2,4-dichlorophenoxyacetic acid using a molecularly imprinted polymer as an artificial recognition element[J]. Anal Chem, 1998, 70(3): 628–631. doi:10.1021/ac9711549 |
| [14] |
林珍珍, 张水锋, 曹慧, 等. 超高效液相色谱-串联质谱法测定肉制品中非法添加的14种酸性染料[J]. 中国食品学报, 2013, 13(5): 167–172.
LIN Z Z, ZHANG S F, CAO H, et al. UPLC-MS/MS determination of fourteen acid dyes illegally added in meat products[J]. J Chin Inst Food Sci Technol, 2013, 13(5): 167–172. |
| [15] |
马晓燕, 朱顺达, 肖海龙, 等. 液相色谱-串联质谱法测定食品中喹啉黄、酸性绿S和专利蓝V[J]. 中国食品学报, 2012, 12(4): 182–186.
MA X Y, ZHU S D, XIAO H L, et al. Determination of quinoline yellow, green S and patent blue V in foods by performance liquid chromatography tandem mass spectrometry[J]. J Chin Inst Food Sci Technol, 2012, 12(4): 182–186. |
| [16] |
马婧玮, 李通, 周玲, 等. 烯效唑在棉花及土壤中的残留及消解动态[J]. 农药学学报, 2017, 19(3): 374–380.
MA J W, LI T, ZHOU L, et al. Residue and dissipation of uniconazole in Gossypium spp. and soil [J]. Chin J Pest Sci, 2017, 19(3): 374–380. |
| [17] |
林涛, 邵金良, 刘兴勇, 等. QuEChERS-超高效液相色谱-串联质谱法测定蔬菜中41种农药残留[J]. 色谱, 2014, 33(3): 235–241.
LIN T, SHAO J L, LIU X Y, et al. Determination of 41 pesticide residues in vegetables by QuEChERS-ultra performance liquid chromatography-tandem mass spectrometry[J]. Chin J Chromatogr, 2014, 33(3): 235–241. |
| [18] |
农药残留试验准则: NY/T 788—2004[S]. 北京: 中国农业出版社, 2004.
Guideline on pesticide residue trials: NY/T 788—2004[S]. Beijing: China Agriculture Press, 2004. |
| [19] |
韦婕, 邓婕, 黄慧俐, 等. 高效液相色谱检测呋虫胺在稻田水和土壤中的残留及消解动态[J]. 农药学学报, 2015, 17(2): 195–200.
WEI J, DENG J, HUANG H L, et al. Residue and decline study of dinotefuran in paddy water and soil by high performance liquid chromatographic[J]. Chin J Pest Sci, 2015, 17(2): 195–200. |
 2017, Vol. 19
2017, Vol. 19


