文章信息
- 魏杰, 朱新杰, 王后苗, 尹双义, 杨小艺, 孙辉, 李鹏程, 徐辰武
- WEI Jie, ZHU Xinjie, WANG Houmiao, YIN Shuangyi, YANG Xiaoyi, SUN Hui, LI Pengcheng, XU Chenwu
- 氯酸盐处理对不同基因型玉米苗期性状的影响
- Effect of chlorate treatment on traits related to different genotypes of maize at the seedling stage
- 南京农业大学学报, 2020, 43(3): 423-430
- Journal of Nanjing Agricultural University, 2020, 43(3): 423-430.
- http://dx.doi.org/10.7685/jnau.201907052
-
文章历史
- 收稿日期: 2019-07-25
玉米(Zea mays L.)是重要的粮食作物和饲料作物,氮素是促进玉米增产最关键的因素之一。然而我国氮肥施用过量,氮肥利用率仅约40%。大量氮肥残留在土壤中,带来土壤板结与酸化及水体富营养化等环境问题[1]。2015年初农业部制定的《到2020年化肥使用量零增长行动方案》指出,2015-2019年,逐步将化肥施用量年增长率控制在1%以内;力争到2020年,主要农作物化肥使用量实现零增长。如何在减少肥料投入的同时提高作物产量始终是困扰科学工作者的一个难题,而挖掘作物自身潜力,培育高氮肥利用效率的作物新品种是解决这一系列问题的关键[2]。
玉米氮吸收效率是复杂的数量性状[3],采用双亲分离群体进行QTL定位、精细定位或者利用自然群体开展关联分析是定位、克隆数量性状位点的有效手段。这种研究策略往往需要较大的样本容量,随着测序技术的发展,基因型鉴定的成本不断降低,但是高通量的氮吸收表型鉴定成为限制基因定位和克隆的主要因素。虽然15N标记是鉴定氮高效吸收的有效方法,但是, 15N标记的含量测定成本较高,不适合大样本群体的表型测量[4]。而氯酸盐是一种对植物具有毒害的硝酸盐类似物,植物吸收氯酸盐后会抑制植株生长,吸收氯酸盐越多毒害表型越明显。氯酸盐和硝酸盐具有相似的结构式,植物对氯酸盐和硝酸盐具有相同的吸收机制,植物对氯酸盐越敏感氮吸收效率越高,该特点使氯酸盐试验成为鉴定植物氮吸收效率的有效手段。目前,利用氯酸盐试验已从拟南芥和水稻中成功克隆了硝酸盐转运蛋白 AtNRT1.1B[5]和 OsNRT1.1B[4]。对玉米的研究结果也表明可以用氯酸盐耐性来筛选、鉴定硝酸盐吸收以及硝酸盐还原酶突变体[6]。但是目前关于氯酸盐处理对玉米植株形态、生理生化表型的影响报道仍相对较少。本文选取6个国内常用玉米自交系材料,利用氯酸盐模拟硝酸盐的方法,研究玉米植株表型性状、酶活性以及矿质营养元素含量等的变化,探究氯酸盐对苗期玉米表型及生理生化表型的影响,为玉米氮高效吸收表型鉴定提供新思路。
1 材料与方法 1.1 供试材料和生长条件选取国内常用的6个玉米自交系材料:Mo17、Dan340、Wu312、Y53、Ye478和B73。每个品种选取大小一致的玉米种子,经10%过氧化氢表面消毒30min,用蒸馏水将其冲洗干净,在饱和CaSO4溶液中浸泡6h后将种子摆在发芽纸上,放置黑暗环境中催芽。种子发芽后,挑选发芽较好的种子,每8粒用发芽纸卷成1卷,作为1个试验重复,放置在水培箱里。水培箱营养液组分为:4 mmol·L-1 KNO3、0.75 mmol·L-1 K2SO4、0.65 mmol·L-1 MgSO4、0.1 mmol·L-1 KCl、0.25 mmol·L-1 KH2PO4、1×10-3 mmol·L-1 H3BO3、1×10-3 mmol·L-1 MnSO 4、1×10-4 mmol·L-1 CuSO4、1×10-3 mmol·L-1 ZnSO4、5×10-6 mmol·L-1(NH4)6Mo7O24和0.1 mmol·L-1 Fe-EDTA。植株生长1周后开始处理,试验设置3个处理:正常处理(CK)采用4 mmol·L-1 KNO 3;氯酸盐处理1(T1)采用2 mmol·L-1 KClO3代替KNO3;氯酸盐处理2(T2)采用4 mmol·L-1 KClO3代替KNO3。每个处理重复4次,采用完全随机设计,水培箱放置于扬州大学试验温室中生长,每3 d更换1次培养液。
1.2 测定项目与方法 1.2.1 玉米表型性状测定玉米幼苗长至2叶期时开始氯酸盐处理,处理1周后,处理植株和对照植株表现出明显差异时取样。每卷选择4株正常的玉米植株测定其表型性状。株高:种子到叶片自然伸展时的最高处;叶长:最后1片完全展开叶的长度;叶绿素含量(SPAD):采用SPAD-502叶绿素仪对最上部完全展开叶的同一部位的SPAD值进行测定,以2次测定结果的平均值作为最终叶绿素含量;主胚根长:用直尺测量主胚根的长度;种子根长:用直尺测量出所有种子根的长度并取其平均值;将地上部和根系分开装入样品袋,于105℃烘箱烘0.5h,然后65℃烘至质量恒定,分别对地上部干质量、根干质量及其总干质量进行测定。
1.2.2 玉米可溶性蛋白含量及酶活性测定谷氨酸合成酶(GOGAT)活性、谷氨酰胺合成酶(GS)活性和硝酸还原酶(NR)活性均采用微量法测定[7-9]。采用BCA法[10]测定玉米叶片中可溶性蛋白含量(Cpr)。试验中用到的试剂、仪器和技术均由苏州科铭生物技术有限公司提供。
1.2.3 玉米矿质营养元素测定将烘干样品的地上部分与根样分别磨成粉状,称取0.1 g样品,加入5mL浓硝酸、3mL超纯水和2滴过氧化氢,在微波消解仪(CEM-MARS5,USA)上消解后,将消解液定容在50mL的容量瓶中并用等离子发射光谱-原子吸收仪(iCPA6300,USA)测定其Ca、Fe、Mn、Mo和Zn的含量。玉米地上部与根系样品氮浓度采用凯式定氮法测定。
1.3 数据分析采用Excel2013和SPSS23.0软件进行方差分析、多重比较和相关分析,图形处理采用R3.4软件。
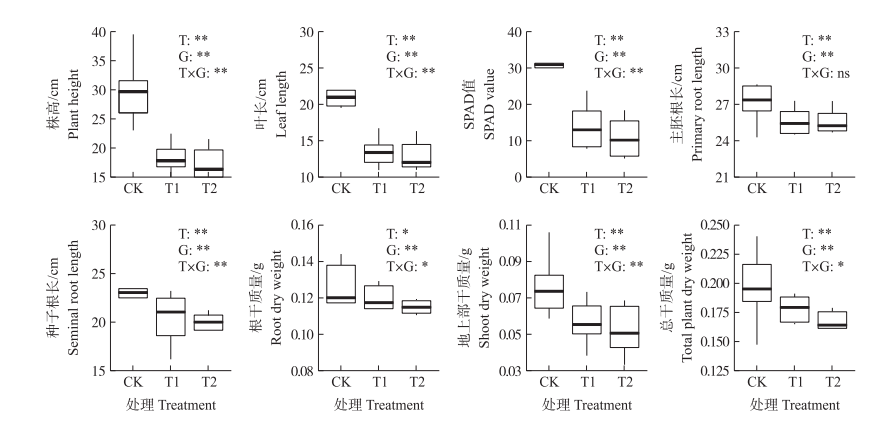
2 结果与分析 2.1 氯酸盐处理对玉米表型的影响方差分析结果可见:处理间和材料间的表型均存在显著或极显著的差异。与对照相比,处理后的株高、叶长和SPAD值等8个性状的测量值都明显降低(图 1、表 1、表 2)。
|
图 1 不同浓度氯酸盐处理对玉米表型的影响 Fig. 1 Effect of chlorate treatment with different concentrations on maize phenotype 图中纵坐标为各个表型测量值;横坐标CK、T1、T2分别表示对照、2mmol·L-1KClO3处理、4mmol·L-1KClO3处理;T表示处理;G表示基因型;T×G表示处理与基因型的互作;*表示在0.05水平差异显著;**表示在0.01水平差异显著;ns表示不存在显著差异。下同。 In this figure, the y-axis shows the measurements of each trait, CK, T1 and T2 in x-axis indicated control, treatment with 2 mmol·L-1 KClO3, and 4 mmol·L-1 KClO3, respectively.T represents the treatment, G represents the genotype, T × G represents the interaction between treatment and genotype; *represents a significant difference at the level of 0.05, **represents a significant difference at the level of 0.01, and'ns'represents no significant difference.The same as follows. |
| 材料 Materials |
处理 Treatment |
株高/cm Plant height |
叶长/cm Leaf length |
SPAD值 SPAD value |
地上部干质量/g Shoot dry weight |
总干质量/g Plant dry weight |
主胚根长/cm Primary root length |
种子根长/cm Seminal root length |
根干质量/g Root dry weight |
| Mo17 | CK | 28.00a | 19.58a | 31.13a | 0.058a | 0.195a | 26.57a | 21.00a | 0.123a |
| T1 | 14.70b | 10.93b | 23.79b | 0.057ab | 0.164ab | 24.86a | 16.13b | 0.116a | |
| T2 | 14.57b | 11.25b | 18.29c | 0.045b | 0.161b | 25.31a | 16.48b | 0.116a | |
| Dan340 | CK | 25.37a | 20.31a | 29.85a | 0.063a | 0.146a | 24.33a | 23.46a | 0.084a |
| T1 | 17.40b | 12.82b | 16.79b | 0.053a | 0.133a | 21.62b | 18.25b | 0.080a | |
| T2 | 16.82b | 12.36b | 13.55c | 0.056a | 0.138a | 22.04b | 19.15b | 0.082a | |
| Wu312 | CK | 22.98a | 15.88a | 30.53a | 0.069a | 0.181a | 28.18a | 22.69a | 0.144a |
| T1 | 16.55b | 11.71b | 8.91b | 0.038b | 0.188a | 26.57a | 23.20a | 0.152a | |
| T2 | 14.44b | 10.89b | 5.18c | 0.033b | 0.167a | 26.61a | 19.22a | 0.114b | |
| Y53 | CK | 31.54a | 21.64a | 31.22a | 0.078a | 0.195a | 31.95a | 28.72a | 0.117a |
| T1 | 18.21b | 13.86b | 7.73b | 0.049b | 0.171ab | 27.31a | 22.29b | 0.119a | |
| T2 | 15.66b | 11.70b | 5.39b | 0.042b | 0.161b | 27.26a | 20.77b | 0.119a | |
| Ye478 | CK | 31.33a | 22.07a | 29.79a | 0.084a | 0.240a | 26.46a | 23.40a | 0.143a |
| T1 | 20.30b | 15.16b | 16.07b | 0.068a | 0.191b | 24.53a | 19.79a | 0.129a | |
| T2 | 20.47b | 15.16b | 16.07b | 0.068a | 0.200ab | 24.69a | 20.71a | 0.131a | |
| B73 | CK | 39.43a | 30.15a | 36.66a | 0.106a | 0.223a | 28.65a | 22.44a | 0.117a |
| T1 | 22.37b | 16.66b | 8.12b | 0.073b | 0.187b | 26.00a | 22.57a | 0.113a | |
| T2 | 21.31b | 16.31b | 6.63b | 0.068b | 0.179b | 25.23a | 21.22a | 0.111a | |
|
注:同列不同小写字母表示差异显著(P<0.05)。下同。 Note:Different small letters in the same column indicate significant difference(P<0.05).The same as follows. | |||||||||
| 材料 Materials |
处理 Treatment |
可溶性蛋白质含量/(mg·mL-1) Cpr |
谷氨酸合成酶活性/(nmol·min-1·mg-1) GOGAT activity |
谷氨酰胺合成酶活性/(U·mg-1) GS activity |
硝酸还原酶活性/(μmol·h-1·mg-1) NR activit |
| Mo17 | CK | 2.54c | 76.40a | 0.43b | 0.07a |
| T1 | 3.89b | 10.98b | 0.57a | 0.06b | |
| T2 | 5.41a | 6.50b | 0.53a | 0.04c | |
| Dan370 | CK | 1.68c | 161.43a | 0.62a | 0.04c |
| T1 | 3.07a | 70.84b | 0.39c | 0.06b | |
| T2 | 2.45b | 12.10c | 0.56b | 0.08a | |
| Wu312 | CK | 1.80b | 27.41a | 0.53b | 0.09a |
| T1 | 1.84b | 23.10b | 0.67a | 0.10a | |
| T2 | 2.77a | 14.77c | 0.31c | 0.10a | |
| Y53 | CK | 1.92b | 119.11a | 0.47b | 0.08a |
| T1 | 4.08a | 9.26b | 0.41c | 0.04c | |
| T2 | 3.96a | 10.05b | 0.52a | 0.05b | |
| Ye478 | CK | 2.29c | 28.46a | 0.31b | 0.09a |
| T1 | 2.53b | 25.25b | 0.47a | 0.08a | |
| T2 | 3.27a | 9.77c | 0.42a | 0.03b | |
| B73 | CK | 2.07b | 97.58a | 0.49a | 0.07a |
| T1 | 2.81a | 10.37b | 0.37b | 0.07a | |
| T2 | 2.19b | 11.15b | 0.54a | 0.08a |
从表 1可见:对照与不同处理间的株高均有显著差异,而T1与T2间差异不显著。在T1处理下,Wu312株高降幅最小(27.98%),而Mo17降幅最大(47.5%);6个供试材料的株高平均下降38.96%。对照与不同处理间的叶长均有显著差异,而T1和T2间叶长差异不显著。在T1处理下,Wu312叶长降幅最小(26.26%),而B73降幅最大(44.74%),6个供试材料的叶长平均下降37.93%。对照与不同处理间的SPAD值均有显著差异,Mo17、Dan340和Wu312的SPAD值在T1与T2间有显著差异。在T1处理下,Mo17的SPAD值降幅最小(23.58%),B73降幅最大(77.85%),6个供试材料的SPAD值平均下降55.85%。在T2处理下,Mo17的SPAD值降幅最小(41.25%),B73、Y53和Wu312的SPAD值降幅最大,降幅分别为81.93%、82.74%和83.02%,降幅均超过80%;6个供试材料的SPAD值平均下降64.93%。Dan340和Ye478在对照和处理条件下的地上部干质量无显著差异,其余4个材料在对照和处理条件下的地上部干质量差异显著。在T1处理下,Mo17降幅最小(1.72%),而Wu312降幅最大(44.93%),6个供试材料的地上部干质量平均下降43.42%。在T2处理下,Dan340地上部干质量降幅最小(11.11%),而Wu312降幅最大(52.17%),6个供试材料的地上部干质量平均下降31.58%。T1与T2处理下的主胚根长、种子根长、根干质量和总干质量与对照相比降幅相对较小。
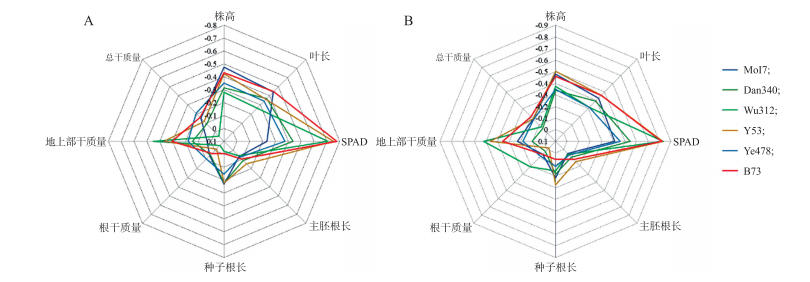
以上结果表明,氯酸盐处理对植物生长均有一定的抑制作用。其中对SPAD值影响最大,而对根干质量影响最小(图 2)。SPAD值、株高、叶长和地上部干质量可以作为筛选氯酸盐耐性材料的参考性状。供试的6个材料中,氯酸盐处理对B73、Y53和Wu312影响较大,而对Mo17、Ye478和Dan340影响较小,可推测B73、Y53和Wu312为氯酸盐敏感性材料,Mo17、Ye478和Dan340为氯酸盐耐性材料。
|
图 2 2 mmol·L-1(A)和4 mmol·L-1(B)氯酸盐处理条件下不同玉米自交系性状表型变化
Fig. 2 Phenotypic changes of maize inbred lines under 2 mmol·L-1(A) and 4 mmol·L-1(B) chlorate treatment
1)图中数值表示表型测量值变化比例。The value in the figure indicated the proportion of change of each trait. 2)株高:Plant height,叶长:Leaf length;主胚根长:Primary root length;种子根长:Seminal root length;根干质量:Root dry weight;地上部干质量:Shoot dry weight;总干质量:Total plant dry weight. |
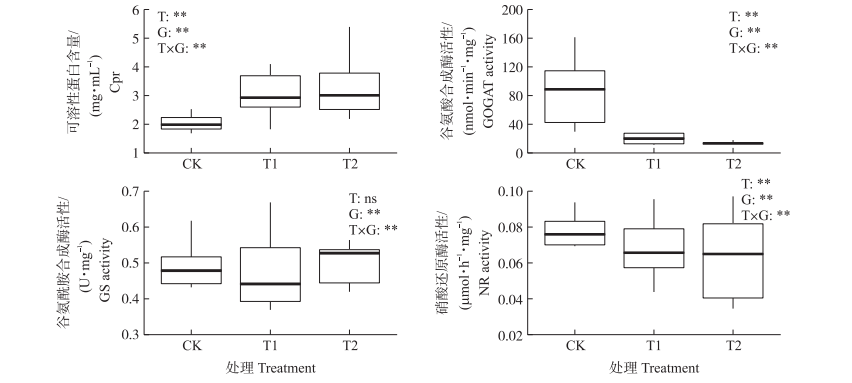
对不同处理下玉米自交系酶活性进行测定并进行方差分析。结果表明:处理间和材料间的可溶性蛋白含量(Cpr)、谷氨酸合成酶(GOGAT)活性和硝酸还原酶(NR)活性均存在显著或极显著的差异,而谷氨酰胺合成酶(GS)活性无显著变化(图 3)。在6个供试材料中,对照与不同处理间的Cpr均有显著差异,Mo17、Dan340和Ye478在T1与T2处理间存在显著差异,其余材料在T1和T2处理间无显著差异。在T1处理中,Wu312的Cpr增幅最低(2.22%),Y53增幅最高(112.50%),6个供试材料的Cpr平均增加32.24%;在T2处理中,B73的Cpr增幅最低(5.80%),Mo17的Cpr增幅最高(112.99%),6个供试材料的Cpr平均增加62.14%(表 2)。在6个供试材料中,对照与不同处理间的GOGAT活性均有显著差异,Dan340、Wu312和Ye478在T1与T2处理间差异显著,其余材料在T1和T2处理间无显著差异。在T1处理中,Ye478的GOGAT活性降幅最低(11.28%),Y53的GOGAT活性降幅最高(92.23%),6个供试材料的GOGAT活性平均下降70.33%;在T2处理中,与对照相比,Wu312的GOGAT活性降幅最低(46.11%),Dan340的GOGAT活性降幅最高(92.50%),6个供试材料的GOGAT活性平均降低87.26%。除B73和Wu312外,对照与不同处理间的NR活性均有显著差异,且T1与T2间也差异显著。在T1处理中,Dan340的NR活性显著增加33.10%,Y53的NR活性显著降低20%;在T2处理中,Dan340的NR活性显著增加50%,Mo17和Ye478的NR活性显著降低,分别降低了42.86%和66.67%。以上结果表明,氯酸盐处理对玉米的Cpr具有显著的促进作用,对玉米的GOGAT有显著的抑制作用。因此,Cpr和GOGAT可用于鉴定玉米氯酸盐耐性品种。
|
图 3 不同浓度氯酸盐处理对玉米可溶性蛋白含量和酶活性的影响 Fig. 3 Effect of chlorate treatment with different concentrations on protein content and enzyme activity in maize Cpr:Protein content; GOGAT:Glutamine oxoglutarate aminotransferase; GS:Glutamine synthetase; NR:Nitrate reduction.The same as follows. |
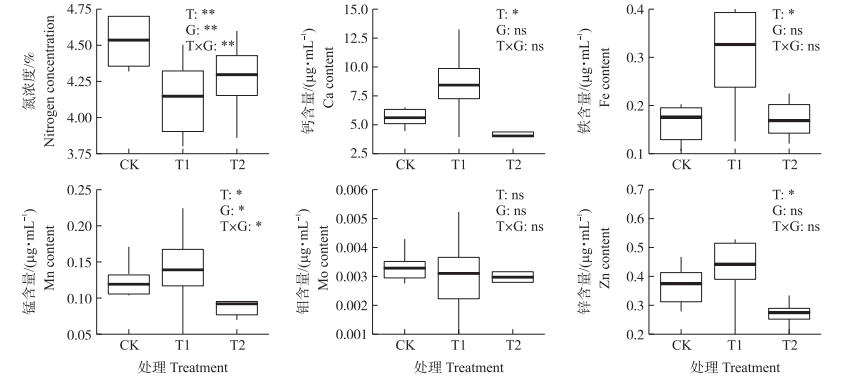
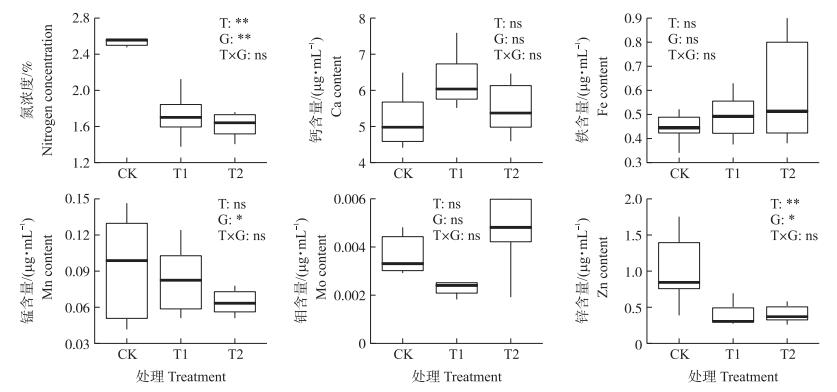
对不同浓度氯酸盐处理的6个玉米自交系矿质元素吸收进行测定,发现经氯酸盐处理后玉米地上部氮浓度明显降低。方差分析结果表明,大部分矿质元素在处理间和材料间均存在显著或极显著差异。其中,地上部分的Ca、Fe、Mn和Zn元素在T1处理中与对照相比显著增加,在T2处理中与对照相比显著降低,不同材料间均表现出显著差异(图 4)。经氯酸盐处理前后玉米根系氮浓度和Zn元素含量均显著降低,且材料间也存在显著或极显著差异。而根系中的Ca、Fe、Mn和Mo元素含量经氯酸盐处理后处理间无显著差异(图 5)。以上结果表明,氯酸盐处理抑制玉米地上部对氮素的吸收,T1处理促进地上部对Ca、Fe、Mn和Zn的吸收。此外,氯酸盐处理还抑制根系对氮和Zn的吸收,但不影响根系对Ca、Fe、Mn和Mo元素的吸收
|
图 4 不同浓度氯酸盐处理对玉米地上部矿质营养元素吸收的影响 Fig. 4 Effect of chlorate treatment with different concentrations on absorption of mineral nutrient elements in aboveground part of maize |
|
图 5 不同浓度氯酸盐处理对玉米根中矿质营养元素吸收的影响 Fig. 5 Effect of chlorate treatment with different concentrations on absorption of mineral nutrient elements in maize roots |
从表 3可见:CK、T1和T2处理的玉米地上部干质量与株高、叶长均存在极显著正相关关系,相关系数大于0.67,表明无论有无氯酸盐处理,地上部干质量与株高、叶长都存在紧密联系;在CK条件下,地上部干质量与SPAD值极显著正相关(r=0.717),而在T1和T2处理中,地上部干质量与SPAD值不相关,表明氯酸盐处理影响地上部干质量与SPAD值的相关性。地上部干质量在T1处理中与GS显著相关,在T2处理中与根系中Fe和Mo含量显著相关。
| 性状 Phenotype |
处理Treatment | ||
| CK | T1 | T2 | |
| 株高Plant height | 0.826** | 0.679** | 0.895** |
| 叶长Leaf length | 0.794** | 0.671** | 0.837** |
| SPAD值SPAD value | 0.717** | 0.129 | 0.271 |
| 主胚根长Primary root length | 0.408 | -0.117 | -0.344 |
| 种子根长Seminal root length | 0.140 | -0.112 | -0.379 |
| 根干质量Root dry weight | 0.060 | -0.243 | -0.041 |
| 总干质量Plant dry weight | 0.641** | 0.286 | 0.456* |
| 可溶性蛋白质含量Cpr | -0.021 | 0.074 | -0.354 |
| 谷氨酸合成酶活性GOGAT | -0.035 | -0.145 | -0.188 |
| 谷氨酰胺合成酶活性GS | -0.271 | -0.546** | 0.330 |
| 硝酸还原酶活性NR | 0.173 | -0.051 | -0.243 |
| 氮浓度(地上部) Nitrogen concentration (Shoot) | -0.514 | 0.420 | 0.372 |
| 钙(地上部) Ca(Shoot) | 0.156 | 0.016 | -0.030 |
| 铁(地上部) Fe(Shoot) | 0.301 | 0.272 | -0.072 |
| 锰(地上部) Mn(Shoot) | -0.101 | 0.135 | 0.168 |
| 钼(地上部) Mo(Shoot) | 0.065 | 0.010 | 0.186 |
| 锌(地上部) Zn(Shoot) | -0.197 | -0.222 | 0.042 |
| 氮浓度(根) Nitrogen concentration(Root) | -0.057 | 0.089 | 0.418 |
| 钙(根) Ca(Root) | 0.281 | 0.133 | 0.626 |
| 铁(根) Fe(Root) | -0.114 | 0.091 | 0.696* |
| 锰(根) Mn(Root) | 0.472 | 0.352 | 0.117 |
| 钼(根) Mo(Root) | -0.173 | -0.335 | 0.186 |
| 锌(根) Zn(Root) | 0.535 | 0.280 | 0.103 |
|
注:相关系数采用Pearson相关系数,**P<0.01,*P<0.05。 Note:Pearson correlation coefficient was used for correlation coefficient, **P<0.01, *P<0.05. | |||
氯酸盐和硝酸盐具有相似的结构式,植物对氯酸盐和硝酸盐具有相同的吸收机制,植物对氯酸盐越敏感氮吸收效率越高[4]。在水稻中,籼稻比粳稻具有更高的硝酸盐吸收活力。Hu等[4]对籼、粳稻进行氯酸盐耐性鉴定发现,籼稻品种'IR24'为高氯酸盐敏感性,粳稻品种'日本晴'为低氯酸盐敏感性,在氯酸盐处理下'日本晴'株高和叶长显著高于'IR24',叶色大部分偏绿,而'IR24'发黄甚至枯死;Teng等[11]发现'ZYQ8'(籼稻)氯酸盐敏感性显著高于'JX17'(粳稻)。因此氯酸盐耐性可作为硝态氮高效吸收的指标。
多项研究表明,玉米叶片SPAD值可以作为玉米氮高效的次级选择指标[12-14];高氮和低氮条件下,玉米不同材料地上部干质量的差异是进行耐低氮材料筛选的有效指标[15]。本研究发现,氯酸盐处理对玉米各个性状有不同程度的抑制作用,对SPAD值、株高、叶长和地上部干质量的影响较大,其中受氯酸盐响应最为明显的是SPAD值。株高、叶长、地上部干质量和SPAD值对氯酸盐的响应可以作为筛选氯酸盐耐性材料的有效指标。在本试验供试的6个材料中,Y53、B73和Wu312可能是高氯酸盐敏感性材料,受氯酸盐影响较大。而Mo17经过氯酸盐处理后表型性状发生变化最小,推测Mo17为低氯酸盐敏感性材料。
3.2 氯酸盐处理对玉米酶活性和矿质元素吸收的影响本研究中,经氯酸盐处理后,玉米苗叶片中Cpr含量明显增加,GOGAT活性明显降低,而GS活性变化差异不大。GOGAT在高等植物中以2种形式存在,分别为Fd-gogat和NADH-gogat,其中Fd-gogat在叶片中占主导地位,它与植物光合作用和呼吸作用有关。Lam等[16]研究表明,光合作用有利于Fd-gogat的表达及合成。Fd-gogat中ARE1基因编码叶绿体蛋白,ARE1功能缺失型突变体可延缓水稻植株衰老[17]。本试验中经过氯酸盐处理的叶片显著变小,SPAD值显著降低,不利于植物光合作用,阐明了GOGAT活性显著降低的原因。在矿质营养元素方面,氯酸盐处理对玉米吸收氮素有一定的抑制作用,也不利于根系对Zn的吸收,但T1处理促进玉米地上部对Ca、Fe、Mn和Zn元素的吸收。
本试验以氯酸盐模拟硝酸盐的方法探究氯酸盐处理对玉米表型及生理的影响来筛选氮高效材料。现已发现玉米不同材料吸收和利用氮素的效率存在显著差异,且这种差异受遗传控制[18]。Mo17和B73的遗传背景有很大差异[19],而在本试验中也可推断出B73为高氯酸盐敏感性材料,Mo17为低氯酸盐敏感性材料。在水稻研究中,已经利用各种水稻种质资源,如野生种、地方品种及其他优异种质资源材料,结合高通量组学技术,进行高效分子育种[20]。玉米种质资源丰富,其本身基因组具有丰富的遗传变异[21],以氯酸盐模拟硝酸盐处理苗期玉米,找出对氯酸盐敏感性差异大的材料,构建作图群体,结合高通量测序和生物信息学技术,定位相关QTL,对于选育玉米氮高效品种具有重要意义。
| [1] |
Chen X P, Cui Z L, Fan M S, et al. Producing more grain with lower environmental costs[J]. Nature, 2014, 514(7523): 486-489. DOI:10.1038/nature13609 |
| [2] |
Chao D Y, Lin H X. Nitrogen-use efficiency:transport solution in rice variations[J]. Nature Plants, 2015, 1: 15096. DOI:10.1038/nplants.2015.96 |
| [3] |
兰天茹.基于关联分析挖掘玉米硝酸还原酶基因ZmNR2功能位点[D].杨凌:西北农林科技大学,2019. Lan T R.Mining functional loci of nitrate reductase gene ZmNR2 based on association analysis in maize[D].Yangling:Northwest A&F University,2019(in Chinese with English abstract). http://cdmd.cnki.com.cn/Article/CDMD-10712-1019844808.htm |
| [4] |
Hu B, Wang W, Ou S J, et al. Variation in NRT1.1B contributes to nitrate-use divergence between rice subspecies[J]. Nature Genetics, 2015, 47(7): 834-838. DOI:10.1038/ng.3337 |
| [5] |
Tsay Y F, Schroeder J I, Feldmann K A, et al. The herbicide sensitivity gene CHL1 of Arabidopsis encodes a nitrate-inducible nitrate transporter[J]. Cell, 1993, 72(5): 705-713. DOI:10.1016/0092-8674(93)90399-B |
| [6] |
Mclure P R, Omholt T E, Pace G M. Anion uptake in maize roots:interactions between chlorate and nitrate[J]. Physiologia Plantarum, 2010, 68(1): 107-112. |
| [7] |
Cordovilla M D P, Perez J, Ligero F, et al. Partial purification and characterization of NADH-glutamate synthase from faba bean (Vicia faba) root nodules[J]. Plant Science, 2000, 150(2): 121-128. |
| [8] |
Fedorova K, Kayumov A, Woyda K, et al. Transcription factor TnrA inhibits the biosynthetic activity of glutamine synthetase in Bacillus subtilis[J]. FEBS Letters, 2013, 587(9): 1293-1298. DOI:10.1016/j.febslet.2013.03.015 |
| [9] |
Sakra F S, Arslan H, Krmz S, et al. Nitrate reductase activity(NRA)in Asphodelus aestivus Brot.(Liliaceae):distribution among organs, seasonal variation and differences among populations[J]. Flora, 2010, 205(2010): 527-531. |
| [10] |
Campion E M, Loughran S T, Walls D. Protein quantitation and analysis of purity[J]. Methods in Molecular Biology, 2011, 681(681): 229-258. |
| [11] |
Teng S, Tian C G, Chen M S, et al. QTLs and candidate genes for chlorate resistance in rice (Oryzas ativa L.)[J]. Euphytica, 2006, 152(2): 141-148. DOI:10.1007/s10681-006-9189-1 |
| [12] |
马庆, 李猛, 王慧, 等. 我国玉米育种与生产中189份自交系氮利用效率评价[J]. 玉米科学, 2015, 23(5): 6-11. Ma Q, Li M, Wang H, et al. Nitrogen use efficiency of 189 maize inbred lines in breeding and production in China[J]. Journal of Maize Sciences, 2015, 23(5): 6-11 (in Chinese with English abstract). |
| [13] |
汤继华, 谢惠玲, 黄绍敏, 等. 缺氮条件下玉米自交系叶绿素含量与光合效率的变化[J]. 华北农学报, 2005, 20(5): 10-12. Tang J H, Xie H L, Huang S M, et al. The changes of the content for chlorophyll and photosynthetic productivity in maize inbred lines under the low nitrogen stress[J]. Acta Agriculturae Boreali-Sinica, 2005, 20(5): 10-12 (in Chinese with English abstract). DOI:10.3321/j.issn:1000-7091.2005.05.002 |
| [14] |
陈范骏, 米国华, 春亮, 等. 玉米氮效率的杂种优势分析[J]. 作物学报, 2004, 30(10): 1014-1018. Chen F J, Mi G H, Chun L, et al. Analysis of heterosis for nitrogen use efficiency in maize[J]. Acta Agronomica Sinica, 2004, 30(10): 1014-1018 (in Chinese with English abstract). DOI:10.3321/j.issn:0496-3490.2004.10.009 |
| [15] |
向春阳, 常强, 马兴林, 等. 玉米不同基因型对氮营养胁迫的反应[J]. 黑龙江八一农垦大学学报, 2002, 14(4): 5-7. Xiang C Y, Chang Q, Ma X L, et al. Response to nitrogen stress on maize genotypes[J]. Journal of Heilongjinag August First Land Reclamation University, 2002, 14(4): 5-7 (in Chinese with English abstract). DOI:10.3969/j.issn.1002-2090.2002.04.002 |
| [16] |
Lam H M, Coschigano K T, Oliveira I C, et al. The molecular-genetics of nitrogen assimilation into amino acids in higher plants[J]. Annual Review of Plant Biology, 1996, 47(1): 569-593. DOI:10.1146/annurev.arplant.47.1.569 |
| [17] |
Wang Q, Nian J Q, Xie X Z, et al. Genetic variations in ARE1 mediate grain yield by modulating nitrogen utilization in rice[J]. Nature Communications, 2018, 9(1): 735. DOI:10.1038/s41467-017-02781-w |
| [18] |
米国华, 刘建安, 张福锁. 玉米杂交种的氮农学效率及其构成因素剖析[J]. 中国农业大学学报, 1998, 3(S4): 97-104. Mi G H, Liu J A, Zhang F S. Analysis on agronomic nitrogen efficiency and its components of maize hybrids[J]. Journal of China Agricultural University, 1998, 3(S4): 97-104 (in Chinese with English abstract). |
| [19] |
Yang N, Xu X W, Wang R R, et al. Contributions of Zea mays subspecies mexicana haplotypes to modern maize[J]. Nature Communications, 2017, 8: 1874. DOI:10.1038/s41467-017-02063-5 |
| [20] |
王威, 张联合, 李华, 等. 水稻营养吸收和转运的分子机制研究进展[J]. 中国科学:生命科学, 2015, 45(6): 569-590. Wang W, Zhang L H, Li H, et al. Recent progress in molecular dissection of nutrient uptake and transport in rice[J]. Scientia Sinica:Vitae, 2015, 45(6): 569-590 (in Chinese with English abstract). |
| [21] |
戴景瑞, 鄂立柱. 我国玉米育种科技创新问题的几点思考[J]. 玉米科学, 2010, 18(1): 1-5. Dai J R, E L Z. Scientific and technological innovation of maize breeding in China[J]. Journal of Maize Sciences, 2010, 18(1): 1-5 (in Chinese with English abstract). |




