文章信息
- 纪晓霞, 刘小倩, 刘颖, 王凯, 张源淑
- JI Xiaoxia, LIU Xiaoqian, LIU Ying, WANG Kai, ZHANG Yuanshu
- 高精料日粮诱导奶牛乳腺应激和凋亡中血管紧张素转化酶2的作用
- Effect of high concentration diet on angiotensin converting enzyme 2 in mammary gland stress and apoptosis in dairy cows
- 南京农业大学学报, 2019, 42(3): 513-518
- Journal of Nanjing Agricultural University, 2019, 42(3): 513-518.
- http://dx.doi.org/10.7685/jnau.201808017
-
文章历史
- 收稿日期: 2018-08-13
肾素-血管紧张素系统(RAS)是具有内分泌特性的肽能系统, 由经典的ACE-AngⅡ-AT1R和新的ACE2-Ang1-7-MasR 2条代谢通路组成。血管紧张素转化酶(ACE)是经典通路中的关键酶, 其催化产物血管紧张素Ⅱ(AngⅡ)是途径中的核心, 生理剂量的AngⅡ可通过与其靶细胞膜上的受体结合发挥多种效应。过量的AngⅡ可导致血压升高、血管和组织纤维化、氧化应激以及组织损伤等[1-2]。随着血管紧张素转化酶2(ACE2)的发现, 形成了RAS的新ACE2-Ang 1-7-MasR通路。2条通路相互拮抗共同维持着RAS的平衡。新通路中ACE2可以降解AngⅡ产生血管紧张素1-7(Ang 1-7), 后者通过结合MasR来拮抗AngⅡ, 从而发挥抗炎抗损伤的作用[3-4]。近年来, AngⅡ诱导的细胞氧化应激损伤和促凋亡及ACE2的抵抗作用的研究引起广泛关注[5-6], 但在乳腺方面的研究尚没有相关报道。
本课题组近期研究发现, ACE2在泌乳山羊乳腺中有表达, 并在内源性脂多糖(LPS)致奶山羊隐性乳房炎时, 其表达随乳腺上皮细胞损伤的发展呈下降趋势, 并伴有AngⅡ含量的增高, 推测ACE2的降低导致AngⅡ的积聚, 可能是乳腺上皮损伤的原因之一[7-8]。刘小倩等[6]的研究证实牛乳腺中有ACE2和ACE的存在, 长期饲喂高精料日粮对奶牛乳腺造成一定程度的炎性损伤, 乳腺中RAS处于激活状态。这些试验结果提示, 乳腺局部存在RAS, 同在其他组织一样, AngⅡ仍然是关键的效应因子, 其产生过量对乳腺健康是不利的。ACE2可以降解AngⅡ, 其在乳腺中是否如在其他组织中一样具有抗氧化应激和抗凋亡作用, 目前的研究报道较少。
本试验拟以泌乳期奶牛为研究对象, 通过研究高精料长期饲喂致泌乳奶牛乳腺氧化应激和细胞凋亡时乳腺局部RAS, 特别是ACE2的变化, 探讨ACE2在乳腺氧化应激及凋亡损伤中的作用。
1 材料与方法 1.1 主要试剂及仪器羟自由基(· OH)、一氧化氮合酶(NOS)、超氧化物歧化酶(SOD)试剂盒均购于南京建成生物研究所; 牛TNF-α、IL-1β、Caspase-3、Bax、Bcl-2、AngⅡ和Ang1-7 ELISA试剂盒均购于南京奥青生物技术公司; 羊抗兔ACE2、ACE多克隆抗体购自美国abcam公司; GAPDH抗体购于南京生兴生物有限公司; 山羊抗兔IgG购于上海生工生物工程有限公司; BCA蛋白定量试剂盒、蛋白裂解液购于上海碧云天生物技术公司; 蛋白标准品购于北京索莱宝公司; PVDF膜购于Millipore公司; 超敏ECL化学发光液购于Tanon公司。
5804R低温高速离心机(德国Eppendorff公司); RT-6000酶标仪(Rayto公司); BS 223S电子天平(德国Sartorius公司); LWD200-37T显微镜(CEWEI公司); 电泳/电转仪(美国Bio-Rad公司); 发光图像分析系统(美国Tanon公司)等。
1.2 试验动物分组及饲养6头健康、体质量相当、分娩日期接近的泌乳期荷斯坦奶牛, 购自南京农业大学畜牧试验站奶牛场。随机分为2组:①正常对照组:m(精) : m(粗)=4 : 6;②高精料组:m(精) : m(粗)=6 : 4。采用单栏、定时、定量喂料, 自由饮水, 每日于04:00、12:30、19:00各饲喂1次。基础日粮组成见表 1。试验用奶牛基础日粮采用Cornell-Penn-Miner System(NRC 2001)设计的日粮配方。
| % | ||||||
| 饲料成分 Ingredient |
对照组 [m(精):m(粗)= 4:6] Control group |
高精料组 [m(精):m(粗)= 6:4] High grain diet group |
营养组成 Nutrient composition |
对照组 [m(精):m(粗)= 4:6] Control group |
高精料组 [m(精):m(粗)= 6:4] Hign Grain diet group |
|
| 玉米青贮Corn silage | 30.0 | 20.0 | 净能Net energy | 6.36 | 6.71 | |
| 苜蓿Alfalfa | 30.0 | 20.0 | 粗蛋白Crude protein | 16.99 | 16.92 | |
| 玉米Corn | 24.3 | 32.0 | 粗脂肪Crude fat | 3.93 | 4.07 | |
| 麸皮Bran | 0.0 | 12.4 | 中性洗涤纤维 Neutral detergent fibers |
36.54 | 31.45 | |
| 豆粕Soybean meal | 13.5 | 13.0 | 酸性洗涤纤维 Acid detergent fibers |
22.51 | 17.56 | |
| 碳酸氢钙Dicalcium bicarbonate | 0.85 | 0.45 | ||||
| 石粉Stone powder | 0.0 | 0.8 | 非纤维性碳水化合物 Non-fibrous carbohydrates |
33.76 | 39.32 | |
| 食盐Salt | 0.35 | 0.35 | ||||
| 预混料Premix | 1.0 | 1.0 | 钙Ca | 0.88 | 0.89 | |
| 总计Total | 100 | 100 | 磷P | 0.43 | 0.43 | |
| 注: 1)1 kg预混料中含维生素D 2 500 U, 维生素A 6 000 U, 维生素E 80 mg, 锌62.5 mg, 铜6.25 mg, 锰50 mg, 碘0.125 mg, 铁62.5 mg, 钴0.125 mg, 钼0.125 mg; 2)净能单位为MJ · kg-1。 Note: 1)Provided per kg of premix:vitamin D 2 500 U, vitamin A 6 000 U, vitamin E 80 mg, Ze 62.5 mg, Cu 6.25 mg, Mn 50 mg, I 0.125 mg, Fe 62.5 mg, Co 0.125 mg; Mo 0.125 mg.2)Net energy unit is MJ · kg-1. |
||||||
经测定, 饲喂至第20周, 乳品质下降, 乳中体细胞数(SCC)明显升高[6]。此时进行乳腺活体取样, 置于液氮速冻后, 部分-80 ℃保存。部分组织样品于4%多聚甲醛中固定。
组织匀浆的制备:用预冷的PBS冲洗组织, 去除残留血液, 称质量后将组织剪碎。取0.1 g乳腺组织置于900 μL PBS中, 置组织匀浆机中4 000 r · min-1破碎组织, 12 000 r · min-1离心10 min, 吸取上层组织破碎匀浆上清液, 待用。
1.3.2 高精料日粮对奶牛乳腺氧化应激指标的影响采用试剂盒测定· OH浓度和总NOS(TNOS)、SOD活性。具体操作方法见试验盒说明书。
1.3.3 高精料日粮诱导奶牛乳腺炎症指标的变化用ELISA试剂盒测定各孔的吸光值(A450), 计算出炎症因子TNF-α、IL-1β质量浓度。操作步骤按试剂盒说明书进行。
1.3.4 高精料日粮对奶牛乳腺凋亡指标的影响采用ELISA试剂盒检测乳腺组织匀浆上清液中Caspase-3、Bax和Bcl-2含量。操作按试剂盒说明书进行。
1.3.5 高精料日粮诱导奶牛乳腺损伤对AngⅡ和Ang1-7浓度的影响采用ELISA试剂盒检测乳腺组织匀浆上清液中AngⅡ和Ang1-7浓度。操作按试剂盒说明书进行。其中AngⅡ试剂盒中标准品稀释后浓度分别为120、80、40、20和10 ng · L-1。Ang1-7试剂盒中标准品稀释后浓度分别为300、200、100、50和25 ng · L-1。
1.3.6 高精料日粮诱导奶牛乳腺损伤中对ACE2和ACE蛋白表达的影响采用Western blot法检测乳腺组织中ACE2和ACE蛋白表达水平。操作方法参照Wang等[7]的方法。ACE2一抗1 : 3 000稀释, ACE一抗1 : 5 000稀释, GAPDH一抗1 : 5 000稀释。蛋白条带的灰度利用Image J软件分析, 均以GAPDH作内参, 目的条带与内参相比得到相对表达量。
1.4 数据统计与分析采用SPSS 16.0软件统计分析, 差异显著性检验采用单因素方差分析(One-way ANOVA, LSD)。所有数值以平均值±标准误(x±SE)表示。
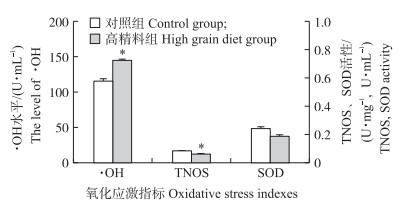
2 结果与分析 2.1 高精料日粮对奶牛乳腺氧化应激指标的影响从图 1可见:与对照组相比, 高精料组奶牛乳腺组织· OH水平显著上升(P < 0.05), TNOS活性显著降低(P < 0.05), SOD活性下降, 但差异不显著(P>0.05)。结果提示, 饲喂高精料日粮可造成奶牛乳腺氧化应激。
|
图 1 高精料日粮对奶牛乳腺氧化应激指标的影响(n=3) Fig. 1 Effect of high grain diet in dairy cow on oxidative stress indexes(n=3) *, **分别表示与对照组相比差异显著(P < 0.05)和差异极显著(P < 0.01)。下同。 *, ** mean significant difference compare with control group at 0.05 level and 0.01 level, respectively. The same as follows. |
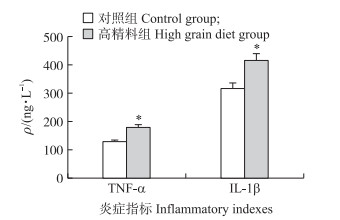
乳腺组织中炎症细胞因子的分泌情况如图 2所示:高精料饲喂组炎症因子TNF-α和IL-1β质量浓度均显著高于对照组(P < 0.05)。提示, 饲喂高精料日粮可增加奶牛乳腺炎症因子的表达和释放。
|
图 2 高精料日粮诱导奶牛乳腺炎症指标的变化(n=3) Fig. 2 High grain diet induces changes in mammary gland inflammation indexes in dairy cow(n=3) |
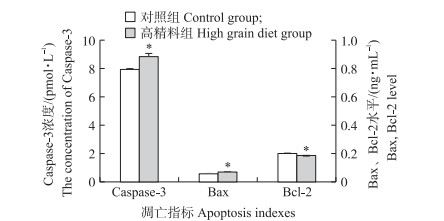
乳腺组织中凋亡指标的检测结果如图 3所示:高精料饲喂组促凋亡蛋白Caspase-3和Bax水平均较对照组显著升高(P < 0.05)。抗凋亡蛋白Bcl-2水平显著下降(P < 0.05)。结果提示, 饲喂高精料日粮可导致奶牛乳腺发生凋亡损伤。
|
图 3 高精料日粮对奶牛乳腺凋亡指标的影响(n=3) Fig. 3 Effect of high grain diet in dairy cow on apoptosis indexes(n=3) |
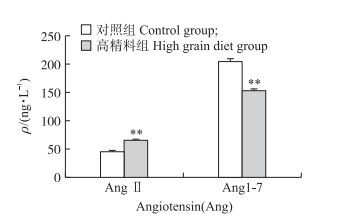
如图 4所示:与对照组相比, 高精料饲喂导致奶牛乳腺AngⅡ质量浓度极显著升高(P < 0.01)。Ang1-7浓度则极显著下降(P < 0.01)。结果提示, AngⅡ释放增多, Ang1-7产生减少, 乳腺处于损伤状态。
|
图 4 高精料日粮诱导奶牛乳腺损伤对AngⅡ和Ang1-7质量浓度的影响(n=3) Fig. 4 Effect of high grain diet induced mammary gland damage in dairy cow on AngⅡ and Ang1-7 concentration(n=3) |
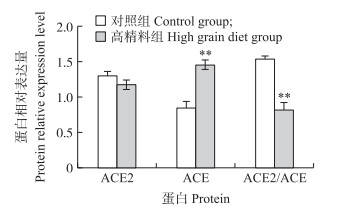
如图 5所示:高精料饲喂导致奶牛乳腺局部ACE2蛋白表达水平下降, 但与对照组相比差异不显著(P>0.05), 但乳腺组织中ACE蛋白表达则极显著升高(P < 0.01)。高精料组ACE2/ACE比值极显著下降(P < 0.01)。即高精料日粮致奶牛乳腺应激及凋亡损伤时, ACE的激活处于优势。
|
图 5 高精料日粮致奶牛乳腺损伤对ACE2、ACE蛋白表达的影响(n=3) Fig. 5 Effect of high grain diet induced mammary gland damage in dairy cow in ACE2 and ACE protein expression(n=3) |
肾素-血管紧张素系统(renin-angiotensin-system, RAS)是循环系统的重要组成部分, 由经典的ACE-AngⅡ-AT1R/AT2R和新的ACE2-Ang1-7-MasR 2条代谢通路组成, 在维持血压稳定、调节水和无机盐的平衡等方面起着至关重要的作用[9]。许多研究已经证实, 在循环系统以外, 体内的多个组织和器官中也存在独立的RAS系统, 称为局部RAS系统, 它们的组成与循环系统一致, 但作用却不尽相同[10]。在乳腺组织中, 同样也被证实存在RAS所有成员的表达, 并且发现乳腺局部存在的RAS同样也是通过ACE-AngⅡ-AT1R/AT2R和新的ACE2-Ang1-7-MasR 2条通路的相互拮抗, 共同维持乳腺细胞的正常生理功能[11]。
已有的研究结果证实, RAS介导或参与了局部组织的促炎和抗炎的调节作用[12]。在多种组织炎性损伤时, 局部RAS处于激活或过度激活状态, 而作为RAS最重要的活性成分, 高水平AngⅡ因可激活还原型辅酶Ⅱ(NADPH)依赖性氧化酶、生成活性氧ROS及炎症因子等, 促进炎症反应, 是促进炎症反应的主要介质[13-14]。ACE2通过降解AngⅡ, 抑制其对炎症上调效应, 生成Ang1-7, 激活MasR, 从而起到拮抗AngⅡ的作用, 实现炎症的下调效应[15]。近年来, 越来越多的研究显示RAS具有调节细胞凋亡的作用, 其中ACE2已被证明在机体多数组织器官中都具有良好的抗氧化应激、降低炎症损伤和减少细胞凋亡的作用。
Santos等[3]研究发现, ACE2能够引起炎症通路上的AngⅡ降解, 生成具有抗炎作用的Ang1-7, 通过MasR抑制下游的NF-κB和MAPK等信号通路的激活, 减少TNF-α等细胞炎症因子的表达和释放, 从而缓解细胞炎症损伤。Xiao等[4]研究发现在急性肺栓塞时, 肺组织中ACE2/ACE值下降, 促凋亡蛋白Bax与Caspase-3表达水平较正常更高, 抑制凋亡蛋白Bcl-2表达水平下降, 提示维持ACE2/ACE的稳定是抑制细胞凋亡的重要手段。Chen等[16]发现细菌脂多糖(LPS)诱导原代培养的大鼠肺微血管内皮细胞发生凋亡, ACE2/ACE值降低, 从而降低LPS诱导的细胞凋亡和炎症。本实验室Wang等[7]研究发现, LPS作用于小鼠乳腺, 可以引起小鼠乳腺发生炎症, 在这个过程中, 小鼠血液中AngⅡ的浓度升高, 在LPS诱导的小鼠乳腺上皮细胞炎症模型中, AngⅡ浓度增加, 提示AngⅡ在乳腺炎症损伤中, 如在其他组织中一样, 是促炎作用的主要介质。刘小倩[17]用AngⅡ诱导牛MAC-T细胞发生氧化应激、炎性损伤和细胞凋亡, 证实ACE2/ACE的稳定是AngⅡ诱导损伤的主要原因。在本试验中, 我们从饲喂高精料导致奶牛乳腺自由基激活、炎性细胞因子释放及细胞凋亡的角度, 以乳腺局部RAS 2条通路中的主要产物(AngⅡ、Ang1-7)和核心(ACE、ACE2)为主线, 探讨了ACE2-Ang-1-7和ACE-AngⅡ 2条通路在乳腺组织氧化应激及细胞凋亡损伤中的相互作用, 结果发现高精料长期饲喂可引起奶牛乳腺自由基激活、炎症因子释放、细胞凋亡, 还发现高精料长期饲喂致奶牛乳腺氧化应激或细胞凋亡损伤时, 乳腺局部AngⅡ水平升高, 同时ACE2和Ang1-7水平均有降低, ACE2/ACE值降低。本结果与以上学者[16-17]在肺等组织上的研究结果一致。
综合以上结果, 我们推测在牛乳腺组织发生氧化应激及凋亡损伤时, AngⅡ浓度增加, ACE2表达下调, 推测AngⅡ和ACE2仍然是关键的调控因子。同在其他组织中一样, 维持ACE2/ACE的稳定可能是抑制乳腺氧化应激及细胞凋亡的重要手段, 其机制有待进一步研究。
| [1] |
Muñoz-Durango N, Fuentes C, Castillo A, et al. Role of the renin-angiotensin-aldosterone system beyond blood pressure regulation:molecular and cellular mechanisms involved in end-organ damage during arterial hypertension[J]. International Journal of Molecular Sciences, 2016, 17(7): 797. DOI:10.3390/ijms17070797 |
| [2] |
Suzuki Y, Ruiz-Ortega M, Lorenzo O, et al. Inflammation and angiotensin Ⅱ[J]. The International Journal of Biochemistry & Cell Biology, 2003, 35(6): 881-900. |
| [3] |
Santos R A S, Ferreira A J, Verano-Braga T, et al. Angiotensin-converting enzyme 2, angiotensin-(1-7)and Mas:new players of the renin-angiotensin system[J]. Journal of Endocrinology, 2013, 216(2): 1-17. |
| [4] |
Xiao H L, Zhao L X, Yang J, et al. Association between ACE2/ACE balance and pneumocyte apoptosis in a porcine model of acute pulmonary thromboembolism with cardiac arrest[J]. Molecular Medicine Reports, 2018, 17(3): 4221-4228. |
| [5] |
Li Y, Cao Y, Zeng Z, et al. Angiotensin-converting enzyme 2/angiotensin-(1-7)/Mas axis prevents lipopolysaccharide-induced apoptosis of pulmonary microvascular endothelial cells by inhibiting JNK/NF-κB pathways[J]. Scientific Reports, 2015, 5: 8209. DOI:10.1038/srep08209 |
| [6] |
刘小倩, 刘颖, 荣超, 等. ACE2在奶牛乳腺中的表达定位及其抗炎性损伤作用的研究[J]. 畜牧兽医学报, 2017, 48(3): 552-560. Liu X Q, Liu Y, Rong C, et al. Expression Localization of angiotensin converting enzyme 2(ACE 2)in dairy cow mammary gland and its anti-inflammation effect[J]. Acta Veterinaria et Zootechnica Sinica, 2017, 48(3): 552-560 (in Chinese with English abstract). |
| [7] |
Wang K, Liu X, Hang X, et al. The correlation between inflammatory injury induced by LPS and RAS in EpH4-Ev cells[J]. International Immunopharmacology, 2017, 46: 23-30. DOI:10.1016/j.intimp.2017.02.016 |
| [8] |
曹洋, 叶平生, 荣超, 等. 高精料日粮对干奶期奶山羊肝脏中游离氨基酸重分配的影响[J]. 南京农业大学学报, 2016, 39(2): 289-296. Cao Y, Ye P S, Rong C, et al. The effects of high concentrate diets on the redistribution offree amino acids in the liver of goats in dry period[J]. Journal of Nanjing Agricultural University, 2016, 39(2): 289-296 (in Chinese with English abstract). DOI:10.7685/jnau.201507017 |
| [9] |
Ribeiro-Oliveira A, Jr, Nogueira A I, Pereira R M, et al. The renin-angiotensin system and diabetes:an update[J]. Vascular Health & Risk Management, 2008, 4(4): 787-803. |
| [10] |
Sadik N A, Metwally N S, Shaker O G, et al. Local renin-angiotensin system regulates the differentiation of mesenchymal stem cells into insulin-producing cells through angiotensin type 2 receptor[J]. Biochimie, 2017, 137: 132-138. DOI:10.1016/j.biochi.2017.03.002 |
| [11] |
荣超.血管紧张素转换酶2(ACE2)在奶牛乳腺中的表达分布及其抗损伤作用[D].南京: 南京农业大学, 2016. Rong C. Study on angiotensin converting enzyme2(ACE2)in bovine mammary: its expression localization and function of anti-injury[D]. Nanjing: Nanjing Agricultural University, 2018(in Chinese with English abstract). http://cdmd.cnki.com.cn/Article/CDMD-10307-1017260065.htm |
| [12] |
Agarwal D, Welsch M A, Keller J N, et al. Chronic exercise modulates RAS components and improves balance between pro-and anti-inflammatory cytokines in the brain of SHR[J]. Basic Research in Cardiology, 2011, 106(6): 1069-1085. DOI:10.1007/s00395-011-0231-7 |
| [13] |
Diep Q N, Amiri F, Touyz R M, et al. PPAR alpha activator effects on AngⅡ-induced vascular oxidative stress and inflammation[J]. Hypertension, 2002, 40(6): 866-871. DOI:10.1161/01.HYP.0000037969.41360.CC |
| [14] |
Maneesai P, Bunbupha S, Kukongviriyapan U, et al. Effect of asiatic acid on the AngⅡ-AT1R-NADPH oxidase-NF-κB pathway in renovascular hypertensive rats[J]. Naunyn-Schmiedeberg's Archives of Pharmacology, 2017, 390(10): 1073-1083. DOI:10.1007/s00210-017-1408-x |
| [15] |
de Morais S D B, Shanks J, Zucker I H. Integrative physiological aspects of brain ras in hypertension[J]. Current Hypertension Reports, 2018, 20(2): 10. DOI:10.1007/s11906-018-0810-1 |
| [16] |
Chen Q F, Kuang X D, Yuan Q F, et al. Lipoxin A4 attenuates LPS-induced acute lung injury via activation of the ACE2-Ang-(1-7)-Mas axis[J]. Innate Immun, 2018, 5(24): 285-296. |
| [17] |
刘小倩.血管紧张素转化酶2(ACE2)在奶牛乳腺细胞应激和凋亡损伤中的保护作用[D].南京: 南京农业大学, 2018. Liu X Q. Protective effect of ACE2 on cellular stress and apoptosis injuries in mammary gland epithelial cells of cows[D]. Nanjing: Nanjing Agricultural University, 2018(in Chinese with English abstract). |




