文章信息
- 金四华, 杨磊, 童雨翠, 范心凤, 何婷婷, 汪加发, 李永胜, 耿照玉
- JIN Sihua, YANG Lei, TONG Yucui, FAN Xinfeng, HE Tingting, WANG Jiafa, LI Yongsheng, GENG Zhaoyu
- 肉鸭PRKAA1和PRKAA2基因表达水平及其与剩余采食量性状的相关性分析
- Expression levels of PRKAA1 and PRKAA2 and their correlations with residual feed intake in meat-type ducks
- 南京农业大学学报, 2018, 41(5): 925-930
- Journal of Nanjing Agricultural University, 2018, 41(5): 925-930.
- http://dx.doi.org/10.7685/jnau.201802012
-
文章历史
- 收稿日期: 2018-02-06
2. 黄山强英鸭业有限公司, 安徽 黄山 245461;
3. 黄山市畜牧兽医技术推广中心, 安徽 黄山 245000
2. Huangshan Qiangying Duck Breeding Co., Ltd., Huangshan 245461, China;
3. Extension Center for Animal Husbandry and Veterinary Medicine of Huangshan City, Huangshan 245000, China
我国是世界上肉鸭生产和消费量最大的国家,肉鸭生产已成为我国畜牧业重要组成部分。现代肉鸭生产中,饲料成本大约占生产总成本的60%~70%,因此提高饲料效率、降低生产成本是提高肉鸭生产效率和养殖效益的重要手段。近年来,剩余采食量(residual feed intake,RFI)作为重要经济指标首次引入到肉鸭的育种工作中[1]。RFI是指动物实际采食量与用于维持生长的预期采食量之差,RFI反映的是由畜禽本身遗传背景决定的代谢差异[2],与畜禽的体型大小及生产性能等性状相互独立,因此RFI是衡量畜禽饲料效率的有效指标。国内外学者研究表明,影响RFI的因素主要包括机体组成、营养物质的吸收率、新陈代谢能力、免疫反应、能量代谢与利用率等[3-5],其中能量利用率是影响RFI的重要因素[6]。
单磷酸腺苷激活蛋白激酶(AMP-activated protein kinase,AMPK)是一种丝氨酸/苏氨酸激酶,是真核生物细胞内一种重要的能量调节器[7]。AMPK是由α、β、γ 3种亚基组成的高度保守的异源三聚体蛋白激酶,α亚基含有激酶活性调控区,具有α1、α2两种异构形式,主要通过N-端Thr172的磷酸化调控AMPK的活性。PRKAA1 (AMP-activated protein kinase catalytic subunit alpha-1)基因和PRKAA2基因分别编码AMPK α1和α2亚基,在细胞中充当细胞能量感受器,负责调控细胞内AMP/ATP值,在能量平衡的调节过程中起重要作用[8]。Apoorv等[9]在小鼠中研究发现,PRKAA1和PRKAA2基因参与机体的能量代谢过程。田万强[10]研究报道,PRKAA1基因多态性与肌内脂肪含量显著相关,PRKAA2基因第4外显子多态性与背膘厚、眼肌面积等生长性状显著关联。Zhong等[11]研究表明,PRKAA1和PRKAA2基因可通过磷酸化调控乙酰辅酶A的活性,从而感受机体的能量变化。Jin等[12]在黄羽肉鸡中研究发现,AMPK家族基因的多态性与肉鸡的生长、采食量和饲料效率性状显著相关。因此,PRKAA1和PRKAA2是影响饲料效率的重要候选基因。
目前,关于PRKAA1与PRKAA2基因的表达水平与肉鸭饲料效率的相关性报道较少。因此,本试验以具有完整系谱记录的H系肉鸭为研究对象,采用荧光定量PCR法(qPCR)检测PRKAA1和PRKAA2在高、低饲料效率组间肉鸭胸大肌、腿肌和肝脏中的差异表达水平及其与剩余采食量性状的相关性,为研究PRKAA1和PRKAA2基因对饲料效率的调控以及选育高饲料效率肉鸭提供试验依据。
1 材料与方法 1.1 试验材料供试材料由黄山强英鸭业有限公司提供,试验鸭具有4个世代完整的系谱记录。挑选1日龄体质量相近的H系肉公鸭混合饲养至21日龄,所有试验鸭饲养于同一栋鸭舍,统一饲养管理。试验期间自由采食和饮水,正常免疫。基础日粮参考我国《肉鸭饲养标准:NY/T 2122—2012》,饲料配方由2阶段组成。2阶段日粮营养水平见表 1。
| % | ||
| 日粮营养组成 Ingredients |
1~14日龄 1-14 day old |
15~42日龄 15-42 day old |
| 代谢能Metabolizable energy | 11.82 | 12.35 |
| 粗蛋白Crude protein | 19.00 | 18.00 |
| 钙Calcium | 0.95 | 0.80 |
| 总磷Total phosphorus | 0.62 | 0.51 |
| 非植酸磷Nonphytate phosphorus | 0.40 | 0.30 |
| 赖氨酸Lysine | 1.28 | 1.15 |
| 蛋氨酸Methionine | 0.48 | 0.40 |
| 胱氨酸Cystine | 0.30 | 0.29 |
| 注:代谢能单位是MJ · kg-1。The unit of metabolizable energy is MJ · kg-1. | ||
21日龄时全群称体质量,并挑选健康强健、体质量相近的1 000只肉公鸭转至单笼饲喂。试验鸭自由采食和饮水,参照黄山强英鸭业有限公司饲养管理规程和免疫程序,试验至42日龄。记录所有个体21日龄体质量(BW21)、42日龄体质量(BW42)、日采食量(ADFI)和日增重(ADG)。根据采食量和日增重,计算代谢体质量(MBW0.75)、饲料转化率(FCR)和剩余采食量(RFI)。RFI=ADFI-(a0+a1 × MBW0.75+a2 × ADG),其中a0为截距,a1、a2为回归系数。RFI的计算由SAS 9.4线性拟合函数完成。
根据所有个体RFI的排序并综合考虑FCR等性状,筛选出高、低RFI个体各8只,断颈屠宰后采集胸大肌、腿肌和肝脏,将采集的组织样放入1.5 mL装有RNA Later(Ambion,美国)的冻存管中,4 ℃过夜后迅速置于-80 ℃冰箱中保存备用。
1.3 总RNA提取与cDNA第1链合成采用OMEGA试剂盒(R6834,美国)提取胸大肌、腿肌和肝脏中的总RNA。利用NanoDrop 2000分光光度计(ThermoFisher Scientific,美国)测定总RNA浓度、A230、A260与A280,用10 g · L-1琼脂糖凝胶电泳检测RNA样品完整性。
以总RNA为模板,按照EasyScript First-Strand cDNA Synthesis Super Mix(TransGen Biotech,北京)合成cDNA第1链。反应体系:总RNA 1.0 μg,Oligo(dT)181.0 μL,2×ES Reaction Mix 10.0 μL,EasyScript RT/RI Enzyme Mix 1.0 μL,加ddH2O至20.0 μL。摇匀后42 ℃孵育15 min;85 ℃5 s,温度降至4 ℃,终止反应,产物置于-20 ℃保存备用。
1.4 引物设计、反转录质量检测及目的基因标准品制备根据GenBank中PRKAA1、PRKAA2和β-actin的mRNA序列,按照荧光定量PCR(qPCR)跨内含子引物设计原则,采用在线Primer 3.0软件设计引物,采用NCBI Primer-BLAST进行引物特异性检测。引物序列由上海生工生物科技有限公司合成(表 2)。
| 基因 Gene |
序列号 GenBank sequence |
引物对序列(5′→3′) Primer pairs sequence |
产物长度/bp Products size |
退火温度/℃ Annealing temperature |
| PRKAA1 | XM_013105491.1 | GAGTGCCATTCTTGGTAGC/CGACACACTTCAGCCATGAT | 157 | 60 |
| PRKAA2 | XM_005020808.3 | TCGGGAGGTCTGTGAGAAAT/AGGTAGAACTCGCTGGCTTG | 147 | 60 |
| β-actin | NM_001310421.1 | TTACCAACACCCACACCCTT/TGCTGCTGATACCTTCACCA | 13 960 |
PCR扩增程序:95 ℃ 5 min;95 ℃ 30 s,60 ℃ 30 s,72 ℃ 30 s,34个循环;72 ℃ 5 min。PCR反应体系:cDNA模板1.5 μL,上、下游引物(10 μmol · L-1)各1.0 μL,PCR Master Mix 12.5 μL,加ddH2O至总体积25.0 μL。PCR反应产物经20 g · L-1琼脂糖凝胶电泳检测,分析内参基因和目的基因反转录质量;采用DNA纯化回收试剂盒切胶回收目的片段,将其用pGM-T载体连接后转化大肠杆菌Top10感受态细胞,挑取转化子接种于含有氨苄青霉素的LB培养基中,连接过夜后,挑选阳性转化子进行测序。用质粒提取试剂盒提取序列比对正确的阳性克隆质粒pGM-T-PRKAA1和pGM-T-PRKAA2,采用NanoDrop 2000分光光度计测其浓度后作为标准品备用。
1.5 荧光定量PCR检测采用SYBR Green Ⅰ嵌合荧光检测法制作标准曲线。将每个待测样品反转录产物等体积混合,用cDNA混合样优化qPCR反应的退火温度、引物浓度和模板浓度等条件, 最终确定的qPCR引物浓度为0.25 μmol · L-1,退火温度为60 ℃,模板10倍稀释。将构建的标准品质粒进行101、102、103、104、105和106系列稀释,以其作为标准品进行qPCR反应,每个样品3个重复,并设置阴性对照,按照CT及标准品浓度分别对目的基因和内参基因制作标准曲线。利用ABI PRISM 7500荧光定量仪(Applied Biosystem,美国)进行qPCR反应。qPCR反应程序:95 ℃预变性5 min;95 ℃ 10 s,60 ℃ 10 s,共40个循环;95 ℃ 15 s,60 ℃ 1 min,95 ℃ 30 s,60 ℃ 15 s。qPCR反应体系(15.0 μL):2 × SYBR Green PCR Mater Mix 7.5 μL, cDNA 1.0 μL, 上、下游引物(10 μmol · L-1)各0.25 μL,RNase-free ddH2O 6.0 μL。每个试验样品3个重复,每组用RNase-free ddH2O代替模板作阴性对照。
1.6 统计分析所有数据经过Excel 2010预处理,根据目的基因和内参基因的CT值,采用2-ΔΔCT法计算目的基因的相对表达量[13]。采用SAS 9.4软件(SAS Institute Inc.,Cary,NC)中t检验分析基因差异表达规律。用Bivariate Correlation程序分析目的基因表达量与剩余采食量性状的相关性。试验数据以x±SE表示。
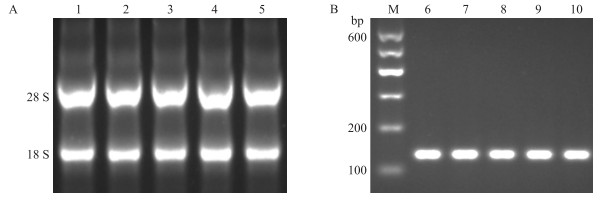
2 结果与分析 2.1 总RNA及反转录质量检测由图 1-A可见:提取的总RNA经琼脂糖凝胶电泳检测,分为清晰的18 S和28 S条带,表明提取的总RNA完整性较好。经NanoDrop 2000检测,所有样品A260/A280值为1.8~2.0,A260/A230值大于2.0,表明总RNA纯度较好。以β-actin为内参基因,通过琼脂糖凝胶检测能够看到清晰的139 bp目的条带,表明反转录生成的cDNA完整性好(图 1-B)。
|
图 1 总RNA(A)和β-actin的PCR产物(B)的电泳检测 Figure 1 The agarose electrophoresis of total RNA(A)and PCR products of β-actin(B) M. DNA标准品DNA marker;1-5.总RNA Total RNA;6-10. β-actin. |
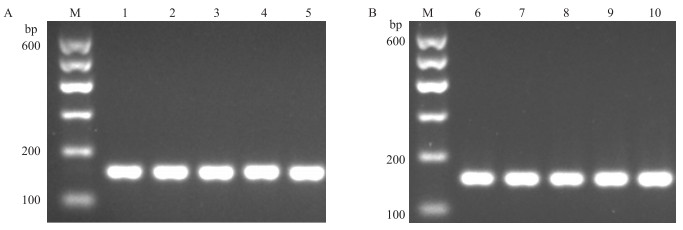
由图 2可知:目的基因PCR扩增产物条带特异性好,片段大小与预计片段长度157 bp和147 bp相符。PCR鉴定的阳性转化子送公司进行测序,测序结果与GenBank数据库中的PRKAA1和PRKAA2序列进行比对,同源性为100%,表明目的片段标准品构建成功,可以满足后续定量PCR试验的需要。
|
图 2 PRKAA1 (A)和PRKAA2 (B)基因PCR产物的电泳图 Figure 2 PCR products of the PRKAA1 (A)and PRKAA2 (B)gene by agarose electrophoresis M. DNA标准品DNA marker;1-5. PRKAA1基因的PCR产物PCR products of PRKAA1;6-10. PRKAA2基因PCR产物PCR products of PRKAA 2. |
根据RFI排序,选择高、低RFI个体各8只,2组个体日采食量、日增重、代谢体质量、饲料转化率和剩余采食量的描述性统计分析见表 3。结果表明,高RFI组肉鸭日采食量、饲料转化率和剩余采食量极显著高于低RFI组(P < 0.01),日增重显著低于低RFI组(P < 0.05)。
| 性状Trait | 高RFI组HRFI group | 低RFI组LRFI group |
| 日采食量/(g·d-1) Average daily feed intake(ADFI) | 290.67±16.19A | 263.91±13.61B |
| 日增重/(g·d-1) Average daily gain(ADG) | 128.76±7.25b | 139.84±7.28a |
| 代谢体质量/g Metabolic body weight(MBW0.75) | 352.69±16.92 | 351.71±15.75 |
| 饲料转化率Feed conversion ratio(FCR) | 2.26±0.03A | 1.88±0.02B |
| 剩余采食量/(g·d-1) Residual feed intake | 21.64±1.18A | -19.66±2.12B |
| 注:同一行不同小写和大写字母分别表示差异显著(P < 0.05)和差异极显著(P < 0.01)。 Note:Different lowercase and uppercase letters in the same line indicate significant differences at 0.05 and 0.01 levels,respectively. | ||
由图 3-A可知:PRKAA1 mRNA在高、低RFI组肉鸭胸大肌、腿肌和肝脏中均有表达,在低RFI组肉鸭胸大肌中表达量极显著高于高RFI组(P < 0.01),在腿肌中表达量显著高于高RFI组(P < 0.05)。高、低RFI组肝脏中PRKAA1 mRNA表达水平差异不显著。由图 3-B可见:PRKAA2 mRNA在高、低RFI组胸大肌、腿肌和肝脏中均有表达,低RFI组肉鸭胸大肌和腿肌中相对表达量显著高于高RFI组(P < 0.05),肝脏中两组PRKAA2 mRNA表达量无显著差异。

|
图 3 高、低RFI组肉鸭胸大肌、腿肌和肝脏中PRKAA1 (A)与PRKAA2 (B)mRNA的差异表达 Figure 3 Differential expression of PRKAA1 (A)and PRKAA2 (B)mRNA in the pectoralis major muscle, leg muscle and liver in meat-type ducks between HRFI and LRFI group *,* *表示差异显著(P < 0.05)和差异极显著(P < 0.01)。下同。 *, * * indicate significant differences at 0.05 and 0.01 levels. The same as follows. |
由表 4可知:PRKAA1 mRNA在胸大肌中表达量与日采食量、饲料转化率和RFI均呈显著负相关(P < 0.05),腿肌中表达量与日采食量和RFI显著负相关(P < 0.05)。PRKAA2 mRNA在胸大肌中表达量与日采食量和RFI显著负相关(P < 0.05),腿肌中表达量与RFI呈显著负相关关系(P < 0.05)。
| 基因 Gene |
组织 Tissue |
日采食量 ADFI |
日增重 ADG |
代谢体质量 MBW0.75 |
饲料转化率 FCR |
剩余采食量 RFI |
| PRKAA1 | 胸大肌Pectoralis major muscle | -0.52* | 0.15 | -0.21 | -0.41* | -0.45* |
| 腿肌Leg muscle | -0.41* | 0.22 | -0.17 | -0.53 | -0.47* | |
| PRKAA2 | 胸大肌Pectoralis major muscle | -0.44* | 0.24 | -0.06 | -0.57 | -0.55* |
| 腿肌Leg muscle | -0.26 | 0.49 | 0.35 | -0.47 | -0.62* |
饲料效率性状是现代肉鸭育种中重要经济性状,剩余采食量(RFI)作为衡量饲料效率的重要指标被引入到肉鸭育种中。RFI是一个负向选择性状,RFI值越小,则动物饲料利用率越高。RFI的遗传力值为0.25~0.45,是一个中等遗传力性状,因而可以通过遗传选育方法对RFI进行改良[14-15]。近年来,随着测序技术和全基因组关联分析策略的快速发展,国内外学者对影响RFI的基因及其信号通路进行分析,发现调控能量代谢的基因是影响饲料效率的重要候选基因[16-17]。
AMPK是机体内能量代谢的重要参与者,其活性主要受细胞内能量状态(AMP/ATP)的调控[7],在机体能量平衡过程中起重要作用。PRKAA1和PRKAA2属于AMPK家族的重要成员,其含有AMP和ATP结合位点,并可通过磷酸化过程调控AMPK活性,进而影响细胞的能量平衡[18]。早期研究表明,PRKAA1和PRKAA2基因敲除的小鼠通过抑制胰岛素分泌进而调控机体的能量代谢[19],PRKAA2基因单倍型与人的2型糖尿病显著相关[20]。Kelly等[21]在肉牛中研究表明,PRKAA1基因与剩余采食量性状有关,是影响饲料效率的重要候选基因。
目前,关于PRKAA1和PRKAA2的研究主要集中在人类疾病、模式生物及大家畜中,在肉鸭中报道较为少见。本试验结果表明,PRKAA1基因在低RFI组(高饲料效率)胸大肌中表达量极显著高于高RFI组,低RFI组腿肌中表达量显著高于高RFI组;PRKAA2基因在低RFI组胸大肌和腿肌中表达量显著高于高RFI组。因PRKAA1和PRKAA2基因含有AMP和ATP结合位点,低RFI组PRKAA1和PRKAA2基因表达量显著上调,可引起AMP/ATP值上升,进一步激活AMPK活性,使机体能够快速感受细胞的能量变化状态,提高能量利用效率,从而提高饲料利用率[22-23]。Dyck等[24]研究报道,PRKAA2基因可通过磷酸化转录因子来调控机体的能量变化,从而保持机体能量平衡。Young等[25]对猪RFI研究表明,猪饲料利用率与能量代谢密切相关,饲料效率高的猪能量利用率也高。相关性分析表明,胸大肌PRKAA1基因表达量与日采食量、FCR和RFI显著负相关,腿肌中表达量与日采食量和RFI显著负相关;胸大肌RPKAA2基因表达量与日采食量和RFI显著负相关,这与Bottje等[6]研究结果一致。此外,Kelly等[21]研究也表明,ADP控制的氧化磷酸化基因在低RFI组肉牛中表达量显著高于高RFI组。因此,提高能量利用率,减少能量消耗,能够提高肉鸭饲料效率。
| [1] |
侯水生. 2016年水禽产业现状、技术研究进展及展望[J].
中国畜牧杂志, 2017, 53(6): 143-147.
Hou S S. Current situation, technical progress and prospect of waterfowl industry in 2016[J]. Chinese Journal of Animal Science, 2017, 53(6): 143-147. (in Chinese with English abstract) |
| [2] | Aggrey S E, Karnuah A B, Sebastian B, et al. Genetic properties of feed efficiency parameters in meat-type chickens[J]. Genet Sel Evol, 2010, 42: 25. DOI: 10.1186/1297-9686-42-25 |
| [3] | Aggrey S E, Lee J, Karnuah A B, et al. Transcriptomic analysis of genes in the nitrogen recycling pathway of meat-type chickens divergently selected for feed efficiency[J]. Anim Genet, 2014, 45(2): 215-222. DOI: 10.1111/age.2014.45.issue-2 |
| [4] | Yi G, Yuan J, Bi H, et al. In-depth duodenal transcriptome survey in chickens with divergent feed efficiency using RNA-Seq[J]. PLoS One, 2015, 10(9): e0136765. DOI: 10.1371/journal.pone.0136765 |
| [5] | Lee J, Karnuah A B, Rekaya R, et al. Transcriptomic analysis to elucidate the molecular mechanisms that underlie feed efficiency in meat-type chickens[J]. Mol Genet Genomics, 2015, 290(5): 1673-1682. DOI: 10.1007/s00438-015-1025-7 |
| [6] | Bottje W, Kong B W. Cell biology symposium:feed efficiency:mitochondrial function to global gene expression[J]. J Anim Sci, 2013, 91(4): 1582-1593. DOI: 10.2527/jas.2012-5787 |
| [7] | Hardie D G, Schaffer B E, Brunet A. AMPK:an energy-sensing pathway with multiple inputs and outputs[J]. Trends Cell Biol, 2016, 26(3): 190-201. DOI: 10.1016/j.tcb.2015.10.013 |
| [8] | Dranchak P K, Ekenstedt K J, Valberg S J, et al. Chromosomal assignments for the equine AMPK family genes[J]. Anim Genet, 2006, 37(3): 293-294. DOI: 10.1111/age.2006.37.issue-3 |
| [9] | Apoorv T S, Karthik C, Babu P P. AMP-activated protein kinase(AMPK)is decreased in the mouse brain during experimental cerebral malaria[J]. Neurosci Lett, 2018, 662: 290-294. DOI: 10.1016/j.neulet.2017.10.054 |
| [10] |
田万强.牛AMPK家族7个基因SNP检测及其与生长和肉质性状的关联分析[D].杨凌: 西北农林科技大学, 2013: 50-59.
Tian W Q. Single nucleotide polymorphism of 7 genes of AMPK family and associations with growth and meat quality traits in cattle[D]. Yangling: Northwest A & F University, 2013: 50-59(in Chinese with English abstract). http://cdmd.cnki.com.cn/Article/CDMD-10712-1013347290.htm |
| [11] | Zhong W, Xie Y, Abdallah M, et al. Cellular stress causes reversible, PRKAA1/2-, and proteasome-dependent ID2 protein loss in trophoblast stem cells[J]. Reproduction, 2010, 140(6): 921-930. DOI: 10.1530/REP-10-0268 |
| [12] | Jin S, Moujahid M E, Duan Z, et al. Association of AMPK subunit gene polymorphisms with growth, feed intake, and feed efficiency in meat-type chickens[J]. Poult Sci, 2016, 95(7): 1492-1497. DOI: 10.3382/ps/pew081 |
| [13] | Livak K J, Schmittgen T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2-ΔΔCT method[J]. Methods, 2001, 25(4): 402-408. DOI: 10.1006/meth.2001.1262 |
| [14] | Zhang Y, Guo Z B, Xie M, et al. Genetic parameters for residual feed intake in a random population of Pekin duck[J]. Asian-Australas J Anim Sci, 2017, 30(2): 167-170. |
| [15] | Yuan J, Dou T, Ma M, et al. Genetic parameters of feed efficiency traits in laying period of chickens[J]. Poult Sci, 2015, 94(7): 1470-1475. DOI: 10.3382/ps/pev122 |
| [16] | Bottje W G, Lassiter K, Piekarski-Welsher A, et al. Proteogenomics reveals enriched ribosome assembly and protein translation in pectoralis major of high feed efficiency pedigree broiler males[J]. Front Physiol, 2017, 8: 306. DOI: 10.3389/fphys.2017.00306 |
| [17] | Jing L, Hou Y, Wu H, et al. Transcriptome analysis of mRNA and miRNA in skeletal muscle indicates an important network for differential residual feed intake in pigs[J]. Sci Rep, 2015, 5: 11953. DOI: 10.1038/srep11953 |
| [18] | Hardie D G. Sensing of energy and nutrients by AMP-activated protein kinase[J]. Am J Clin Nutr, 2011, 93(Suppl): 891-896. |
| [19] | Sun G, Tarasov A I, McGinty J, et al. Ablation of AMP-activated protein kinase alpha1 and alpha2 from mouse pancreatic beta cells and RIP2.Cre neurons suppresses insulin release in vivo[J]. Diabetologia, 2010, 53(5): 924-936. DOI: 10.1007/s00125-010-1692-1 |
| [20] | Sun M W, Lee J Y, de Bakker P I, et al. Haplotype structures and large-scale association testing of the 5'-AMP-activated protein kinase genes PRKAA2, PRKAB1, and PRKAB2 with type 2 diabetes[J]. Diabetes, 2006, 55(3): 849-855. DOI: 10.2337/diabetes.55.03.06.db05-1418 |
| [21] | Kelly A K, Waters S M, McGee M, et al. mRNA expression of genes regulating oxidative phosphorylation in the muscle of beef cattle divergently ranked on residual feed intake[J]. Physiol Genomics, 2011, 43(1): 12-23. DOI: 10.1152/physiolgenomics.00213.2009 |
| [22] | Hardie D G. AMP-activated/SNF1 protein kinases:conserved guardians of cellular energy[J]. Nat Rev Mol Cell Biol, 2007, 8(10): 774-785. DOI: 10.1038/nrm2249 |
| [23] | Canto C, Auwerx J. PGC-1alpha, SIRT1 and AMPK, an energy sensing network that controls energy expenditure[J]. Curr Opin Lipidol, 2009, 20(2): 98-105. DOI: 10.1097/MOL.0b013e328328d0a4 |
| [24] | Dyck J R, Kudo N, Barr A J, et al. Phosphorylation control of cardiac acetyl-CoA carboxylase by cAMP-dependent protein kinase and 5'-AMP activated protein kinase[J]. Eur J Biochem, 1999, 262(1): 184-190. DOI: 10.1046/j.1432-1327.1999.00371.x |
| [25] | Young J M, Dekkers J C M. The genetic and biological basis of residual feed intake as a measure of feed efficiency[M]. Wageningen: Wageningen Academic Publishers, 2012: 153-166. |




