文章信息
- 余雅琳, 杨德坤, 高菲, 李琦, 孙露露, 梁剑茹, 周立祥
- YU Yalin, YANG Dekun, GAO Fei, LI Qi, SUN Lulu, LIANG Jianru, ZHOU Lixiang
- 植物多酚吸持-硫酸铁沉淀法去除水中氨氮的效果及影响因素研究
- Factors affecting removal of ammonium nitrogen in simulated wastewater through complexation by natural plant polyphenols and subsequent precipitation by ferric sulfate
- 南京农业大学学报, 2018, 41(1): 113-119
- Journal of Nanjing Agricultural University, 2018, 41(1): 113-119.
- http://dx.doi.org/10.7685/jnau.201702037
-
文章历史
- 收稿日期: 2017-02-27
氨氮是衡量水质的重要指标, 去除氨氮是废水处理不可或缺的环节[1-2]。目前常见的处理方法包括硝化与反硝化的生物法; 反渗透、气提、离子交换、吸附和超临界水氧化等物化方法[3]。吸附法以操作简单, 低能耗、低成本和高安全性以及可回收氨氮等优点受到广泛关注, 然而, 基于固-液相吸附的传统固体吸附材料对氨氮的吸附存在吸附量不高和成本较高等缺点。例如, 对氨氮有较大吸附能力的天然沸石吸附量也多数在10 mg·g-1以下[4-5]。因此, 开发廉价、高效的吸附剂具有重要的意义, 但迄今比沸石更加优良的天然吸附剂仍不多见[6]。
来源于植物根、树皮和果实的天然植物多酚类物质Y (以下简称“植物多酚Y”)因带有大量酚羟基[7], 且其pHPZC一般为5~6[8], 所以pH值在中性以上环境下, 酚羟基会解离而带负电荷, 从而具有较大的铵离子结合量。植物多酚产品有相当部分可溶(可与氨氮络合), 不溶的一部分则以极细小的颗粒态存在(可吸附氨氮), 植物多酚溶于水后形成稳定的悬浮液(胶体)[7]。吸持氨氮的这种植物多酚胶体易通过铁、铜等金属盐沉淀, 从而使废水中的氨氮得以去除和回收[7]。我们曾报道, 通过植物多酚Y对氨氮进行吸持, 然后采用硫酸铁沉淀法对猪场废水中氨氮吸持去除率是天然沸石的3.3倍[7]。由于猪场废水共存许多与氨离子竞争植物多酚吸附位的阳离子等物质(如盐分), 因此, 这种吸持-沉淀法在仅含单一氨氮的模拟废水中的效果, 常见阳离子对其的影响以及pH值、温度与植物多酚加入量在仅含单一氨氮的模拟废水系统中的影响等问题还鲜有报道, 开展这些研究对推广这种新方法有重要意义。
1 材料与方法 1.1 供试材料植物多酚Y购于郑州双阳化工有限公司, 植物多酚含量不小于73%, 不溶物含量不大于2.5%, 最大溶解度为41.5%(25 ℃), pH7.39, 总氮(TN)含量5.47 g·kg-1, 总磷(TP)含量1.12 g·kg-1。其结构和基本理化性质详见文献[7]。
单一氨氮模拟废水:按试验需要浓度用NH4Cl配制; K+、Na+、Mg2+、Ca2+等金属阳离子均由其氯盐按需要浓度配制; 用H2SO4或NaOH调节废水pH值。
1.2 等温吸持沉淀试验向一系列三角瓶中分别加入150 mg植物多酚Y, 再加入50.0 mL质量浓度分别为30、80、150、300、500、800和1 000 mg·L-1的单一氨氮模拟废水, 调节废水pH值为7.5;180 r·min-1、15 ℃下振荡3 h后(预试验发现此时Y对氨氮的吸持已完全达到平衡)加入沉淀剂硫酸铁溶液使其在体系中最终质量浓度为15 mg·L-1, 充分摇匀后静置30 min, 取上清液过0.45 μm滤膜后测定剩余氨氮浓度(预试验发现:亲水性滤膜对模拟废水中氨氮的吸持损失小于0.2%;加入15 mg·L-1硫酸铁时对氨氮浓度无显著影响)。
1.3 影响氨氮吸持-沉淀去除的因素试验 1.3.1 温度温度设置为10、20、30、40和50 ℃。其他条件为:起始氨氮质量浓度500 mg·L-1, 植物多酚Y质量浓度为3 000 mg·L-1, pH7.5, 振荡平衡后其余步骤按1.2节进行。
1.3.2 废水pH值废水pH值分别调节为3.0、5.0、6.0、7.0、8.0、9.0和10.0后, 其余条件同1.3.1节, 28 ℃振荡平衡后其余操作步骤按1.2节的方法进行。
1.3.3 植物多酚Y投加量向一系列三角瓶中分别加入不同量的植物多酚Y, 使体系中Y的最终起始质量浓度为500、1 000、3 000、5 000和10 000 mg·L-1。其他条件为:氨氮质量浓度800 mg·L-1、pH7.5, 28 ℃、180 r·min-1振荡平衡后, 其余步骤按1.2节的方法进行。
1.3.4 单一共存阳离子向一系列三角瓶中分别加入150 mg植物多酚Y和50 mL氨氮和单一金属阳离子K+、Na+、Ca2+、Mg2+的混合液, 其中体系中起始氨氮质量浓度为800 mg·L-1, K+、Na+、Ca2+、Mg2+的质量浓度分别为25、100和250 mg·L-1。其他条件和步骤按1.3.3节的方法进行。
1.3.5 植物多酚Y的红外表征利用Nexus 870型光谱仪对吸持氨氮前、后的植物多酚Y进行红外表征。
1.4 测定方法及结果计算氨氮采用文献[9]纳氏试剂分光光度法测定; 采用雷磁pHS-3C精密pH计测定pH值。
植物多酚Y对氨氮的吸持量qt(mg·L-1)和去除率η(%)分别按公式(1)和(2)计算。
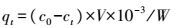
|
(1) |
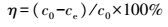
|
(2) |
式中:c0为吸持前溶液的氨氮质量浓度(mg·L-1); ce为吸持平衡时溶液里剩余的氨氮质量浓度(mg·L-1); ct为t时刻溶液里的氨氮质量浓度(mg·L-1); V为溶液的体积(mL); W为植物多酚Y的投加量(g); η为去除率。
Freundlich和Langmuir等温模型分别用公式(3) [10]和公式(4) [11-12]拟合。
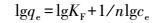
|
(3) |

|
(4) |
式中:qe为吸持平衡时单位质量Y吸持的氨氮量(mg·g-1); qm为单位质量Y表面吸持满单分子层氨氮时的饱和吸持量(mg·g-1); KF为Freundlich系数; KL为Langmuir系数; 1/n为Freundlich常数。
热力学参数通过公式(5)计算。
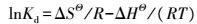
|
(5) |
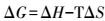
|
(6) |
式中:Kd为热力学常数(Kd=qe/ce); T为热力学温度(K); R为普适气体常数, 8.314 J·mol-1·K-1; ΔHΘ为焓变(kJ·mol-1); ΔSΘ为熵变(J·mol-1·K-1); ΔG为吉布斯自由能(kJ·mol-1); qe与ce同公式(3)和(4)。
试验所得数据采用Excel 2003、SPSS 19.0软件进行整理和统计分析, 用Origin 8.0绘图。
2 结果与讨论 2.1 植物多酚Y对氨氮的吸持等温线从图 1可知:Y对氨氮的吸持量与初始氨氮浓度呈正相关关系, 当废水初始氨氮质量浓度由30 mg·L-1逐步升高到1 000 mg·L-1时, Y对氨氮的吸持量从2.80 mg·g-1增大至31.9 mg·g-1。这比我们以前报道的Y对猪场废水的氨氮吸持量为15.5 mg·g-1的数值高出近1倍[7], 这可能是由于模拟废水中仅含单一氨氮, 而猪场废水中还含有其他常见的竞争性离子。Y对氨氮的吸持量与初始氨氮浓度呈正相关关系, 这是因为当Y的使用量一定时, 其表面积也是一定的; 在氨氮初始浓度较低时, Y对氨氮的吸持位点还没达到饱和。随着溶液中氨氮初始浓度的升高, 可供交换的氨氮增多, 溶液与Y表面所形成的氨氮浓度差增大[13], 因此, 氨氮初始浓度在30~1 000 mg·L-1范围内升高时, Y对模拟废水中氨氮的吸持量也逐步提高。

|
图 1 氨氮初始浓度对植物多酚Y吸持氨氮的影响 Figure 1 Effects of ammonium initial concentration on ammonium adsorption by plant polyphenols Y |
分别用Freundlich和Langmuir吸持等温式对Y吸持氨氮进行拟合, 拟合的吸持等温线参数见表 1。Freundlich和Langmuir等温模型的R2分别为0.983和0.687。
| Freundlich | Langmuir | |||
| 1/n | KF/(L·g-1) | qm/(mg·g-1) | KL/(L·mg-1) | |
| 0.67 | 0.267 | 46.51 | 0.001 4 | |
Freundlich吸持等温模型很好地描述植物多酚Y对模拟废水中氨氮的吸持特征。1/n=0.67 < 1, 说明28 ℃的温度条件有利于Y吸持氨氮, 且吸持较易进行[14]。Langmuir吸持等温方程拟合, 求得物质Y对氨氮的最大吸持量qm为46.51 mg·g-1, KL为0.001 4 L·mg-1。该吸持量比常见的沸石(6 mg·g-1)[4]、生物炭(3.5 mg·g-1)[6]高很多, 甚至高于一些阳离子交换树脂(12.5 mg·g-1)[15]。比较Freundlich的R2(0.983)和Langmuir的R2(0.687)可知, 对于植物多酚Y, Langmuir吸持等温式的拟合效果并不十分理想。Langmuir等温模型只适用于解释单分子层的化学吸持情况, 故推断Y对氨氮的吸持行为并非单纯的以化学作用为主的单分子层吸持, 而是发生在固液交界面的多分子层吸持。
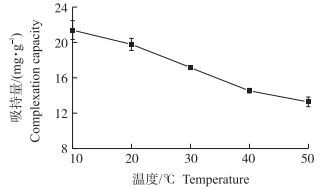
2.2 植物多酚Y对氨氮的吸持热力学温度对植物多酚Y吸持氨氮具有较大影响。如图 2所示, 在10~50 ℃范围内, Y对氨氮的吸持量与温度呈负相关, 温度升高, Y对氨氮的吸持量逐渐减少。10 ℃时Y对氨氮的吸持量达到21.4 mg·g-1, 当温度升高到40 ℃时, 吸持量下降到14.5 mg·g-1, 降幅达32.2%。
|
图 2 温度对植物多酚Y吸持氨氮的影响 Figure 2 Effects of temperature on ammonia nitrogen adsorption by plant polyphenols Y |
利用公式(5)计算植物多酚Y吸持氨氮的热力学参数。当吸持温度变化不大时, ΔHΘ可近似看作常数[16]。因此, 通过ln (qe/ce)对1/T作图可得一条直线(图 3), 由直线的截距和斜率可求得ΔH和ΔS及各温度条件下的ΔG(表 2)。在不同的温度下, ΔG均为负值。这表明Y对氨氮的吸持是自发进行的, 但随着温度的升高, ΔG值也升高。温度越高, 吸持反应的自发性越差, 越不有利于吸持的进行。本试验的研究结果与之一致。ΔH < 0, 表明Y对氨氮的吸持为放热过程, 这与温度升高Y对氨氮的吸附量减少相吻合。另外, ΔS < 0, 说明Y对氨氮的吸持为熵减的过程, 吸持体系的混乱度随着温度的升高而减少, 因此, 温度越高, 吸持量越低。Yu等[17]认为:当ΔG在0~-20 kJ·mol-1范围内变化时, 吸附剂对吸附质发生的主要是物理吸附; 当ΔG在-80~-400 kJ·mol-1范围内变化时, 吸附剂对吸附质发生的主要是化学吸附。植物多酚Y吸持氨氮的ΔG为-7.4 kJ·mol-1左右, 在0~-20 kJ·mol-1范围内, 因此, 植物多酚Y对氨氮的吸持可能主要是物理吸持。

|
图 3 植物多酚Y对氨氮吸持的热力学参数图 Figure 3 Plot of ln (qe/ce)vs 1/T for the adsorption of ammonia nitrogen by plant polyphenols Y |
| ΔH/(kJ·mol-1) | ΔS/(J·mol-1·K-1) | ΔG/(kJ·mol-1) | ||||
| 10 ℃ | 20 ℃ | 30 ℃ | 40 ℃ | 50 ℃ | ||
| -10.1 | -8.8 | -7.6 | -7.5 | -7.4 | -7.3 | -7.2 |
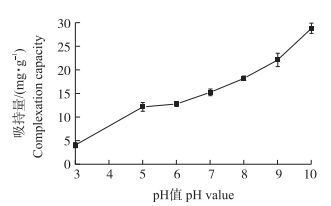
在植物多酚Y吸持氨氮的过程中, 废水pH值对吸持量影响较大。如图 4所示, 在pH值3~10范围内, Y对氨氮的吸持量与废水初始pH值呈正相关关系, 吸持量随着pH值的升高而增大。pH值从3上升到5时, 吸持量从4.04 mg·g-1迅速上升到12.1 mg·g-1, 涨幅达到200%。当pH值从5上升到7时, 吸持量上升到15.2 mg·g-1。可见, 在pH < 7时, pH值越低, pH值对吸持量的影响越大。在中性范围附近(pH6~8), 吸持量随pH值的升高而缓慢增大, H+浓度每增大1个数量级, 吸持量增加20%左右。在pH值为10时, 吸持量可达28.8 mg·g-1。该结果与我们以前的研究结果[7]相一致, 只是后者的pH影响不如前者大。
|
图 4 pH值对植物多酚Y吸持氨氮的影响 Figure 4 Effects of pH values on ammonia nitrogen adsorption by plant polyphenols Y |
pH对吸持量的影响与Y本身的性质有关, 也与氨氮在溶液中的存在形式有关[18]。在水溶液中, 氨氮的存在形式有两种:NH4+和NH3·H2O, 二者在溶液中以可逆形式存在:NH3·H2O
在本研究当中, 当溶液pH值为3时, 氨氮主要以NH4+形式存在于溶液中。在此pH条件下, 溶液中大量存在H+。NH4+的直径为0.286 nm, H+的直径为0.240 nm, H+离子半径小于NH4+离子半径, 因此H+比NH4+离子更易与吸持位点结合, 致使Y对氨氮的吸持量降低。当溶液pH值为10时, 溶液中的H+浓度很低, 与溶液中大量存在的OH-相比, H+浓度几乎可以忽略不计, 而Y是带有大量酚羟基的物质, 故高浓度的OH-能使它解离从而带上了更多的负电荷, 所以pH值升高Y的吸持量增大。
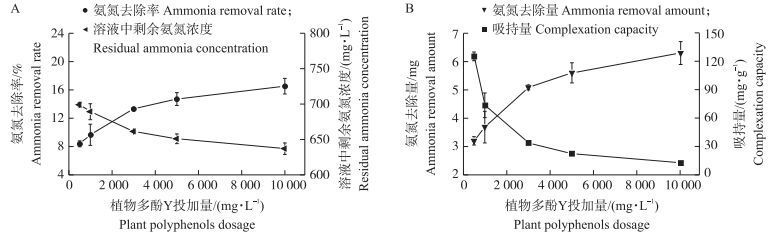
2.4 植物多酚Y投加量对吸持氨氮的影响从图 5-A可知:氨氮吸持量与去除率随植物多酚Y投加量的增加而增大。当Y投加量由500 mg·L-1增加到3 000 mg·L-1时, 氨氮的去除率从8.38%增加至13.3%, 投加量进一步增加至10 000 mg·L-1时, 氨氮去除率可达16.5%, 而且Y的投加量越大, 废水中剩余氨氮的浓度也越低。投加量的增加, 废水中氨氮去除量也越大(图 5-B)。随着投加量的增加, 氨氮的吸持总量升高, 但是因为投加量大幅增加单位质量Y的吸持量则呈下降趋势, 这与Yu等[17]、Widiastuti等[21]、刘海伟等[22]和郭俊元[16]的研究结果一致。
|
图 5 植物多酚Y投加量对去除氨氮(A)和吸持氨氮(B)的影响 Figure 5 Effects of plant polyphenols Y dosage on ammonia nitrogen removal (A)and ammonia nitrogen adsorption (B) |
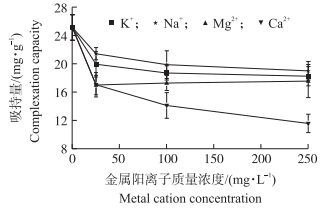
从图 6可知:K+、Na+、Mg2+、Ca2+4种金属阳离子质量浓度为25 mg·L-1时, Y对氨氮的吸持量分别从25.1 mg·g-1下降到了19.9、21.4、17.0和17.0 mg·g-1, 降幅达到20.8%、14.8%、32.4%和32.2%。当4种金属阳离子的质量浓度从100 mg·L-1大幅升高到250 mg·L-1时, 吸持量并没有随着阳离子质量浓度的大幅升高而大幅降低。除了Ca2+使吸持量降幅较大外(高达52%), K+、Na+、Mg2+质量浓度的升高没有使吸持量发生显著降低, 即这种影响在K+、Na+、Mg2+这3种阳离子质量浓度超过25 mg·L-1时会趋于稳定。Ca2+对吸持量的影响较其他三者大, Ca2+离子从25 mg·L-1升高到250 mg·L-1, 吸持量持续下降。因此, 在Y对氨氮进行静态吸持时, Ca2+的影响显著, 而且在同一质量浓度下4种阳离子间的差异也是显著的, 阳离子影响程度从大到小分别为Ca2+、Mg2+、K+、Na+。离子质量浓度为250 mg·L-1时Ca2+的影响分别是Mg2+、K+和Na+的1.4、1.7、和2.1倍。
|
图 6 金属阳离子对植物多酚Y氨氮吸持量的影响 Figure 6 Effects of metal cations on ammonium adsorption by plant polyphenols Y |
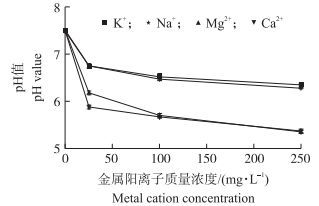
由图 7可知:吸持平衡后废水pH值均随K+、Na+、Ca2+、Mg2+离子浓度的增加而出现下降, 且下降的趋势与图 6的变化趋势一致。含K+、Na+模拟废水的pH值变化差异不显著, 含Ca2+、Mg2+模拟废水的pH值变化差异不显著, 但2种价态的阳离子间差异显著。二价阳离子(Ca2+、Mg2+)较一价阳离子(K+、Na+)使废水pH值下降幅度更大, 这说明这些离子与植物多酚Y的酚羟基上的H+发生了离子交换, 占据了羟基的吸附位点, 导致Y对氨氮吸附的下降。由于二价同电荷离子竞争吸附能力强于一价离子, 因此, Ca2+、Mg2+的影响明显强于K+、Na+。
|
图 7 吸持平衡后含不同阳离子的模拟废水pH值的变化 Figure 7 Changes in pH value of model wastewater with different metal cation after adsorption equilibrium |
有研究者也发现, 一些由植物材料制备得到的吸附材料富含纤维素、半纤维素和木质素, 其表面可能会有大量的极性基团, 如羧基、酚基、酮基、醚基、醇基和醛基等[15], 这些具有束缚污染物能力的极性基团可能与植物材料吸附废水中氨氮的机制有直接相关关系[23]。Y是天然的高分子物质, 属于植物材料, 其表面带有大量的酚羟基, 但K+、Na+、Ca2+和Mg2+等阳离子因不具d-轨道[24-26], 故它们只是与NH4+-N竞争吸持位点, 使吸持量有所下降, 而不会直接与Y上的官能团螯合, 使Y在吸持阶段就形成共聚体而被沉淀。在Y吸持猪场粪污废水中氨氮的试验中也印证了这一点, 猪场粪污废水含有大量K+、Na+、Ca2+、Mg2+等阳离子, 故Y对猪场粪污废水中的氨氮吸持量下降, 最佳吸持条件下的吸持量只有19.3 mg·g-1[7], 较在模拟废水中的最佳吸持量31.9 mg·g-1下降了31%。
2.6 植物多酚Y的红外表征对吸附氨氮前、后的植物多酚Y作傅里叶红外光谱表征(图 8), 吸附氨氮后植物多酚Y的大部分特征峰没有出现明显模糊或减弱, 只有微弱的位移, 1 583.0 cm-1处的吸收峰移动至1 580.2 cm-1, 788.4 cm-1处的吸收峰移动至789.0 cm-1等。吸附后3 667.8 cm-1处的峰消失, 3 183.8 cm-1处出现了缔合的-NH3的特征峰, 那是因为游离的-OH被-NH4+交换下来所致。红外频谱显示Y表面的烷基、羧基和羟基等功能基团均没有发生明显变化。

|
图 8 吸附氨氮前、后植物多酚Y的红外光谱图 Figure 8 FTIR spectra of the plant polyphenols Y before and after ammonium adsorption a.吸附前Before adsorption; b.吸附后After adsorption. |
值得指出的是, 与固体吸附剂对水溶液中污染元素的常规吸附不同, 本研究中的“吸附”实质是植物多酚Y与氨氮络合并在硫酸铁作用下沉淀的多作用力的结果。因此, 很难对对这种络合有氨氮的植物多酚Y进行再生而循环利用。如前所述, “植物多酚Y-氨氮-硫酸铁”三元沉淀物中氨氮含量最大可达44.4 mg·g-1, 实际工作中可考虑将其直接作为含氮的有机物用于农业生产。
3 结论植物多酚Y对氨氮的最大吸持量可达46.5 mg·g-1。其对氨氮的吸持量与pH值呈正相关、与温度呈负相关关系; 氨氮去除率随投加量的增加而增加; 共存阳离子K+、Na+、Mg2+、Ca2+的存在对Y吸持氨氮有一定抑制作用, 影响程度从大到小依次为Ca2+、Mg2+、K+、Na+。植物多酚Y对氨氮通过液-液相吸附的吸持继而采用沉淀剂沉淀是具有应用潜力的除氨氮新(物化)方法, 值得进一步深入研究。
| [1] | EPA. Aquatic Life Ambient Water Quality Criteria For Ammonia-Freshwater:EPA-822/R-13/001[S/OL].[2017-01-01]. https://www.epa.gov/sites/production/files/2015-08/documents/aquatic-life-ambient-water-quality-criteria-for-ammonia-freshwater-2013.pdf. |
| [2] | Yang J, Zhang X, Xie Y, et al. Ecogenomics of zooplankton community reveals ecological threshold of ammonia nitrogen[J]. Environmental Science and Technology, 2017, 51(5): 3057. DOI: 10.1021/acs.est.6b05606 |
| [3] | Halim A A, Aziz H A, Johari M A M, et al. Comparison study of ammonia and COD adsorption on zeolite, activated carbon and composite materials in landfill leachate treatment[J]. Desalination, 2010, 262(1): 31-35. |
| [4] |
刘琳, 吴树彪, 郭建斌, 等. 天然沸石对猪场厌氧发酵液中氨氮吸附作用的试验研究[J].
农业环境科学学报, 2011, 30(10): 2130-2135.
Liu L, Wu S B, Guo J B, et al. Adsorption of ammonia nitrogen in effluent from pig manure biogas plant by zeolite[J]. Journal of Agro-Environment Science, 2011, 30(10): 2130-2135. (in Chinese with English abstract) |
| [5] |
程治化. 改性沸石吸附去除氨氮及再生研究[D]. 北京: 北京化工大学, 2014: 1-39.
Cheng Z H. Ammonium removal from water by modified zeolite and the regeneration study[D]. Beijing:Beijing University of Chemical Technology, 2014:1-39(in Chinese with English abstract). http://cdmd.cnki.com.cn/Article/CDMD-10010-1015515946.htm |
| [6] |
马锋锋, 赵保卫, 刁静茹, 等. 牛粪生物炭对水中氨氮的吸附特性[J].
环境科学, 2015, 36(5): 1678-1685.
Ma F F, Zhao B W, Diao J R, et al. Ammonium adsorption characteristics in aqueous solution by dairy manure biochar[J]. Environmental Science, 2015, 36(5): 1678-1685. (in Chinese with English abstract) |
| [7] |
余雅琳, 高菲, 杨德坤, 等. 植物多酚吸持硫酸铁沉淀法去除猪场粪污废水中氨氮的研究[J].
农业环境科学学报, 2017, 36(11): 2343-2348.
Yu Y L, Gao F, Yang D K, et al. Removal of ammonium nitrogen from piggery wastewater by complexation with natural plant polyphenols[J]. Journal of Agro-Environment Science, 2017, 36(11): 2343-2348. DOI: 10.11654/jaes.2017-0644 (in Chinese with English abstract) |
| [8] | Rahman M M, Akter N, Karim M R, et al. Optimization, kinetic and thermodynamic studies for removal of Brilliant Red (X-3B) using Tannin gel[J]. Journal of Environmental Chemical Engineering, 2014, 2(1): 76-83. DOI: 10.1016/j.jece.2013.11.023 |
| [9] |
国家环境保护总局, 《水和废水监测分析方法》编委会.水和废水监测分析方法[M]. 4版.北京:中国环境科学出版社, 2002.
Editorial Board of Water and Wastewater Monitoring and Analysis Methods, Ministry of Environmental Protection of P.R.China.Water and Wastewater Monitoring and Analysis Methods[M]. 4th ed. Beijing:China Environmental Science Press, 2002. |
| [10] | Freundlich H. Über die adsorption in lösungen[J]. Zeitschrift für Physikalische Chemie, 1906, 62(5): 121-125. |
| [11] | Langmuir I. The constitution and fundamental properties of solids and liquids. Ⅱ. Liquids[J]. Journal of the American Chemical Society, 1917, 39: 1848-1906. DOI: 10.1021/ja02254a006 |
| [12] | Langmuir I. The adsorption of gases on plane surfaces of glass, mica and platinum[J]. Journal of the American Chemical Society, 1918, 40: 1361-1403. DOI: 10.1021/ja02242a004 |
| [13] | Ho Y S. Selection of optimum sorption isotherm[J]. Carbon, 2004, 42(10): 2115-2116. DOI: 10.1016/j.carbon.2004.03.019 |
| [14] | Alkan M, Dogan M, Turhan Y, et al. Adsorption kinetics and mechanism of maxilon blue 5G dye on sepiolite from aqueous solutions[J]. Chemical Engineering Journal, 2008, 139(2): 213-223. DOI: 10.1016/j.cej.2007.07.080 |
| [15] |
赵飞, 惠晓梅, 郭栋生. 阳离子交换树脂吸附焦化废水中氨氮影响因素研究[J].
水处理技术, 2011, 37(11): 34-37.
Zhao F, Hui X M, Guo D S. Study on influencing factors of ammonia nitrogen adsorption in coking wastewater by cation exchange resin[J]. Technology of Water Treatment, 2011, 37(11): 34-37. (in Chinese with English abstract) |
| [16] |
郭俊元. 微生物絮凝与改性沸石吸附联合处理猪场废水的研究[D]. 长沙: 湖南大学, 2013: 23-69.
Guo J Y. Treatment of swine wastewater using bioflocculation and adsorption with chemically modified zeolite[D]. Changsha:Hunan University, 2013:23-69(in Chinese with English abstract). http://cdmd.cnki.com.cn/Article/CDMD-10532-1013347888.htm |
| [17] | Yu Y, Zhuang Y Y, Wang Z H. Adsorption of water-soluble dye onto functionalized resin[J]. Journal of Colloid Interface Science, 2001, 242: 288-293. DOI: 10.1006/jcis.2001.7780 |
| [18] |
张华. 柚皮基活性炭制备及吸附应用机理研究[D]. 南宁: 广西大学, 2013: 12-49.
Zhang H. Preparation of activated carbon with grapefruit peel and study on adsorption mechanism of application[D]. Nanning:Guangxi University, 2013:12-49(in Chinese with English abstract). http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=D523516 |
| [19] |
张继义, 韩雪, 武英香, 等. 炭化小麦秸秆对水中氨氮吸附性能的研究[J].
安全与环境学报, 2012, 12(1): 32-36.
Zhang J Y, Han X, Wu Y X, et al. Adsorption properties of carbonized wheat straw to remove ammonia nitrogen in water[J]. Journal of Safety and Environment, 2012, 12(1): 32-36. (in Chinese with English abstract) |
| [20] |
阳维薇, 王中琪. 改性玉米秸秆吸附处理含氨氮养猪废水[J].
广东化工, 2011, 38(5): 159-160.
Yang W W, Wang Z Q. Treatment of swine wastewater containing NH3-N with modified corn stalk[J]. Guangdong Chemical Industry, 2011, 38(5): 159-160. (in Chinese with English abstract) |
| [21] | Widiastuti N, Wu H W, Ang H M, et al. Removal of ammonium from greywater using natural zeolite[J]. Desalination, 2011, 277(1/2/3): 15-23. |
| [22] |
刘海伟, 刘云, 王海云, 等. pH和共存阳离子对草莓茎吸附水体氨氮的影响[J].
环境科学, 2010, 31(8): 1884-1889.
Liu H W, Liu Y, Wang H Y, et al. Effects of pH and coexisting cations on ammonia adsorption from aqueous solution by strawberry stem powde[J]. Environmental Science, 2010, 31(8): 1884-1889. (in Chinese with English abstract) |
| [23] | Pagnanelli F, Mainelli S, Veglio F, et al. Heavy metal removal by olive pomace:biosorbent characterisation and equilibrium modelling[J]. Chemical Engineering Science, 2003, 58(20): 4709-4717. DOI: 10.1016/j.ces.2003.08.001 |
| [24] | Nakajima A, Sakaguchi T. Recovery of uranium by tannin immobilized on agarose[J]. Journal of Chemical Technology and Biotechnology Biotechnology, 1987, 40(4): 223-232. |
| [25] | Anirudhan T S, Suchithra P S. Synthesis and characterization of tannin-immobilized hydrotalcite as a potential adsorbent of heavy metal ions in effluent treatments[J]. Applied Clay Science, 2008, 42(1): 214-223. |
| [26] | Chibata I, Tosa T, Mori T, et al. Immobilized tannin-a novel adsorbent for protein and metal ion[J]. Enzyme and Microbial Technology, 1986, 8(3): 130-136. DOI: 10.1016/0141-0229(86)90099-2 |




