文章信息
- 战莘晔, 殷红, 史洪杰, 王一, 吕晓, 黄珊, 金丽颖
- ZHAN Shenye, YIN Hong, SHI Hongjie, WANG Yi, LÜ Xiao, HUANG Shan, JIN Liying
- UV-B辐射增强对粳稻剑叶光系统Ⅱ的影响
- Effect of UV-B radiation on photosynthetic system Ⅱ of japonica rice flag leaf
- 南京农业大学学报, 2017, 40(5): 941-948
- Journal of Nanjing Agricultural University, 2017, 40(5): 941-948.
- http://dx.doi.org/10.7685/jnau.201607027
-
文章历史
- 收稿日期: 2016-07-24
2. 鞍山市气象局, 辽宁 鞍山 114004;
3. 阜新蒙古族自治县气象局, 辽宁 阜新 123100;
4. 辽宁省气象装备保障中心, 辽宁 沈阳 110001;
5. 锦州市生态与农业气象中心, 辽宁 锦州 121000;
6. 咸宁市气象局, 湖北 咸宁 437000
2. Anshan Meteorological Administration, Anshan 114004, China;
3. Fuxin Mongolian Autonomous County Meteorological Administration, Fuxin 123100, China;
4. Liaoning Meteorological Equipment Support Center, Shenyang 110001, China;
5. Jinzhou Ecological and Agricultural Meteorological Center, Jinzhou 121000, China;
6. Xianning Meteorological Administration, Xianning 437000, China
大气化学成分的全球性变化伴随着臭氧保护层的大幅度减少, 导致到达地表的UV-B辐射显著上升[1-2]。制冷设备频繁的使用氟氯烃以及随后释放到大气中的气体已成为平流层臭氧消耗的主要原因[3]。臭氧能够大量吸收太阳辐射当中的紫外部分, 臭氧对其的吸收随波长的减小而增多, 臭氧对于长波紫外辐射(UV-A, 320~400 nm)的吸收很少, 而对于波长小于280 nm的短波紫外辐射(UV-C)则可被极少量的臭氧完全吸收。因此, 平流层当中的臭氧层减薄则会主要导致中波紫外辐射(UV-B, 280~320 nm)的增多, UV-B辐射的增加不仅对人类活动、动物、微生物等都有着重要的影响, 对生态系统、植物等的影响也都不可忽视。
UV-B辐射对PSⅡ影响很大[4]。UV-B辐射对PSⅠ和PSⅡ的效应不同, 且能使2个光系统间的能量重新分配[5]。UV-B辐射导致不同藻类的DNA和PSⅡ损伤, 高速的PSⅡ修复率可能是植物对自然界中UV-B辐射适应的一种方式[6]。师生波等[7]研究认为, 受体侧是UV-B辐射对PSⅡ造成影响的主要场所, 当UV-B辐射强度与时间都增加时, PSⅡ光化学效率会减慢。吴杏春等[8]在对水稻PSⅡ反应中心活性的研究中发现, UV-B辐射加强会抑制PSⅡ反应中心活性, 影响电子由PSⅡ反应中心供体侧向电子受体的传递, 受损严重的过程主要集中在电子由Pheo传递给QA时, 也就是QA发生还原反应时受损严重。PSⅡ反应中心开放程度在一般情况下能够用光化学淬灭来反映, 因此, 当PSⅡ反应中心开放程度很大时, 光化学猝灭也会很大[9]。如果PSⅡ反应中心的聚光色素吸收过量光能, 造成自身延迟将其传递给作用中心色素时, 将会损害光合机制, 这时以热耗散的形式来消耗这部分多余光能也就是非光化学淬灭, 一定程度上降低了对光合机构的破坏[10]。周心渝等[11]研究认为半夏在遭受UV-B增强胁迫时会以提高其自身热耗散能力来抵御其对自身的破坏。
近年来, UV-B辐射对生态环境的影响已逐步受到重视。但针对UV-B辐射对北方粳稻的研究则相对较少, 且剑叶作为水稻中最重要的叶片具有非常高的研究价值。本研究以东北地区粳型超级稻品种‘沈农265’为对象, 探究UV-B辐射对粳稻剑叶光系统Ⅱ的影响, 为在全球气候变化条件下进一步提高北方粳稻区水稻生产力提供依据。
1 材料与方法 1.1 试验设计试验于2014年5—10月在沈阳农业大学水稻研究所试验场地(123°33′ E, 41°49′ N)进行。选取北方粳稻品种‘沈农265’为试验材料, 采用盆栽方式种植并选用大田水稻土作为生长土壤。沈阳地区夏季自然光照实际日平均UV-B辐射(数据来源于沈阳市气象局)约为21 W·m-2, 试验分为对照组CK(采用自然光照)和处理组T1、T2(即在自然光照条件下增设紫外灯管), 处理组辐射强度分别比对照增加1.05和2.10 W·m-2(相当于沈阳地区夏季日平均UV-B辐射增加5%和10%)。
4月中旬育苗, 选取粳稻3叶期长势较为一致的幼苗移栽于无孔实验桶中, 实验桶下口径20 cm, 上口径32.5 cm, 深度29 cm, 每桶3穴, 每穴1株, 对照组CK和处理组T1、T2各种植42桶, 孕穗期、抽穗开花期、灌浆期、成熟期每个处理设6次重复, 共计30桶, 余下12桶用于测产。进行常规水肥管理。UV-B处理采用紫外灯管(40 W, 北京电光源研究所生产), 使用可调灯架安装在植株上方, 处理期间随株高的变化调整距粳稻顶端约30~40 cm的高度, 以保证植株受到相同剂量的UV-B辐射。每支灯管上都配有灯罩, 为了防雨和便于供电, 每组灯管都配套灯罩且在放置时呈东西方向排列, 目的是减少遮阴对试验的影响。每天08:00—16:00进行辐射处理(阴雨天除外), 直至成熟收获。试验期间在孕穗期、抽穗开花期、灌浆期、成熟期对剑叶进行活体测量和取样。其中剑叶光合速率以及叶绿素荧光参数6次重复, 光合响应曲线3次重复。
1.2 测定项目及方法 1.2.1 叶绿素a快速荧光诱导动力学曲线及其各参数的测定利用植物多功能效率仪(M-PEA, Hansatech, UK)在粳稻剑叶生长各时期进行测定。在CK、T1和T2中各选出6株长势较为一致的植株挂牌标记, 并在晴朗无云的上午(09:30—11:00) 进行植株活体测定, 暗适应期间用暗适应夹夹住待测剑叶, 至少暗适应30 min后才能进行粳稻剑叶荧光诱导动力学曲线及其参数的测定。利用FMS-2型便携式荧光测定系统(Hansatech, UK)对粳稻剑叶的叶绿素荧光动力学参数进行测定, 每处理重复6次。测定前叶片在自然光照下(约为21 W·m-2)测定ΦPSⅡ等光反应参数, 测定完成后, 叶片应暗适应20~30 min, 测定其暗反应参数, 测定时设定光照强度为1 000 μmol·m-2·s-1。
1.2.2 快速叶绿素荧光动力学参数的计算叶绿素荧光参数参考李鹏民[12]的方法, 各指标具体计算方法见表 1。
| 指标Item | 计算公式及符号含义Calculation formula and symbolic meaning |
| ABS/CSm | ABS/CSm≈FM, 单位面积吸收的光能(在t=tFM时) Absorption per excited cross-section |
| Dlo/CSm | Dlo/CSm=(ABS/CSm)-(TRo/CSm), 单位面积的热耗散(在t=tFM时) Dissipation per excited cross-section |
| TRo/CSm | TRo/CSm=φPo*(ABS/CSm), 单位面积捕获的光能(在t=tFM时) Trapping per excited cross-section |
| ETo/CSm | ETo/CSm=φEo*(ABS/CSm), 单位面积电子传递的量子产额(在t=tFM时) Electron transport per excited cross-section |
| RC/CSm | RC/CSm=φPo*(VJ/Mo)*(ABS/CSm), 单位面积有活性反应中心的数量Density of PS Ⅱ reaction centers per excited cross-section |
| ABS/RC | ABS/RC=Mo*(1/VJ)*(1/φPo), 单位反应中心吸收的光能Absorption per active reaction centers |
| DIo/RC | DIo/RC=(ABS/RC)-(TRo/RC), 单位反应中心耗散掉的能量Dissipation per active reaction centers |
| TRo/RC | TRo/RC=Mo*(1/VJ), 单位反应中心捕获的用于还原QA的能量Trapping per active reaction centers |
| ETo/RC | ETo/RC=Mo*(1/VJ)*φo, 单位反应中心捕获的用于电子传递的能量Electron transport per active reaction centers |
| Sm | Sm=(Area)/(FM-Fo), 标准化后的荧光诱导曲线、荧光强度F=FM及y轴之间的面积 |
| N | N=Sm*Mo*(1/VJ), 从开始照光到到达FM的时间段内QA被还原的次数 |
| φPo | φPo=1-(Fo/Fm), 表示最大光化学效率(t=0) |
| φo | φo=(1-VJ)=ETo/Tro, 反应中心捕获的激子中用来推动电子传递到电子传递链中超过QA的其他电子受体的激子占用来推动QA还原激子的比率(在t=0时) |
| φEo | φEo=[1-(Fo/Fm)]·φo=ETo/ABS, 表示反应中心吸收的光能用于电子传递的量子产额 |
| Mo | Mo=4(F300 μs-Fo)/(Fm-Fo), 荧光诱导曲线的初始斜率 |
| Fv/Fm | 原初光能转换效率Primary conversion of light energy |
| qP | qP=(F′m-Fs)/(F′m-F′o), 光化学猝灭系数Photochemical quenching |
| NPQ | NPQ=Fm/F′m-1, 非光化学猝灭系数Non-photochemical quenching |
| rETR | rETR=ΦPSⅡ*PAR*0.84*0.5, 光合电子传递的相对速率Relative electronic transport rate |
| PIabs | PIabs=RC/ABS*[φPo*(1-φPo)]*[φo*(1-φo)], 以吸收光能为基础的性能指数Performance index on absorption basis |
数据的处理与制图采用Excel 2003进行; 用SPSS 17.0对数据进行方差分析, 采用LSD法对数据进行多重比较。
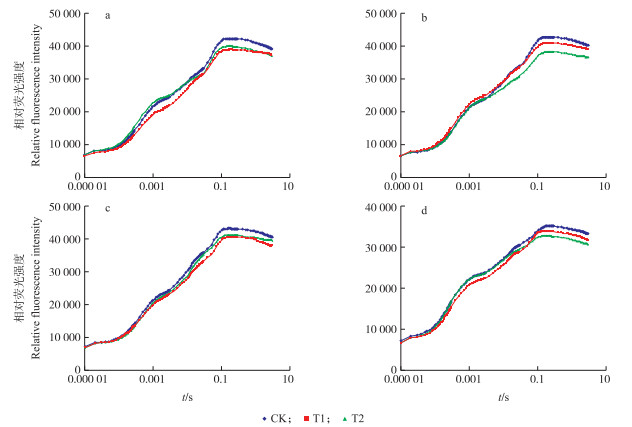
2 结果与分析 2.1 UV-B辐射增强对粳稻剑叶PSⅡ反应中心供体侧和受体侧的影响由图 1可以看出:穗开花期和灌浆期, 对照和处理在O-J段荧光值差异不大, 而孕穗和成熟期则表现出一些差异(几个基本的特征位点:O相为10~50 μs时的荧光, J相为2 ms时的荧光, I相为30 ms时的荧光, P相为0.3~2 s时的荧光)。说明UV-B增强影响了Pheo将电子传给QA, QA-传递给QB的过程; J-I阶段, 各个时期荧光值都表现出差异, 均为T2更低, 说明T2使快还原型PQ库被还原的数量减少; 在I-P阶段, 各时期荧光值基本呈现出CK大于T1、T2的趋势, 说明UV-B减缓了慢还原型的PQ库发生还原的过程, 且各个时期的P点的荧光值从大到小的处理为CK、T1、T2。说明UV-B辐射会降低剑叶最终的荧光产量, 且成熟期与其他各个时期相比荧光强度显著下降。原因可能是随着辐射时间的累积, 对PSⅡ供体侧伤害加重, 活性下降。
|
图 1 不同处理孕穗期(a)、抽穗开花期(b)、灌浆期(c)和成熟期(d)粳稻剑叶快速荧光诱导动力学曲线的变化 Figure 1 The changes of chlorophyll fluorescence transient of flag leaf in booting(a), heading and flowering(b), filling(c)and maturity(d)stages of japonica rice under different treatment CK为对照, 自然光照; T1和T2为处理, 在自然光照条件下增设紫外灯管, 辐射强度分别比对照增加1.05和2.10 W·m-2。 CK:Natural light.The treatments were set as T1, T2 in which the UV-B radiation was increased by 1.05 and 2.10 W·m-2respectively. The same as follows. |
为方便比较不同处理与对照的各项参数值, 以CK的荧光参数为1, 用两处理的荧光参数与CK的比值绘制雷达图。如图 2所示, 随着UV-B辐射强度的增加, 与CK相比, Sm、N、φPo、φo、φEo在各个时期均呈降低趋势, 其中Sm在抽穗开花期和成熟期T1、T2处理分别显著下降了12.71%、16.25%和26.98%、24.96%;N在其他时期降低不明显, 但在成熟期T1、T2显著降低, 分别为29.73%和18.11%;φPo在各个时期降低均不显著; φo在成熟期T1处理下降低了7.47%, 在T2处理下显著降低了20.34%;φEo在孕穗期两处理分别降低了4.37%和17.84%, 在成熟期T1处理下只降低了0.93%, T2处理下降低了18.61%, T2处理效果显著高于T1;Mo则与以上参数变化趋势相反, 在各个时期均呈增加趋势, 且Mo在成熟期T1、T2处理下显著上升, 分别增加了19.61%和5.89%。

|
图 2 不同处理孕穗期(a)、抽穗开花期(b)、灌浆期(c)和成熟期(d)粳稻剑叶受体侧参数的变化 Figure 2 The changes of acceptor side parameters of flag leaf in booting(a), heading and flowering(b), filling(c)and maturity(d)stages of japonica rice under different treatment |
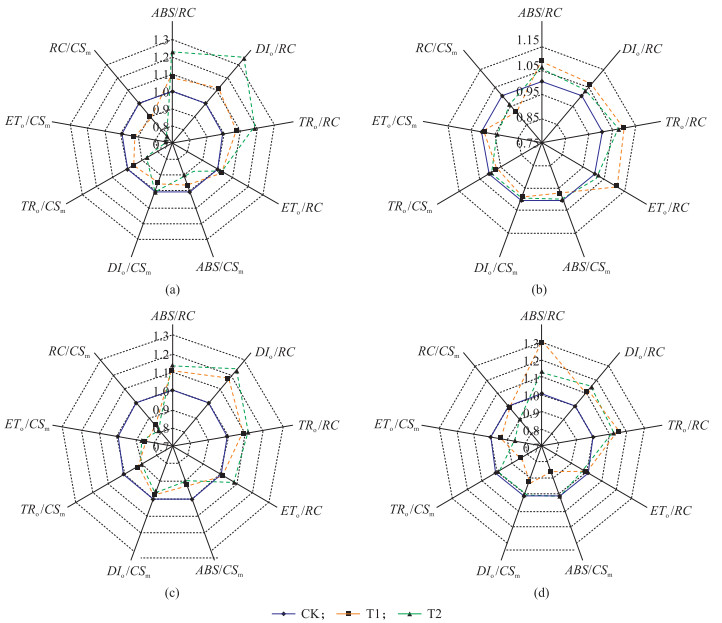
随着UV-B辐射强度的增加, 与CK相比, ABS/RC、DIo/RC、TRo/RC、ETo/RC在各个时期均呈增加趋势, ABS/CSm、DIo/CSm、TRo/CSm、ETo/CSm、RC/CSm在各个时期基本呈现出降低趋势。其中ABS/RC在孕穗期T1、T2处理下分别增加了7.71%和22.82%, 在成熟期分别增加了29.21%、12.54%。DIo/RC在孕穗期T2处理下显著增加了34.2%;在灌浆期T1、T2处理下的DIo/RC也显著升高, 增幅分别为17.41%和22.74%;TRo/RC在成熟期T1、T2处理下增幅分别为15.05%、12.09%;ETo/RC在所有处理中均升高, 但变化不明显。ABS/CSm在孕穗期和灌浆期T1、T2处理下分别降低了4.11%、10.23%和7.52%、9.95%;DIo/CSm在4个时期的降幅不大, T1处理大于T2处理; ETo/CSm在孕穗期分别降低了8.11%、26.12%, 在灌浆期分别下降了15.12%、13.4%;RC/CSm在孕穗期分别降低了10.01%、24.46%, 在灌浆期显著下降了15.86%、18.82%。T2处理对孕穗期和灌浆期剑叶比活性参数的影响大于T1处理。
|
图 3 不同处理孕穗期(a)、抽穗开花期(b)、灌浆期(c)和成熟期(d)粳稻剑叶比活性参数的变化 Figure 3 The changes of parameters of specific activity of flag leaf in booting(a), heading and flowering(b), filling(c)and maturity(d)stages of japonica rice under different treatment |
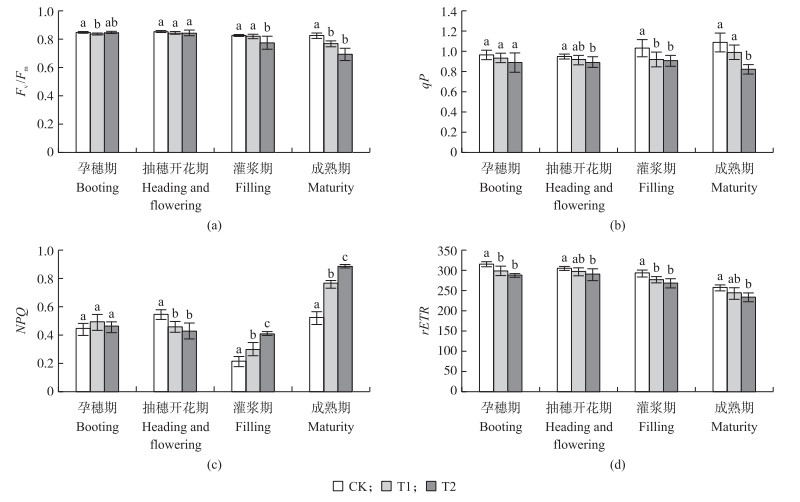
随UV-B辐射的增强, 剑叶的Fv/Fm在粳稻4个生育期均呈减小趋势; 灌浆期T2处理降幅较大, 降低了5.56%, 成熟期T1、T2分别极显著降低了6.7%和15.72%(图 4-a)。粳稻4个生育期剑叶的qP随UV-B辐射的增强均减小, 且T2的降低程度大于T1;在灌浆期和成熟期两处理下的qP降幅较大, 分别显著降低了11.07%, 12.32%和9.26%、24.58%(图 4-b)。随UV-B辐射的增强, 孕穗期、抽穗开花期和灌浆期剑叶的NPQ均升高, 灌浆期和成熟期T1极显著增加了39.09%和92.92%, T2极显著增加了45.72%和69.83%(图 4-c)。随着UV-B辐射的增强, 4个生育期剑叶的rETR均降低(图 4-d)。说明UV-B辐射增强对粳稻灌浆期和成熟期剑叶荧光动力学基本参数影响较大。
|
图 4 UV-B辐射增强对粳稻剑叶荧光动力学基本参数的影响 Figure 4 Effects of enhanced UV-B radiation on basic parameters of fluorescence in flag leaf of japonica rice 不同小写字母表示处理间在0.05水平差异显著。 The different small letters mean significant difference at 0.05 level among treatments. The same as follows. |
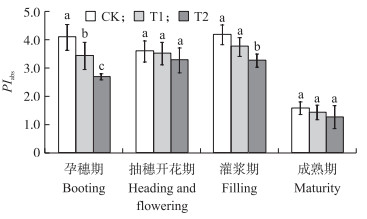
PIabs反映的是以吸收光能为基础的性能指数。4个生育期, 两处理剑叶的PIabs均呈现降低趋势, 在孕穗期和灌浆期, T1、T2处理的性能指数分别下降16.04%、34.45%和10.01%、21.89%;且T2性能指数显著下降(图 5)。说明UV-B辐射增强对水稻性能指数的抑制程度较大, 尤其在孕穗期和灌浆期。T2对PIabs的抑制程度大于T1。
|
图 5 UV-B辐射增强对粳稻剑叶性能指数的影响 Figure 5 Effects of enhanced UV-B radiation on PIabs in flag leaf of japonica rice |
本研究中, UV-B处理下, PSⅡ受体侧各参数在不同时期表现不同, Sm、N、φPo、φEo和φo、在剑叶生长各个时期都呈降低趋势, 意味着UV-B减小了PQ库的容量, QA被还原的次数也随之降低, 最大光化学效率也减小, QA下游电子传递的量子减少, 反应中心开放水平呈降低趋势; UV-B辐射在各生长期不同程度上抑制了单位面积上吸收的光能、耗散的能量、捕获的用于还原QA以及电子传递的能量。唐莉娜等[13]研究结果证明, UV-B辐射降低了叶绿体中电子受体PQ库的开放程度, 并阻碍电子传递损伤PSⅡ反应中心活性, 影响最大的过程是在PSⅡ原初电子受体QA的光还原过程, 即抑制了PSⅡ反应中心的原初光能转化效率同时还抑制了其潜在活性, 最终降低了水稻的光合作用。这与本文结论一致。对植物进行UV-B处理, 既伤害作物叶片等光合器官, 又增强其自身不断进行修复调整的过程, 一旦超出了自身负荷, UV-B辐射所带来的负效应就会积累, 最终加速叶片衰老和死亡[6], 本研究中PSⅡ供体侧活性整体下降也说明了是由于UV-B辐射的长时间积累伤害导致的。周党卫等[14]从光电子传递内在机制上阐述了至少有两个机制能促发光抑制, 一个发生在受体侧, 另一个发生在供体侧, 受体侧部分当遇强光照射时, PSⅡ反应中心会受到激发而产生电子, 并由Pheo传递给QA, 造成QA的还原, 这会减慢电子传递过程中经过QA的速率, 电子在QA-的大量累积会导致电荷重新排列组合, 易生成三线态叶绿素(3P680), 当它与周围氧气接触时易形成单线态氧, 它能够降解色素和蛋白质; 供体侧部分在遇到强光照射时, 产生的电子不易传出, 电子的累积造成了供体侧的强氧化势, 对于PSⅡ中的电子传递也起到抑制作用。
大豆PSⅡ反应中心光能转化效率受UV-B辐射胁迫而降低, PSⅡ反应中心受到了光化学损伤[15]。乔媛等[16]和胡志峰等[17]等也都得到类似的结论。在本研究中, 各生长时期的Fv/Fm随UV-B强度的增大而减小, 这与以上研究结论一致。UV-B辐射胁迫下的大豆qP和NPQ都显著低于对照[18]。本试验中, qP随UV-B强度的增大而减小, qP的降低反映了UV-B辐射减少了PSⅡ中的QA-重新氧化形成QA的数量, PSⅡ的电子传递活性受到影响。而张美萍等[19]在研究中认为NPQ随辐射强度的变化说明色素吸收的光能大部分用来热耗散, 而非光合电子传递, 通过耗散过剩的光能来抵御UV-B过强的辐射, 这也在一定程度上保护了PSⅡ反应中心, 这与本文结论一致, 粳稻在生长后期NPQ的提高是一种自我保护机制, 随UV-B辐射的增强而增大。
随着UV-B处理的增强, 剑叶最终的荧光产量会降低, PQ库的容量变小, QA被还原的频率减慢, 次数降低, 最大光化学效率降低, 反应中心开放水平降低, PSⅡ反应中心吸收的光能用于其他方面的用途增多, 用于电子传递方面的量子份额减少, 但荧光动力学曲线当中的O-J段的初始斜率受UV-B辐射诱导而增大。UV-B辐射的增强降低了粳稻剑叶各生长期单位面积上吸收的光能、热耗散、捕获的光能、电子传递的量子产额以及活性反应中心的数量, 促进了单位反应中心的各项比活性参数, 但UV-B辐射的增强也导致剑叶在各个生长期原初光能转换效率、光化学猝灭系数、光合电子传递相对速率及性能指数(以吸收光能为基础)的降低。
| [1] | Ballaré C L, Caldwell M M, Flint S D, et al. Effects of solar ultraviolet radiation on terrestrial ecosystems. Patterns, mechanisms and interactions with climate change[J]. Photochemical and Photobiological Sciences, 2011, 10(2): 226–241. DOI: 10.1039/c0pp90035d |
| [2] | Bais A F, McKenzie R L, Bernbard G, et al. Ozone depletion and climate change:impacts on UV radiation[J]. Photochemical and Photobiological Sciences, 2011, 10(2): 182–198. DOI: 10.1039/c0pp90034f |
| [3] | Vijay P S, Jitendra K, Samiksha S, et al. Dimethoate modifies enhanced UV-B effects on growth, photosynthesis and oxidative stress in mung bean(Vigna radiata L.)seedlings:implication of salicylic acid[J]. Pesticide Biochemistry and Physiology, 2014, 116: 13–23. DOI: 10.1016/j.pestbp.2014.09.007 |
| [4] | Nedunchezhian N, Kulandaivelu G. Effects of ultraviolet-B enhanced radiation and temperature on growth and photochemical activities in Vigna unguiculata[J]. Biologia Plantarum, 1996, 38(2): 205–214. DOI: 10.1007/BF02873847 |
| [5] |
刘晓, 贺俊芳, 姬倩茹, 等. 增强UV-B辐射对植物光能传递过程的影响[J].
光子学报, 2010, 39(9): 1582–1587.
Liu X, He J F, Ji Q R, et al. Effects of ultraviolet-B radiation on plant light energy transfer process[J]. Acta Photonica Sinica, 2010, 39(9): 1582–1587. (in Chinese with English abstract) |
| [6] |
陈慧泽, 韩榕. 植物响应UV-B辐射的研究进展[J].
植物学报, 2015, 50(6): 790–801.
Chen H Z, Han R. Plants respond to UV-B radiation:a review[J]. Chinese Bulletin of Botany, 2015, 50(6): 790–801. DOI: 10.11983/CBB14176 (in Chinese with English abstract) |
| [7] |
师生波, 尚艳霞, 朱鹏锦, 等. 增补UV-B辐射对高山植物美丽风毛菊叶片PS Ⅱ光化学效率的影响[J].
草地学报, 2011, 19(4): 539–545.
Shi S B, Shang Y X, Zhu P J, et al. Effect of enhanced UV-B radiation on PS Ⅱ photochemistry efficiency in alpine plants Saussurea superba[J]. Acta Agrestia Sinica, 2011, 19(4): 539–545. DOI: 10.11733/j.issn.1007-0435.2011.04.001 (in Chinese with English abstract) |
| [8] |
吴杏春, 林文雄, 黄忠良. UV-B辐射增强对两种不同抗性水稻叶片光合生理及超显微结构的影响[J].
生态学报, 2007, 27(2): 554–564.
Wu X C, Lin W X, Huang Z L. Influence of enhanced ultraviolet-B radiation on photosynthetic physiologies and ultrastructure of leaves in two different resistivity rice cultivars[J]. Acta Ecologica Sinica, 2007, 27(2): 554–564. (in Chinese with English abstract) |
| [9] | Belshe E F, Durako M J, Blum J E. Photosynthetic rapid light curves(RLC)of Thalassia testudinum exhibit diurnal variation[J]. Journal of Experimental Marine Biology and Ecology, 2007, 342(2): 253–268. DOI: 10.1016/j.jembe.2006.10.056 |
| [10] |
张守仁. 叶绿素荧光动力学参数的意义及讨论[J].
植物学通报, 1999, 16(4): 444–448.
Zhang S R. A discussion on chlorophyll fluorescence kinetics parameters and their significance[J]. Chinese Bulletin of Botany, 1999, 16(4): 444–448. (in Chinese with English abstract) |
| [11] |
周心渝, 曹瑞霞, 张红敏, 等. 半夏光合生理特性及总生物碱对增强UV-B的响应[J].
西南大学学报(自然科学版), 2013, 35(6): 166–172.
Zhou X Y, Cao R X, Zhang H M, et al. The response of photosynthetic physiological characters and total alkaloids of pinellia ternate to enhanced UV-B radiation[J]. Journal of Southwest University(Natural Science Edition), 2013, 35(6): 166–172. (in Chinese with English abstract) |
| [12] |
李鹏民. 快速叶绿素荧光诱导动力学在植物逆境生理研究中的应用[D]. 泰安: 山东农业大学, 2006.
Li P M. Application of chlorophyll a fluorescence transient in study of plant physiology under stress conditions[D]. Tai'an:Shandong Agricultural University, 2006(in Chinese with English abstract). http://cdmd.cnki.com.cn/Article/CDMD-10434-2007135638.htm |
| [13] |
唐莉娜, 林文雄, 吴杏春, 等. UV-B辐射增强对水稻生长发育及其产量形成的影响[J].
应用生态学报, 2002, 13(10): 1278–1282.
Tang L N, Lin W X, Wu X C, et al. Effects of enhanced ultraviolet-B radiation on growth development and yield formation in rice(Oryza sativa L.)[J]. Chinese Journal of Applied Ecology, 2002, 13(10): 1278–1282. DOI: 10.3321/j.issn:1001-9332.2002.10.017 (in Chinese with English abstract) |
| [14] |
周党卫, 韩发, 滕中华, 等. UV-B辐射增强对植物光合作用的影响及植物的相关适应性研究[J].
西北植物学报, 2002, 22(4): 1004–1010.
Zhou D W, Han F, Teng Z H, et al. Advance of plant response and adaptation under enhanced UV-B radiation and the effect of enhanced UV-B on plant photosynthesis[J]. Acta Bot Boreal-Occident Sin, 2002, 22(4): 1004–1010. (in Chinese with English abstract) |
| [15] |
李涵茂, 胡正华, 杨燕萍, 等. UV-B辐射增强对大豆叶绿素荧光特性的影响[J].
环境科学, 2009, 30(12): 3669–3675.
Li H M, Hu Z H, Yang Y P, et al. Influence of enhanced UV-B radiation on chlorophyll fluorescence characteristics of soybean[J]. Environmental Science, 2009, 30(12): 3669–3675. DOI: 10.3321/j.issn:0250-3301.2009.12.037 (in Chinese with English abstract) |
| [16] |
乔媛, 殷红, 李虎, 等. 增强UV-B辐射对水稻叶绿素荧光特性的影响[J].
华北农学报, 2014, 29(2): 146–151.
Qiao Y, Yin H, Li H, et al. Influence of enhanced UV-B radiation on chlorophyll fluorescence characteristics of rice[J]. Acta Agriculturae Bureali-Simica, 2014, 29(2): 146–151. DOI: 10.7668/hbnxb.2014.02.027 (in Chinese with English abstract) |
| [17] |
胡志峰, 郁继华, 马彦霞, 等. UV-B辐射增强对两种不同类型番茄幼苗生长和叶绿素荧光猝灭的影响[J].
甘肃农业大学学报, 2009, 44(6): 33–38.
Hu Z F, Yu J H, Ma Y X, et al. Effects of inhanced UV-B on growth and chlorophyll fluorescence quenching in two types of tomato seedling[J]. Journal of Gansu Agricultural University, 2009, 44(6): 33–38. (in Chinese with English abstract) |
| [18] |
徐志防, 罗广华, 王爱国, 等. 强光及活性氧对大豆光合作用的影响[J].
植物学报, 1999, 41(8): 862–866.
Xu Z F, Luo G H, Wang A G, et al. Effects of strong light and active oxygen on photosynthesis in soybean[J]. Acta Botanica Sinica, 1999, 41(8): 862–866. (in Chinese with English abstract) |
| [19] |
张美萍, 王勇, 韩榕, 等. 增强UV-B辐射对水稻叶绿素荧光参数的影响[J].
山西师范大学学报(自然科学版), 2014, 28(1): 67–70.
Zhang M P, Wang Y, Han R, et al. The influence of photosynthetic on rice flag under enhanced UV-B radiation[J]. Journal of Shanxi Normal University(Natural Science Edition), 2014, 28(1): 67–70. (in Chinese with English abstract) |




