文章信息
- 卿彦, 王礼军, 吴义强, 罗莎, 吴清林, 颜宁.
- Qing Yan, Wang Lijun, Wu Yiqiang, Luo Sha, Wu Qinglin, Yan Ning.
- 纤维素纳米晶体胆甾相液晶形成与应用
- Cholesteric Liquid Crystal from Cellulose Nanocrystal: Formation and Application
- 林业科学, 2019, 55(4): 152-159.
- Scientia Silvae Sinicae, 2019, 55(4): 152-159.
- DOI: 10.11707/j.1001-7488.20190416
-
文章历史
- 收稿日期:2017-03-30
- 修回日期:2017-08-14
-
作者相关文章
纤维素纳米晶体(cellulose nanocrystal,CNC)由天然存在的纤维素(来源于木材、竹材、背囊动物和细菌等)经强酸水解获得,不仅拥有精细的纳米结构、丰富的表面活性基团和优异的力学性能,而且在特定浓度下还可自组装形成胆甾相液晶(杨洁等,2012;Moon et al., 2011;Sena et al., 2011)。胆甾相液晶又名手性向列型液晶,其手性向列结构表现出特有的光学性能,如选择性反射、圆二色性和旋光性等,在防伪识别、光信息储存、智能窗口和液晶显示等先进材料领域具有广阔的应用前景(Yang et al., 2012;Shopsowitz et al., 2010)。
Marchessault等(1959)发现并揭示了纤维素纳米晶体的手性排列现象。纤维素纳米晶体在低浓度溶液中随机分散,当溶液浓度上升到一定程度时,随机分散的纳米晶体自发组织成有序排列,形成典型的手性向列结构(Revol et al., 1992)。随着研究工作逐渐深入,学者们还发现超声波、温度、磁场和电解质等对CNC胆甾相液晶的形成和性能具有显著影响,通过调节这些因素,可以制备出特定结构的胆甾相液晶。纤维素纳米晶体胆甾相液晶既可直接合成具有特殊光学性质的薄膜材料,也可作为一种特殊的液晶模板复制其特有结构合成其他先进功能材料。如Shopsowitz等(2010)将SiO2溶胶加入具有手性向列结构的CNC溶液中,缓慢蒸发溶剂再高温煅烧后获得了手性向列结构可调的多功能玻璃。
本研究概述了国内外CNC胆甾相液晶的制备方法及其调控手段,综述了CNC胆甾相液晶的形成机制、结构与和学特性,总结了CNC胆甾相液晶在温敏型功能材料、光电功能材料和手性介孔功能材料等领域的应用,并展望了其未来发展趋势。
1 CNC胆甾相液晶制备与调控 1.1 CNC胆甾相液晶制备纤维素包含结晶区和非结晶区,通过氢键和范德华力维持着纤维形态(李伟等,2010;王林格等,2004)。利用强酸对纤维素非结晶区内缩醛键更易攻击的特性,控制反应条件可得到纤维素纳米晶体(卿彦等,2012; Tian et al., 2016)。木材、棉花、细菌和被囊动物是制备纤维素纳米晶体的典型原料,由其制备的纤维素纳米晶体长70~1 000 nm,宽3~50 nm(表 1)。
|
|
Revol等(1992)提出棒状的木质纤维素纳米晶体溶液在低浓度情况下可以形成胆甾相液晶后,研究者们相继发现来自不同原料的纤维素纳米晶体溶液在溶剂挥发过程中也可以形成胆甾相液晶。文献报道这些CNC虽然都能形成胆甾相液晶,但是临界浓度(Ca)不同(表 1)。细菌纤维素纳米晶体溶液形成胆甾相液晶的临界浓度最低,可能是由于细菌纤维素具有较大的长径比和较低的电荷密度造成的(Revol et al., 1992; Elazzouzi-Hafraoui et al., 2007; Hirai et al., 2008)。
目前,CNC胆甾相液晶制备主要包括以下步骤:1)通过控制酸浓度(48%~65%)、水解温度(20~70 ℃)和水解时间(0.5~10 h)等反应条件,将纯的纤维素原料水解成表面带负电荷且具有较大长径比的纤维素纳米晶体(长100~200 nm、宽5~10 nm);2)将酸解后的CNC溶液用去离子水稀释,终止水解反应,并通过多次离心、透析去掉残余的酸(Kelly et al., 2014);3)以高分子质量的聚合物溶液(如聚乙二醇溶液)为反透析液,对低浓度的CNC溶液进行浓缩,得到较高浓度的CNC溶液;4)将CNC溶液于室温条件下自然干燥,CNC在静电斥力和分子间作用力驱动下,自组装形成具有手性向列结构的胆甾相液晶。
1.2 CNC胆甾相液晶调控在纳米尺度上调控自组装,是近年来新兴的研究热点之一,研究者们一直期待能像操控分子一样操控纤维素纳米晶体(Giese et al., 2015; Liu et al., 2015; Azzam et al., 2016)。在CNC胆甾相液晶中,螺距是一个重要的特征参数,通过调节螺距,可以有效改变CNC胆甾相液晶的光学性质。改变螺距主要有物理法和化学法(表 2),但需要注意的是,不论是采用物理法还是化学法,都必须在纤维素纳米晶体成膜之前进行,当纤维素纳米晶体液晶干燥成膜后,螺距将被固定。
|
|
调控CNC胆甾相液晶螺距的物理法主要通过超声波、温度、磁场和真空干燥等方式实现。超声波通过“空化效应”可提高CNC在溶剂中的分散性和自组装行为,达到调控螺距的目标。Beck等(2010)在蒸发自组装前,对CNC溶液进行超声处理,结果发现CNC胆甾相液晶超声处理后螺距增大。Liu等(2014)系统研究了超声时间对胆甾相液晶螺距的调控规律,结果显示,纤维素胆甾相液晶螺距与超声时间呈正相关,超声处理10 min,纤维素胆甾相液晶在偏光显微镜下呈蓝色,当持续超声至50 min,胆甾相液晶呈红色。随着超声时间增长,CNC获得更多外界能量,运动加剧,分散性增大,螺距也随之增大,选择性反射的波长发生明显红移。
在溶剂挥发过程中,温度对CNC自组装的动力学和热力学行为都具有重要影响。Pan等(2010)通过调整CNC溶液在挥发溶剂自组装过程中的温度,发现随着温度升高,CNC胆甾相液晶的螺距明显减小,并且这种短螺距在液晶薄膜中得以保存。分析其原因主要是因为温度升高,有效加快了CNC溶液的蒸发速率,改变了其动力学和热力学行为,CNC胆甾相液晶薄膜螺距变小。
磁场也是调控CNC胆甾相液晶螺距的有效方法。Pan等(2010)、Kimura等(2005)研究指出,CNC胆甾相液晶在磁场中作用时间越长,螺距越大。分析其原因主要是因为在磁场作用下的时间延长,越来越多的CNC倾向于磁场方向,从而使CNC扭转的周期增大,即螺距增大。
Chen等(2014a)通过真空干燥辅助自组装方法成功制备了CNC液晶薄膜,并发现在真空干燥条件下,溶液浓度对最终形成的液晶薄膜螺距具有调控作用,由此推测,在一定真空度下,溶液的存在阻碍了CNC组装,使得CNC胆甾相液晶的螺距随着溶液浓度增加变大,但是随着浓度的进一步提高,螺距减小,最后再提高浓度时,螺距又增大。然而,CNC溶液浓度对螺距调控的真正原因还未完全揭示。
1.2.2 化学法调控CNC胆甾相液晶螺距的化学法主要通过添加电解质和添加剂等方式实现。常用的电解质有NaCl、HCl和KCl等(Revol et al., 1992; Dong et al., 1997a),添加剂有葡萄糖、PVA和刚果红等(Gray, 2014;Cheung et al., 2013; Dong et al., 1997b)。电解质可改变CNC溶液的离子强度,影响体系的分散性、稳定性和液晶性。添加剂不改变体系的离子强度,但是可提高胶体体系的凝胶化作用,从而实现对CNC胆甾相液晶螺距的调控。
在纯净的CNC水相体系中,溶液的离子强度取决于CNC表面电荷。当在溶液中添加电解质时,离子强度由CNC表面电荷与外加电解质共同决定。Revol等(1992)研究发现,CNC溶液中添加电解质,螺距减小。Pan等(2010)将NaCl添加到CNC溶液中,发现CNC胆甾相液晶薄膜的螺距与NaCl添加量呈负相关关系。这是由于电解质对CNC表面负电荷起到了屏蔽作用,使CNC之间的静电作用力减小,从而导致螺距减小。
在CNC溶液中添加呈电中性的添加剂,虽然不改变溶液离子强度,但是提高了CNC的凝胶化作用,CNC自组装受阻。Gray(2014)在CNC溶液中添加D-(+)-葡萄糖,研究螺距与D-(+)-葡萄糖添加量的关系,结果显示,随着D-(+)-葡萄糖含量增加,液晶螺距先减小后增大。这是因为D-(+)-葡萄糖对CNC产生2方面作用:一方面,加强CNC的扭转作用,减小螺距;另一方面,增加黏度,阻碍CNC的组装,增大螺距。D-(+)-葡萄糖在低浓度时对溶液黏度影响不大,CNC的扭转作用被增强,导致螺距减小;但在较高浓度时,溶液黏度剧增,CNC的扭转效果小于黏度引起的阻碍效果,最终导致螺距增大。
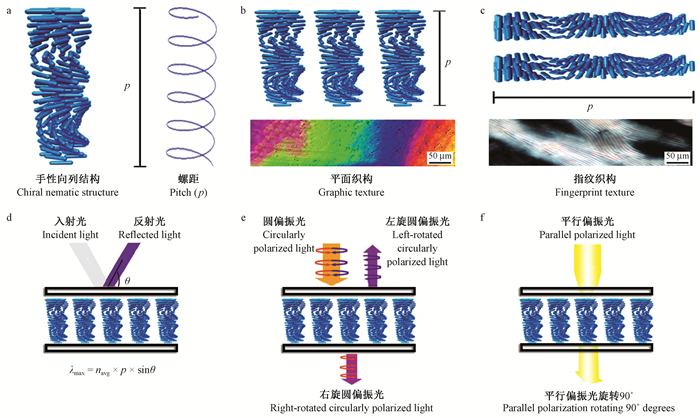
2 CNC胆甾相液晶结构及光学特性CNC为一维棒状纳米材料(图 1a),具有强烈的自动剪切取向趋势,达到临界浓度即可形成CNC胆甾相液晶。在CNC胆甾相液晶中,CNC分层排列,同层内CNC长轴取向相同,而轴心位置不同;不同层内CNC长轴取向会按层逐一向左旋转一定角度,整体呈现螺旋状。当CNC长轴随层向左旋转360°时,层与层之间的距离称为螺距,用p表示(图 1a)。
|
图 1 CNC胆甾相液晶结构及其光学特性 Fig. 1 CNC cholesteric phase liquid crystal structure and optical properties a.CNC胆甾相结构b.平面织构c.指纹织构d.选择性反射e.圆二色性f.旋光性 a.Cholesteric structure; b.Graphic texture; c.Fingerprint texture; d.Selective reflection property; e.Circular dichroism property; f.Optical rotation property. |
按照螺旋轴取向,CNC胆甾相液晶主要分为2种织构,即平面织构和指纹织构。平面织构中,CNC胆甾相液晶螺旋轴与光源方向平行,基片与螺旋轴垂直(图 1b),在偏光显微镜下能够观察到虹彩现象(图 1b下),是CNC胆甾相液晶具有的手性向列结构引起的布拉格反射(De souza et al., 2004)或双折射造成的(Majoinen et al., 2012)。指纹织构中,CNC胆甾相液晶螺旋轴与光源方向垂直,基片与螺旋轴平行(图 1c),在偏光显微镜下可以观察到明暗相间的衍射条纹(Beck-Candanedo et al., 2005)(图 1c下)(曾加等, 2000; Saha et al., 2012; Mo et al., 2009)。
手性向列结构使得CNC胆甾相液晶具有独特的光学性能,如选择性反射、圆二色性和旋光性等(Furumi et al., 2003)。当一束白光照射在CNC胆甾相液晶上时,可能反射出紫色光(图 1d),是因为光到达CNC胆甾相液晶发生了选择性反射,这种反射遵循晶体衍射的布拉格反射方程λ=npsinφ (式中:λ为反射光的波长;n为平均折射率;φ为入射光与晶面的夹角;p为胆甾相液晶的螺距)。CNC胆甾相液晶的螺距p一般为数百纳米,其反射波长在可见光波长范围内(De souza et al., 2004; Edgar et al., 2001)。
圆二色性是指当一束圆偏振光入射到CNC胆甾相液晶上时,光波的电振动矢量发生左旋(逆时针旋转),即圆偏振光被分成左旋与右旋2束偏振光。根据CNC胆甾相液晶左旋的特点,右旋偏振光透过液晶,左旋偏振光被反射(图 1e)。旋光性是指当线偏振光经过CNC胆甾相液晶时,其振动方向逐渐扭转一个角度,即偏振光的振动平面在CNC胆甾相液晶手性向列结构内逐渐被旋转。所以当光线穿过CNC胆甾相液晶后,光的振动平面发生一定的偏转(图 1f),透射光的振动平面与入射光的振动平面存在一定的偏转角(Zhu et al., 2016)。
3 CNC胆甾相液晶形成机制CNC胆甾相液晶属于溶致液晶(一种包含溶剂化合物在内的2种或多种化合物形成的液晶),溶致液晶在形成过程中存在2个临界浓度Ca与Ci:Ca为各向异性相开始出现的浓度,Ci为各向异性相完全形成时的浓度。当溶液浓度小于Ca时,溶液为各向同性相,不会出现液晶相;当溶液浓度大于Ca小于Ci时,各向同性相与各向异性相同时存在,发生相分离;当溶液浓度大于Ci时,溶液处于单一的各向异性相,胆甾相液晶形成(Dong et al., 1996; Werbowyj et al., 1976)。对于CNC胆甾相液晶的形成机制主要有2种观点:一种观点认为CNC表面上电荷的螺旋排列引发CNC手性排列,另一种观点认为CNC本身的扭曲结构引起CNC手性排列。
Mu等(2014)研究了CNC自组装形成胆甾相液晶的过程,其认为CNC自组装分为2个阶段,即两相共存阶段和单一的各向异性阶段;然而,低浓度时各相同性没有做出详细讨论。Dumanli等(2014)为更详细揭示整个自组装过程,通过控制CNC溶液浓度,将CNC溶液蒸发自组装过程分为各向同性、两相共存和各向异性3个阶段:第1阶段,溶液浓度低,CNC主要发生布朗运动,稳定地分散于水溶液中,呈现各向同性;第2阶段,随着水分蒸发,溶液的浓度增至临界浓度Ca,CNC在静电斥力和分子间作用力驱动下进行自组装排列,形成手性向列结构,各向异性相开始出现,此时溶液两相共存;第3阶段,随着水分继续蒸发,溶液浓度不断增加,当浓度超过Ci时,CNC有序排列更加紧密,各向同性相完全转变为各向异性相。
4 CNC胆甾相液晶在功能材料中的应用 4.1 温敏型功能材料温敏型功能材料是指对温度刺激具有响应性的智能材料,在化学、生物和纺织等领域应用前景广阔。随着科学技术不断发展,单一的温敏型聚合物已不能满足要求,如聚N-异丙基丙烯酰胺(PNIPAAm)具有温敏性,但不具有液晶性(Wang et al., 2015),可通过调控温度这一外界条件调节CNC溶液溶剂的挥发速度,制备螺距不同的液晶材料,但该方法不具可逆性。为解决这一难题,一些研究者试图将温敏型聚合物接枝到CNC上。
Yi等(2009)采用原子转移自由基聚合法(ATRP)在CNC表面接枝聚甲基丙烯酸N, N-二甲基氨基乙酯(PDMAEMA)制备PDMAEMA-g-CNC共聚物,这种温敏型功能材料不仅具有典型的指纹织构,而且其螺距具有温度可调控性(图 2a、b)。升高温度时,PDMAEMA聚合物疏水性增强,分子链从无规线团状态转变为规整的线条状,这种转变降低了CNC之间的排斥力,扭曲程度加大,螺距随温度升高而减小;降低温度时,分子链重新从规整的线条状转变为无规线团状,这种转变增加了CNC之间的排斥力,扭曲程度减小,螺距随温度降低而增大。

|
图 2 CNC胆甾相液晶功能材料的应用 Fig. 2 The application of CNC cholesteric phase liquid crystal materials a.温敏型功能材料 b.温敏型功能材料模型 c.光电功能材料d.光电功能材料模型 e.手性介孔功能材料 f.手性介孔功能材料模型 a.The temperature response of functional materials; b.The temperature response model of the functional material(Yi et al., 2009); c.The photoelectric functional materials; d.The photoelectric functional material mode(Chen et al., 2014b); e.The chiral mesoporous of functional materials; f.The chiral mesoporous of functional material model(Khan et al., 2015). |
光电功能材料在储能和传感等领域应用广泛,对其研究开发是当前的研究热点。CNC胆甾相液晶不仅具有精细的纳米结构和特有的光学性能,而且能与导电性能优异的材料复合,制备出新型光电功能材料。Zhang等(2013)通过原位聚合方法获得了PANI/CNC光电功能材料,该材料的导电性随着添加CNC比例增加而减小;但是,CNC胆甾相液晶在PANI/CNC光电功能材料中表现出不稳定性,其螺旋形态和扭转力的控制仍是一个值得关注的问题。Chen等(2014b)采用超声预处理制备了一种大尺寸、无裂缝且具有虹彩光学性质的氧化石墨烯GO/CNC复合材料薄膜(图 2c、d),没有超声时,CNC与GO无序排列,各向同性,干燥得到没有虹彩特性的薄膜;经过超声预处理后,CNC与GO得到能量进行自组装,形成手性向列结构,干燥得到虹彩特性的薄膜。GO/CNC薄膜在光学传感器、可协调反射滤波器、安全材料等领域有较好的应用前景。
4.3 手性介孔功能材料手性介孔功能材料可利用超分子聚集体、胶体晶体和溶致液晶等模板制备而成。Thomas等(2003)以羟丙基纤维素为模板制备了高比表面积的介孔硅,但手性向列结构没有得以保存。同样,Shin等(2007)以CNC为模板通过煅烧得到了高比表面积的二氧化钛材料,但手性向列结构仍未保留。
为解决手性向列结构难以复制的问题,Khan等(2015)以酚醛树脂为前驱体与CNC溶液混合干燥得到一个多彩的手性薄膜,固化后再用NaOH溶解掉CNC,获得了具有手性向列结构的介孔酚醛树脂(图 2e、f)。手性向列介孔酚醛树脂能根据颜色变化反映含水量变化,且经过盐酸和甲醛处理后仍具有同样的效果。复合材料含水量的变化引起羟甲基密度变化,进而改变螺距来影响布拉格反射,在宏观上表现为颜色变化。
Schlesinger等(2015)以无机硅材料作为前驱体与CNC溶液混合蒸发自组装得到手性复合材料,再通过去CNC模板得到手性介孔无机硅材料。该种手性介孔无机硅材料可以通过改变无机硅的含量或者自组装基底材质来控制螺距,且其结构可以在水中稳定存在,因此在组织工程学、功能膜等领域具有潜在的应用价值。
5 结论与展望CNC胆甾相液晶以其特有的选择性反射、圆二色性和旋光性在防伪识别、光信息储存、智能窗口和液晶显示等先进材料领域表现出极大的应用潜力。国内外学者围绕CNC胆甾相液晶的制备方法、调控手段、形成机制和光学特性等方面开展了一系列研究,并在温敏型功能材料、光电功能材料和手性介孔材料等应用领域取得了一定成果。然而,如何诱导CNC快速形成性能稳定的胆甾相液晶尚处于起步阶段;同时利用CNC胆甾相液晶的特殊结构与优异特性研发新型先进功能材料,拓宽CNC胆甾相液晶的应用领域也是急需解决的关键课题。具体而言,在今后的研究工作中应围绕以下几方面展开:1)改良CNC制备技术,获得表面电性稳定、粒径分布均一的纤维素纳米晶体,为CNC胆甾相液晶的形成提供结构基础;2)深入研究CNC胆甾相液晶的形成机制,融合其他领域的先进技术与方法替代现有的缓慢蒸发自组装法,开发绿色快速的CNC胆甾相液晶制造方法;3)系统研究温度、磁场、添加剂和电解质等因素对CNC胆甾相液晶的物理、力学、光学等性能的影响机制,建立多元调控模型,引导CNC胆甾相液晶往智能化、数字化方向发展;4)利用其他功能性纳米粒子在CNC诱导下能形成胆甾相液晶的特性,复制CNC胆甾相液晶手性向列结构,研发更多的性能卓越的功能材料。
李伟, 王锐, 刘守新. 2010. 纳米纤维素的制备. 化学进展, 22(10): 2060-2070. (Li W, Wang R, Liu S X. 2010. Preparation of nanocrystalline cellulose. Progress in Chemistry, 22(10): 2060-2070. [in Chinese]) |
卿彦, 蔡智勇, 吴义强, 等. 2012. 纤维素纳米纤丝研究进展. 林业科学, 48(7): 145-152. (Qing Y, Cai Z Y, Wu Y Q, et al. 2012. Study progress on cellulose nanofibril. Scientia Silvae Sinicae, 48(7): 145-152. [in Chinese]) |
王林格, 黄勇. 2004. 纤维素衍生物胆甾相液晶体系的结构及光学性能. 液晶与显示, 19(1): 10-13. (Wang L G, Huang Y. 2004. Structure and optical property of cellulose derivatives cholesteric liquid crystalline system. Chinese Journal of Liquid Crystals and Displays, 19(1): 10-13. DOI:10.3969/j.issn.1007-2780.2004.01.003 [in Chinese]) |
杨洁, 叶代勇. 2012. 纳米纤维素晶须表面接枝及其液晶性能研究进展. 化工进展, 31(9): 1990-1997. (Yang J, Ye D Y. 2012. Progress of surface grafted nano cellulose whiskers and liquid crystals. Chemical Industry and Engineering Progress, 31(9): 1990-1997. [in Chinese]) |
曾加, 黄勇. 2000. 纤维素及其衍生物的胆甾型液晶结构. 高分子材料科学与工程, 16(6): 13-17. (Zeng J, Huang Y. 2000. Cholesteric structure of cellulose derivative liquid crystals. Polymer Materials Science and Engineering, 16(6): 13-17. DOI:10.3321/j.issn:1000-7555.2000.06.004 [in Chinese]) |
Angles M N, Dufresne A. 2000. Plasticized starch/tunicin whiskers nanocomposites. 1.Structural analysis. Macromolecules, 33(22): 8344-8353. |
Araki J, Wada M, Kuga S, et al. 1998. Flow properties of microcrystalline cellulose suspension prepared by acid treatment of native cellulose. Colloids and Surfaces A, 142(1): 75-82. DOI:10.1016/S0927-7757(98)00404-X |
Araki J, Wada M, Kuga S, et al. 1999. Influence of surface charge on viscositybehavior of cellulose microcrystal suspension. Journal of Wood Science, 45(3): 258-261. DOI:10.1007/BF01177736 |
Araki J, Kuga S. 2001. Effect of trace electrolyte on liquid crystal type of cellulosemicrocrystals. Langmuir, 17(15): 4493-4496. DOI:10.1021/la0102455 |
Azzam F, Siqueira E, Fort S, et al. 2016. Tunable aggregation and gelation of thermoresponsive suspensions of polymer-grafted cellulose nanocrystals. Biomacromolecules, 17(6): 2112-2119. DOI:10.1021/acs.biomac.6b00344 |
Beck-Candanedo S, Roman M, Gray D. 2005. Effect of reaction conditions on theproperties and behavior of wood cellulose nanocrystal suspensions. Biomacromolecules, 6(2): 1048-1054. DOI:10.1021/bm049300p |
Beck S, Bouchard J, Berry R. 2010. Controlling the reflection wavelength of iridescent solid films of nanocrystalline cellulose. Biomacromolecules, 12(1): 167-172. |
Castro-Guerrero C F, Gray D G. 2014. Chiral nematic phase formation by aqueous suspensions of cellulose nanocrystals prepared by oxidation with ammonium persulfate. Cellulose, 21(4): 2567-2577. DOI:10.1007/s10570-014-0308-1 |
Chen Q, Liu P, Sheng C, et al. 2014a. Tunable self-assembly structure of graphene oxide/cellulose nanocrystal hybrid films fabricated by vacuum filtration technique. RSC Advances, 4(74): 39301-39304. DOI:10.1039/C4RA05921B |
Chen Q, Liu P, Nan F, et al. 2014b. Tuning the iridescence of chiral nematic cellulose nanocrystal films with a vacuum-assisted self-assembly technique. Biomacromolecules, 15(11): 4343-4350. DOI:10.1021/bm501355x |
Cheung C C Y, Giese M, Kelly J A, et al. 2013. Iridescent chiral nematic cellulose nanocrystal/polymer composites assembled in organic solvents. ACS Macro Letters, 2(11): 1016-1020. DOI:10.1021/mz400464d |
De Souza Lima M M, Borsali R. 2004. Rodlike cellulose microcrystals:structure, properties, and applications. Macromolecular Rapid Communications, 25(7): 771-787. DOI:10.1002/(ISSN)1521-3927 |
Dong X M, Kimura T, Revol J F, et al. 1996. Effects of ionic strength on the isotropic-chiral nematic phase transition of suspensions of cellulose crystallites. Langmuir, 12(8): 2076-2082. DOI:10.1021/la950133b |
Dong X M, Gray D G. 1997a. Effect of counterions on ordered phase formation in suspensions of charged rodlike cellulose crystallites. Langmuir, 13(8): 2404-2409. DOI:10.1021/la960724h |
Dong X M, Gray D G. 1997b. Induced circular dichroism of isotropic and magnetically-oriented chiral nematic suspensions of cellulose crystallites. Langmuir, 13(11): 3029-3034. DOI:10.1021/la9610462 |
Dumanli A G, Kamita G, Landman J, et al. 2014. Controlled, bio-inspired self-assembly of cellulose-based chiral reflectors. Advanced Optical Materials, 2(7): 646-650. DOI:10.1002/adom.201400112 |
Edgar C D, Gray D G. 2001. Induced circular dichroism of chiral nematic cellulose films. Cellulose, 8(1): 5-12. DOI:10.1023/A:1016624330458 |
Elazzouzi-Hafraoui S, Nishiyama Y, Putaux J L, et al. 2007. The shape and size distribution of crystalline nanoparticles prepared by acid hydrolysis of native cellulose. Biomacromolecules, 9(1): 57-65. |
Furumi S, Yokoyama S, Otomo A, et al. 2003. Electrical control of the structure and lasing in chiral photonic band-gap liquid crystals. Applied Physics Letters, 82(1): 16-18. DOI:10.1063/1.1534613 |
Giese M, Blusch L K, Khan M K, et al. 2015. Functional materials from cellulose-derived liquid-crystal templates. Angewandte Chemie International Edition, 54(10): 2888-2910. DOI:10.1002/anie.201407141 |
Gray D G. 2014. Isolation and handedness of helical coiled cellulosic thickenings from plant petiole tracheary elements. Cellulose, 21(5): 3181-3191. DOI:10.1007/s10570-014-0382-4 |
Heux L, Chauve G, Bonini C. 2000. Nonflocculating and chiral-nematic self-ordering of cellulose microcrystals suspensions in nonpolar solvents. Langmuir, 16(21): 8210-8212. DOI:10.1021/la9913957 |
Hirai A, Inui O, Horii F, et al. 2008. Phase separation behavior in aqueous suspensions of bacterial cellulose nanocrystals prepared by sulfuric acid treatment. Langmuir, 25(1): 497-502. |
Kelly J A, Giese M, Shopsowitz K E, et al. 2014. The development of chiral nematic mesoporous materials. Accounts of Chemical Research, 47(4): 1088-1096. DOI:10.1021/ar400243m |
Khan M K, Bsoul A, Walus K, et al. 2015. Photonic patterns printed in chiral nematic mesoporous resins. Angewandte Chemie International Edition, 127(14): 4378-4382. |
Kimura F, Kimura T, Tamura M, et al. 2005. Magnetic alignmentof the chiral nematic phase of a cellulose microfibril suspension. Langmuir, 21(5): 2034-2037. DOI:10.1021/la0475728 |
Liu D, Wang S, Ma Z, et al. 2014. Structure-color mechanism of iridescent cellulose nanocrystal films. RSC Advances, 4(74): 39322-39331. DOI:10.1039/C4RA06268J |
Liu B, Cao Y, Huang Z, et al. 2015. Silica biomineralization via the self-assembly of helical biomolecules. Advanced Materials, 27(3): 479-497. DOI:10.1002/adma.v27.3 |
Majoinen J, Kontturi E, Ikkala O, et al. 2012. SEM imaging of chiral nematic films cast from cellulose nanocrystal suspensions. Cellulose, 19(5): 1599-1605. DOI:10.1007/s10570-012-9733-1 |
Marchessault R H, Morehead F F, Walter N M. 1959. Liquid crystal systems from fibrillar polysaccharides. Nature, 184(4686): 632-633. DOI:10.1038/184632a0 |
Mo Z, Zhao Z, Chen H, et al. 2009. Heterogeneous preparation of cellulose-polyaniline conductive composites with cellulose activated by acids and its electrical properties. Carbohydrate Polymers, 75(4): 660-664. DOI:10.1016/j.carbpol.2008.09.010 |
Moon R J, Martini A, Nairn J, et al. 2011. Cellulose nanomaterials review:structure, properties and nanocomposites. Chemical Society Reviews, 40(7): 3941-3994. DOI:10.1039/c0cs00108b |
Mu X, Gray D G. 2014. Formation of chiral nematic films from cellulose nanocrystal suspensions is a two-stage process. Langmuir, 30(31): 9256-9260. DOI:10.1021/la501741r |
Pan J, Hamad W, Straus S K. 2010. Parameters affecting the chiral nematic phase of nanocrystalline cellulose films. Macromolecules, 43(8): 3851-3858. DOI:10.1021/ma902383k |
Revol J F, Bradford H, Giasson J, et al. 1992. Helicoidal self-ordering of cellulose microfibrils in aqueous suspension. International Journal of Biological Macromolecules, 14(3): 170-172. DOI:10.1016/S0141-8130(05)80008-X |
Saha A, Tanaka Y, Han Y, et al. 2012. Irreversible visual sensing of humidity using a cholesteric liquid crystal. Chemical Communications, 48(38): 4579-4581. DOI:10.1039/c2cc16934g |
Schlesinger M, Giese M, Blusch L K, et al. 2015. Chiral nematic cellulose-gold nanoparticle composites from mesoporous photonic cellulose. Chemical Communications, 51(3): 530-533. DOI:10.1039/C4CC07596J |
Sena C, Godinho M H, Oliveira C L P, et al. 2011. Liquid crystalline cellulosic elastomers:freestanding anisotropic films under stretching. Cellulose, 18(5): 1151-1163. DOI:10.1007/s10570-011-9575-2 |
Shin Y, Exarhos G J. 2007. Template synthesis of porous titania using cellulose nanocrystals. Materials Letters, 61(11): 2594-2597. |
Shopsowitz K E, Qi H, Hamad W Y, et al. 2010. Free-standing mesoporous silica films with tunable chiral nematic structures. Nature, 468(7322): 422. DOI:10.1038/nature09540 |
Shopsowitz K E, Hamad W Y, MacLachlan M J. 2011. Chiral nematic mesoporous carbon derived from nanocrystalline cellulose. Angewandte Chemie International Edition, 50(46): 10991-10995. DOI:10.1002/anie.v50.46 |
Thomas A, Antonietti M. 2003. Silica nanocasting of simple cellulose derivatives:towards chiral pore systems with long-range order and chiral optical coatings. Advanced Functional Materials, 13(10): 763-766. DOI:10.1002/(ISSN)1616-3028 |
Tian C, Yi J, Wu Y, et al. 2016. Preparation of highly charged cellulose nanofibrils using high-pressure homogenization coupled with strong acid hydrolysis pretreatments. Carbohydrate Polymers, 136: 485-492. DOI:10.1016/j.carbpol.2015.09.055 |
Wang B, Walther A. 2015. Self-assembled, iridescent, crustacean-mimetic nanocomposites with tailored periodicity and layered cuticular structure. ACS Nano, 9(11): 10637-10646. DOI:10.1021/acsnano.5b05074 |
Werbowyj R S, Gray D G. 1976. Liquid crystalline structure in aqueous hydroxypropyl cellulose solutions. Molecular Crystals and Liquid Crystals, 34(4): 97-103. DOI:10.1080/15421407608083894 |
Yang J, Ye D Y. 2012. Liquid crystal of nanocellulose whiskers grafted with acrylamide. Chinese Chemical Letters, 23(3): 367-370. DOI:10.1016/j.cclet.2011.12.014 |
Yi J, Xu Q, Zhang X, et al. 2009. Temperature-induced chiral nematic phase changes of suspensions of poly (N, N-dimethylaminoethyl methacrylate)-grafted cellulose nanocrystals. Cellulose, 16(6): 989-997. DOI:10.1007/s10570-009-9350-9 |
Zhang D, Zhang L, Wang B, et al. 2013. Nanocomposites of polyaniline and cellulose nanocrystals prepared in lyotropic chiral nematic liquid crystals. Journal of Materials, 2013(614507): 1-6. |
Zhu H, Luo W, Ciesielski P N, et al. 2016. Wood-derived materials for green electronics, biological devices, and energy applications. Chemical Reviews, 116(16): 9305-9374. DOI:10.1021/acs.chemrev.6b00225 |
 2019, Vol. 55
2019, Vol. 55

